- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Синтез наночастиц неорганических веществ. (Лекция 7) презентация
Содержание
- 1. Синтез наночастиц неорганических веществ. (Лекция 7)
- 2. Одной из наиболее важных задач при синтезе
- 3. Образование зародышей и рост наночастиц Монодисперсные наночастицы
- 4. Образование наночастиц Радиус наночастиц рассчитывается по формуле:
- 5. Особенности роста наночастиц в растворах При смешивании
- 6. СПОСОБЫ СТАБИЛИЗАЦИИ НАНОЧАСТИЦ ДЛЯ ПРЕДОТВРАЩЕНИЯ АГРЕГАЦИИ Электростатическая
- 7. Стабилизации наночастиц против агрегации можно добиться
- 8. Особенности синтеза наночастиц металлов и полупроводников 2.
- 9. Наиболее часто используются следующие стабилизаторы 1. Органические
- 11. Одна из схем (а) синтеза наночастиц металлов
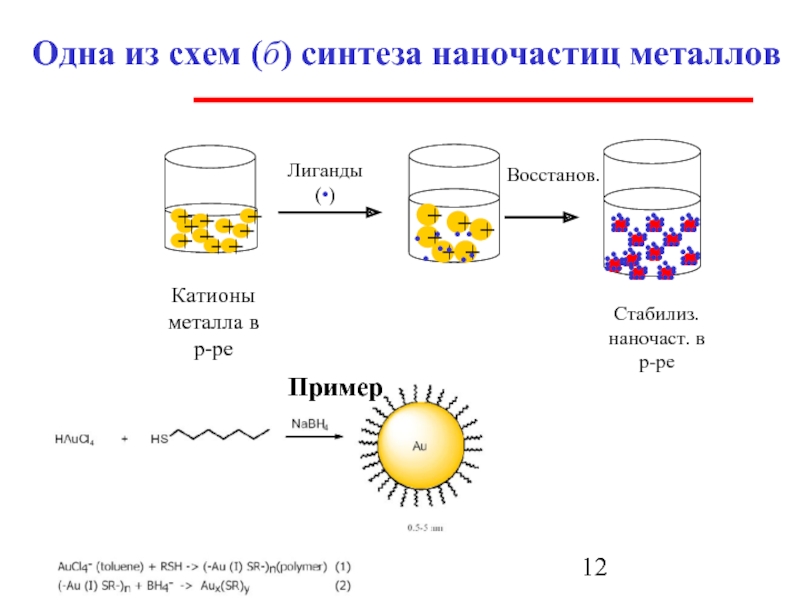
- 12. Одна из схем (б) синтеза наночастиц металлов Пример
- 13. Синтез наночастиц металлов в органических
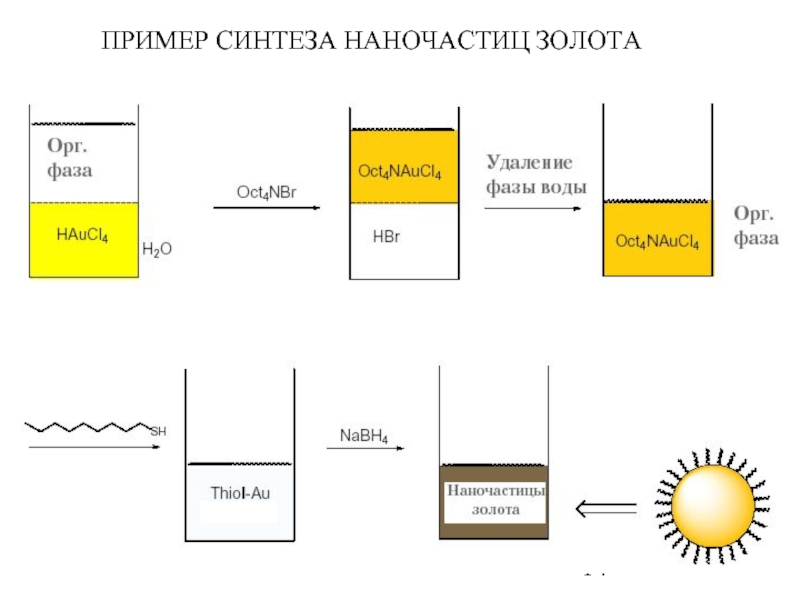
- 14. ПРИМЕР СИНТЕЗА НАНОЧАСТИЦ ЗОЛОТА
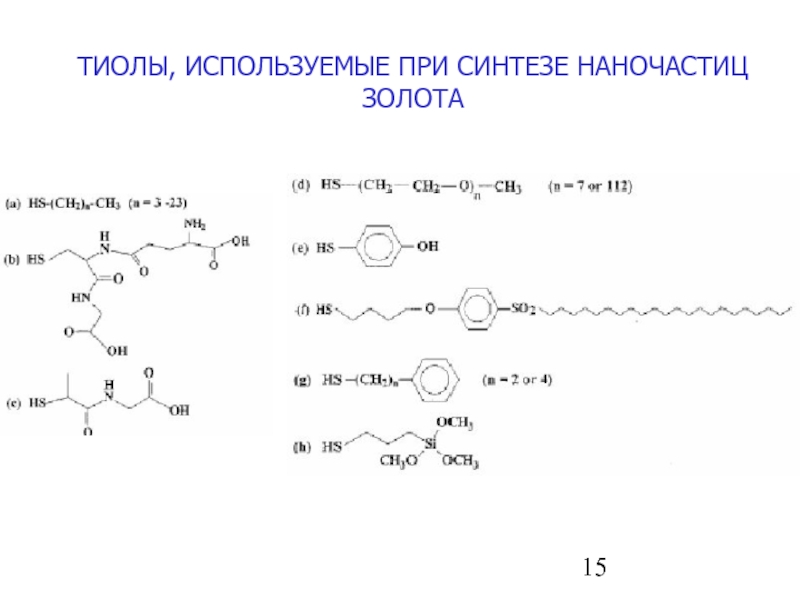
- 15. ТИОЛЫ, ИСПОЛЬЗУЕМЫЕ ПРИ СИНТЕЗЕ НАНОЧАСТИЦ ЗОЛОТА
- 16. ОСОБЕННОСТИ СВОЙСТВ НАНОЧАСТИЦ МЕТАЛЛОВ, СТАБИЛИЗИРОВАННЫХ МОНОСЛОЯМИ -ВЫСОКАЯ
- 17. ИЗОБРАЖЕНИЯ КОЛЛОИДНЫХ ЧАСТИЦ ЗОЛОТА, ПОЛУЧЕННЫЕ МЕТОДОМ ТЭМ
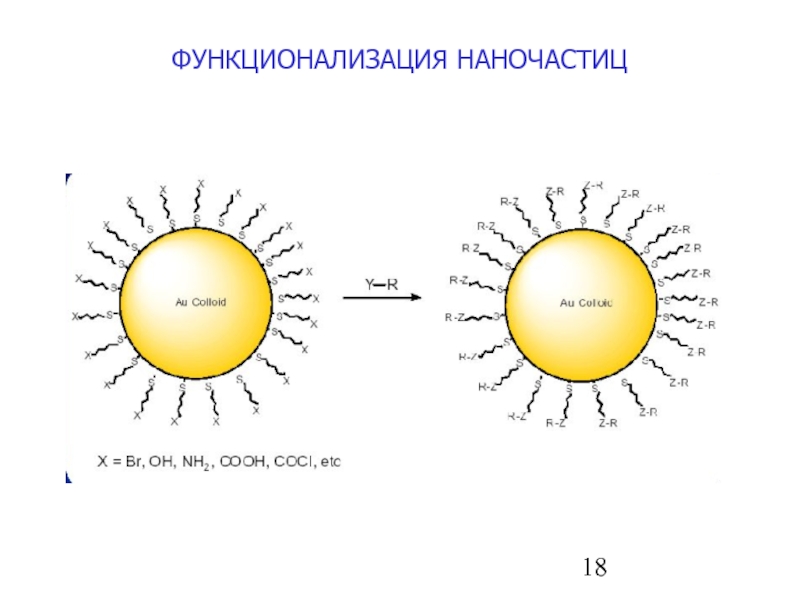
- 18. ФУНКЦИОНАЛИЗАЦИЯ НАНОЧАСТИЦ
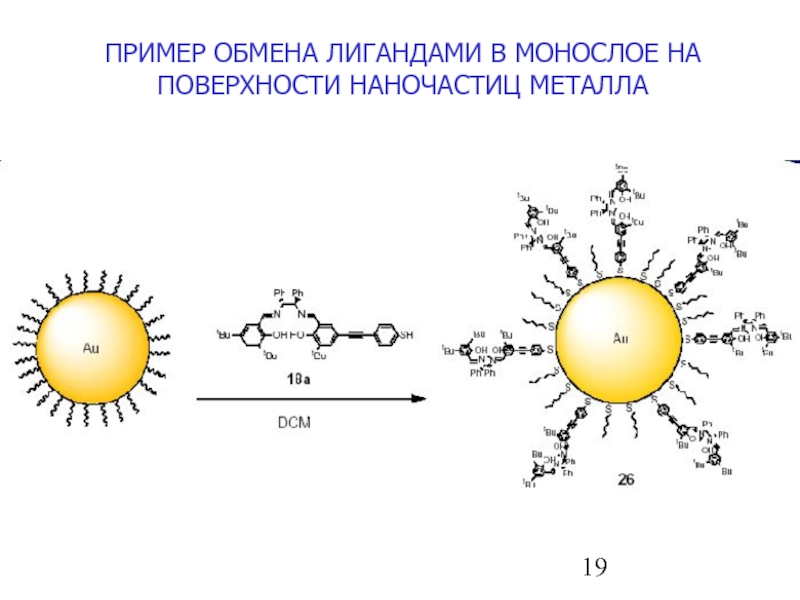
- 19. ПРИМЕР ОБМЕНА ЛИГАНДАМИ В МОНОСЛОЕ НА ПОВЕРХНОСТИ НАНОЧАСТИЦ МЕТАЛЛА
- 20. Синтез наночастиц CdS Общая схема: Chem.
- 21. Для синтеза наночастиц CdSe используют два раствора:
- 22. ПРИМЕР СИНТЕЗА НАНОЧАСТИЦ CdSe, СТАБИЛИЗИРОВАННЫХ ТОРО Молекулы
- 23. ПОЛУЧЕНИЕ МОНОДИСПЕРСНЫХ НАНОЧАСТИЦ МЕТОДОМ РАЗМЕРНО-СЕЛЕКТИВНОГО ОСАЖДЕНИЯ Идея
- 24. СРЕДНЕВЕКОВЫЙ ВИТРАЖ, СОДЕРЖАЩИЙ ЦВЕТНЫЕ СТЕКЛА, ОКРАШЕННЫЕ НАНОЧАСТИЦАМИ БЛАГОРОДНЫХ МЕТАЛЛОВ
- 25. Одним из способов синтеза наночастиц контролируемого размера
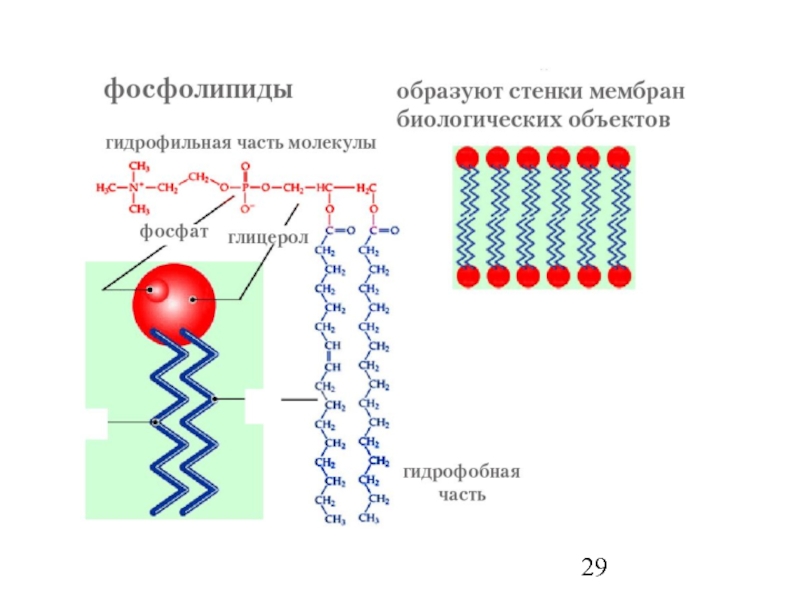
- 26. Гидрофильные части ПАВ образованы химическими группами, несущими
- 27. СИНТЕЗ НАНОЧАСТИЦ МЕТАЛЛОВ В МИКРОЭМУЛЬСИИ ВОДА/ ОРГАНИЧЕСКАЯ
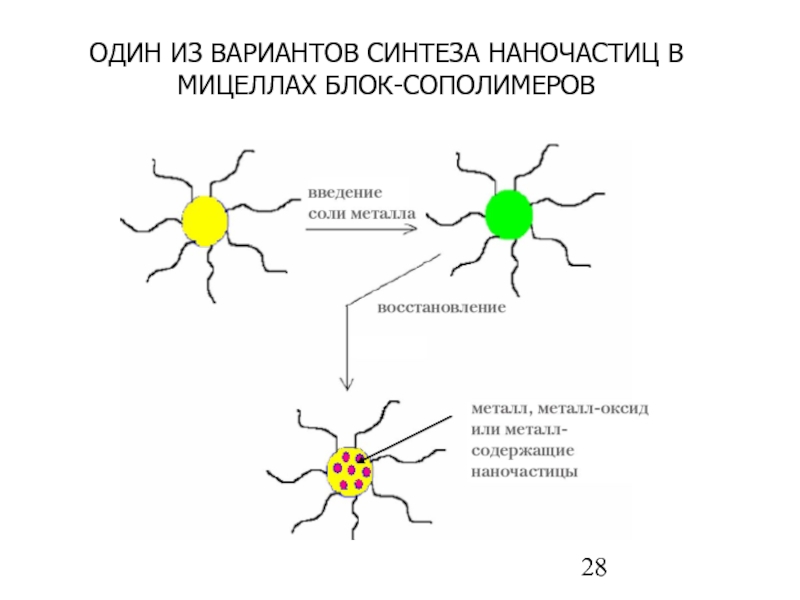
- 28. ОДИН ИЗ ВАРИАНТОВ СИНТЕЗА НАНОЧАСТИЦ В МИЦЕЛЛАХ БЛОК-СОПОЛИМЕРОВ
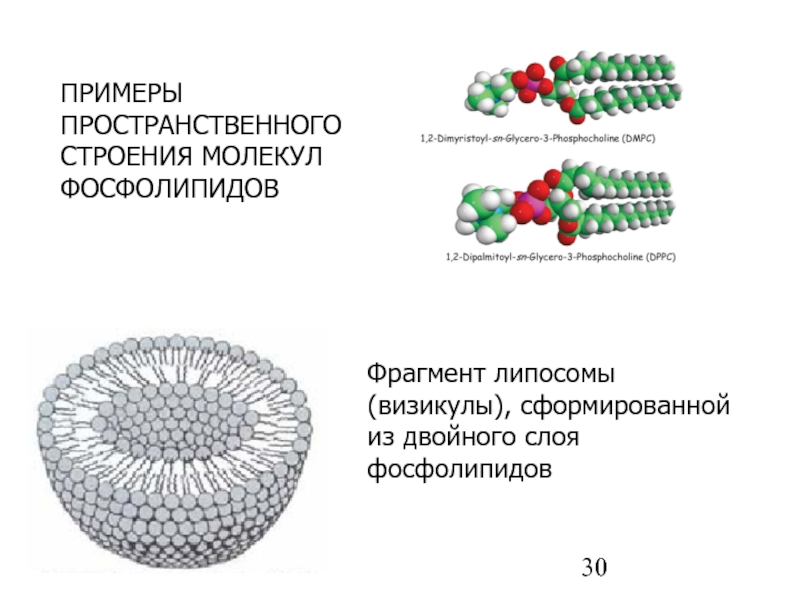
- 30. Фрагмент липосомы (визикулы), сформированной из двойного слоя фосфолипидов ПРИМЕРЫ ПРОСТРАНСТВЕННОГО СТРОЕНИЯ МОЛЕКУЛ ФОСФОЛИПИДОВ
- 31. Капсулирование широко используется в фармацевтической и косметической
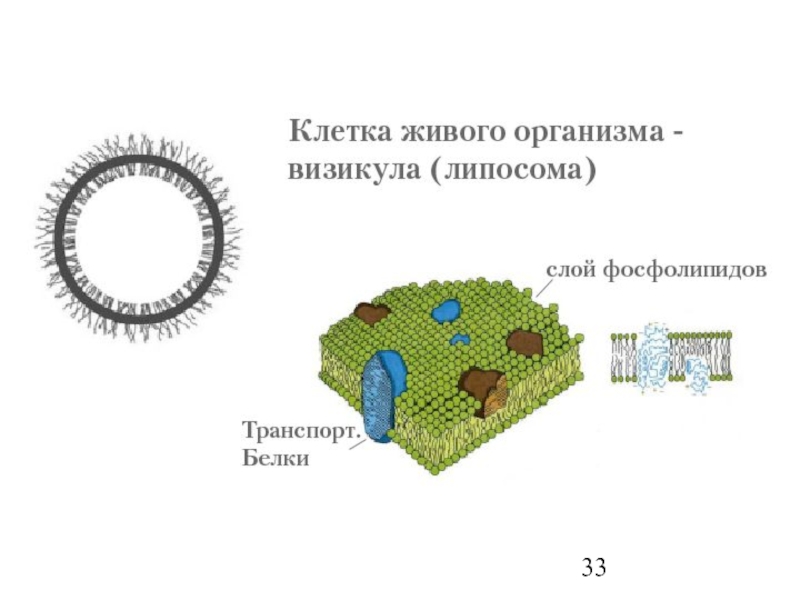
- 32. ЛИПОСОМЫ РАЗЛИЧАЮТСЯ 1. ПО КОЛИЧЕСТВУ СЛОЕВ В
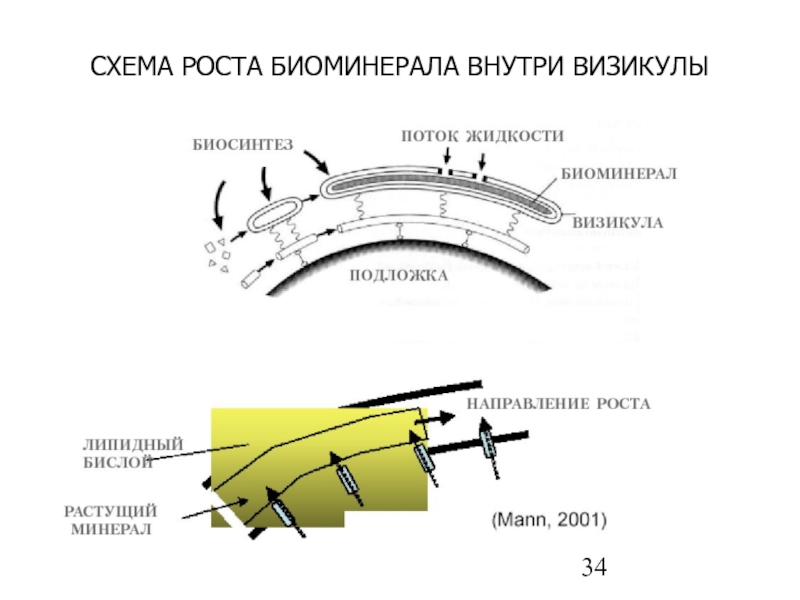
- 34. СХЕМА РОСТА БИОМИНЕРАЛА ВНУТРИ ВИЗИКУЛЫ
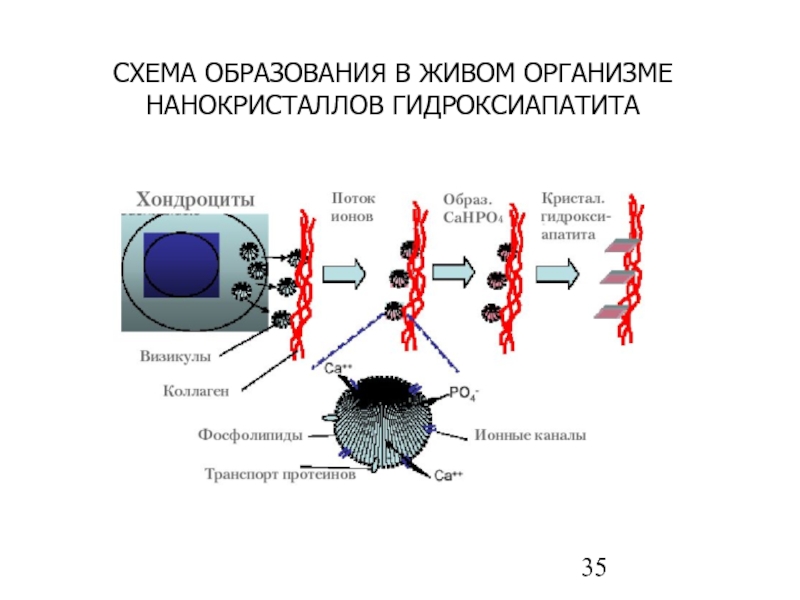
- 35. СХЕМА ОБРАЗОВАНИЯ В ЖИВОМ ОРГАНИЗМЕ НАНОКРИСТАЛЛОВ ГИДРОКСИАПАТИТА
- 36. Ферритин сохраняет железо в некоторых растениях
- 37. Glen C. King1, Sang H. Choi1 и
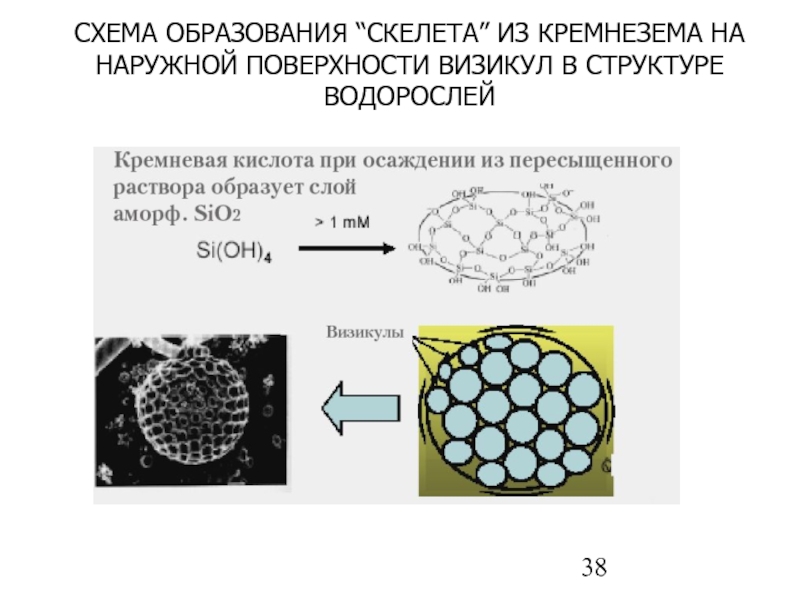
- 38. СХЕМА ОБРАЗОВАНИЯ “СКЕЛЕТА” ИЗ КРЕМНЕЗЕМА НА НАРУЖНОЙ ПОВЕРХНОСТИ ВИЗИКУЛ В СТРУКТУРЕ ВОДОРОСЛЕЙ
- 39. ДЕНДРИМЕРЫ КАК НАНОРЕАКТОРЫ ДЛЯ СИНТЕЗА НАНОЧАСТИЦ БЛАГОРОДНЫХ
- 40. НАНОРЕАКТОРЫ В ОРГАНИЧЕСКОЙ ХИМИИ Пример образования одного из стерео-изомеров в капсуле “призма”
- 41. ПОСЛОЙНЫЙ СИНТЕЗ НАНОКАПСУЛ, СТЕНКАМИ КОТОРЫХ ЯВЛЯЮТСЯ МОЛЕКУЛЫ
- 42. ПРИМЕНЕНИЕ НАНО- И МИКРОКАПСУЛ ДЛЯ КАПСУЛИРОВАНИЯ МОЛЕКУЛ ПРОТЕИНОВ ПРОТЕИН - α - chymotrypsin
- 43. Капсулы из PSS/PAH являются проницаемыми для OH-
- 44. ПОСЛОЙНЫЙ СИНТЕЗ БИО-НАНОРЕАКТОРОВ, СТЕНКАМИ КОТОРЫХ ЯВЛЯЮТСЯ МОЛЕКУЛЫ
Слайд 2Одной из наиболее важных задач при синтезе наночастиц неорганических соединений является
Данные наночастицы имеют:
- ОДИНАКОВЫЙ РАЗМЕР (УСЛОВНО С РАЗБРОСОМ НЕ БОЛЕЕ 5 проц.),
ФОРМУ И КРИСТАЛЛИЧЕСКУЮ СТРУКТУРУ.
ОБЛАСТЬ ПРИМЕНЕНИЯ ТАКИХ НАНОЧАСТИЦ -
- СИСТЕМАТИЧЕСКИЕ ИССЛЕДОВАНИЯ ЭЛЕКТРОННЫХ, ОПТИЧЕСКИХ И ДР. СВОЙСТВ ВЕЩЕСТВА В НАНОРАЗМЕРНОМ СОСТОЯНИИ,
- В КАЧЕСТВЕ ОСНОВНЫХ ЭЛЕМЕНТОВ В РЯДЕ ИЗДЕЛИЙ ОПТОЭЛЕКТРОНИКИ,
- В КАЧЕСТВЕ “СТРОИТЕЛЬНЫХ БЛОКОВ” СВЕРХРЕШЕТОК И КОЛЛОИДНЫХ КРИСТАЛЛОВ И Т.Д,
Слайд 3Образование зародышей и рост наночастиц
Монодисперсные наночастицы образуются, если процессы образования зародышей
Процесс образования зародышей должен быть быстрым, а процесс роста - медленным.
а) Образование зародышей происходит, если достигнут их
критический размер
б). Увеличение размера зародышей контролируется
диффузионными процессами
LaMer et al. J. Am. Chem. Soc. 1950, 72, 4847
Слайд 4Образование наночастиц
Радиус наночастиц рассчитывается по формуле:
ΔG = 4πσ(r2 – [2r3 /
Где r = радиус наночастицы,
r* = критический радиус зародыша
σ = поверхностное натяжение
ΔG(наночастицы) = n(ΔGобъемн. вещ. – ΔGатома) + σA
Где A = площадь поверхности
Слайд 5Особенности роста наночастиц в растворах
При смешивании реагентов формируется большое число центров
Если концентрация реагентов мала, то рост размера частиц останавливается.
Рост размера частиц в соответствии с эффектом Оствальда может быть остановлен стабилизаторами
Оствальдом показано, что более мелкие частицы в растворе растворяются больше, чем крупные и за счет этого происходит укрупнение наночастиц. Как только частицы укрупняются, их растворимость снижается.
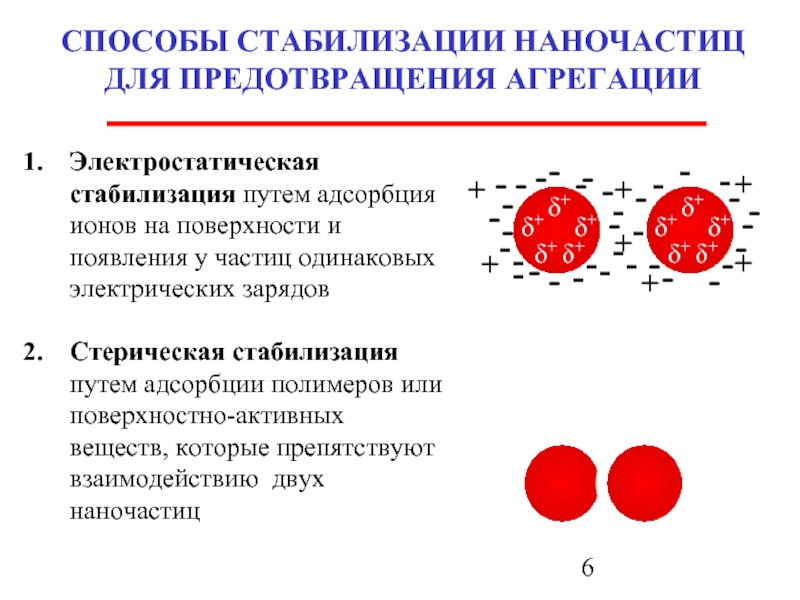
Слайд 6СПОСОБЫ СТАБИЛИЗАЦИИ НАНОЧАСТИЦ ДЛЯ ПРЕДОТВРАЩЕНИЯ АГРЕГАЦИИ
Электростатическая стабилизация путем адсорбция ионов на
Стерическая стабилизация путем адсорбции полимеров или поверхностно-активных веществ, которые препятствуют взаимодействию двух наночастиц
Слайд 7 Стабилизации наночастиц против агрегации можно добиться за счет уменьшения энергии
Слайд 8Особенности синтеза наночастиц металлов и полупроводников
2. Растворители, а именно: воду, полярные
органические растворители.
3. Восстановители: молекулярный водород, гидриды,
органические соединения и т.д.
При синтезе необходимо выбирать:
1. Исходные соединения.
4. Стабилизаторы.
Слайд 9Наиболее часто используются следующие стабилизаторы
1. Органические лиганды, тиолы, амины, фосфаты
2.
3. Полимеры
4. Растворители, эфиры, тиоэфиры
5. Полиоксоанионы
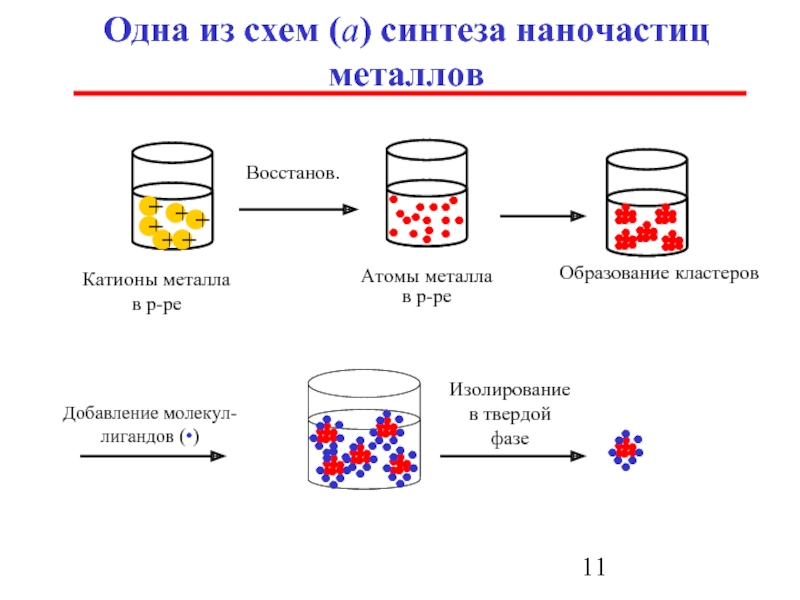
Слайд 11Одна из схем (а) синтеза наночастиц металлов
+
+
+
+
+
+
Восстанов.
Катионы металла в р-ре
Атомы металла
Добавление молекул-лигандов (•)
Образование кластеров
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
Изолирование в твердой фазе
Слайд 13
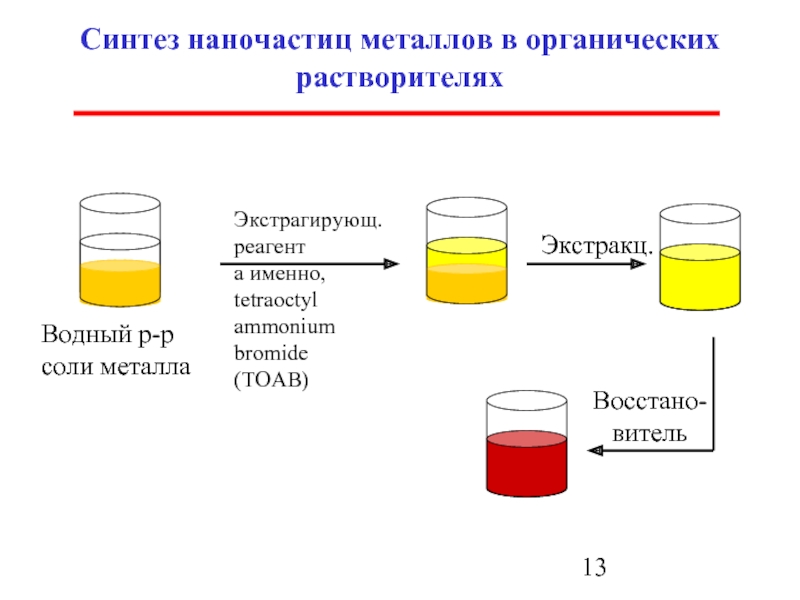
Синтез наночастиц металлов в органических растворителях
Водный р-р соли металла
Экстрагирующ. реагент
а
Восстано-
витель
Экстракц.
Слайд 16ОСОБЕННОСТИ СВОЙСТВ НАНОЧАСТИЦ МЕТАЛЛОВ, СТАБИЛИЗИРОВАННЫХ МОНОСЛОЯМИ
-ВЫСОКАЯ УДЕЛЬНАЯ ПОВЕРХНОСТЬ,
-КОНТРОЛИРУЕМЫЙ В ДИАПАЗОНЕ 1-5
- РАСТВОРИМОСТЬ В ОРГ. РАСТВОРИТЕЛЯХ,
- СПОСОБНОСТЬ К ОБМЕНУ ЛИГАНДАМИ,
- ВОЗМОЖНОСТЬ ФУНКЦИОНАЛИЗАЦИИ МОНОСЛОЯ ОРГ. ВЕЩЕСТВА
Слайд 17ИЗОБРАЖЕНИЯ КОЛЛОИДНЫХ ЧАСТИЦ ЗОЛОТА, ПОЛУЧЕННЫЕ МЕТОДОМ ТЭМ
Наночастицы получены по схеме (б)
Слайд 20Синтез наночастиц CdS
Общая схема:
Chem. Mater. 1999, 11, 3595
Данный синтез выполняют
В 1993 г. C.Murray предложил способ синтеза наночастиц полупроводников A2B6 с использованием растворителя ТОРО - три-н-октилфосфиноксида.
Слайд 21Для синтеза наночастиц CdSe используют два раствора: первый – раствор диметилкадмия
Синтез должен продолжаться несколько часов, и в ходе процесса можно вынимать часть раствора и получить таким образом несколько образцов с разными средними размерами наночастиц.
Слайд 22ПРИМЕР СИНТЕЗА НАНОЧАСТИЦ CdSe, СТАБИЛИЗИРОВАННЫХ ТОРО
Молекулы TOPO обеспечивают не только контролируемый
Слайд 23ПОЛУЧЕНИЕ МОНОДИСПЕРСНЫХ НАНОЧАСТИЦ МЕТОДОМ РАЗМЕРНО-СЕЛЕКТИВНОГО ОСАЖДЕНИЯ
Идея метода заключается в постепенном уменьшении
На практике данный метод реализуют следующим образом. Приготовив оптически чистый раствор наночастиц, при непрерывном помешивании в него по каплям добавляют осадитель до появления опалесценции, что означает образование флокулята. Отделяя его на центрифуге и заново растворяя, мы получим коллоидный раствор уже с меньшей дисперсией по размерам. Проделав этот цикл несколько раз получают коллоидный раствор с еще более моноразмерными наночастицами. В качестве пары растворитель-осадитель могут использоваться: бутанол/метанол, пиридин/гексан, хлороформ/метанол, толуол/метанол и др.
Таким способом получают, например, монодисперсные наночастицы CdSe с размером 4 нм и его разбросом, не превышающим нескольких процентов.
Слайд 24СРЕДНЕВЕКОВЫЙ ВИТРАЖ, СОДЕРЖАЩИЙ ЦВЕТНЫЕ СТЕКЛА, ОКРАШЕННЫЕ НАНОЧАСТИЦАМИ БЛАГОРОДНЫХ МЕТАЛЛОВ
Слайд 25Одним из способов синтеза наночастиц контролируемого размера является применение при синтезе
В качестве таких нанореакторов, как правило, используют мицеллы коллоидных растворов и капсулы, образованные ПАВ.
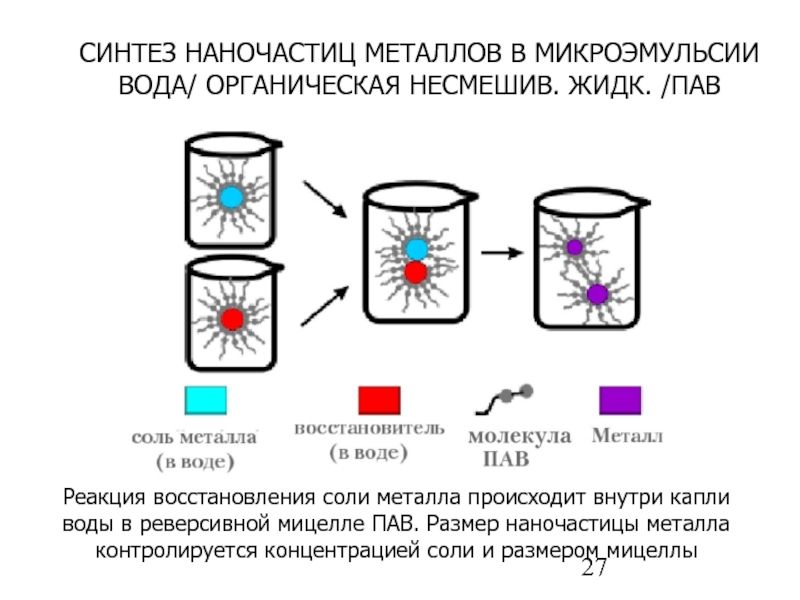
Методика синтеза наночастиц заключается в предварительном приготовлении растворов одного или двух реагирующих веществ, закапсулированных в данные мицеллы, и последующем смешивании данных растворов. При этом, образование вещества наночастицы происходит не в объеме раствора, а внутри каждой мицеллы.
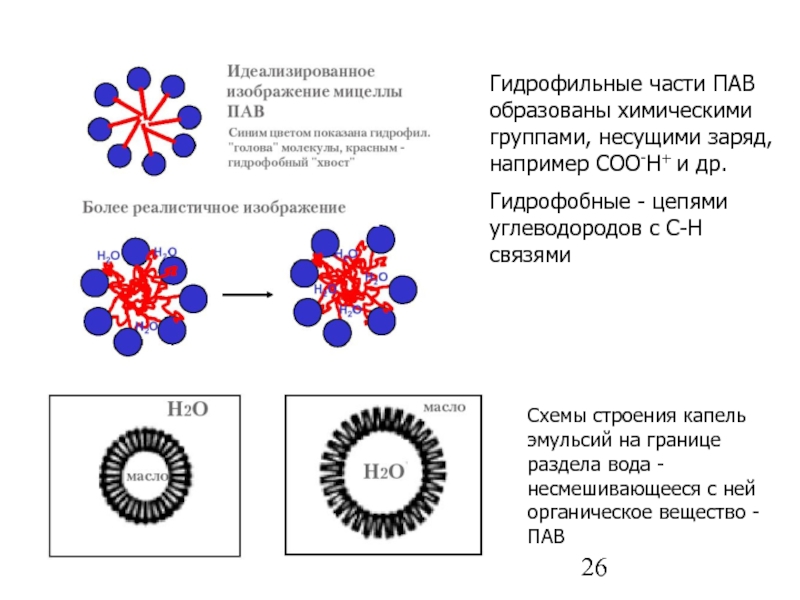
Слайд 26Гидрофильные части ПАВ образованы химическими группами, несущими заряд, например COO-H+ и
Гидрофобные - цепями углеводородов c C-H связями
Схемы строения капель эмульсий на границе раздела вода - несмешивающееся с ней органическое вещество - ПАВ
Слайд 27СИНТЕЗ НАНОЧАСТИЦ МЕТАЛЛОВ В МИКРОЭМУЛЬСИИ ВОДА/ ОРГАНИЧЕСКАЯ НЕСМЕШИВ. ЖИДК. /ПАВ
Реакция восстановления
Слайд 30Фрагмент липосомы (визикулы), сформированной из двойного слоя фосфолипидов
ПРИМЕРЫ ПРОСТРАНСТВЕННОГО СТРОЕНИЯ МОЛЕКУЛ
Слайд 31Капсулирование широко используется в фармацевтической и косметической областях для контроля за
Активными компонентами являются:
- лекарства,
- гормоны,
- витамины,
- масла,
- энзимы и др.
Слайд 32ЛИПОСОМЫ РАЗЛИЧАЮТСЯ
1. ПО КОЛИЧЕСТВУ СЛОЕВ В ОБОЛОЧКЕ
2. ПО РАЗМЕРУ -
- БОЛЬШИЕ (100 -500 нм),
- ГИГАНТСКИЕ (ДО 5 мкм В ДИАМЕТРЕ)
Слайд 36
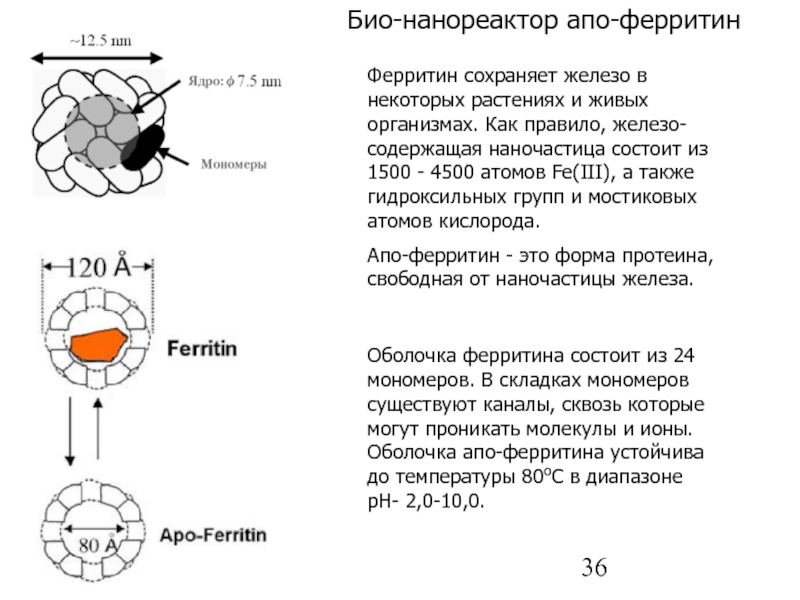
Ферритин сохраняет железо в некоторых растениях и живых организмах. Как правило,
Апо-ферритин - это форма протеина, свободная от наночастицы железа.
Био-нанореактор апо-ферритин
Оболочка ферритина состоит из 24 мономеров. В складках мономеров существуют каналы, сквозь которые могут проникать молекулы и ионы. Оболочка апо-ферритина устойчива до температуры 80оС в диапазоне рН- 2,0-10,0.
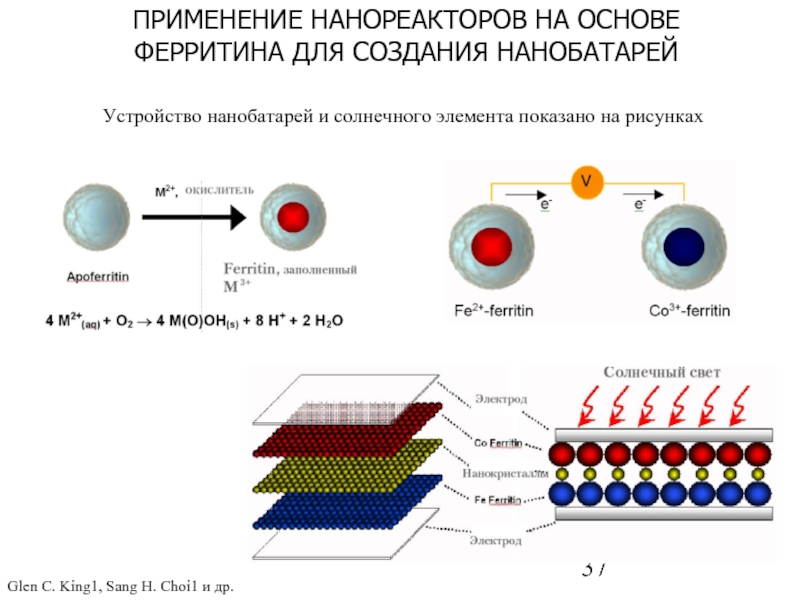
Слайд 37Glen C. King1, Sang H. Choi1 и др.
ПРИМЕНЕНИЕ НАНОРЕАКТОРОВ НА
Устройство нанобатарей и солнечного элемента показано на рисунках
Слайд 38СХЕМА ОБРАЗОВАНИЯ “СКЕЛЕТА” ИЗ КРЕМНЕЗЕМА НА НАРУЖНОЙ ПОВЕРХНОСТИ ВИЗИКУЛ В СТРУКТУРЕ
Слайд 39ДЕНДРИМЕРЫ КАК НАНОРЕАКТОРЫ ДЛЯ СИНТЕЗА НАНОЧАСТИЦ БЛАГОРОДНЫХ МЕТАЛЛОВ
Адсорбция и капсулирование катионов
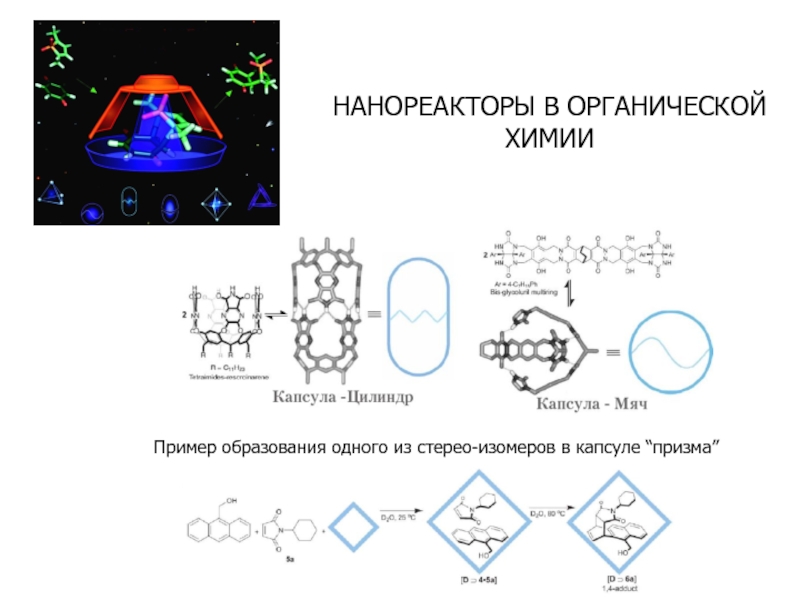
Слайд 40НАНОРЕАКТОРЫ В ОРГАНИЧЕСКОЙ ХИМИИ
Пример образования одного из стерео-изомеров в капсуле “призма”
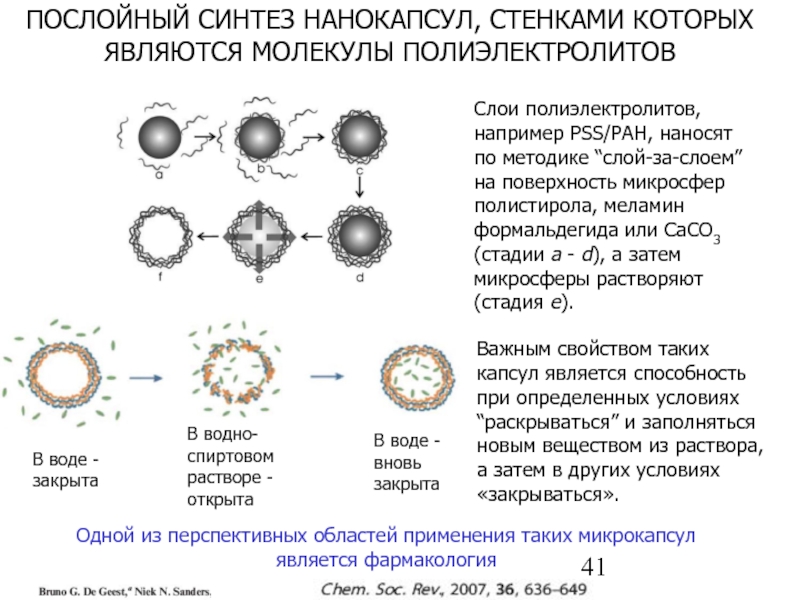
Слайд 41ПОСЛОЙНЫЙ СИНТЕЗ НАНОКАПСУЛ, СТЕНКАМИ КОТОРЫХ ЯВЛЯЮТСЯ МОЛЕКУЛЫ ПОЛИЭЛЕКТРОЛИТОВ
Слои полиэлектролитов,
Важным свойством таких капсул является способность при определенных условиях “раскрываться” и заполняться новым веществом из раствора, а затем в других условиях «закрываться».
В воде - закрыта
В водно-спиртовом растворе - открыта
В воде - вновь закрыта
Одной из перспективных областей применения таких микрокапсул является фармакология
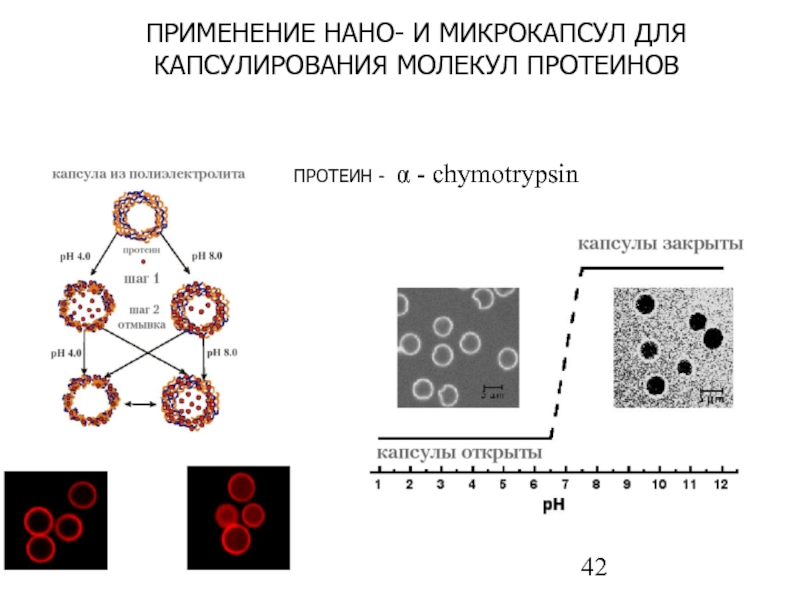
Слайд 42ПРИМЕНЕНИЕ НАНО- И МИКРОКАПСУЛ ДЛЯ КАПСУЛИРОВАНИЯ МОЛЕКУЛ ПРОТЕИНОВ
ПРОТЕИН - α -
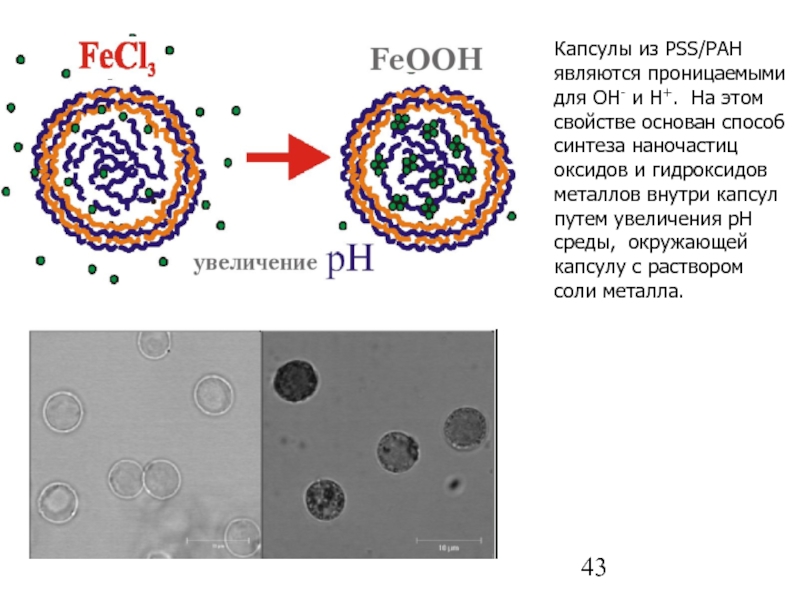
Слайд 43Капсулы из PSS/PAH являются проницаемыми для OH- и H+. На этом
Слайд 44ПОСЛОЙНЫЙ СИНТЕЗ БИО-НАНОРЕАКТОРОВ, СТЕНКАМИ КОТОРЫХ ЯВЛЯЮТСЯ МОЛЕКУЛЫ ПОЛИЭЛЕКТРОЛИТОВ, ЭНЗИМЫ И НЕОРГАНИЧЕСКИЕ
Пример био-нанореактора, состоящего из мультислоя PSS/PEI, энзимов и наночастиц оксида железа



![Образование наночастицРадиус наночастиц рассчитывается по формуле:ΔG = 4πσ(r2 – [2r3 / 3r*])Где r = радиус](/img/tmb/2/121335/b49c3c806c154c5971c216ca433a6a9e-800x.jpg)