- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Распределение молекул по скоростям презентация
Содержание
- 1. Распределение молекул по скоростям
- 2. Распределение молекул по скоростям Закон Максвелла описывается
- 3. Относительное число молекул скорости которых лежат
- 4. Т.к. Найдем значение наиболее вероятной скорости
- 5. При повышении температуры площадь, ограниченная кривой, остаётся
- 6. Cреднее значение скорости Каждому интервалу
- 7. Средняя арифметическая скорость Средняя квадратичная скорость Наиболее вероятная скорость Скорости, характеризующие состояние газа:
- 8. 2. Экспериментальная проверка распределения Максвелла Немецкий физик
- 9. Молекулярный пучок ловушка Опыт Ламмерта (1929 г.)
- 10. 3. Барометрическая формула - давление на высоте
- 11. 4. Распределение Больцмана Заменив в барометрической формуле
- 12. 5. Опыты Перрена Перрен (1909 г.) –
- 13. 6. Средняя длина свободного пробега Между двумя
- 14. Явления переноса в термодинамически неравновесных системах
- 16. Согласно кинетической теории газов: - средняя длина
- 17. 2. Теплопроводность. Перенос энергии в форме
- 18. 3. Внутреннее трение (вязкость). Механизм возникновения внутреннего
- 19. Физические основы термодинамики Первое начало термодинамики. Работа
- 20. 1. Первое начало термодинамики Внутренняя энергия может
- 21. 2. Работа газа при изменении его объема
- 22. 3. Число степеней свободы молекулы Средняя энергия
- 23. y x z а) i=3 б) i=5
- 24. 4.Теплоемкость идеального газа Теплоемкостью тела называется величина,
- 25. Уравнение Майера молярная теплоемкость при постоянном давлении
- 26. 5. Адиабатический процесс Адиабатическим называется процесс, протекающий
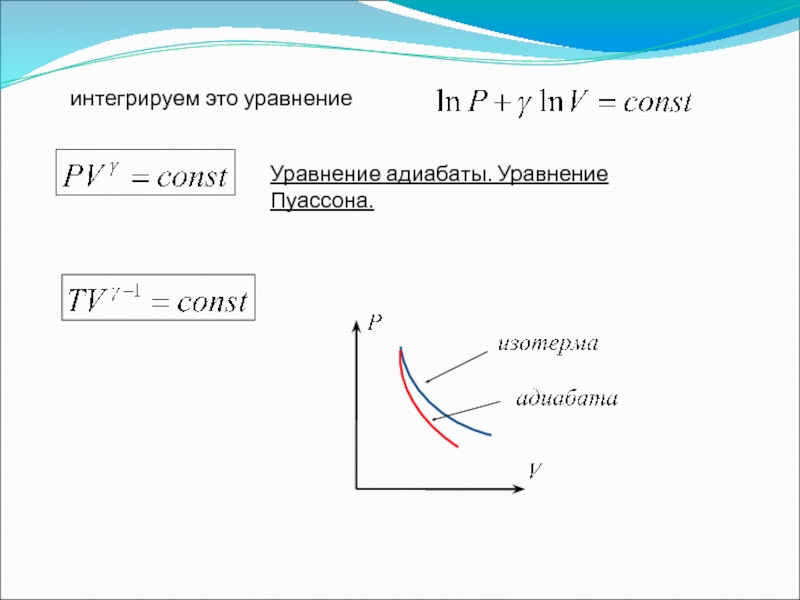
- 27. интегрируем это уравнение Уравнение адиабаты. Уравнение Пуассона.
- 28. Политропическим называется такой процесс, при котором давление
- 29. 6. Работа, совершаемая идеальным газом при различных
- 30. Для изотермического процесса: n=1 Для адиабатического процесса:
- 31. Реальные газы Отклонение газов от идеальности Уравнение Ван-дер-Ваальса Экспериментальные изотермы
- 32. 1. Отклонение газов от идеальности Поведение идеальных
- 33. Критерием различных агрегатных состояний вещества является соотношение
- 34. 2. Уравнение Ван-дер-Ваальса – уравнение состояния реального
- 35. 3. Экспериментальные изотермы Мано-метр Газ (или пар),
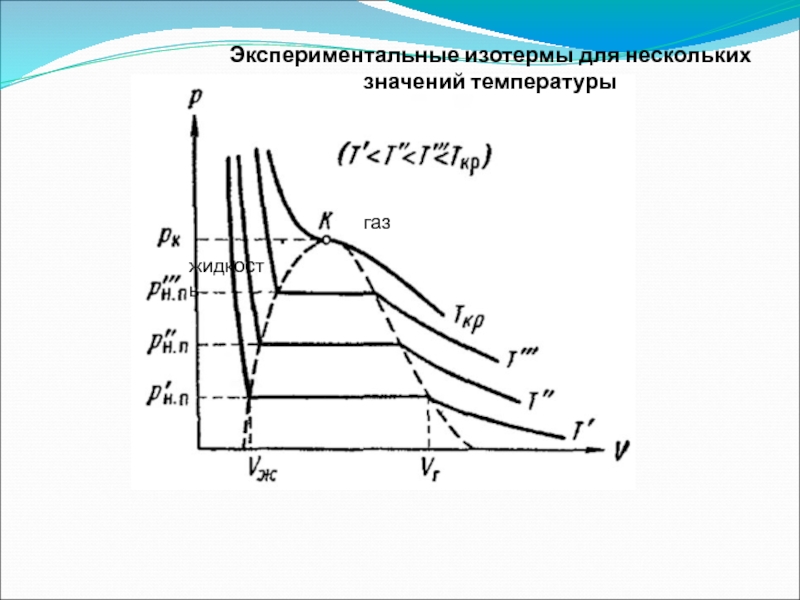
- 36. Экспериментальные изотермы для нескольких значений температуры газ жидкость
- 37. Внутренняя энергия реального газа Эффект Джоуля-Томсона Ожижение газов
- 38. 1. Внутренняя энергия реального газа Внутренняя энергия
- 39. 2. Эффект Джоуля-Томсона Пропуская газ по теплоизолированной
- 40. При адиабатическом расширении газа: U+pV
- 41. Расчет для моля газа Из уравнения Ван
- 42. Преобразуем третье слагаемое: подставим Преобразуем: Знак ΔТ определяется знаком выражения в скобках
- 43. ΔТ=0 при При При
- 44. Обратимые и необратимые процессы. Коэффициент полезного действия
- 45. 1. Обратимые и необратимые процессы. Коэффициент полезного
- 46. 1) При расширении газ получает тепло 2)
- 47. 2. Второе начало термодинамики Невозможны такие процессы,
- 48. 3. Цикл Карно и его КПД для
- 49. - тепло получаемое за цикл от нагревателя
- 50. Неравенство Клаузиуса. Энтропия. Свойства энтропии. Теорема Нернста.
- 51. КПД необратимой тепловой машины всегда меньше, чем
- 52. 2. Энтропия. Сумма приведенных количеств тепла, полученных
- 53. Приращение энтропии равно элементарному количеству тепла, получаемому
- 54. 3. Свойства энтропии. Теорема Нернста. Рассмотрим цикл,
- 55. Т.о., энтропия изолированной системы может только возрастать
- 56. Теорема Нернста: при стремлении абсолютной температуры к
- 57. Электростатика Электрический заряд и его свойства Закон
- 58. 1. Электрический заряд и его свойства Существование
- 59. 2. Закон Кулона Закон Кулона: Сила взаимодействия
- 60. - закон Кулона в вакууме
- 61. 3. Электрическое поле. Напряженность поля. Поток вектора
- 62. Линии напряженности проводим так, что касательная к
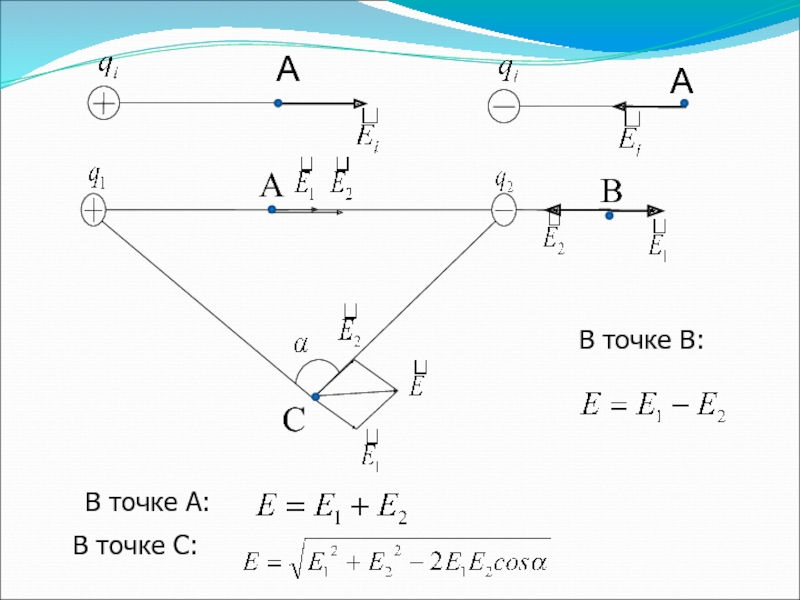
- 63. В точке А: В точке В: В точке С:
- 64. Поток вектора напряженности численно равен количеству линий
- 65. 4. Теорема Гаусса и ее применение к
- 66. Пример: Определить поток вектора напряженности
- 67. Теорема Гаусса для электростатического поля в вакууме:
- 68. Применение теоремы Гаусса к расчету некоторых электростатических
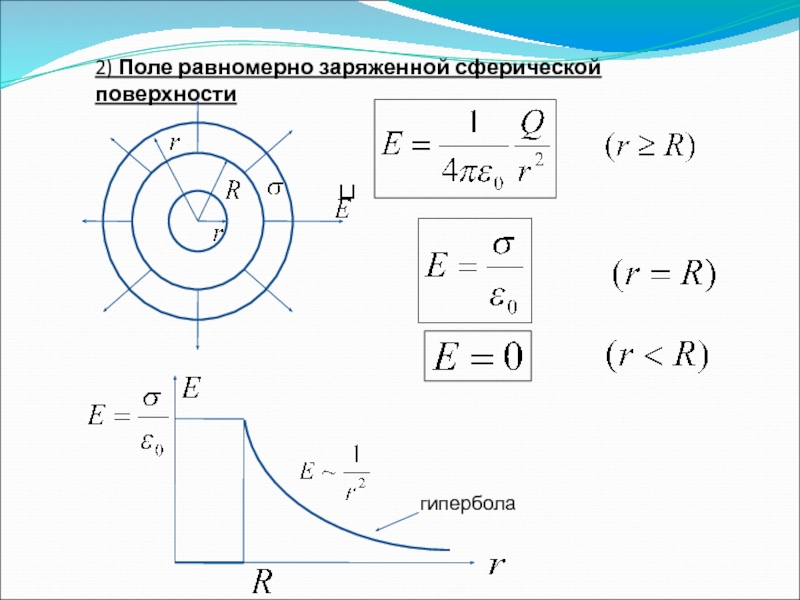
- 69. 2) Поле равномерно заряженной сферической поверхности гипербола
- 70. 3) Поле объемно заряженного шара Напряженность
- 71. - линейная плотность зарядов 4) Поле равномерно заряженного бесконечного цилиндра
- 72. Потенциал электростатического поля Работа сил электростатического
- 73. 1. Работа сил электростатического поля Вычислим работу,
- 74. Работа потенциальных сил на замкнутом пути равна
- 75. Потенциал – энергетическая характеристика поля Работа, совершаемая
- 76. 3.Связь между напряженностью электростатического поля и потенциалом
- 77. Для графического изображения распределения потенциала пользуются эквипотенциальными
- 78. 2) Поле равномерно заряженной сферической поверхности радиуса
Слайд 1Распределение молекул по скоростям
Экспериментальная проверка распределения Максвелла
Барометрическая формула
Распределение Больцмана
Опыты Перрена
Средняя длина
Слайд 2Распределение молекул по скоростям
Закон Максвелла описывается некоторой функцией f(υ), называемой функцией
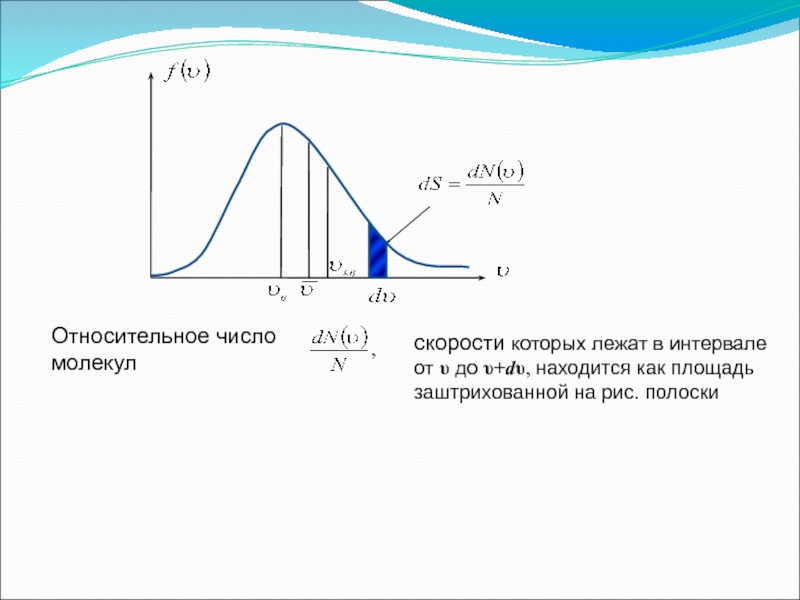
Функция f(υ) определяет относительное число молекул
скорости которых лежат в интервале от υ до υ+dυ, т.е.
где m0 – масса молекулы, k – постоянная Больцмана
-Закон распределения молекул идеального газа по скоростям (распределение Максвелла)
(1)
Слайд 3Относительное число молекул
скорости которых лежат в интервале от υ до
Слайд 4Т.к.
Найдем значение наиболее вероятной скорости υв , продифференцировав выражение (1) по
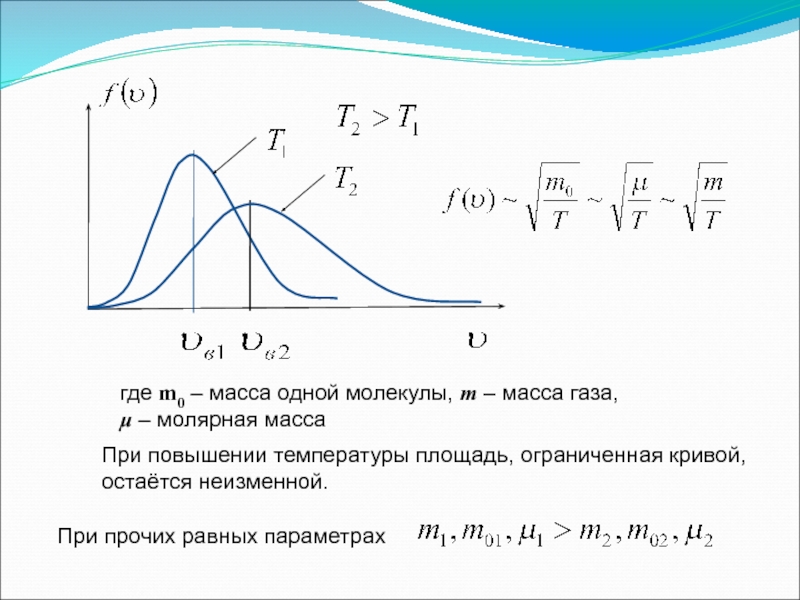
Слайд 5При повышении температуры площадь, ограниченная кривой, остаётся неизменной.
При прочих равных параметрах
где
μ – молярная масса
Слайд 6Cреднее значение скорости
Каждому интервалу соответствует
- сумма значений скоростей всех N молекул.
Средняя арифметическая скорость
Слайд 7Средняя арифметическая скорость
Средняя квадратичная скорость
Наиболее вероятная скорость
Скорости, характеризующие состояние газа:
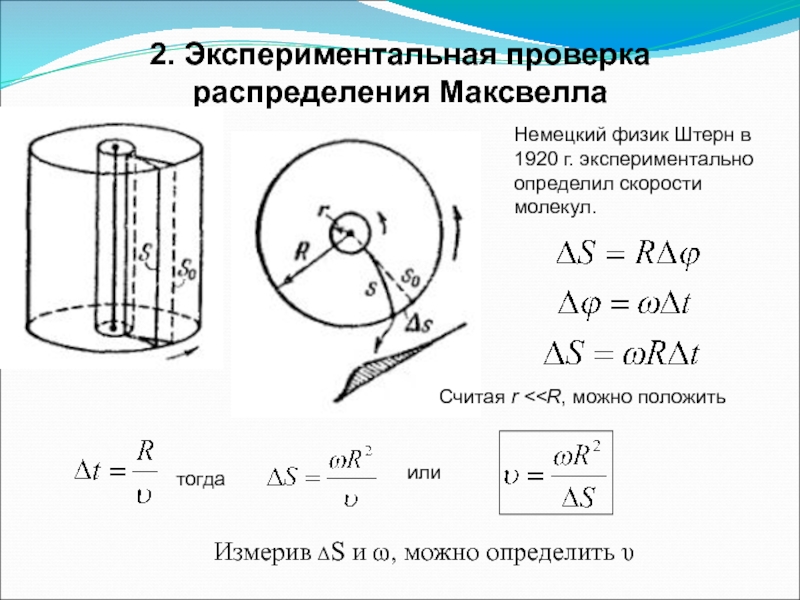
Слайд 82. Экспериментальная проверка распределения Максвелла
Немецкий физик Штерн в 1920 г. экспериментально
Считая r < тогда или Измерив ΔS и ω, можно определить υ
Слайд 9Молекулярный пучок
ловушка
Опыт Ламмерта (1929 г.)
t1 – время за которое молекулы пролетают
t1 должно совпадать со временем t2, за которое диски повернутся на угол φ
Слайд 103. Барометрическая формула
- давление на высоте h
- барометрическая формула
Предположения: 1) поле
2) температура постоянна;
3) масса всех молекул одинакова.
Слайд 114. Распределение Больцмана
Заменив в барометрической формуле
получим закон изменения числа молекул
Распределение Больцмана
Две тенденции распределения молекул по высоте: 1) притяжение молекул к Земле (чем больше m и меньше T); 2) тепловое движение стремится разбросать молекулы по высоте.
Слайд 125. Опыты Перрена
Перрен (1909 г.) – опыты по определению числа Авогадро.
Рассмотрим
Δh – толщина слоя.
Число частиц, попадающих в поле зрения микроскопа:
Распределение молекул по высоте
- вес броуновской частицы
Слайд 136. Средняя длина свободного пробега
Между двумя последовательными столкновениями молекулы проходят некоторый
Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называется эффективным диаметром молекул d.
- средняя скорость
- среднее число соударений за 1 с
Эффективное сечение молекул
Слайд 14Явления переноса в термодинамически неравновесных системах
Диффузия
Теплопроводность
Вязкость
К явлениям переноса относятся теплопроводность (обусловлена
Слайд 15
С макроскопической точки зрения перенос массы вещества подчиняется закону Фика: масса вещества ΔM, переносимая за время Δt через площадку ΔS, прямо пропорциональна градиенту плотности Δρ/Δx
D — коэффициент диффузии.
Знак минус показывает, что перенос массы происходит в направлении убывания плотности .
[D]=м2/с
1. Диффузия. Явление диффузии заключается в том, что происходит самопроизвольное проникновение и перемешивание частиц двух соприкасающихся газов, жидкостей и даже твердых тел; диффузия продолжается, пока существует градиент плотности.
Слайд 16Согласно кинетической теории газов:
- средняя длина свободного пробега
средняя скорость движения молекул,
d
n0 – концентрация молекул.
Слайд 172. Теплопроводность.
Перенос энергии в форме теплоты подчиняется закону Фурье:
Количество теплоты
χ — коэффициент теплопроводности
Знак минус показывает, что при теплопроводности энергия переносится в направлении убывания температуры
[q]= Дж/с
ρ - плотность газа, сV – удельная теплоемкость газа при постоянном объеме
Слайд 183. Внутреннее трение (вязкость). Механизм возникновения внутреннего трения между параллельными слоями
Сила внутреннего трения между двумя слоями газа (жидкости) подчиняется закону Ньютона:
где η — коэффициент вязкости, du/dz — градиент скорости, показывающий быстроту изменения скорости в направлении z, перпендикулярном направлению движения слоев, S — площадь, на которую действует сила f.
Коэффициент вязкости вычисляется по формуле:
Слайд 19Физические основы термодинамики
Первое начало термодинамики.
Работа газа при изменении его объема.
Число степеней
Теплоемкость идеального газа.
Адиабатический и политропический процессы.
Работа, совершаемая идеальным газом при различных процессах.
Слайд 201. Первое начало термодинамики
Внутренняя энергия может изменяться за счет двух различных
Совершения над телом работы А’
Сообщения телу количества теплоты Q путем теплопередачи
Изменение внутренней энергии
Первое начало термодинамики
Теплота, передаваемая системе, расходуется на увеличение ее внутренней энергии и на совершение системой работы против внешних сил.
Слайд 212. Работа газа при изменении его объема
Элементарная работа, совершаемая газом при
Элементарная работа
Полная работа А, совершаемая газом при изменении его объема от V1 до V2 находится путем интегрирования
Слайд 223. Число степеней свободы молекулы
Средняя энергия поступательного движения молекулы:
Числом степеней свободы
Средняя кинетическая энергия молекулы:
Внутренняя энергия 1 моля идеального газа:
Внутренняя энергия произвольной массы газа:
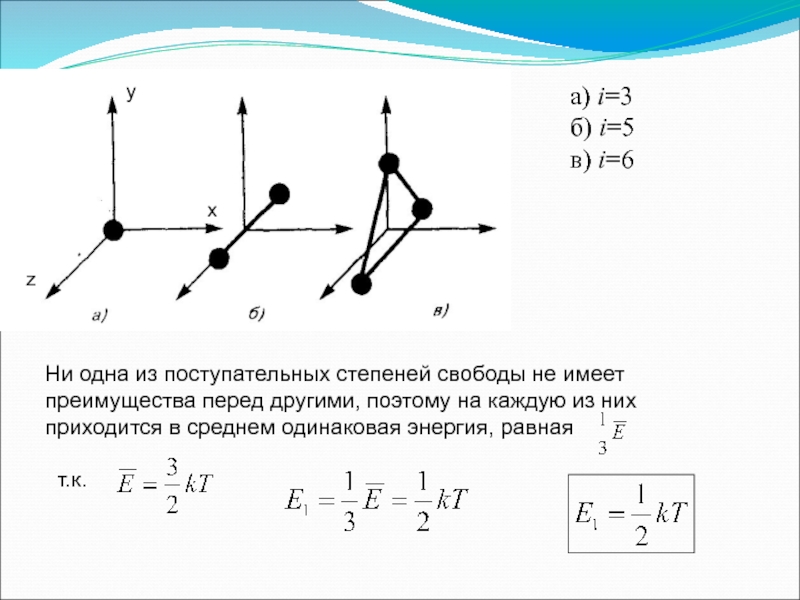
Слайд 23y
x
z
а) i=3
б) i=5
в) i=6
Ни одна из поступательных степеней свободы не имеет
т.к.
Слайд 244.Теплоемкость идеального газа
Теплоемкостью тела называется величина, равная количеству тепла, которое нужно
Удельной теплоемкостью вещества называется величина, равная количеству теплоты, необходимому для нагревания
1 кг вещества на 1 градус.
молярная теплоемкость вещества (теплоемкость одного моля)
молярная теплоемкость при постоянном объеме
Слайд 25Уравнение Майера
молярная теплоемкость при постоянном давлении
показатель адиабаты
При нагревании газа при постоянном
Слайд 265. Адиабатический процесс
Адиабатическим называется процесс, протекающий без теплообмена с внешней средой.
(1)
Подставляем
Слайд 28Политропическим называется такой процесс, при котором давление и объем идеального газа
Изобарический процесс
Изотермический процесс
Адиабатический процесс
Изохорический процесс
Слайд 296. Работа, совершаемая идеальным газом при различных процессах
Рассмотрим случай
Работа, совершаемая
Слайд 30Для изотермического процесса: n=1
Для адиабатического процесса:
Работа, совершаемая газом при изотермическом процессе
При
При изохорическом процессе:
Слайд 31Реальные газы
Отклонение газов от идеальности
Уравнение Ван-дер-Ваальса
Экспериментальные изотермы
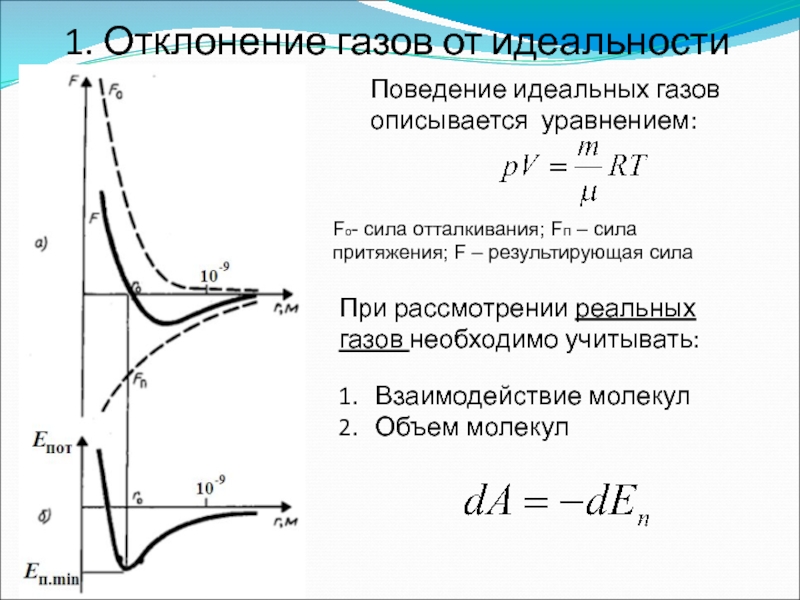
Слайд 321. Отклонение газов от идеальности
Поведение идеальных газов описывается уравнением:
При рассмотрении реальных
Взаимодействие молекул
Объем молекул
Fо- сила отталкивания; Fп – сила притяжения; F – результирующая сила
Слайд 33Критерием различных агрегатных состояний вещества является соотношение величин En.min и kT
En.min
kT – определяет порядок средней кинетической энергии хаотического теплового движения молекул.
Если En.min << kT , то вещество находится в газообразном состоянии
Если En.min >> kT , то вещество находится в твердом состоянии
Если En.min ≈ kT , то вещество находится в жидком состоянии
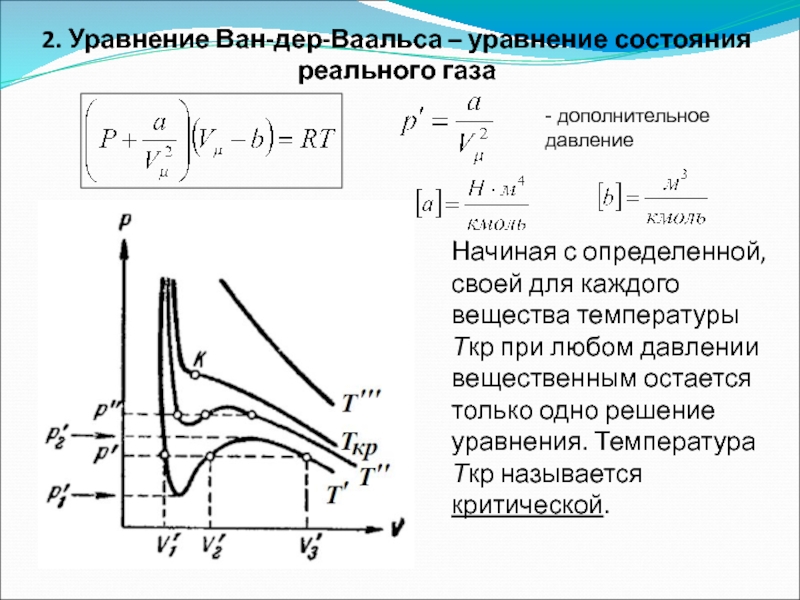
Слайд 342. Уравнение Ван-дер-Ваальса – уравнение состояния реального газа
Начиная с определенной, своей
- дополнительное давление
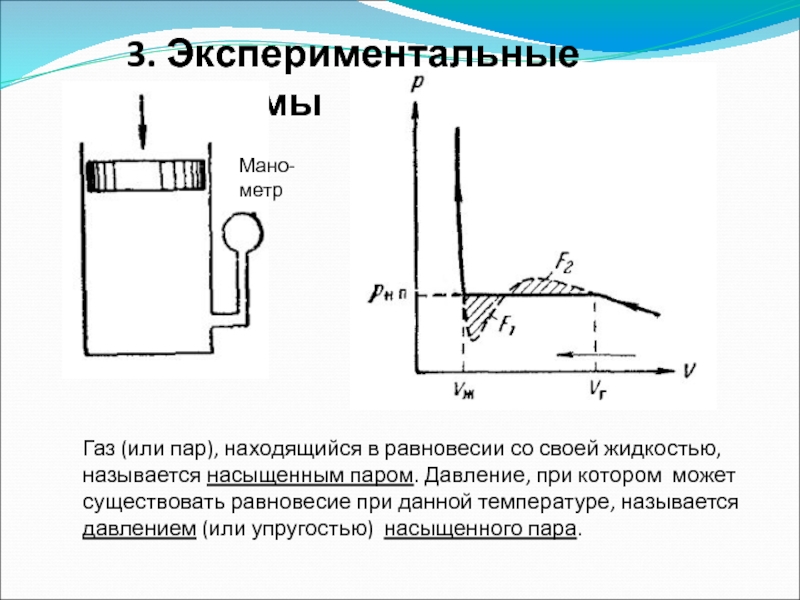
Слайд 353. Экспериментальные изотермы
Мано-метр
Газ (или пар), находящийся в равновесии со своей жидкостью,
Слайд 381. Внутренняя энергия реального газа
Внутренняя энергия реального газа
- кинетическая энергия
- взаимная потенциальная энергия молекул
Кинетическая энергия молекул, содержащихся в моле газа равна:
Интегрируем:
- Внутренняя энергия реального газа
Работа против внутренних сил идет на увеличение потенциальной энергии системы
- внутреннее давление
Слайд 392. Эффект Джоуля-Томсона
Пропуская газ по теплоизолированной трубке с пористой перегородкой, Джоуль
Слайд 40При адиабатическом расширении газа:
U+pV - энтальпия – величина, которая
Работа совершаемая над порцией газа :
(*)
Слайд 41Расчет для моля газа
Из уравнения Ван дер Ваальса для газа до
Внутренняя энергия до расширения:
Подставив в (*) , получим:
После расширения газ можно считать идеальным.
Слайд 42Преобразуем третье слагаемое:
подставим
Преобразуем:
Знак ΔТ определяется знаком выражения в скобках
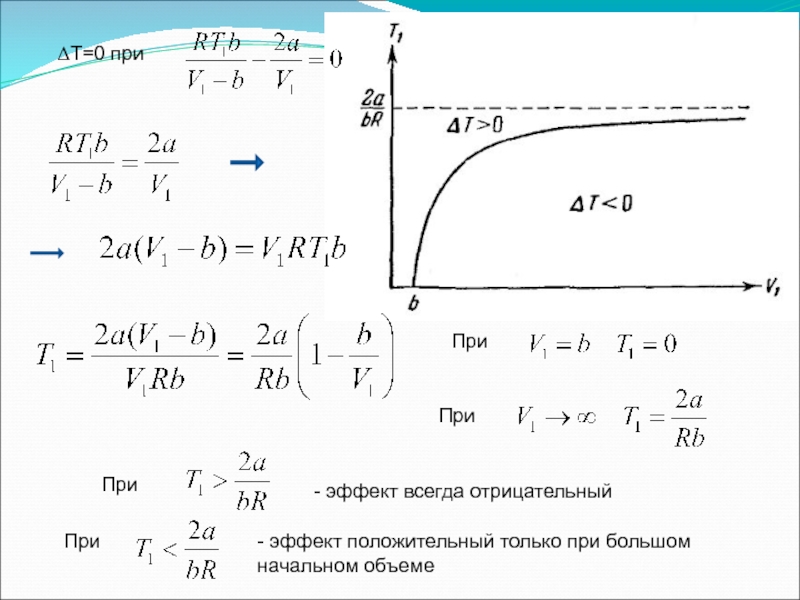
Слайд 43ΔТ=0 при
При
При
При
- эффект всегда отрицательный
При
- эффект положительный
Слайд 44Обратимые и необратимые процессы. Коэффициент полезного действия тепловой машины.
Второе начало термодинамики.
Цикл
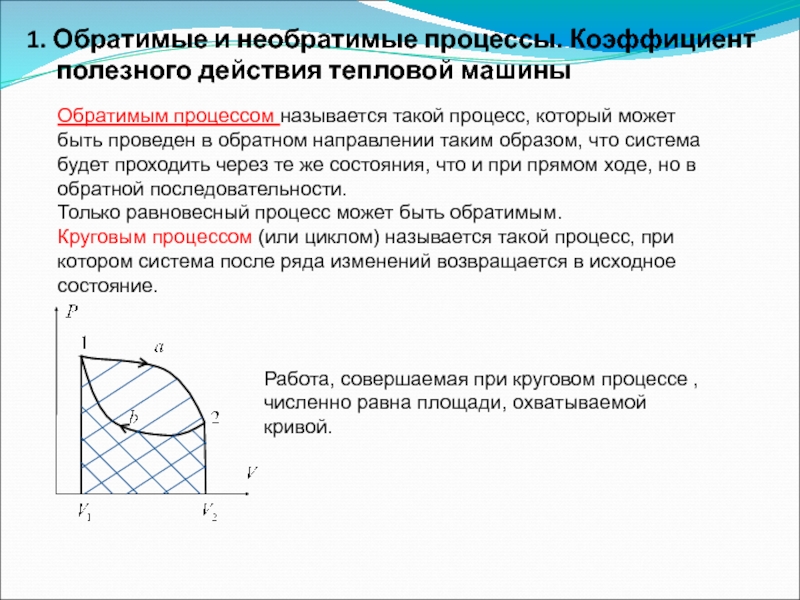
Слайд 451. Обратимые и необратимые процессы. Коэффициент полезного действия тепловой машины
Обратимым процессом
Только равновесный процесс может быть обратимым.
Круговым процессом (или циклом) называется такой процесс, при котором система после ряда изменений возвращается в исходное состояние.
Работа, совершаемая при круговом процессе , численно равна площади, охватываемой кривой.
Слайд 461) При расширении газ получает тепло
2) При сжатии от него отнимается
Складываем эти уравнения:
- полная работа, совершаемая за цикл
Тепловой машиной называется периодически действующий двигатель, совершающий работу за счет получаемого извне тепла.
I начало термодинамики: невозможен вечный двигатель первого рода, т.е. периодически действующий двигатель, совершающий работу в большем количестве, чем получаемая им извне энергия.
КПД определяется как отношение совершаемой за цикл работы к получаемому за цикл теплу
Слайд 472. Второе начало термодинамики
Невозможны такие процессы, единственным конечным результатом которых был
Невозможны такие процессы, единственным конечным результатом которых явилось бы отнятие от некоторого тела определенного количества теплоты и превращение его полностью в работу.
Невозможен вечный двигатель второго рода, т.е. такой периодически действующий двигатель, который получал бы тепло от одного резервуара и превращал бы его полностью в работу.
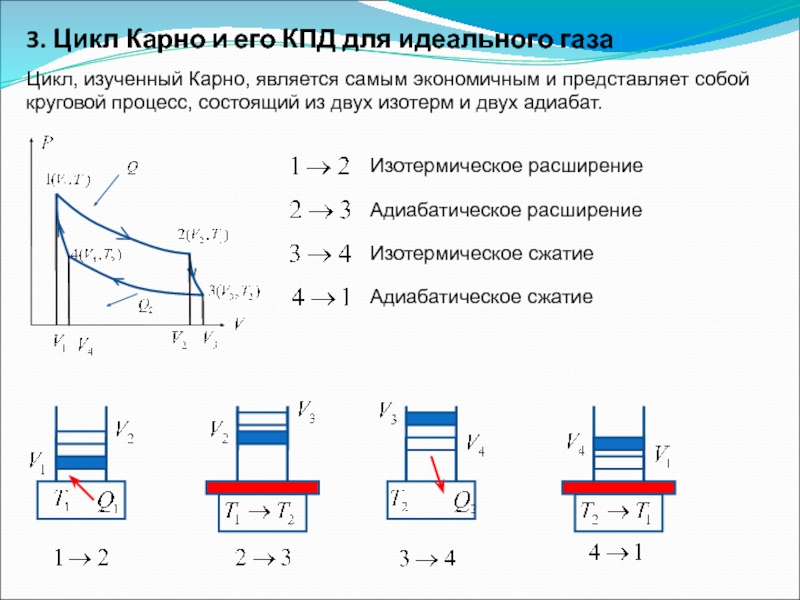
Слайд 483. Цикл Карно и его КПД для идеального газа
Цикл, изученный Карно,
Изотермическое расширение
Адиабатическое расширение
Изотермическое сжатие
Адиабатическое сжатие
Слайд 49- тепло получаемое за цикл от нагревателя
- тепло отдаваемое за цикл
КПД цикла Карно зависит только от температуры нагревателя и холодильника. Это выражение дает КПД любой обратимой машины.
Слайд 51КПД необратимой тепловой машины всегда меньше, чем КПД обратимой.
- Неравенство Клаузиуса
Отношение
1. Неравенство Клаузиуса
Если система совершает цикл, в ходе которого вступает в теплообмен с двумя тепловыми резервуарами, температуры которых постоянны, то сумма приведенных количеств тепла равна 0, если цикл обратим, и меньше 0, если цикл необратим.
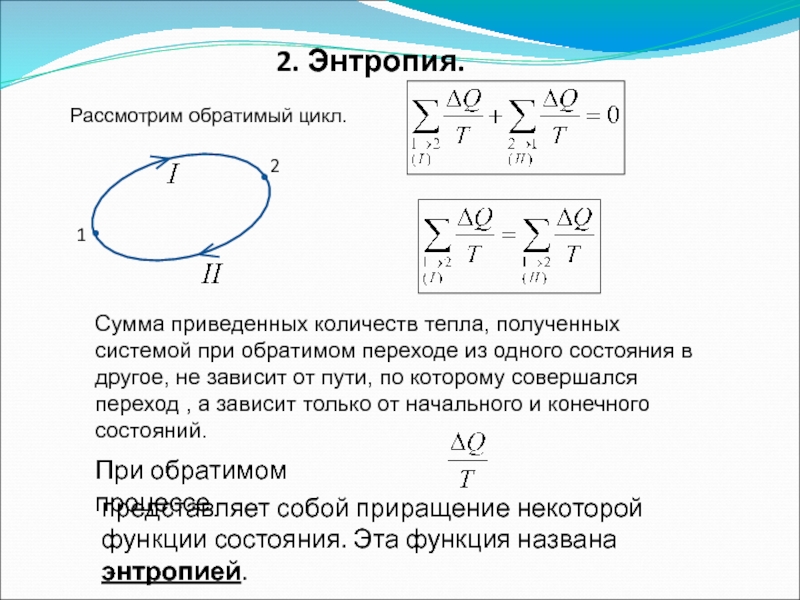
Слайд 522. Энтропия.
Сумма приведенных количеств тепла, полученных системой при обратимом переходе из
При обратимом процессе
представляет собой приращение некоторой функции состояния. Эта функция названа энтропией.
Рассмотрим обратимый цикл.
Слайд 53Приращение энтропии равно элементарному количеству тепла, получаемому обратимо системой извне, отнесенному
Сумма приращений энтропии должна быть равна разности значений в конечном и начальном состояниях
Энтропия – аддитивная величина.
Слайд 543. Свойства энтропии. Теорема Нернста.
Рассмотрим цикл, состоящий из обратимой и необратимой
Если система изолирована, т.е. не обменивается теплом с внешней средой:
Ранее получили
Объединяя эти выражения, получим
Для элементарного процесса:
Слайд 55Т.о., энтропия изолированной системы может только возрастать (если в системе протекает
Убывать энтропия изолированной системы не может.
Обратимый адиабатический процесс протекает при постоянной энтропии.
Если система отдает тепло внешним телам, энтропия системы уменьшается.
Найдем изменение энтропии при обратимом изотермическом процессе
Вынося постоянную температуру Т за знак суммы, получим:
где Q12 – количество теплоты, полученное системой при обратимом изотермическом переходе из состояния 1 в состояние 2.
Слайд 56Теорема Нернста: при стремлении абсолютной температуры к нулю, энтропия любого тела
Энтропия любого тела с температурой Т может быть представлена в виде:
Формула Больцмана для энтропии:
Энтропия определяется логарифмом числа микросостояний, с помощью которых может быть реализовано данное макросостояние.
Для изолированной системы:
Энтропия не может убывать.
Предоставленная самой себе система переходит из менее вероятных состояний в более вероятные.
Слайд 57Электростатика
Электрический заряд и его свойства
Закон Кулона
Электрическое поле. Напряженность поля. Поток вектора
Теорема Гаусса и ее применение к вычислению напряженности поля
Слайд 581. Электрический заряд и его свойства
Существование электрического заряда в двух видах
Квантование
3) Закон сохранения заряда
Единица электрического заряда – Кулон (Кл) – электрический заряд, проходящий через поперечное сечение проводника при токе силой 1А за время 1с.
Проводники Диэлектрики Полупроводники
Слайд 592. Закон Кулона
Закон Кулона: Сила взаимодействия двух неподвижных точечных зарядов, находящихся
k – коэффициент пропорциональности
- величины зарядов
- расстояние между зарядами
F –кулоновская сила
В системе СИ:
- электрическая постоянная
Слайд 613. Электрическое поле. Напряженность поля. Поток вектора напряженности
Всякий заряд изменяет свойства
Напряженностью электрического поля называется векторная величина, численно равная отношению силы, действующей на положительный точечный заряд, находящейся в данной точке поля к величине этого заряда.
Напряженность поля, создаваемого точечным зарядом:
Слайд 62Линии напряженности проводим так, что касательная к ним в каждой точке
Слайд 64Поток вектора напряженности численно равен количеству линий напряженности, пронизывающих поверхность S
Количество
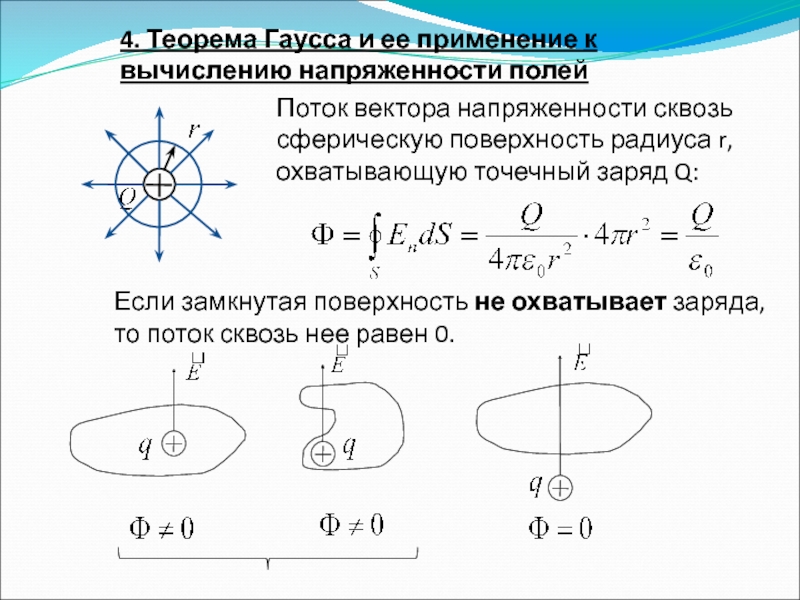
Слайд 654. Теорема Гаусса и ее применение к вычислению напряженности полей
Поток вектора
Если замкнутая поверхность не охватывает заряда, то поток сквозь нее равен 0.
Слайд 66Пример: Определить поток
вектора напряженности
электростатического поля через сферическую поверхность, охватывающую
.
Слайд 67Теорема Гаусса для электростатического поля в вакууме:
Поток вектора напряженности электрического поля
Поле образовано зарядами (q1, q2, … qn)
В соответствии с принципом суперпозиции электростатических полей:
Поэтому:
Если заряд распределен внутри замкнутой поверхности непрерывно с
объемной плотностью
, то теорема Гаусса :
Слайд 68Применение теоремы Гаусса к расчету некоторых электростатических полей в вакууме
1) Поле
заряд, приходящийся на единицу поверхности (поверхностная плотность зарядов)
По теореме Гаусса:
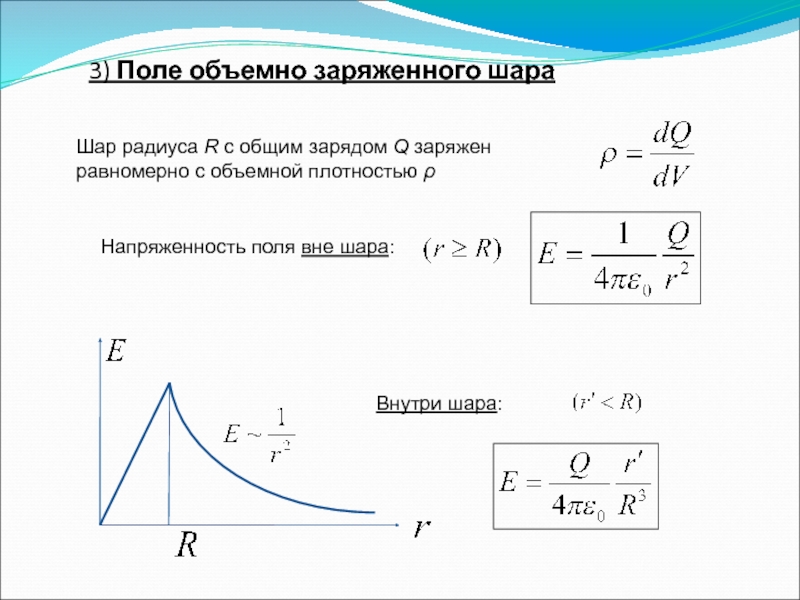
Слайд 703) Поле объемно заряженного шара
Напряженность поля вне шара:
Шар радиуса R
Внутри шара:
Слайд 72Потенциал электростатического поля
Работа сил электростатического поля
Потенциал электростатического поля
Напряженность как градиент потенциала.
Вычисление потенциала по напряженности поля
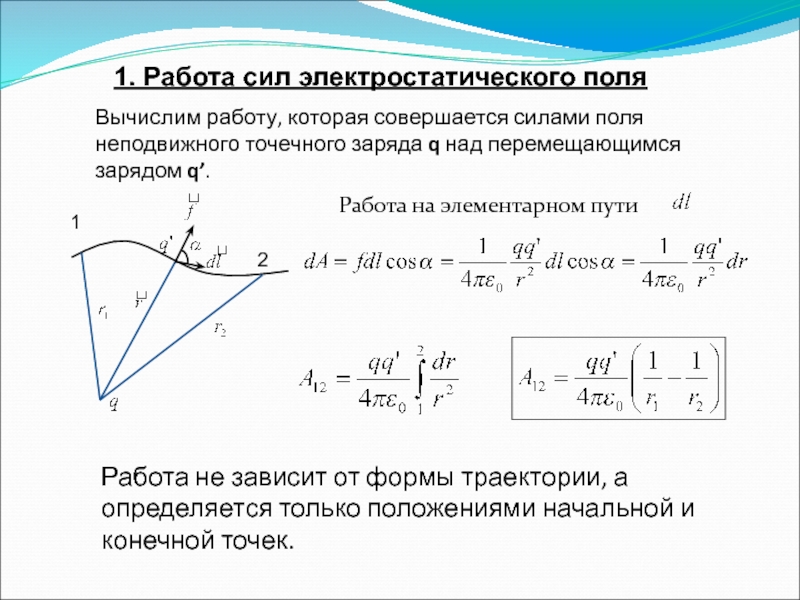
Слайд 731. Работа сил электростатического поля
Вычислим работу, которая совершается силами поля неподвижного
Работа на элементарном пути
Работа не зависит от формы траектории, а определяется только положениями начальной и конечной точек.
Слайд 74Работа потенциальных сил на замкнутом пути равна 0.
Циркуляция вектора напряженности электростатического
2. Потенциал электростатического поля
Работу сил электростатического поля можно представить как разность потенциальных энергий, которыми обладает точечный заряд q’ в начальной и конечной точках поля заряда q
Т.о., потенциальная энергия заряда q’ в поле заряда q:
Слайд 75Потенциал – энергетическая характеристика поля
Работа, совершаемая силами электростатического поля при перемещении
Если перемещать заряд q’ из произвольной точки в бесконечность, где потенциал равен 0, то:
Потенциал – физическая величина, определяемая работой по перемещению единичного положительного заряда при удалении его из данной точки в бесконечность.
Слайд 763.Связь между напряженностью электростатического поля и потенциалом
Работа сил поля над зарядом
- произвольно выбранное в пространстве направление
Напряженность поля равна градиенту потенциала со знаком минус. Знак минус определяется тем, что вектор напряженности направлен в сторону убывания потенциала.
Слайд 77Для графического изображения распределения потенциала пользуются эквипотенциальными поверхностями (геометрическое место точек
4. Вычисление потенциала по напряженности поля
1) Поле равномерно заряженной бесконечной плоскости:
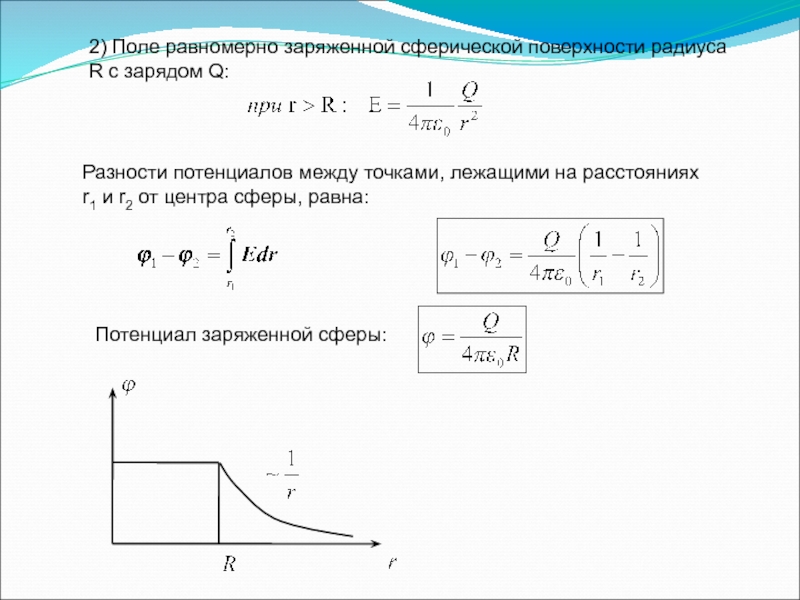
Слайд 782) Поле равномерно заряженной сферической поверхности радиуса R с зарядом Q:
Разности
Потенциал заряженной сферы: