- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Методы разделения белковых смесей. Хроматография презентация
Содержание
- 1. Методы разделения белковых смесей. Хроматография
- 2. План лекции Методы разделения белковых смесей Основные принципы хроматографии ВЭЖХ Инструментальное обеспечение
- 3. Методы разделения белковых смесей Высокоэффективная жидкостная
- 4. Высокоэффективная жидкостная хроматография
- 5. Хроматография Хроматография - динамический метод анализа, основанный
- 6. История
- 7. Виды хроматографии Критерии классификации способ ввода
- 8. По способу введения пробы Элюентная хроматография (проявительная)
- 9. ТФЭ (SPE) Устройства для автоматизации ТФЭ Колонки
- 10. ТФЭ Назначение ТФЭ: очистка пробы от нежелательных
- 11. По агрегатному состоянию фаз Газовая хроматография Газо-жидкостная
- 12. По механизму взаимодействия Распределительная хроматография Ионообменная хроматография
- 13. Распределительная хроматография хроматографический метод, при котором неподвижная
- 14. Ионобменная хроматография хроматографии позволяет разделять ионы и
- 15. Адсорбционная хроматография вид хроматографии, основанный на способности
- 16. Эксклюзионная хроматографии (гель-фильтрация) молекулы веществ разделяются по
- 17. Эксклюзионная хроматографии (гель-фильтрация) Объем образца лимитирующий для
- 18. Аффинная хроматография (от лат. affinis – родственный)
- 19. По назначению аналитическая (динамический диапазон)
- 20. ВЭЖХ Высокоэффективная жидкостная хроматография (ВЭЖХ) High performance liquid
- 21. ВЭЖХ Милихром
- 22. ВЭЖХ HP
- 23. ВЭЖХ Люмекс
- 24. ВЭЖХ Чешский прибор
- 25. ВЭЖХ Agilent Technologies Agilent 1290 Infinity
- 27. Основные узлы хроматографа Дегазатор подвижной фазы
- 28. Схема хроматографа (1) Резервуары для растворителей
- 29. Подвижная фаза Обращеннофазовая хроматография метанол
- 30. Насос Насос - обеспечивает стабильный поток подвижной
- 31. Инжектор Назначение – дозированный ввод образца в колонку Работа шестипортового инжектора Дозирующая петля
- 32. Колонка Геометрический объем колонки, Vc - внутреннее
- 33. Сертификат качества на колонку
- 34. Требования к сорбенту 1. колоночный материал должен
- 35. Сорбенты
- 36. Виды детекторов ультрафиолетовый (УФ, UV)
- 37. Детекторы
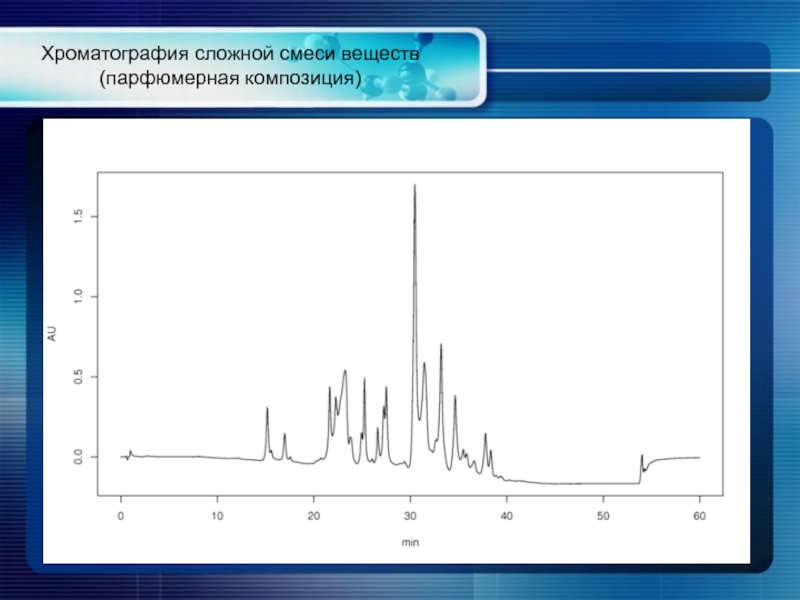
- 38. Хроматография сложной смеси веществ (парфюмерная композиция)
- 39. Параметры tM - время удерживания несорбируемого соединения;
- 40. Параметры Площадь пика, S - площадь хроматограммы,
- 41. Объем Объем удерживания вещества, VR -
- 42. Время Абсолютное время удерживания вещества, tR -
- 43. Эффективность Эффективность хроматографической системы - количество ступеней
- 44. Параметры эффективности Приведенное число теоретических тарелок N’
- 45. Смысл Эффективность колонки - характеристика качества колонки,
- 46. Селективность Селективность (относительное удерживание, αR/cm, фактор разделения,
- 47. Селективность Селективность колонки зависит от многих факторов,
- 48. Параметры пиков Коэффициент асимметрии АS - отношение
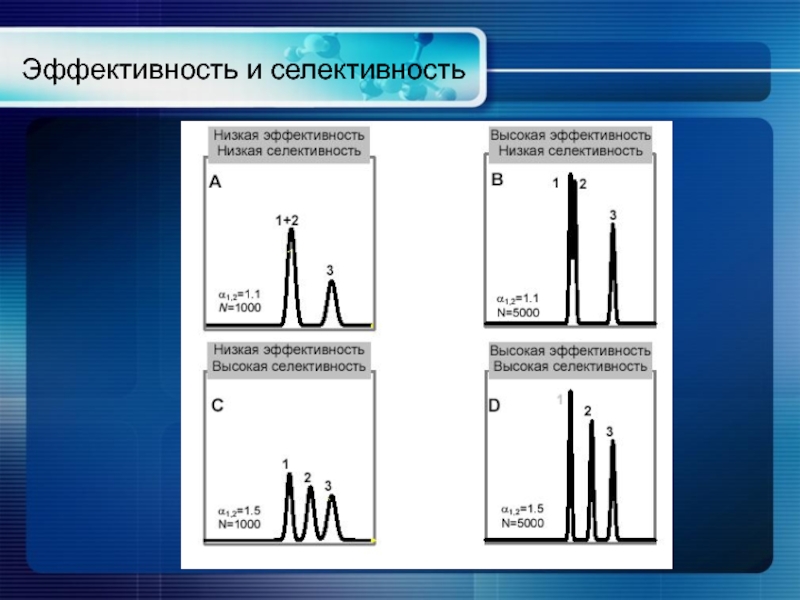
- 49. Эффективность и селективность
- 50. Заключение ВЭЖХ – мощный метод анализа сложных
Слайд 2План лекции
Методы разделения белковых смесей
Основные принципы хроматографии
ВЭЖХ
Инструментальное обеспечение
Слайд 3Методы разделения белковых смесей
Высокоэффективная жидкостная хроматография
разделение по заряду, молекулярной массе,
Электрофорез в ПААГ в присутствии додецилсульфата натрия разделение по величине молекулярных масс
Изоэлектрофокусирование разделение по величине изоэлектрических точек
Двумерный электрофорез изоэлектрическая точка+молекулярная масса
Иммуноблоттинг (Вестерн-блоттинг) - визуализация детекция при помощи антител
Слайд 5Хроматография
Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах сорбции
Неподвижная фаза – твердое вещество или иммобилизованная жидкость
Подвижная фаза (элюэнт) – жидкость или газ
Слайд 7Виды хроматографии
Критерии классификации
способ ввода пробы;
агрегатное состояние фаз;
механизм взаимодействия
назначение.
Слайд 8По способу введения пробы
Элюентная хроматография (проявительная)
Наиболее часто используемый вариант проведения аналитической
Фронтальная хроматография
Смесь непрерывно подают в колонку, при этом на выходе из колонки только первый, наименее удерживаемый компонент можно выделить в чистом виде. Остальные зоны содержат 2 и более компонентов. Родственный метод — твердофазная экстракция (сорбционное концентрирование).
Вытеснительная хроматография
В колонку после подачи разделяемой смеси вводят специальное вещество-вытеснитель, которое удерживается сильнее любого из компонентов смеси. Образуются примыкающие друг к другу зоны разделяемых веществ.
Слайд 9ТФЭ (SPE)
Устройства для автоматизации ТФЭ
Колонки для ТФЭ
Твердофазная экстракция, ТФЭ — разделение
Слайд 10ТФЭ
Назначение ТФЭ:
очистка пробы от нежелательных примесей,
концентирование компонентов пробы,
перевод компонентов пробы на
Основные методы ТФЭ:
одностадийная очистка, когда все нежелательные компоненты пробы собираются на сорбенте, а аналит собирается
двухстадийная очистка и концентрирование, когда проба наносится на патрон вместе с нежелательнимы примесями, а потом с помощью более сильного элюента смывается аналит. Все нежелательные примеси остаются на сорбенте.
трехстадийная очистка и концентрирование: на первом этапе все компоненты наносятся на патрон, на втором смываются легкие нежелательные компоненты, на третьем смывается аналит. Все тяжелые нежелательные примеси остаются на сорбенте.
Слайд 11По агрегатному состоянию фаз
Газовая хроматография
Газо-жидкостная хроматография
Газо-твёрдофазная хроматография
Жидкостная хроматография
Жидкостно-жидкостная хроматография
Жидкостно-твёрдофазная хроматография
Жидкостно-гелевая хроматография
Сверхкритическая
Слайд 12По механизму взаимодействия
Распределительная хроматография
Ионообменная хроматография
Адсорбционная хроматография
Эксклюзионная хроматография
Аффинная хроматография
Осадочная хроматография
Адсорбционно-комплексообразовательная хроматография
Слайд 13Распределительная хроматография
хроматографический метод, при котором неподвижная (стационарная) фаза химически связана с
Подвижной фазой является жидкость (LLC — англ. liquid liquid chromatography), которая служит растворителем, или газ (газовая хроматография). Разделение происходит за счёт различия полярности разделяемых веществ.
Частным случаем распределительной хроматографии является обращённо-фазная хроматография.
Слайд 14Ионобменная хроматография
хроматографии позволяет разделять ионы и полярные молекулы, на основании зарядов
Данный вид хроматографии позволяет разделить практически любые заряженные молекулы, в том числе: крупные — белки, малые—молекулы нуклеотидов и аминокислот. Часто ионообменная хроматография используют как первый этап очистки белков.
Принцип ионообменной хроматографии
Ионообменная хроматография позволяет разделить молекулы, основываясь на ионных взаимодействиях. Неподвижная фаза имеет заряженные функциональные группы, которые взаимодействуют с анализируемыми ионизированными молекулами противоположного заряда. Этот вариант хроматографии классифицируется на два типа — катионную и анионную ионообменную хроматографию:
Катионная ионообменная хроматография задерживает положительно заряженные катионы, так как неподвижная фаза имеет отрицательно заряженные функциональные группы, например, фосфат (PO43−).
Анионная ионообменная хроматография задерживает отрицательно заряженные анионы, так как неподвижная фаза имеет положительно заряженные функциональные группы, например, +N(R)4.
Слайд 15Адсорбционная хроматография
вид хроматографии, основанный на способности твёрдого вещества — неподвижной фазы
Эффективность разделения примесей пропорциональна их величинам адсорбции при условиях эксперимента.
Процесс взаимодействия может сопровождаться химическим взаимодействием примесей с неподвижной фазой, то есть хемосорбцией.
Слайд 16Эксклюзионная хроматографии
(гель-фильтрация)
молекулы веществ разделяются по размеру за счёт их разной способности
Первыми выходят из колонки наиболее крупные молекулы (бо́льшей молекулярной массы), способные проникать в минимальное число пор стационарной фазы. Последними выходят вещества с малыми размерами молекул, свободно проникающие в поры.
! при гель-фильтрации стационарная фаза остается химически инертной и с разделяемыми веществами не взаимодействует.
Разделение феррицианида калия и голубого декстрана (сефадекс G25)
Принцип разделения
Слайд 17Эксклюзионная хроматографии
(гель-фильтрация)
Объем образца лимитирующий для качества хроматографии
Аналитическое разделение: не более 0,1%
Препаративное разделение: не более 8-10% Vc
Низкого давления
агароза,
декстран,
полиакриламид,
сефадекс,
сефакрил,
сефароза,
супердекс.
Высокого давления
полиметакрилат,
полистирол,
силикагель
Сорбенты
Слайд 18Аффинная хроматография
(от лат. affinis – родственный) (биоспецифич. хроматография, хроматография по сродству), метод очистки
В кач-ве лигандов используют соед., взаимод. к-рых с разделяемыми в-вами основано на биол. ф-ции последних.
Что связывается с носителем?
Субстраты,
Ингибиторы
Коферменты
Антитела
Катионы металлов – метало-хелатная хроматография (рекомбинантные белки).
Слайд 19По назначению
аналитическая (динамический диапазон)
препаративная (10 мг – 10 г)
Слайд 20ВЭЖХ
Высокоэффективная жидкостная хроматография (ВЭЖХ)
High performance liquid chromatography (HPLC)
Инструментальная реализация хроматографических методов (Csaba
Один из эффективнейших методов разделения сложных смесей веществ, широко применяемый как в аналитической химии, так и в химической технологии. Основой хроматографического разделения является участие компонентов разделяемой смеси в сложной системе Ван-дер-Ваальсовых взаимодействий (преимущественно межмолекулярных) на границе раздела фаз. Полученные простые смеси анализируются затем обычными физико-химическими методами или специальными методами, созданными для хроматографии.
Слайд 27Основные узлы хроматографа
Дегазатор подвижной фазы
Насос высокого давления + градиентный
Система инжекции (автосэмплер)
Колонка
Детектор
Коллектор фракций
Слайд 28
Схема хроматографа
(1) Резервуары для растворителей (2) дегазатор, (3) Градиентный клапан, (4)
Слайд 29Подвижная фаза
Обращеннофазовая хроматография
метанол
ацетонитрил
вода
ТГФ
Параметры
вязкость
полярность
Слайд 30Насос
Насос - обеспечивает стабильный поток подвижной фазы через колонку под высоким
Градиентный смеситель – обеспечивает градиент концентрации растворителя
Режимы:
изократический
Состав ПФ не изменяется; градиентный смеситель не нужен
градиентный
Состав ПФ изменяется, увеличивая силу элюэнта;
требуется градиентный смеситель
Слайд 31Инжектор
Назначение – дозированный ввод образца в колонку
Работа шестипортового инжектора
Дозирующая петля
Слайд 32Колонка
Геометрический объем колонки, Vc - внутреннее пространство пустой колонки.
Свободный объем, Vo
Длина (высота) колонки, внутренний диаметр колонки, размер частиц сорбента, вид сорбента.
Слайд 34Требования к сорбенту
1. колоночный материал должен обладать достаточной прочностью и жесткостью,
2. сорбент должен обладать достаточно развитой однородной поверхностью и узким фракционным составом частиц.
3. сорбент не должен вступать в необратимые химические взаимодействия как с компонентами элюента, так и с разделяемой пробой.
Слайд 36Виды детекторов
ультрафиолетовый (УФ, UV)
диодноматричный (PDA)
рефрактометрический
флуоресцентный
кондуктометрический
детектор
масс-спектрометрический (МС, MS)
Слайд 39Параметры
tM - время удерживания несорбируемого соединения;
tR1 и tR2 - абсолютные
Высота пика, h - расстояние от максимума пика до его основания, измеренное вдоль оси отклика детектора.
Нулевая (базовая) линия хроматограммы - линия, соответствующая нулевой концентрации анализируемых веществ в элюате.
Шум - помехи, статистические флуктуации нулевой линии хроматограммы. Уровень шума складывается из статистических флуктуации всех параметров, принимающих участие в образовании сигнала детектора.
Дрейф нулевой линии - постепенное смещение регистрируемое на хроматограмме.
Хроматографический пик - участок хроматограммы, соответствующий площади ограниченной функцией хроматограммы в момент выхода определяемого вещества из колонки и базовой линией.
Основание пика - продолжение нулевой линии, соединяющее начало и конец хроматографического пика.
Слайд 40Параметры
Площадь пика, S - площадь хроматограммы, заключенная между пиком и его
Ширина пика у основания, Wb - отрезок основания пика, отсекаемый двумя касательными, проведенными в точках перегибов восходящей и нисходящей ветвей хроматографического пика.
Ширина пика на полувысоте, Wh- отсекаемый пиком отрезок линии, проведенной параллельно основанию пика на середине его высоты.
Слайд 41Объем
Объем удерживания вещества, VR - объем подвижной фазы, затрачиваемой на элюирование
Мертвый объем, VM - объем подвижной фазы между точкой ввода пробы и точкой ее обнаружения (кюветой детектора). Мертвый объем включает в себя свободный объем колонки, объемы устройства ввода пробы (дозатора), детектора, а также объемы коммуникаций между ними.
Приведенный объем удерживания, VR’ - объем удерживания вещества за вычетом мертвого объема:
VR' = VR - VM
Слайд 42Время
Абсолютное время удерживания вещества, tR - время пребывания исследуемого вещества в
Мертвое время, tM - время пребывания несорбируемого вещества в хроматографе. На практике мертвое время определяют от момента ввода пробы несорбируемого вещества в хроматограф до момента регистрации максимума сигнала детектора.
Приведенное время удерживания, tR’ - абсолютное время удерживания за вычетом мертвого времени:
tR'= tR- tM.
Слайд 43Эффективность
Эффективность хроматографической системы - количество ступеней установления равновесия между подвижной и
Число теоретических тарелок, N - величина, характеризующая качество колонки и рассчитываемая по параметрам удерживания выбранного вещества по формуле
N = 16(tR/Wb)2 = 5.545(tR/Wh)2,
где tR - время удерживания пика, Wb - ширина пика на его полувысоте, Wh - ширина пика у основания.
Высота, эквивалентная теоретической тарелке, H - величина, характеризующая качество колонки и рассчитываемая как отношение длины колонки L к числу теоретических тарелок
H = L/N
Слайд 44Параметры эффективности
Приведенное число теоретических тарелок N’ - отношение числа реально полученных
N=100N/L,
где L - длина колонки в см.
Приведенная высота, эквивалентная теоретической тарелке
H’=H/d,
где d - средний (эффективный) диаметр частиц сорбента (мкм), она также является характеристикой эффективности колонки. Вполне удовлетворительным принято считать колонки со значением H равным 3-3,5d. Очень хорошими считаются колонки с Н равным 2d.
Фактор удерживания (коэффициент емкости), k' - один из основополагающих параметров удерживания в жидкостной хроматографии, безразмерная величина, характеризующая удерживание вещества и равная отношению приведенного времени удерживания к мертвому времени
k’=t’R/t’M.
Слайд 45Смысл
Эффективность колонки - характеристика качества колонки, определяемая числом теоретических тарелок и
Слайд 46Селективность
Селективность (относительное удерживание, αR/cm, фактор разделения, α) хроматографической системы - избирательность,
безразмерная величина, равная отношению приведенного объема (времени) удерживания определенного вещества, взятого для сравнения (стандарта) и хроматографируемого в идентичных условиях
αR/cm = kR/kcm = tR'/tcm' = VR'/Vcm’
Слайд 47Селективность
Селективность колонки зависит от многих факторов, варьируя которые можно подобрать оптимальные
Слайд 48Параметры пиков
Коэффициент асимметрии АS - отношение двух отрезков, образуемых на горизонтальной
АS = B/A
Разрешение пиков, RS - расстояние между максимумами выбранных соседних пиков, деленное на полусумму их ширин у основания (выраженных в одних и тех же единицах измерения)
RS = 2(tR2- tR1) / (Wb1+Wb2)
Разрешение как параметр, характеризующий разделение пиков, увеличивается по мере возрастания селективности, отражаемой ростом числителя, и роста эффективности, отражаемой снижением значения знаменателя из-за уменьшения ширины пиков.
Экстраколоночное расширение пика (ЭКР) - размывание хроматографической зоны, происходящее в инжекторе, соединительных капиллярах, в ячейке детектора.
Слайд 50Заключение
ВЭЖХ – мощный метод анализа сложных смесей
Наиболее часто используется обращенно-фазовая ВЭЖХ
Хроматограф
Дегазатор подвижной фазы
Градиентный смеситель
Насос
Инжектор
Колонка
Детектор
Коллектор фракций