- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Metode cromatografice презентация
Содержание
- 1. Metode cromatografice
- 2. Analiza chimică cromatografică este un domeniu al
- 3. separarea precede analiza şi se realizează prin
- 4. Separarea se petrece în coloana cromatografică.
- 5. Amestecul supus separării se introduce sub formă
- 6. Clasificarea tehnicilor cromatografice se distinge cromatografia de
- 7. În cadrul LC se disting, în funcţie
- 8. Cromatografia ionică (de schimb ionic), care se
- 9. Cromatografia de excluziune sterică se desfăşoară pe
- 10. în cazul cromatografiei de gaze (sau mai
- 11. Cromatografia gaz-solid este analogă cu cele discutate
- 12. Cromatograma. Elementele acesteia şi mărimi fundamentale În
- 13. Pe cromatogramă distingem o serie de maxime,
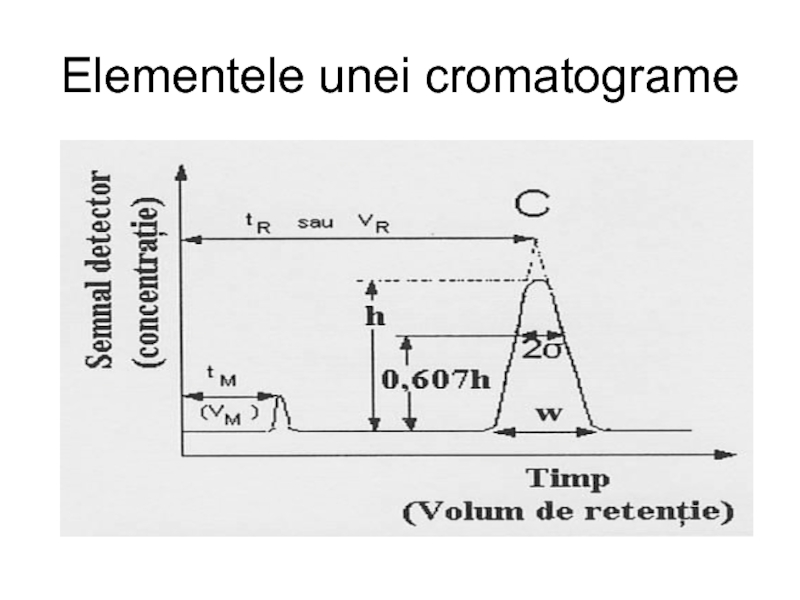
- 14. Elementele unei cromatograme
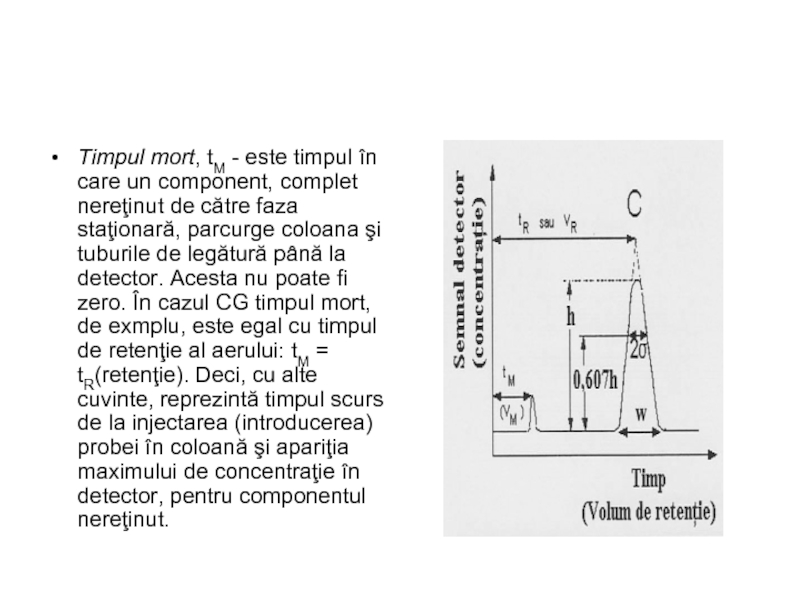
- 15. Timpul mort, tM - este timpul în
- 16. Timpul de retenţie, tR - o
- 17. Volumul de retenţie, VR este volumul de
- 18. Timpul de retenţie ajustat, tR' -
- 19. Corespunzător există şi un volum de retenţie
- 20. Acest volum mort este legat de
- 21. Cromatograme ideale şi reale Aspectul unui pic
- 22. Numărul de talere teoretice al coloanei, n.
- 23. Cu cât valoarea H este mai mare
- 24. Valoarea numărului de talere teoretice, N, constituie
- 25. Rezoluţia, simbolizată RS, este mărimea ce exprimă
- 26. unde ∆tR este diferenţa dintre timpii
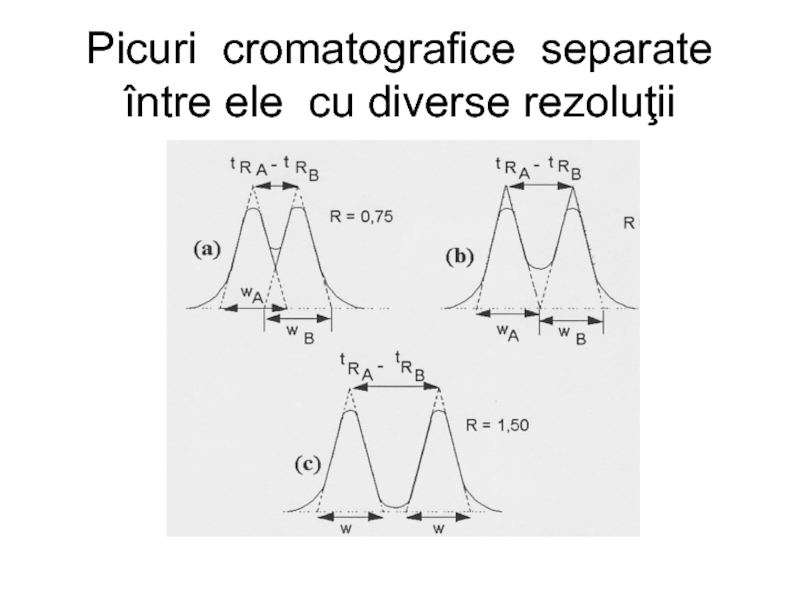
- 27. Picuri cromatografice separate între ele cu diverse rezoluţii
- 28. Ecuaţia lui Van Deemter Această ecuaţie exprimă
- 29. Cea mai simplă şi totodată mai cunoscută
- 30. aceste constante au în realitate fiecare nişte
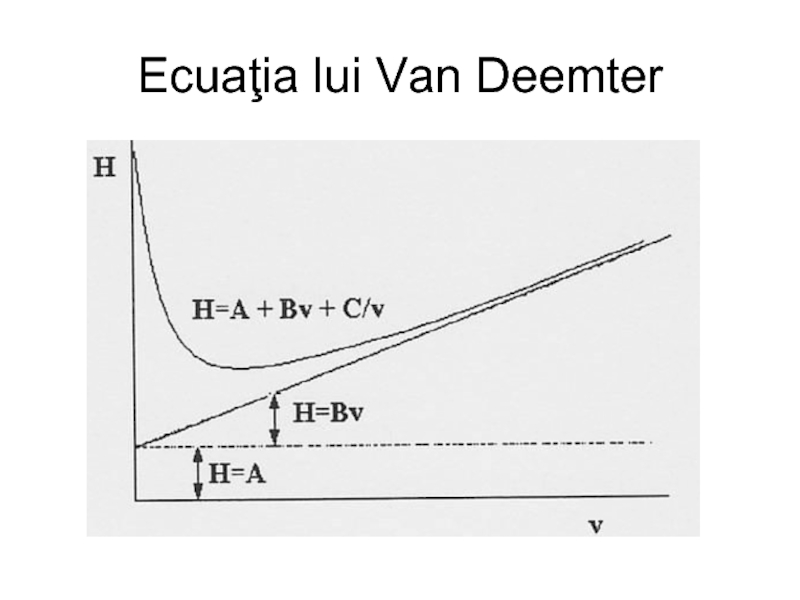
- 31. Ecuaţia lui Van Deemter
Слайд 2Analiza chimică cromatografică este un domeniu al analizei instrumentale care include
Слайд 3separarea precede analiza şi se realizează prin repetarea, de un număr
Una dintre faze este imobilă şi poartă denumirea de fază staţionară (aflată de regulă într-un tub numit coloană) iar cealaltă - faza mobilă - aflată în mişcare, se deplasează prin golurile primei faze.
Слайд 4Separarea se petrece în coloana cromatografică.
Faza mobilă, denumită şi eluent
Слайд 5Amestecul supus separării se introduce sub formă de soluţie la începutul
Слайд 6Clasificarea tehnicilor cromatografice
se distinge cromatografia de lichide (LC) când faza mobilă
cromatografia de gaze (GC) când aceasta este un gaz sau cromatografia cu fluide supracritice la care faza mobilă este un lichid aflat peste temperatura critică.
În cadrul cromatografiei de lichide se mai face distincţie între cromatografia pe coloană deschisă şi cea pe coloană închisă. Pe de altă parte, în cadrul fiecăreia dintre acestea, distingem mai multe variante.
Слайд 7În cadrul LC se disting, în funcţie de mecanismele de separare:
Cromatografia
Слайд 8Cromatografia ionică (de schimb ionic), care se petrece pe o fază
Слайд 9Cromatografia de excluziune sterică se desfăşoară pe faze staţionare poroase dar
Слайд 10în cazul cromatografiei de gaze (sau mai pretenţios cromatografiei în fază
Cromatografia gaz-lichid în care faza staţionară este un lichid nevolatil imobilizat pe un suport solid. Aici suportul poate fi unul granular, poros, situat într-o coloană în aşa-numita cromatografie de gaze “convenţională” sau chiar pe pereţii coloanei, confecţionată de dimensiuni capilare, în “cromatografia pe coloană capilară”.
Слайд 11Cromatografia gaz-solid este analogă cu cele discutate la cromatografia de adsorbţie
Слайд 12Cromatograma. Elementele acesteia şi mărimi fundamentale
În orice tip de cromatografie detectorul
Слайд 13Pe cromatogramă distingem o serie de maxime, numite picuri (peak =
Aceasta apare ori de câte ori în detector nu apare nici un component, în afara eluentului evident
Слайд 15Timpul mort, tM - este timpul în care un component, complet
Слайд 16
Timpul de retenţie, tR - o mărime caracteristică pentru fiecare component
Слайд 17 Volumul de retenţie, VR este volumul de eluent corespunzător timpului de
VR = tRFe (1)
Acesta este legat de timpul tR prin intermediul debitului eluentului, Fe:
Слайд 18
Timpul de retenţie ajustat, tR' - introdus în cromatografie pentru a
t'R = tr - tM (2)
Слайд 20
Acest volum mort este legat de debitul eluentului coloanei, Fe, prin
VM =tMFe
şi reprezintă volumul golurilor din coloană plus volumul tuburilor de legătură de la coloană la detector.
Слайд 21Cromatograme ideale şi reale
Aspectul unui pic dintr-o cromatogramă ideală este acelaşi
Слайд 22Numărul de talere teoretice al coloanei, n. Conform “teoriei talerelor” migrarea
Similar cu distilarea pe coloane prevăzute cu talere, aceste mici incinte ideale au fost denumite "talere teoretice". Lungimea porţiunii dintr-o coloană, ce corespunde unei asemenea incinte, pe parcursul căreia se realizează un echilibru termodinamic, se notează cu H şi poartă numele de înălţime echivalentă a unui taler teoretic. Aceasta caracterizează performanţa coloanei şi se poate calcula din raportul:
Слайд 23Cu cât valoarea H este mai mare separarea este mai bună.
wb = 4σ
Слайд 24 Valoarea numărului de talere teoretice, N, constituie de asemenea o măsură
Слайд 25 Rezoluţia, simbolizată RS, este mărimea ce exprimă gradul de separare a
Слайд 26
unde ∆tR este diferenţa dintre timpii de retenţie ai componentelor B
w1/2= (wA + wB)/2.
Слайд 28Ecuaţia lui Van Deemter
Această ecuaţie exprimă contribuţia diverşilor factori la lărgirea
Слайд 29 Cea mai simplă şi totodată mai cunoscută expresie este cea descoperită
H = A + B⋅v + C
unde A, B şi C sunt, pentru o coloană dată v nişte constante