- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классификация твердых тел презентация
Содержание
- 1. Классификация твердых тел
- 4. Виды симметрии 1 2 3 4 5 6 7 8 9 10
- 5. Трансляционная симметрия - тип симметрии, при которой свойства
- 6. [c] Кварц (SiO2) Кварцевое стекло и расплав Аморфный SiO2
- 7. Композитные Наноразмерные TiO2 ZnO (Фотонные кристаллы, метаматериалы и др.)
- 8. II. Электронные свойства Диэлектрики Отсутствие свободных электронов
- 9. Зонная теория твёрдого тела — квантовомеханическая теория движения электронов в твёрдом теле. Свободные электроны
- 10. II. Химические свойства Неорганические Органические Тип химической
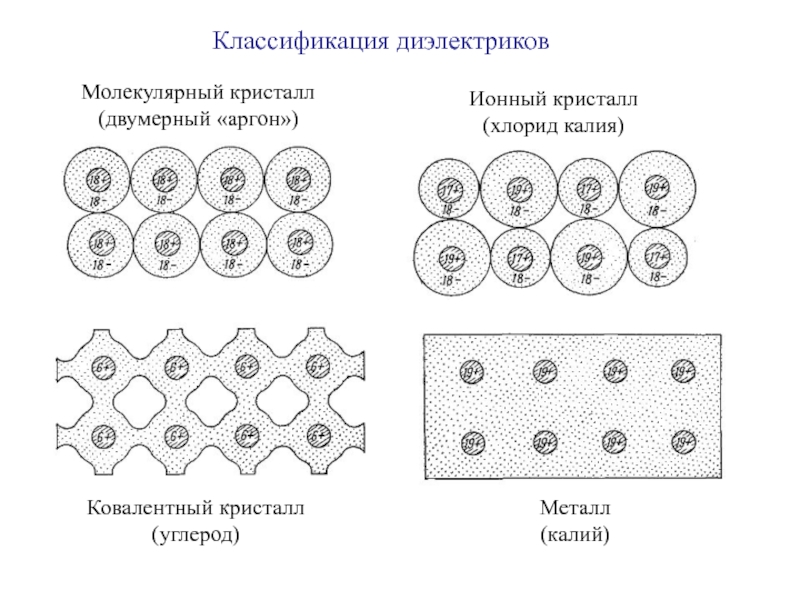
- 11. Молекулярный кристалл (двумерный «аргон») Ионный кристалл (хлорид
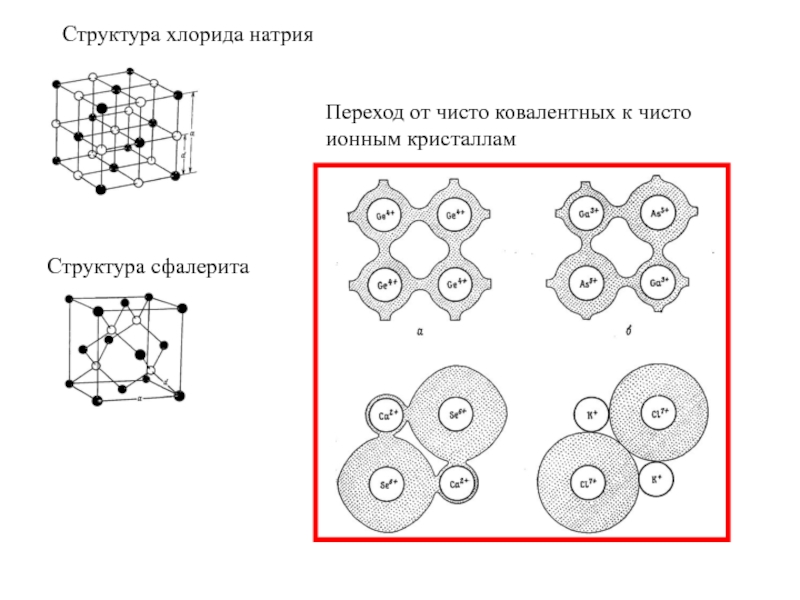
- 12. Структура хлорида натрия Структура сфалерита Переход от чисто ковалентных к чисто ионным кристаллам
Слайд 1Лекция № 2
Классификация твердых тел
Структурные свойства
Монокристаллические
Наличие трансляционной симметрии в макро-объеме
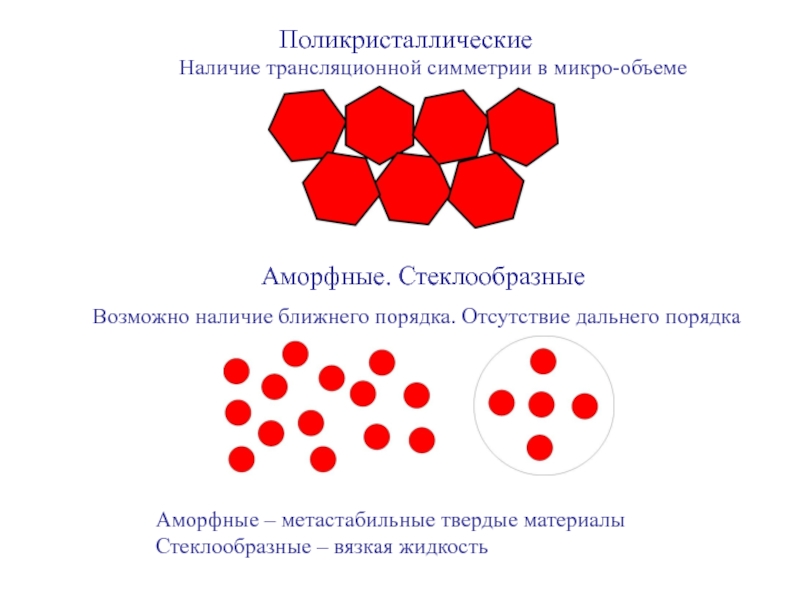
Слайд 2 Поликристаллические
Наличие трансляционной симметрии
Аморфные. Стеклообразные
Возможно наличие ближнего порядка. Отсутствие дальнего порядка
Аморфные – метастабильные твердые материалы
Стеклообразные – вязкая жидкость
Слайд 5Трансляционная симметрия - тип симметрии, при которой свойства рассматриваемой системы не изменяются
Среди всех векторов трансляций кристаллической решётки можно выбрать 3 линейно независимых таким образом, что любой другой вектор трансляции был бы целочисленно-линейной комбинацией этих трёх векторов. Эти три вектора составляют базис кристаллической решётки.
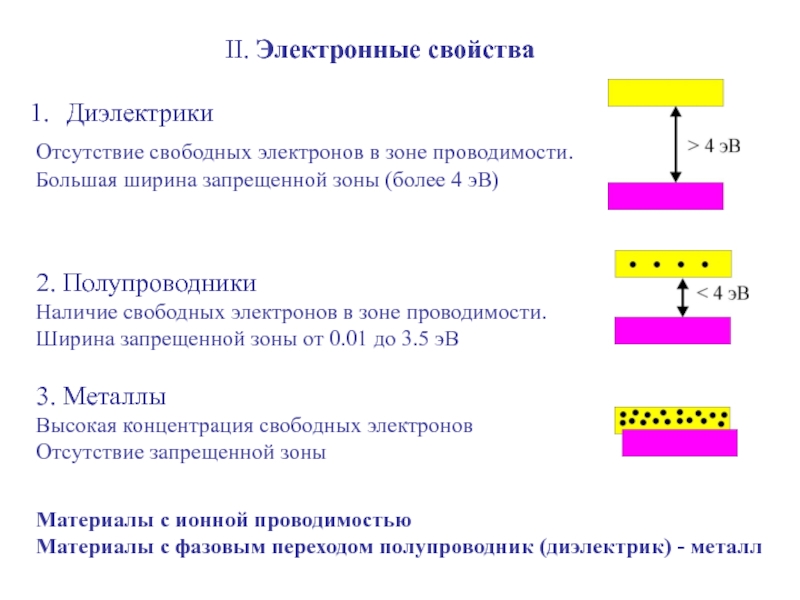
Слайд 8II. Электронные свойства
Диэлектрики
Отсутствие свободных электронов в зоне проводимости.
Большая ширина запрещенной зоны
Материалы с ионной проводимостью
Материалы с фазовым переходом полупроводник (диэлектрик) - металл
2. Полупроводники
Наличие свободных электронов в зоне проводимости.
Ширина запрещенной зоны от 0.01 до 3.5 эВ
3. Металлы
Высокая концентрация свободных электронов
Отсутствие запрещенной зоны
Слайд 9Зонная теория твёрдого тела — квантовомеханическая теория движения электронов в твёрдом теле.
Свободные электроны могут иметь любую энергию
Главные приближения теории:
1. Твёрдое тело представляет собой идеально периодический кристалл.
2. Равновесные положения узлов кристаллической решётки фиксированы, то есть ядра атомов считаются неподвижными (адиабатическое приближение). 3. Многоэлектронная задача сводится к одноэлектронной.
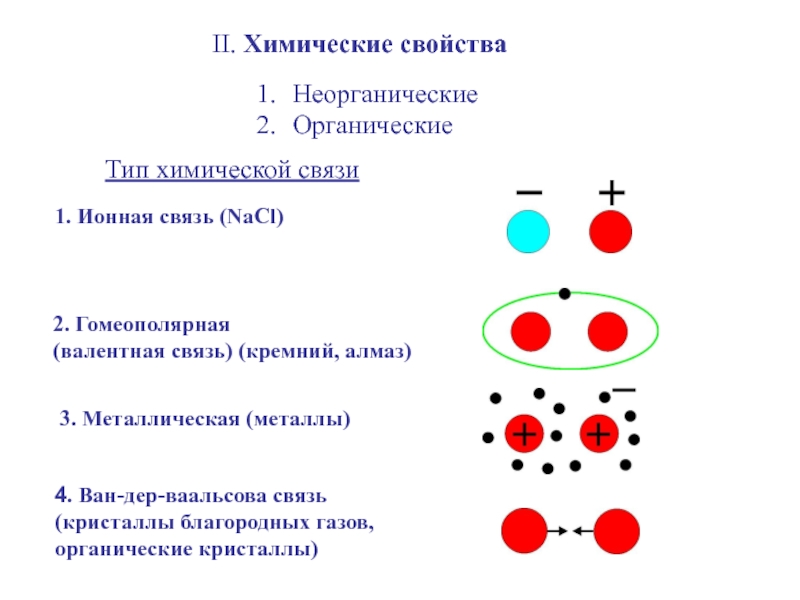
Слайд 10II. Химические свойства
Неорганические
Органические
Тип химической связи
1. Ионная связь (NaCl)
2. Гомеополярная
(валентная связь)
4. Ван-дер-ваальсова связь
(кристаллы благородных газов,
органические кристаллы)
3. Металлическая (металлы)




![[c]Кварц (SiO2) Кварцевое стекло и расплав Аморфный SiO2](/img/tmb/4/332008/304d21c019b328c321968e240f33b213-800x.jpg)