- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические источники тока презентация
Содержание
- 1. Химические источники тока
- 2. Гальванические элементы – это устройства, которые
- 3. Принцип действия ХИТ
- 4. Принцип действия ХИТ
- 5. Принцип действия ХИТ
- 6. Основные термины
- 7. Классификация Первичные
- 8. Классификация Топливный
- 9. Устройство и
- 10. Устройство и
- 11. Устройство и принцип действия гальванического элемента АВ
- 12. Устройство и
- 13. Примеры Электролиз раствора CuCl2 с инертным анодом, рН=7.
- 14. Устройство и принцип действия гальванического элемента
- 15. Устройство и принцип действия гальванического элемента Различают
- 16. Устройство и принцип действия гальванического элемента Компоненты
- 17. Устройство и принцип действия гальванического элемента Электролиты:
- 18. Устройство и принцип действия гальванического элемента Сепараторы
- 19. Э.Д.С. гальванического элемента Э.Д.С. гальванического элемента можно
- 20. Напряжение разомкнутой цепи В литературе по
- 21. Разрядное и зарядное напряжения Напряжение ХИТ
- 22. Мощность и вольт-амперная характеристика ХИТ Зависимость
- 23. Мощность и вольт-амперная характеристика ХИТ Мощность
- 24. Мощность и вольт-амперная характеристика ХИТ Полезная
- 25. Разрядная кривая Разрядная кривая ХИТ позволяет
- 26. Разрядная кривая Можно выделить два участка
- 27. Ёмкость ХИТ Разрядная емкость ХИТ С
- 28. Саморязряд Саморазряд – потеря емкости ХИТ,
- 29. Причины саморазряда Взаимодействие активных веществ электродов
- 30. Причины саморазряда Взаимодействие активного вещества отрицательного
- 31. Причины саморазряда Взаимодействие активных веществ отрицательного
- 32. Нормированный ток Удобным параметром для сравнения
- 33. Ресурс и цикл Технический ресурс аккумулятора
- 34. Марганцево-цинковые элементы с солевым электролитом 1865
- 35. Марганцево-цинковые элементы с солевым электролитом Возможные
- 36. Марганцево-цинковые элементы с солевым электролитом
- 37. Марганцево-цинковые элементы с солевым электролитом Для
- 38. Марганцево-цинковые элементы с солевым электролитом 1
- 39. Марганцево-цинковые элементы с щелочным электролитом Электрохимическая
- 40. Марганцево-цинковые элементы с щелочным электролитом Реакция
- 41. Марганцево-цинковые элементы с щелочным электролитом 1
- 42. Свинцовые (кислотные) аккумуляторы Четыре основные группы:
- 43. Свинцовые (кислотные) аккумуляторы
- 44. Свинцовые (кислотные) аккумуляторы Стационарные аккумуляторы используются
- 45. Свинцовые (кислотные) аккумуляторы Тяговые батареи емкостью
- 46. Свинцовые (кислотные) аккумуляторы Электрохимическая система
- 47. Свинцовые (кислотные) аккумуляторы Стартерные СА состоят
- 48. Свинцовые (кислотные) аккумуляторы Одноименные пластины
- 49. Свинцовые (кислотные) аккумуляторы Решётки из свинцовых
- 50. Свинцовые (кислотные) аккумуляторы Пластины соединены пайкой
- 51. Свинцовые (кислотные) аккумуляторы Один из применяемых сепараторов (мипласт). Выступами обращён к плюсу.
- 52. Свинцовые (кислотные) аккумуляторы Причины выхода из
- 53. Свинцовые (кислотные) аккумуляторы Причины выхода из
- 54. Свинцовые (кислотные) аккумуляторы Причины выхода из
- 55. Свинцовые (кислотные) аккумуляторы Причины выхода из
Слайд 1ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА
Лекция
Лектор: Кондратьев Денис Андреевич
заведующий кафедрой
технологии неорганических веществ электрохимических производств,
кандидат
Слайд 2
Гальванические элементы – это устройства, которые применяют для преобразования энергии окислительно-восстановительной
Слайд 6
Основные термины
Разряд - процесс, во время которого ХИТ отдает энергию во
В ХИТ можно использовать энергию лишь окислительно-восстановительной реакции, и нужно разделить окислительную и восстановительную реакции, проводя их раздельно (но одновременно) на разных электродах.
Батарея – это два или более элемента, соединенные электрически, имеющие общий корпус, выводы и маркировку.
Слайд 7
Классификация
Первичные ХИТ - устройства, допускающие лишь однократное использование заключенных в них
Вторичные – ХИТ, работоспособность которых после разряда может быть восстановлена путем заряда, т.е. пропусканием постоянного электрического тока в направлении, противоположном току разряда. При заряде продукты разряда превращаются в первоначальные реагенты. Вторичные ХИТ подразделяются на аккумуляторы (вторичные элементы) и аккумуляторные батареи.
Слайд 8
Классификация
Топливный элемент (ТЭ) – ХИТ, в котором реагенты непрерывно и раздельно
Слайд 9
Устройство и принцип действия гальванического элемента
Любой гальванический элемент состоит из двух
Электродная электрохимическая реакция протекает на границе раздела фаз между электродом и электролитом. В общем случае эти фазы следующие:
фаза с электронной проводимостью (для подвода или отвода электронов);
фаза с ионной проводимостью (электролит);
реагент (окислитель или восстановитель).
Слайд 10
Устройство и принцип действия гальванического элемента
Реагенты, участвующие в электродных реакциях, называются
АВ в совокупности с электролитом образуют электрохимическую систему.
Слайд 11Устройство и принцип действия гальванического элемента
АВ отрицательного электрода служит восстановитель, отдающий
АВ положительного электрода служит окислитель, присоединяющий электроны. При разряде положительный электрод является катодом.
При разряде электроны движутся от отрицательного электрода во внешнюю (нагрузочную) цепь; при электролизе электроны движутся от отрицательного вывода выпрямителя к отрицательному электроду.
Слайд 12
Устройство и принцип действия гальванического элемента
Гальванический элемент Якоби-Даниэля состоит из медной
Элемент работает за счет энергии реакции:
Zn + Cu2+ = Cu + Zn2+
Слайд 15Устройство и принцип действия гальванического элемента
Различают электроды с твердыми реагентами и
В электроде с твердым реагентом всегда содержатся определенный запас АВ и фаза с электронной проводимостью, служащая для токоотвода. АВ наносится на специальный токоотвод.
Для улучшения работоспособности электрода активные вещества часто используют в составе активных масс – смесей с веществами, придающими массе определенные физико-химические свойства.
Слайд 16Устройство и принцип действия гальванического элемента
Компоненты активных масс:
электропроводные добавки (металлические, угольные,
связующие (карбоксиметилцеллюлоза, фторопласт, полиэтилен, полипропилен и т.д.);
расширители – соединения, препятствующие рекристаллизации частиц активного вещества и способствующие сохранению высокой истинной поверхности электрода;
ингибиторы коррозии (в случае порошковых металлических анодов);
активирующие добавки, способствующие повышению коэффициента использования активного вещества, и т.д.
Слайд 17Устройство и принцип действия гальванического элемента
Электролиты:
водные растворы кислот, щелочей или солей;
электролиты
электролиты на основе органических растворителей;
ионные расплавы;
твердые электролиты.
Слайд 18Устройство и принцип действия гальванического элемента
Сепараторы и их функции:
предотвращение внутренних коротких
механическое удержание активной массы на электродах во избежание ее выкрашивания и осыпания;
замедление роста металлических дендритов при заряде некоторых типов аккумуляторов;
удержание электролита вблизи поверхности электродов (функция электролитоносителя);
уменьшение саморазряда ХИТ вследствие замедления массопереноса растворенных активных веществ к противоположным электродам.
Слайд 19Э.Д.С. гальванического элемента
Э.Д.С. гальванического элемента можно представить как разность равновесных электродных
Е = φр+ – φр-.
Зависимость величины потенциала электродного процесса от различных факторов выражается уравнением:
φ0 – стандартный электродный потенциал данного процесса,
R – универсальная газовая постоянная, Т – абсолютная температура;
z – число электронов, принимающих участие в процессе, F – число фарадея, [Ox] и [Red] – произведения концентраций веществ, участвующих в процессе в окисленной и восстановленной формах.
Слайд 20
Напряжение разомкнутой цепи
В литературе по ХИТ широко используется термин напряжение разомкнутой
UРЦ = φ+ - φ-
UРЦ ≤ Е
Слайд 21
Разрядное и зарядное напряжения
Напряжение ХИТ при разряде Up меньше напряжения разомкнутой
Up = UРЦ – (|η+| + η-) – IROM
При заряде аккумулятора зарядное напряжение UЗ > UРЦ:
UЗ = UРЦ + (η+ + |η-|) + IROM
Слайд 22
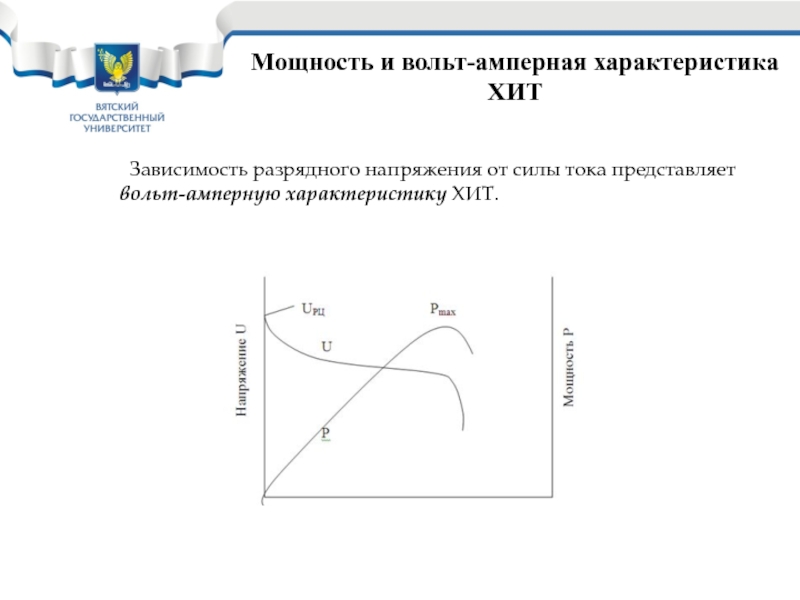
Мощность и вольт-амперная характеристика ХИТ
Зависимость разрядного напряжения от силы тока представляет
Слайд 23
Мощность и вольт-амперная характеристика ХИТ
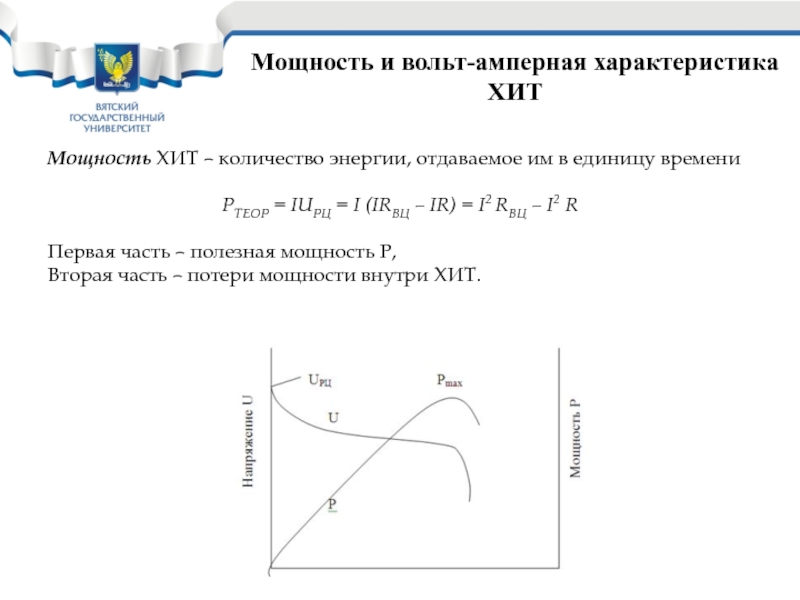
Мощность ХИТ – количество энергии, отдаваемое им
РТЕОР = IUРЦ = I (IRВЦ – IR) = I2 RВЦ – I2 R
Первая часть – полезная мощность Р,
Вторая часть – потери мощности внутри ХИТ.
Слайд 24
Мощность и вольт-амперная характеристика ХИТ
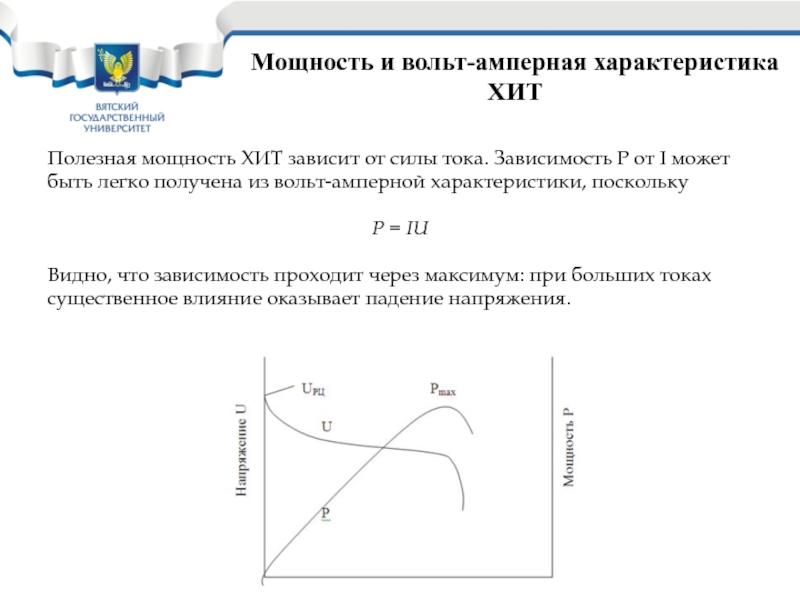
Полезная мощность ХИТ зависит от силы тока.
быть легко получена из вольт-амперной характеристики, поскольку
P = IU
Видно, что зависимость проходит через максимум: при больших токах
существенное влияние оказывает падение напряжения.
Слайд 25
Разрядная кривая
Разрядная кривая ХИТ позволяет судить о величине и степени постоянства
Слайд 26
Разрядная кривая
Можно выделить два участка – постепенного спада напряжения и резкого
Резкое снижение напряжения в конце разряда может быть вызвано:
1. израсходованием активного вещества хотя бы одного электрода;
2. пассивацией одного из электродов;
3. короткими замыканиями между электродами.
Постепенное снижение напряжения при разряде может быть обусловлено:
1. уменьшением НРЦ;
2. увеличением поляризации одного или обоих электродов во времени;
3. увеличением значения RОМ.
Слайд 27
Ёмкость ХИТ
Разрядная емкость ХИТ С – это количество электричества, отдаваемого
источником
режиме разряда.
Если разряд ведется при I = const, то
CI = Iτ
Под τ понимается время достижения Uкон
Слайд 28
Саморязряд
Саморазряд – потеря емкости ХИТ, обусловленная протеканием в нем самопроизвольных процессов.
Слайд 29
Причины саморазряда
Взаимодействие активных веществ электродов с электролитом, обусловленное термодинамической неустойчивостью многих
на отрицательном электроде
Pb + H2SO4 → PbSO4 + H2
на положительном электроде
PbO2 + H2SO4 → PbSO4 + H2O + ½ O2
Слайд 30
Причины саморазряда
Взаимодействие активного вещества отрицательного электрода с окислителями, имеющимися в ХИТ
Pb + 2 Fe3+ + H2SO4 → PbSO4 + 2 Fe2+ + 2 H+
PbO2 + Pb (токоотвод) + 2 H2SO4 → 2 PbSO4 + 2 H2O
Слайд 31
Причины саморазряда
Взаимодействие активных веществ отрицательного и положительного электродов, обусловленное их непосредственным
Диффузионный и конвективный вынос активного вещества, растворенного в электролите, за пределы межэлектродного пространства, например, в ХИТ, работающих в морской воде.
Разряд ХИТ без подключенной внешней нагрузки на мостики с электронной проводимостью, имеющиеся внутри ХИТ между электродами; такие мостики, например, образуются в серебряно-цинковом аккумуляторе и приводят в конечном итоге к коротким замыканиям.
Разряд ХИТ без подключенной внешней нагрузки на электролитные мостики; он может иметь место, если на крышке источника тока находится пролитый электролит или сконденсированная влага, а напряжение ХИТ достаточно, чтобы электролиз воды шел с заметной скоростью (U > 1,7 В).
Слайд 32
Нормированный ток
Удобным параметром для сравнения режимов разряда или заряда ХИТ служит
j = I / C0
Размерность нормированного тока (ч-1) иногда не указывается.
Например, если говорится, что нормированный ток заряда равен 0,3, это означает, что сила зарядного тока (в А) численно составляет 30 % от емкости аккумулятора (в А.ч), а сам заряд будет длиться 1 : 0,3 = 3,33 ч
Слайд 33
Ресурс и цикл
Технический ресурс аккумулятора – число циклов, которое должен выдержать
Цикл представляет собой заряд и последующий за ним разряд.
Слайд 34
Марганцево-цинковые элементы
с солевым электролитом
1865 г. - первый МЦ элемент (Ж.-Л. Лекланше).
Преимущества
-дешевизна (самые дешевые из первичных ХИТ);
-удовлетворительные электрические показатели;
-приемлемая сохраняемость;
-удобства в эксплуатации.
Недостаток – резкое падение напряжения при разряде (конечное напряжение составляет 50 – 70 % начального).
Солевые МЦ ХИТ используют для энергопитания различных бытовых приборов (фонари, игрушки, радиоприемники, часы, и др.).
Слайд 35
Марганцево-цинковые элементы
с солевым электролитом
Возможные электрохимические системы для солевых МЦ элементов:
Zn |
Реакция на положительном электроде:
MnO2 + H2O + e- → MnOOH + OH-
Слайд 36
Марганцево-цинковые элементы
с солевым электролитом
Первичной анодной реакцией является ионизация цинка:
Zn → Zn2+
Последующие
1. в растворе хлорида аммония:
Zn2+ + 2NH4Cl → Zn(NH3)2Cl2↓ + 2H+
2. в растворе хлорида цинка:
4Zn2+ + ZnCl2 + 9H2O → ZnCl2.4ZnO.5H2O↓ + 8H+
Слайд 37
Марганцево-цинковые элементы
с солевым электролитом
Для солевых МЦ ХИТ характерен значительный саморазряд (до
Zn + 2 NH4Cl → ↓Zn(NH3)2Cl2 + H2
Zn + 2 H2O → Zn(OH)2 + H2
Для снижения саморазряда в электролит вводят ингибиторы коррозии: сулема (HgCl2), различные органические ингибиторы.
Слайд 38
Марганцево-цинковые элементы
с солевым электролитом
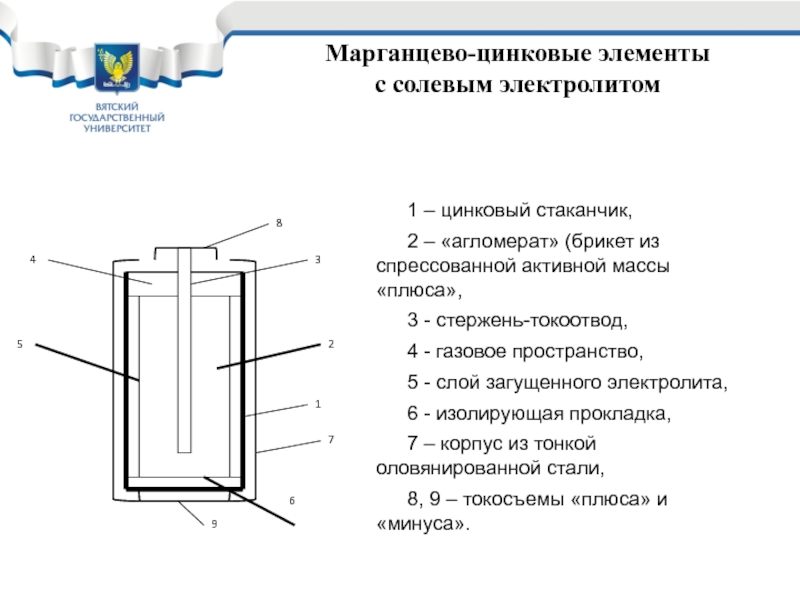
1 – цинковый стаканчик,
2 – «агломерат» (брикет из
3 - стержень-токоотвод,
4 - газовое пространство,
5 - слой загущенного электролита,
6 - изолирующая прокладка,
7 – корпус из тонкой оловянированной стали,
8, 9 – токосъемы «плюса» и «минуса».
Слайд 39
Марганцево-цинковые элементы
с щелочным электролитом
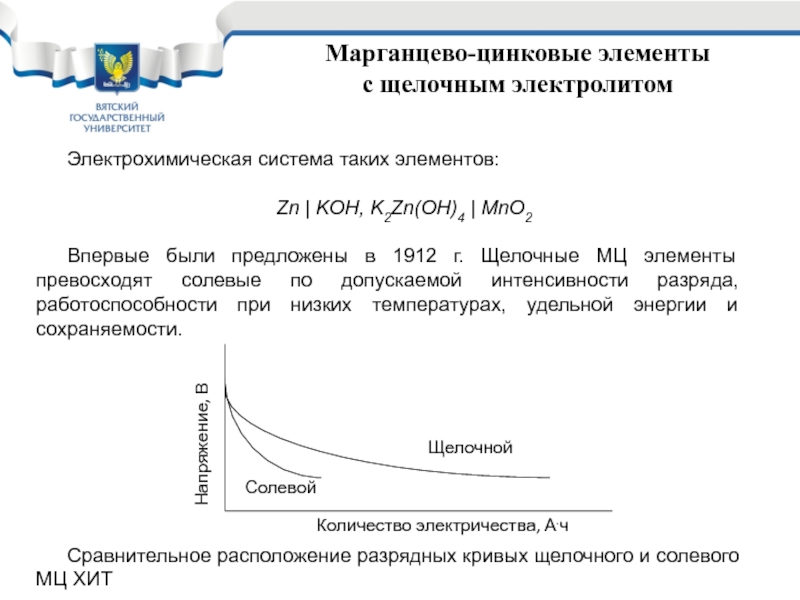
Электрохимическая система таких элементов:
Zn | KOH, K2Zn(OH)4 |
Впервые были предложены в 1912 г. Щелочные МЦ элементы превосходят солевые по допускаемой интенсивности разряда, работоспособности при низких температурах, удельной энергии и сохраняемости.
Сравнительное расположение разрядных кривых щелочного и солевого МЦ ХИТ
Слайд 40
Марганцево-цинковые элементы
с щелочным электролитом
Реакция на цинковом электроде («первичный процесс»):
Zn + 4OH-
После достижения концентрации насыщенного раствора по цинкату раствора начинается его распад с выделением в осадок гидроксида и оксида цинка:
Zn(OH)42- → Zn(OH)2 + 2OH-
Zn(OH)42- → ZnO + H2O + 2OH-
Реакция на положительном электроде:
MnO2 + H2O + e- → MnOOH + OH-
Слайд 41
Марганцево-цинковые элементы
с щелочным электролитом
1 – токоотвод «плюса»,
2 – изоляционная шайба,
3 – внешний металлический корпус,
4 – пастообразный электролит,
5 – АМ «минуса»,
6 – АМ «плюса»,
7 – стальной внутренний стаканчик,
8 – пластмассовая разделяющая прокладка,
9 – токоотвод «минуса»,
10 – полимерная шайба,
11 – отверстие предохранительного клапана,
12 – изолирующая шайба,
13 – внешний токоотвод «минуса»
Слайд 42
Свинцовые (кислотные) аккумуляторы
Четыре основные группы:
Стартерные
Стационарные
Тяговые
Портативные (герметизированные)
Слайд 43
Свинцовые (кислотные) аккумуляторы
Стартерные батареи используют для запуска двигателей
Напряжение батарей 6, 12 или 24 В, емкость от 6 до 215 А.ч.
Электроды в таких батареях намазного типа; типы батарей: СТ (для автомобилей), ТСТ (для тракторов, мощных автомобилей), СТК (для катеров), МТ (для мотоциклов),А, САМ (для самолетов).
Во время движения транспортного средства производится их подзаряд от мотор-генератора для компенсации потери емкости при запуске двигателя и от саморазряда.
Срок службы тонких (1 – 3 мм) пластин 2 – 3 года (150 – 400 циклов). В авиационных батареях толщина пластин ~ 1 мм, в стартерных автомобильных ~ 2 мм
Слайд 44
Свинцовые (кислотные) аккумуляторы
Стационарные аккумуляторы используются в энергетике, на телефонных станциях, в
Они работают в режиме непрерывного подзаряда.
Значительная толщина электродных пластин (10 – 12 мм) обеспечивает их длительный срок службы (10 лет и более; 1000 – 1500 циклов).
Слайд 45
Свинцовые (кислотные) аккумуляторы
Тяговые батареи емкостью от 40 до 1200 А.ч применяют
Значительная толщина электродных пластин (10 – 12 мм) обеспечивает их длительный срок службы (10 лет и более; 1000 – 1500 циклов).
Портативные батареи применяют для питания приборов, инструмента,
аварийного освещения.
Слайд 46
Свинцовые (кислотные) аккумуляторы
Электрохимическая система :
Pb | H2SO4 | PbO2
Концентрированные растворы
Н+ и HSO4-, правильнее записывать с участием бисульфат-ионов:
(-) Pb + HSO4- ↔ PbSO4 + H+ + 2e
(+) PbO2 + HSO4- + 3 H+ + 2 e ↔ PbSO4 + 2 H2O
Суммарная токообразующая реакция:
Pb + PbO2 + 2 H2SO4 ↔ 2 PbSO4 + 2 H2O
Слайд 47
Свинцовые (кислотные) аккумуляторы
Стартерные СА состоят из следующих основных частей:
полублоков отрицательных и
межэлементных соединений;
электролита;
сепараторов;
сосуда;
крышки.
Слайд 48
Свинцовые (кислотные) аккумуляторы
Одноименные пластины соединены в полублоки с помощью баретки –
Межэлементные соединения из того же сплава служат для соединения аккумуляторов в батареи.
Батарея монтируется в моноблоке – общем сосуде из кислотостойкого материала (эбонита, полипропилена, полиамида и др.), разделенном внутри перегородками.
В качестве сепараторов применяют: микропористый эбонит (мипор): микропористый поливинилхлорид (мипласт, поровинил и т.д.), стеклянный войлок и др.
Слайд 49
Свинцовые (кислотные) аккумуляторы
Решётки из свинцовых сплавов для последующей намазки активных масс
Отливка
из
Просечная решётка
из Pb-Ca сплава
Слайд 50
Свинцовые (кислотные) аккумуляторы
Пластины соединены пайкой с помощью БАРЕТКИ.
полублок (-) пластин
полублок (+)
Слайд 51
Свинцовые (кислотные) аккумуляторы
Один из применяемых сепараторов (мипласт). Выступами обращён к плюсу.
Слайд 52
Свинцовые (кислотные) аккумуляторы
Причины выхода из строя стартерных аккумуляторов
коррозия решеток положительного электрода
Причина
Нарушается контакт решетки с активной массой; кроме того, образующийся диоксид свинца имеет больший удельный объем, чем свинец, поэтому помимо утоньшения решётки происходит и её деформация.
Слайд 53
Свинцовые (кислотные) аккумуляторы
Причины выхода из строя стартерных аккумуляторов
оплывание активной массы положительного
Это отпадение от пластин кристаллов и зерен PbO2.
Наблюдается в конце заряда.
Способствует отпадению кристаллов выделяющийся кислород.
Оплывание усиливается при пониженных температурах, при увеличенной концентрации кислоты, а также при повышенной рабочей плотности тока. В этом случае при заряде (+) электрода образуются легко осыпающиеся дендриты PbO2.
Слайд 54
Свинцовые (кислотные) аккумуляторы
Причины выхода из строя стартерных аккумуляторов
необратимая сульфатация пластин
Это образование
Аккумулятор не принимает заряд.
Причина - рекристаллизация сульфата свинца при хранении СА в разряженном состоянии.
По этой причине СА не рекомендуется хранить в разряженном состоянии: периодически его необходимо подзаряжать.
Слайд 55
Свинцовые (кислотные) аккумуляторы
Причины выхода из строя стартерных аккумуляторов
перенос сурьмы из решеток
Причина – анодное растворение сурьмяной составляющей решеток при длительном заряде с образованием ионов Sb (III) и Sb (V), их последующая диффузия к (-) электродам и катодное восстановление ионов сурьмы на (-) электроде в виде мелкодисперсного порошка (на предельном токе).
Одна из мер борьбы – замена сурьмы в решётках на кальций.