- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Процессы, формирующие качество продукции общественного питания презентация
Содержание
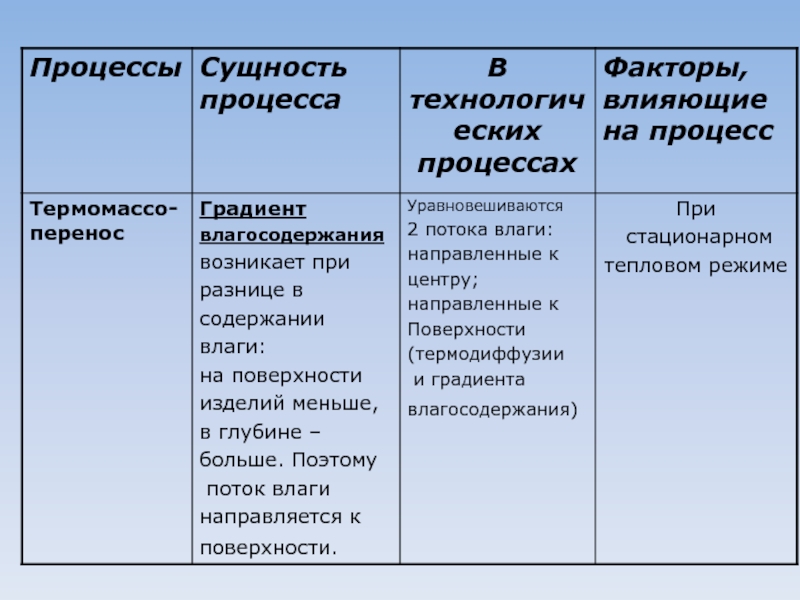
- 1. Процессы, формирующие качество продукции общественного питания
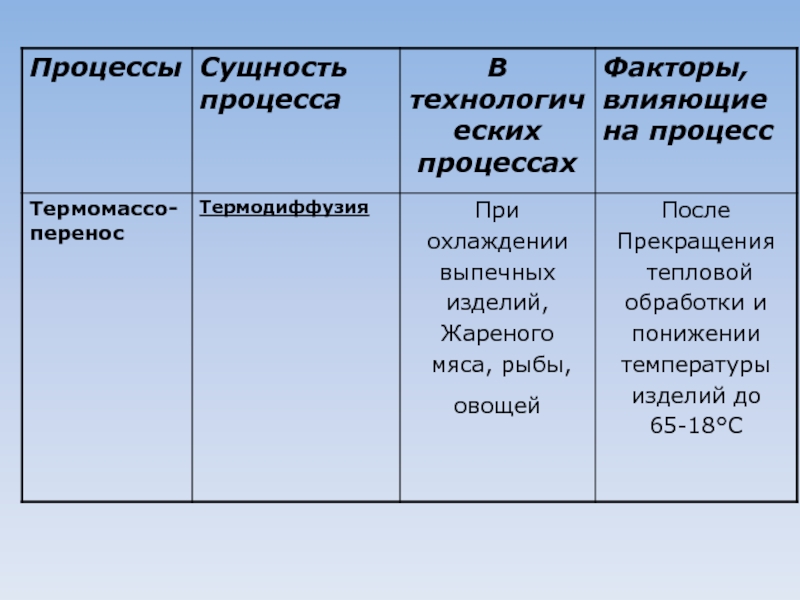
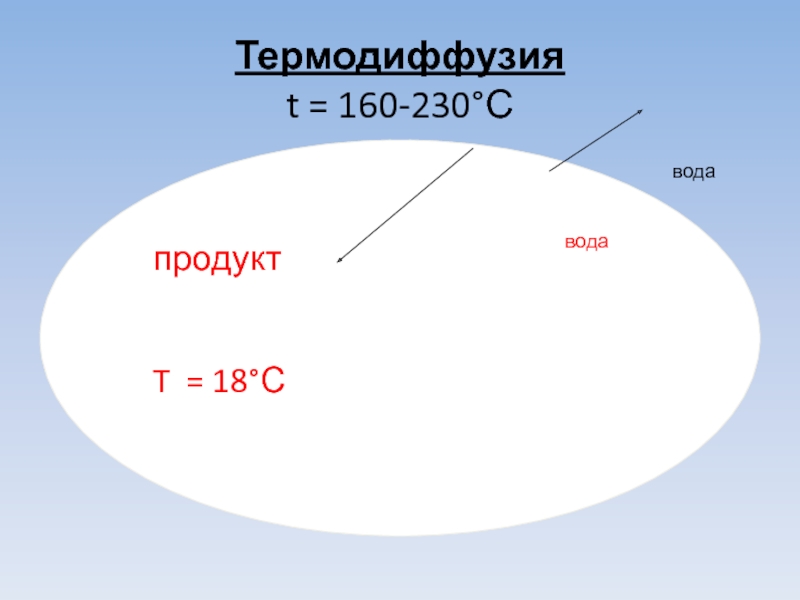
- 10. Термодиффузия t = 160-230°С
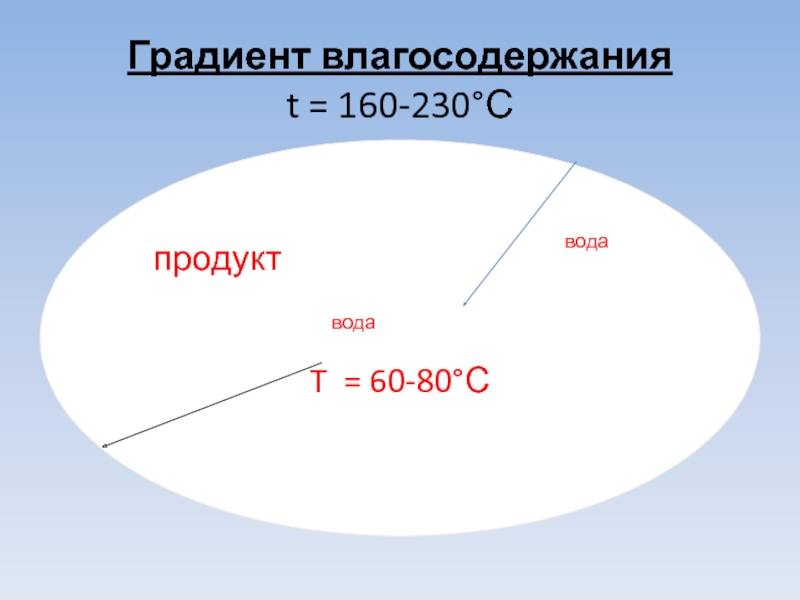
- 11. Градиент влагосодержания t = 160-230°С
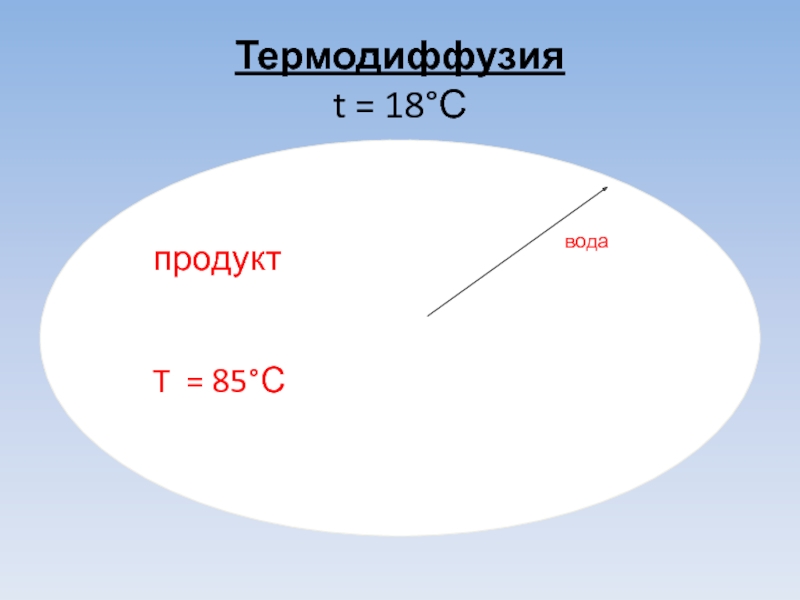
- 12. Термодиффузия t = 18°С
- 13. Тема: Изменения белков при тепловой
- 14. Что такое жизнь?
- 15. «Жизнь – есть способ существования белковых тел» Ф. Энгельс
- 16. Белки Белки – это строительный материал человеческого
- 17. Что такое белки?
- 18. Б Е Л К И
- 19. Функции белков -пластическая - гормональная -транспортная -сигнальная -защитная -регуляторная -энергетическая -сократительная -каталитическая -опорная
- 20. Незаменимые аминокислоты (НАК) лейцин триптофан изолейцин метионин валин треонин лизин фенилаланин
- 21. Химическая природа и строение белков Белки
- 22. По структуре первичная вторичная третичная четвертичная
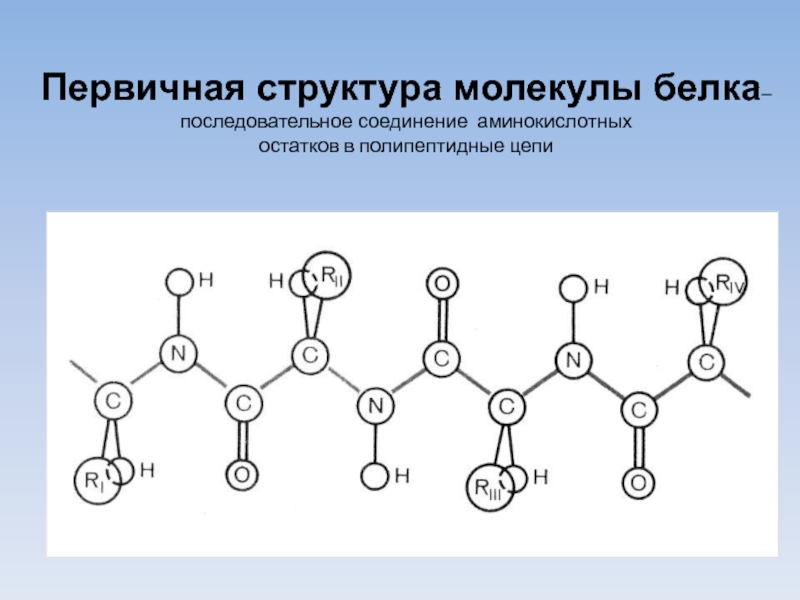
- 23. Первичная структура молекулы белка– последовательное соединение аминокислотных
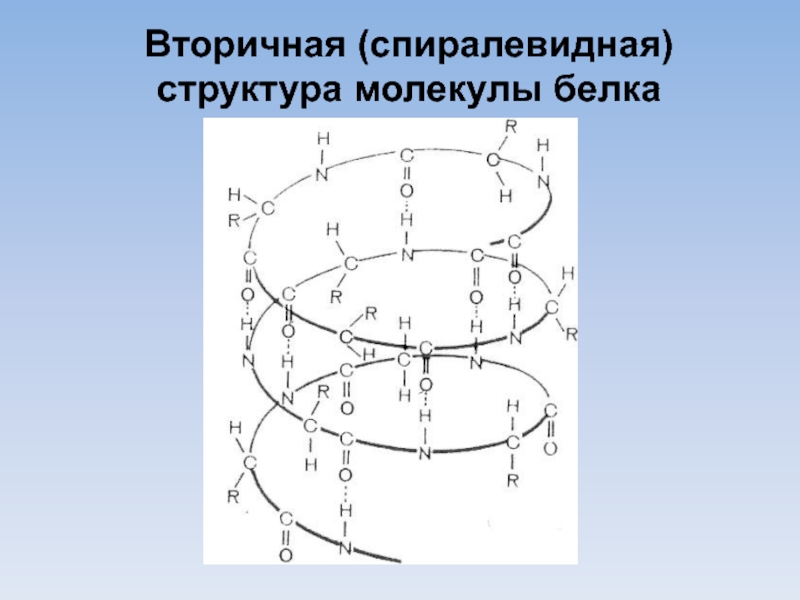
- 24. Вторичная (спиралевидная) структура молекулы белка
- 25. Третичная структура молекулы белка – свертывание полипептидной цепи в глобулу
- 26. Четвертичная структура молекулы
- 27. Технологические свойства белков -гидратация (набухание) -дегидратация -гидролиз -денатурация -пенообразование - деструкция
- 28. Дегидратация потеря белками воды при:
- 29. Гидратация присоединение белками воды при:
- 30. Денатурация изменение наживной пространственной структуры белков
- 31. Денатурация белка
- 32. Этапы денатурации белка 50-55 оС –
- 33. Агрегирование взаимодействие денатурированных молекул белка, которое
- 34. Деструкция глубокое изменение с разрушением молекул
- 36. Пенообразование связано с увеличением поверхности.
- 37. Проблемный вопрос Как влияют изменения
- 38. Проблемный вопрос Какие полуфабрикаты теряют меньше массы натуральные (эскалоп) или панированные (ромштекс)?
- 39. Домашнее задание
Слайд 1
ТЕМА:
ПРОЦЕССЫ, ФОРМИРУЮЩИЕ КАЧЕСТВО ПРОДУКЦИИ ОБЩЕСТВЕННОГО
МДК.03.01. Технология приготовления сложной горячей
Слайд 13
Тема: Изменения белков при тепловой обработке
Цель: выявить изменения
Задачи: понять сущность химических
изменений белков для создания благоприятных условий в технологии приготовления пищи
Слайд 16Белки
Белки – это строительный материал человеческого организма, источник энергии.
Повышают работоспособность органов
Суточная норма потребления белков зависит от физической нагрузки. Высокая норма потребления – 120 гр, низкая – 80 гр.
Слайд 18
Б Е Л К И
(протеины, protes – первый, важнейший)
природные полимеры
Потребность – 80-100 гр. в сутки.
Слайд 19Функции белков
-пластическая - гормональная
-транспортная -сигнальная
-защитная -регуляторная
-энергетическая -сократительная
-каталитическая -опорная
Слайд 20Незаменимые аминокислоты (НАК)
лейцин триптофан
изолейцин метионин
валин треонин
лизин фенилаланин
Слайд 21Химическая природа и строение белков
Белки
По аминокислот
ному
составу
Полноценные
Неполноценные
По строению
Простые
/протеины/
–
аминокислот
Сложные
/протеиды/– из
белковых
и небелковых
частей
По форме
молекулы
Глобулярные
(в виде шара)
Фибриллярные
( в форме волокон)
По растворимости
Растворимые
в воде, солях,
спиртах
Нерастворимые
Слайд 23Первичная структура молекулы белка– последовательное соединение аминокислотных
Слайд 27Технологические свойства белков
-гидратация (набухание)
-дегидратация
-гидролиз
-денатурация
-пенообразование
- деструкция
Слайд 28Дегидратация
потеря белками воды при:
сушке;
замораживании мяса,
рыбы, птицы, овощей;
размораживание мяса,
тепловой обработке продуктов
Слайд 29Гидратация
присоединение белками воды при:
приготовление омлетов;
добавление воды в котлетную массу
образование клейковины при изготовлении теста;
набухание круп, макарон при варке.
Слайд 30Денатурация
изменение наживной пространственной структуры белков под действием:
температуры;
кислот;
щелочей;
ультразвука;
механического
воздействия и др
потеря биологической активности (белков-ферментов при тепловой обработке, сульфитации картофеля, яблок, грибов);
повышение атакуемости пищеварительными ферментами;
потеря способности к гидратации (растворению, набуханию);
потеря устойчивости белковых глобул (свертывание, коагуляция)
Слайд 32Этапы денатурации белка
50-55 оС – в белке проявляются местные
55-60 оС – помутнение распространяется на весь белок
60-65 оС – белок заметно густеет
65-75 оС – образуется студнеобразная нежная масса
75-85 оС – студень уплотняется, хорошо сохраняет форму
85-95 оС – постепенное уплотнение студня
Слайд 33Агрегирование
взаимодействие денатурированных молекул белка, которое сопровождается образованием более крупных частиц
в
в концентрированных (белки яиц) образуется сплошной гель
в обводненных гелях (мышечные белки мяса, птицы, рыбы) уплотняются, дегидратируют, отделяют жидкость в окружающую среду
Слайд 34Деструкция
глубокое изменение с разрушением молекул
1-й этап – образуются аммиак, сера,
2-й этап – гидролиз, образование растворимых азотистых веществ (коллаген → глютин)
Слайд 35
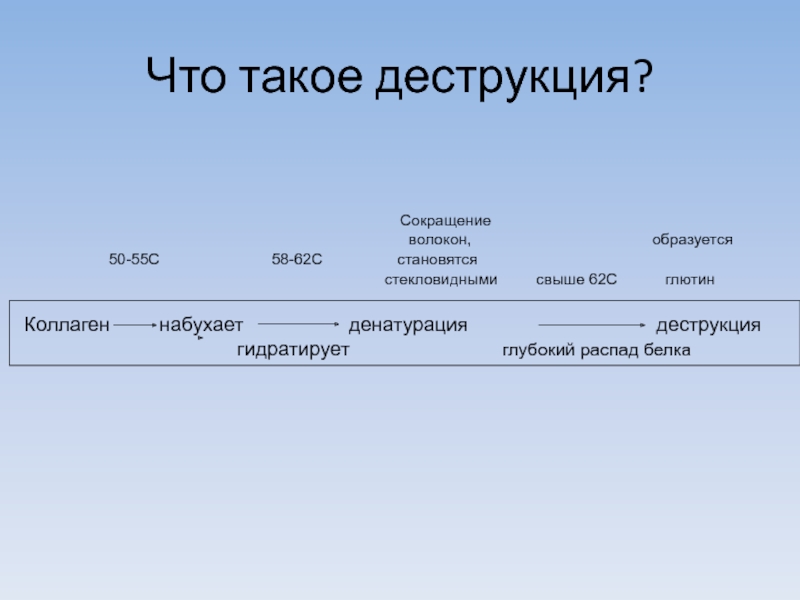
Сокращение
волокон, образуется
50-55С 58-62С становятся
стекловидными свыше 62С глютин
Коллаген набухает денатурация деструкция
гидратирует глубокий распад белка
Что такое деструкция?
Слайд 36Пенообразование
связано с увеличением поверхности.
При взбивании растягиваются пленки белка
Пены характеризуются 2-мя показателями: кратностью и стойкостью.
Кратность – отношения объема пены к жидкой фазе.
Стойкость – время полураспада пены при ее хранении.
Объем газовой фазы – 74% - пена устойчива.(При повышении этого процента пена лопается, изделия оседают).
взбивание белков, сметаны, сливок, бисквитного теста, белкового теста
При взбивании белков соблюдают
следующие правила:
- яйца охлаждают до 5-120С;
- тщательно отделяют белки от желтков;
- посуда и инвентарь должны быть чистые и охлажденные;
- сначала взбивание производят на медленном ходу, постепенно скорость вращения венчика увеличивают.
- добавляют 2-3 капли лимонной кислоты;
- взбивают до увеличения объема белков в 5-8 раз, консистенция белков должна быть пышная, устойчивая к оседанию, удерживается на венчике.
Слайд 37Проблемный вопрос
Как влияют изменения белков на качество готовой продукции
Слайд 38Проблемный вопрос
Какие полуфабрикаты теряют меньше массы натуральные (эскалоп) или
Слайд 39
Домашнее задание
Изучить тему.
Ковалев Н.И. «Технология
Решить задачу: рассчитать потери при тепловой обработке эскалопа, если масса полуфабриката – 125 г, масса жареного – 85 г. Выразить потери в %. Сравнить результат с таблицей № 8 стр. 406-411. Объяснить причины потерь. От каких факторов зависят?
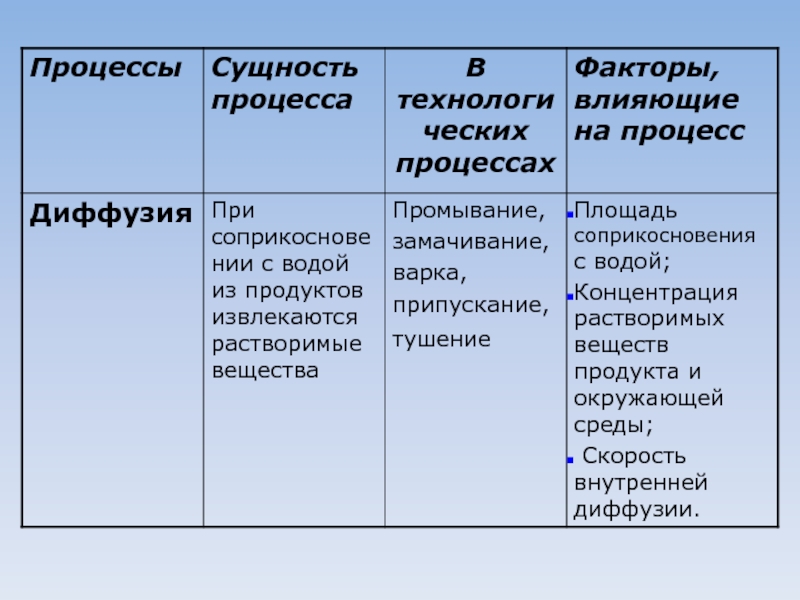
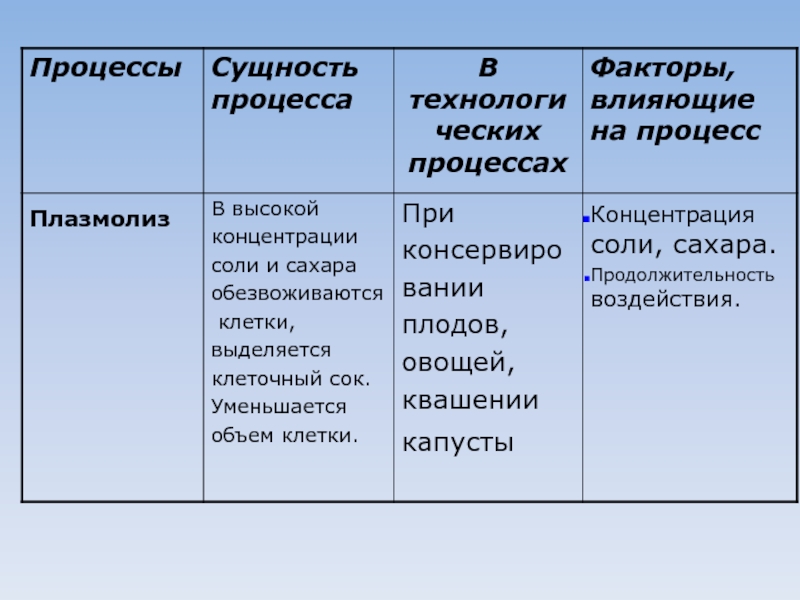
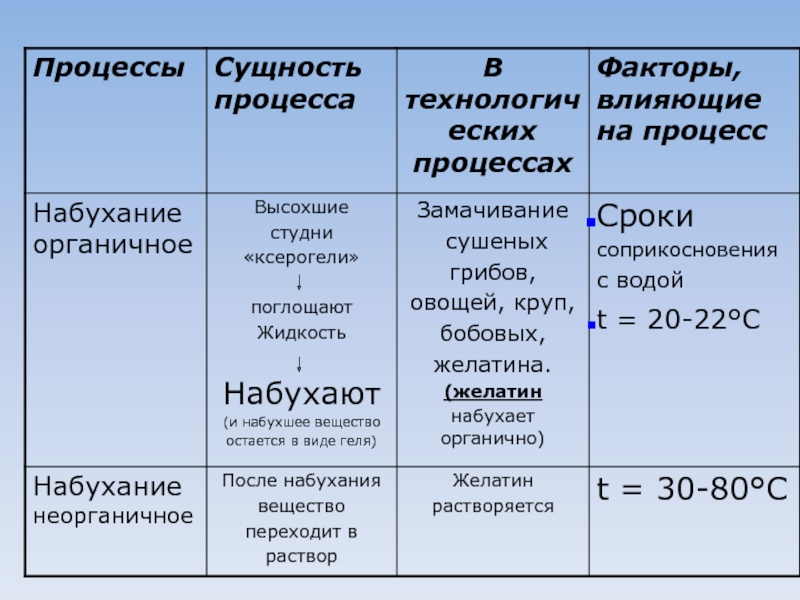
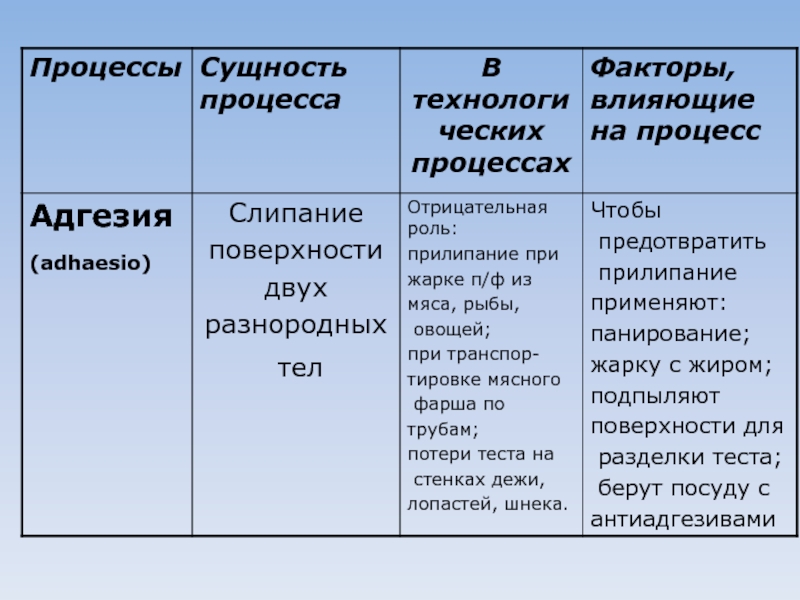
Пивести примеры из кулинарной практики по процессам: диффузия, осмос, набухание, адгезия,
термомассоперенос.
Подготовить доклады:
- Формирование вкуса и аромата.
- Сохранение витаминной ценности
- Изменение цвета.