- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Структура нуклеиновых кислот и белков презентация
Содержание
- 1. Структура нуклеиновых кислот и белков
- 3. Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых
- 4. Нуклеотиды соединяются друг с другом в полимерную
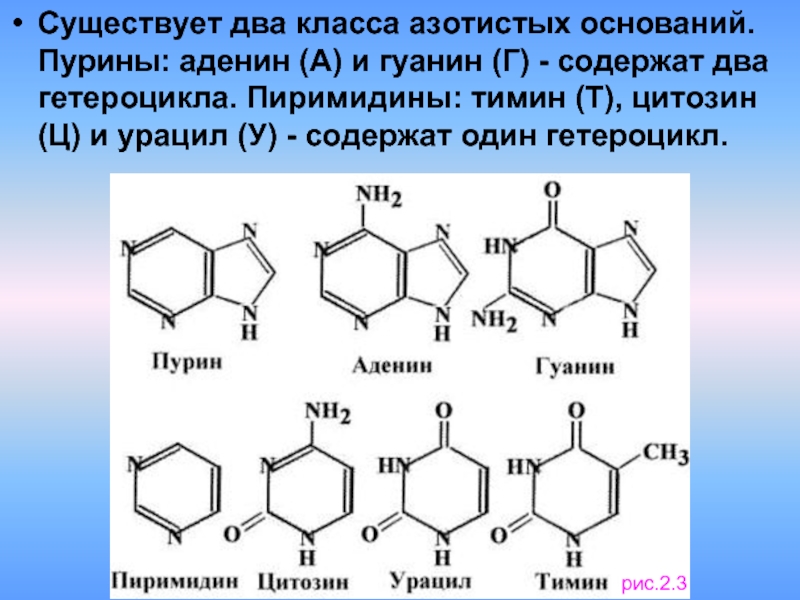
- 5. Существует два класса азотистых оснований. Пурины: аденин
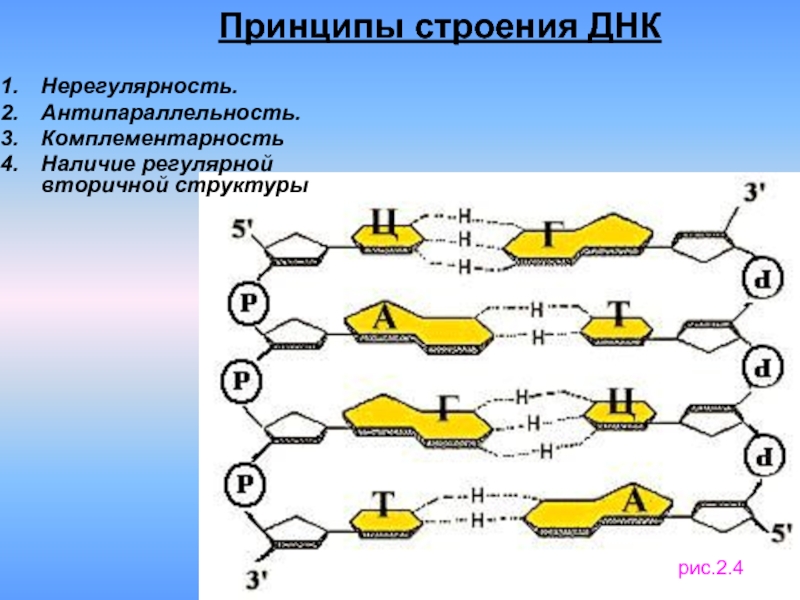
- 6. Принципы строения ДНК Нерегулярность. Антипараллельность.
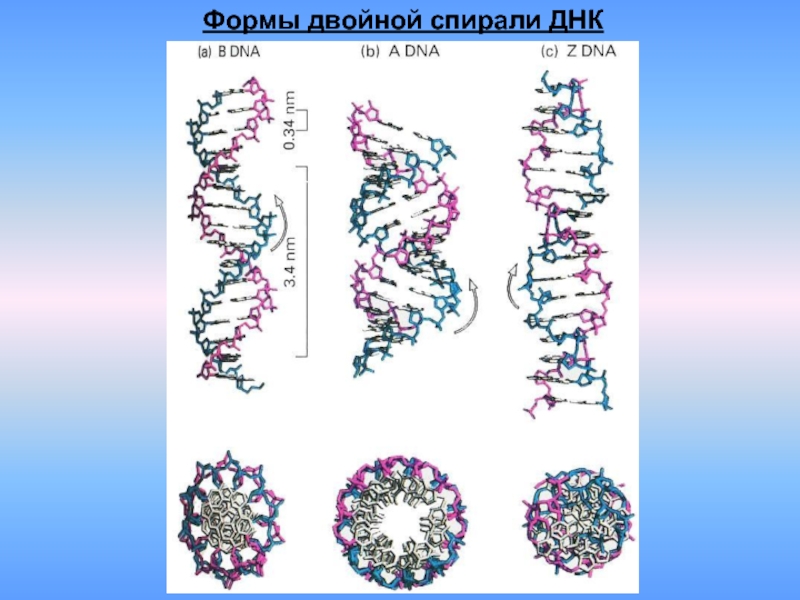
- 7. Формы двойной спирали ДНК
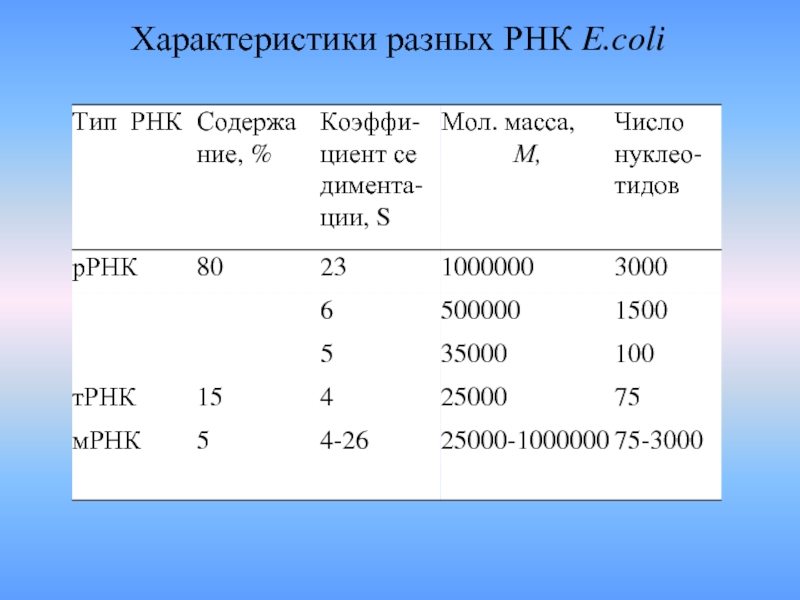
- 8. Характеристики разных РНК E.coli
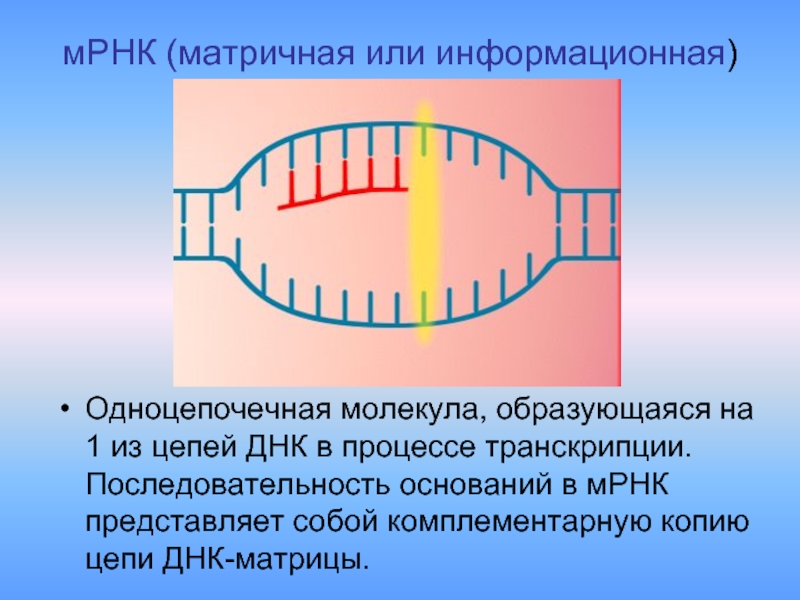
- 9. мРНК (матричная или информационная) Одноцепочечная молекула, образующаяся
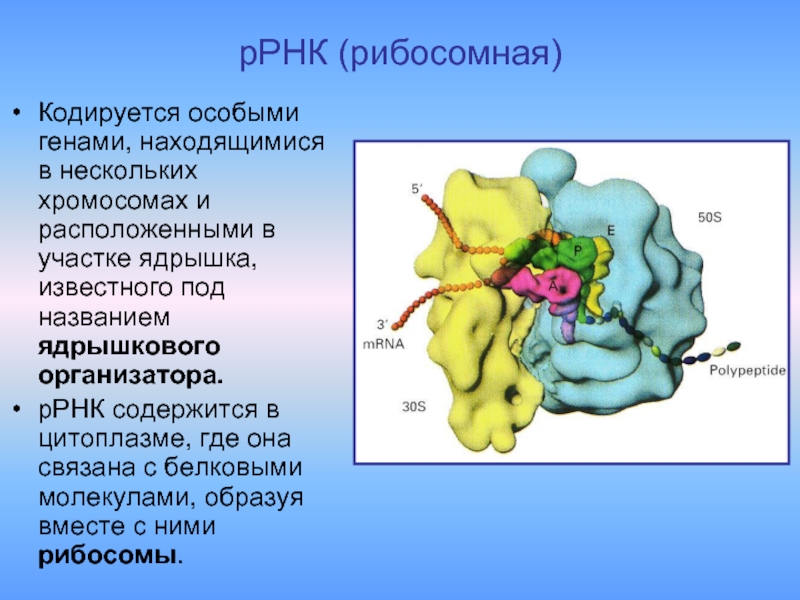
- 10. рРНК (рибосомная) Кодируется особыми генами, находящимися в
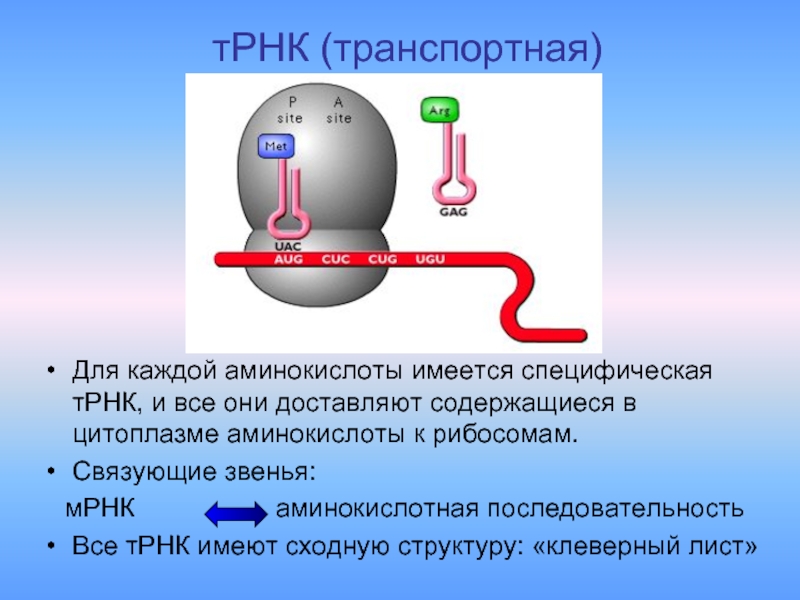
- 11. тРНК (транспортная) Для каждой аминокислоты имеется специфическая
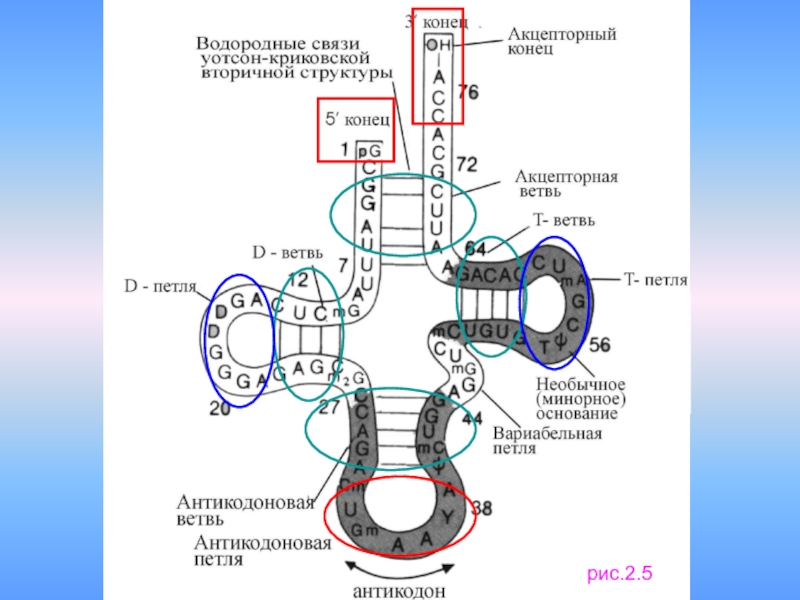
- 12. рис.2.5
- 13. рис.2.6
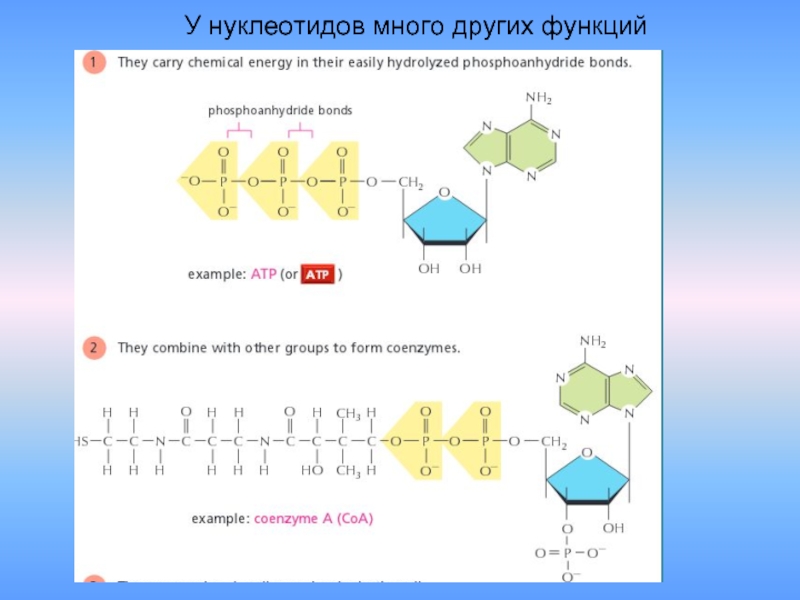
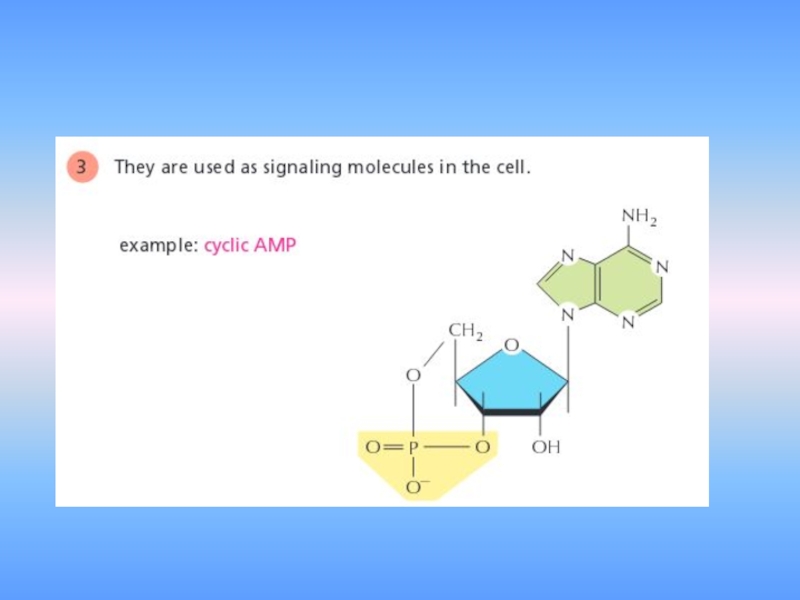
- 14. У нуклеотидов много других функций
- 16. 2. Структура белков Определение: белки -
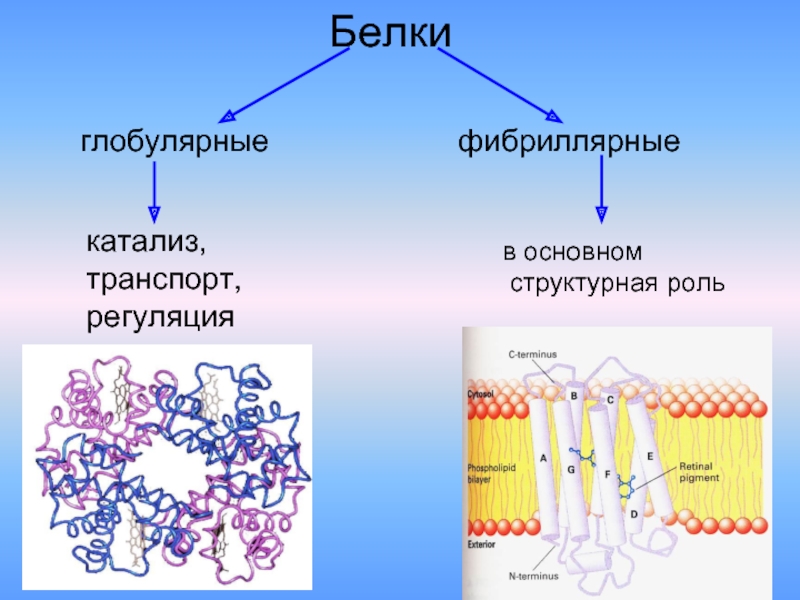
- 17. Белки глобулярные катализ, транспорт, регуляция фибриллярные в основном структурная роль
- 18. Первичная структура белка Определение: первичная структура
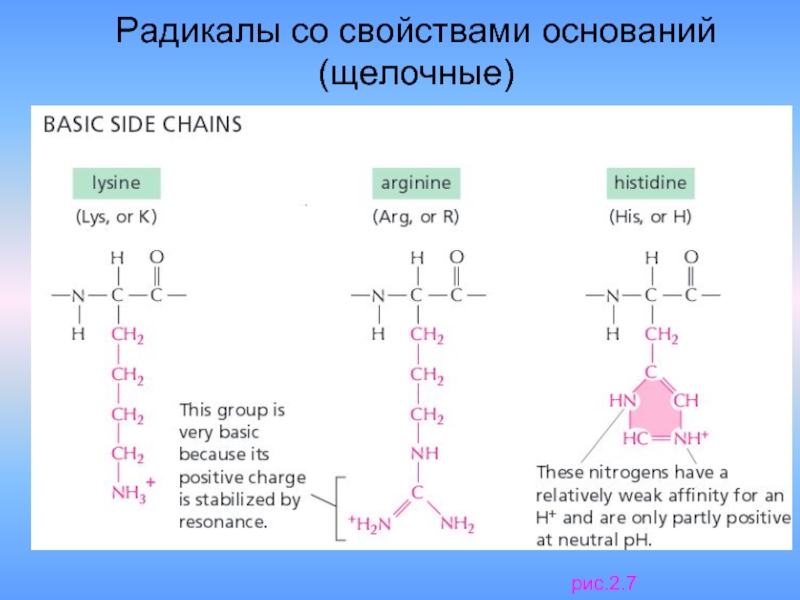
- 19. Радикалы со свойствами оснований (щелочные) рис.2.7
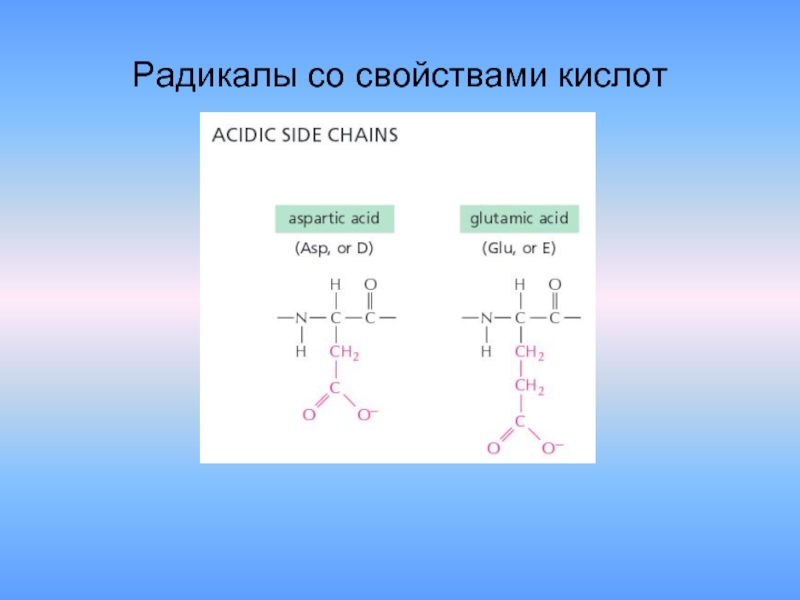
- 20. Радикалы со свойствами кислот
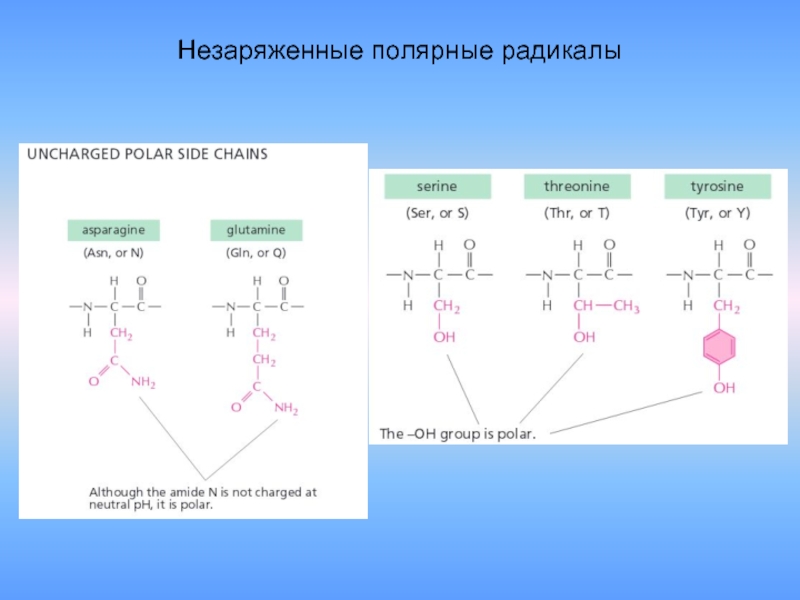
- 21. Незаряженные полярные радикалы
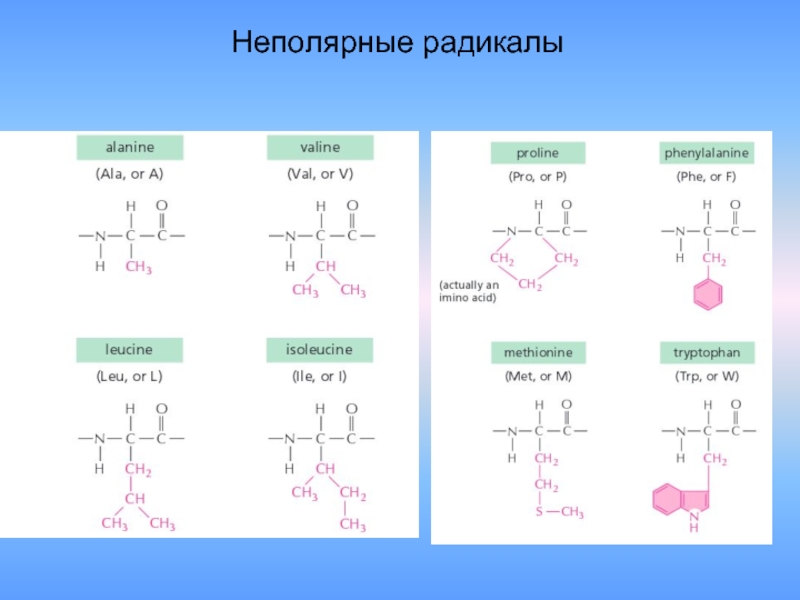
- 22. Неполярные радикалы
- 23. Неполярные радикалы
- 24. Расшифровка первичной структуры белка Ф. Сангер, 1953г.
- 25. Серповидно-клеточная анемия точечная мутация - замена Glu
- 26. Вторичная структура белка Определение: Вторичная структура
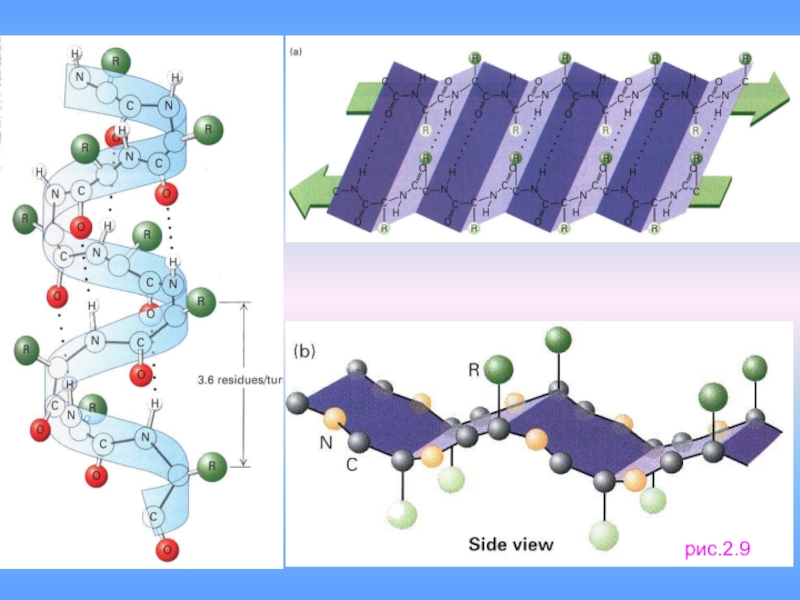
- 27. рис.2.9
- 28. Вторичная структура белка
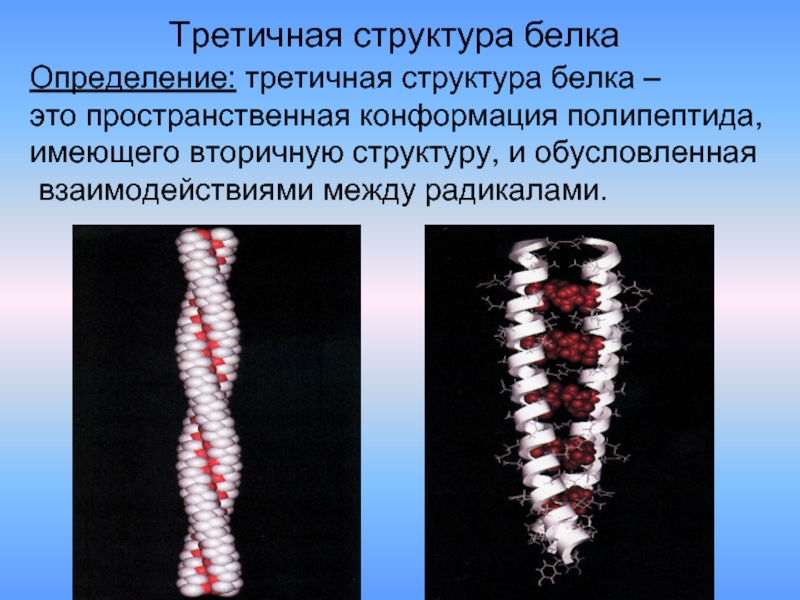
- 29. Третичная структура белка Определение: третичная структура
- 30. Существует четыре типа взаимодействий между радикалами: Ковалентные
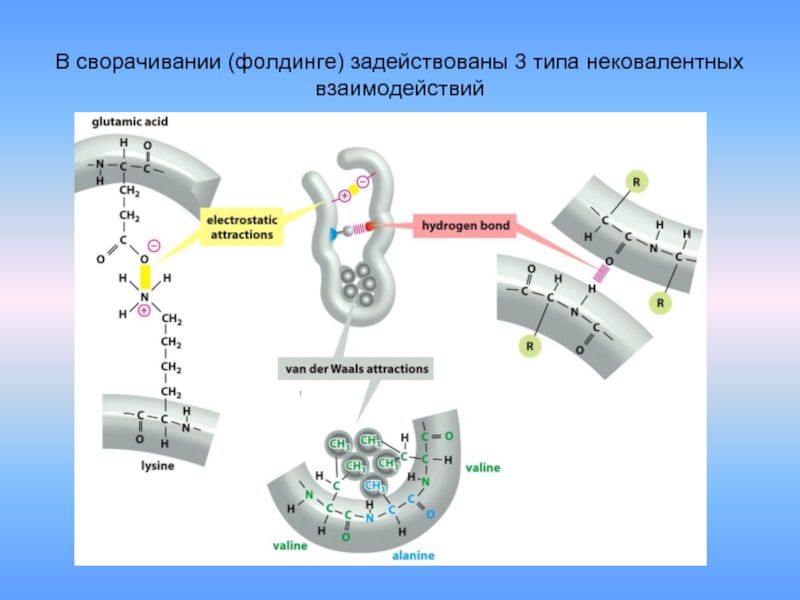
- 31. В сворачивании (фолдинге) задействованы 3 типа нековалентных взаимодействий
- 32. Гидрофобные взаимодействия способствуют укладке белков в компактные конформации
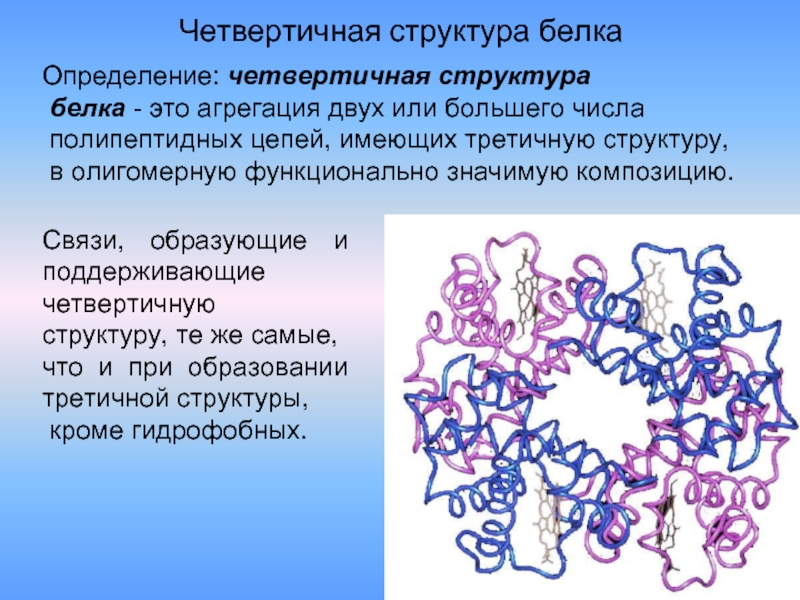
- 33. Четвертичная структура белка Определение: четвертичная структура
- 34. Определение: Белок - это отдельный полипептид
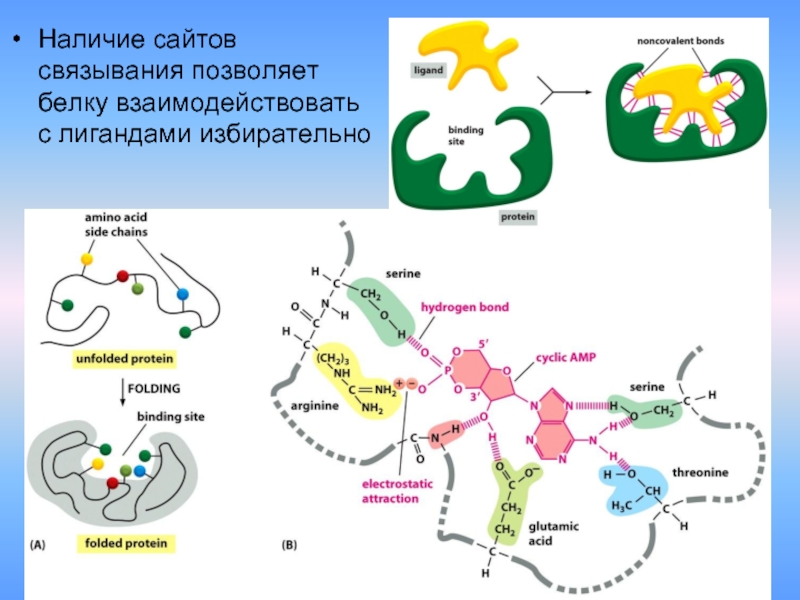
- 35. Наличие сайтов связывания позволяет белку взаимодействовать с лигандами избирательно
- 36. Функции белков 1. Структурная функция 2.
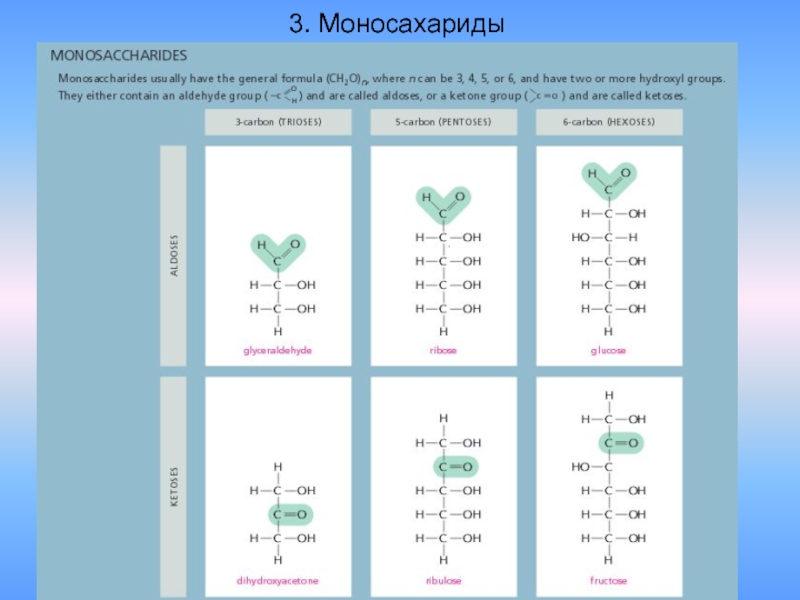
- 37. 3. Моносахариды
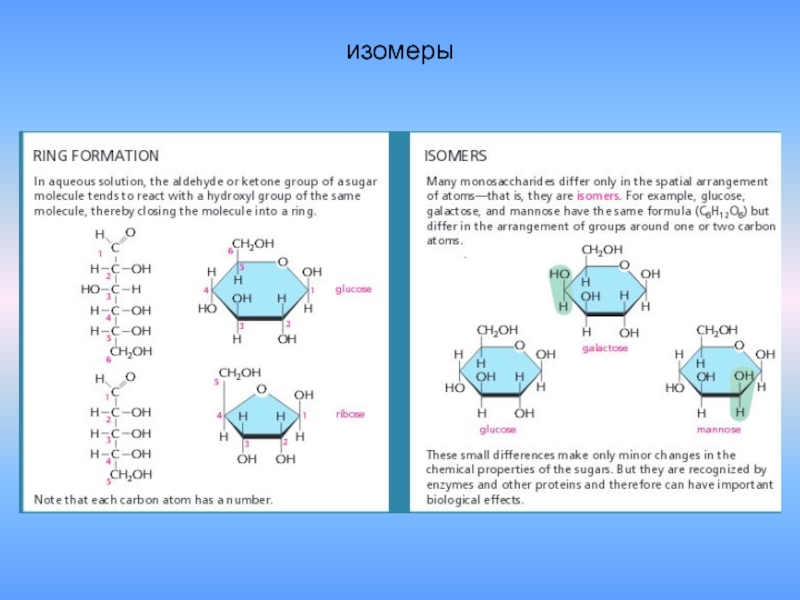
- 38. изомеры
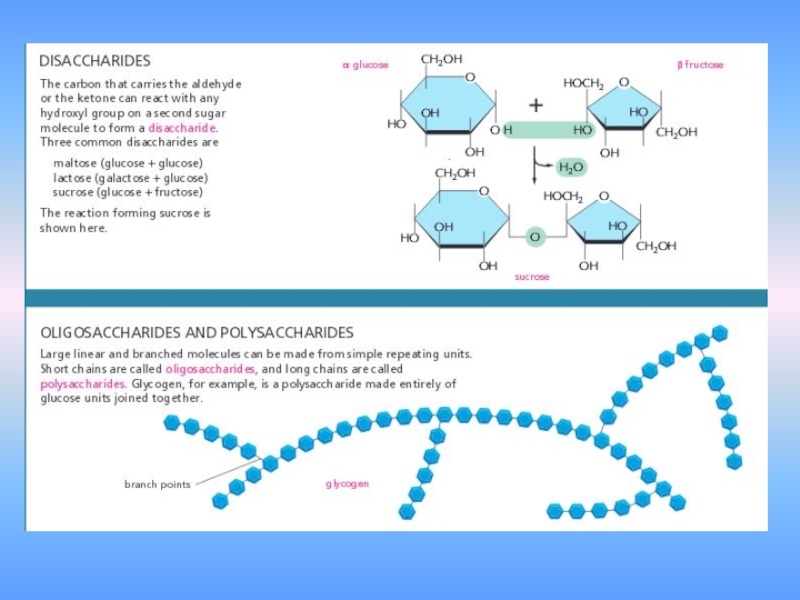
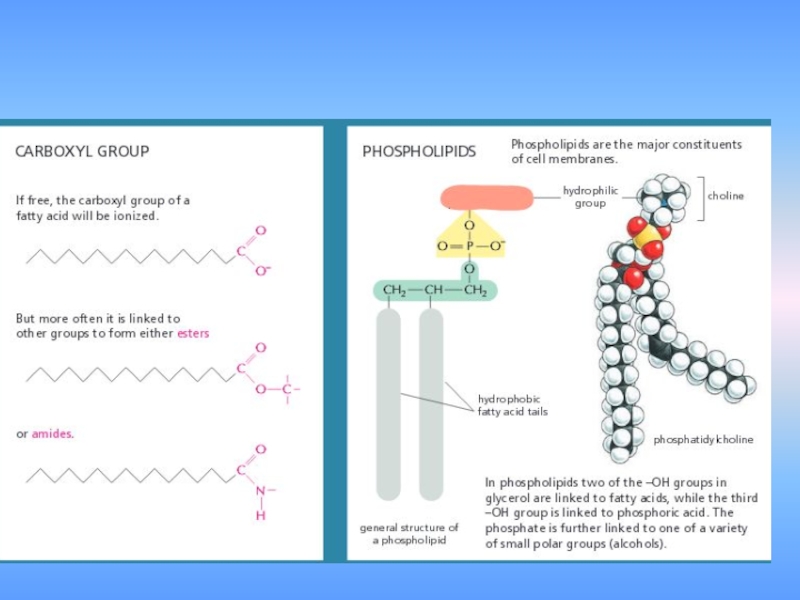
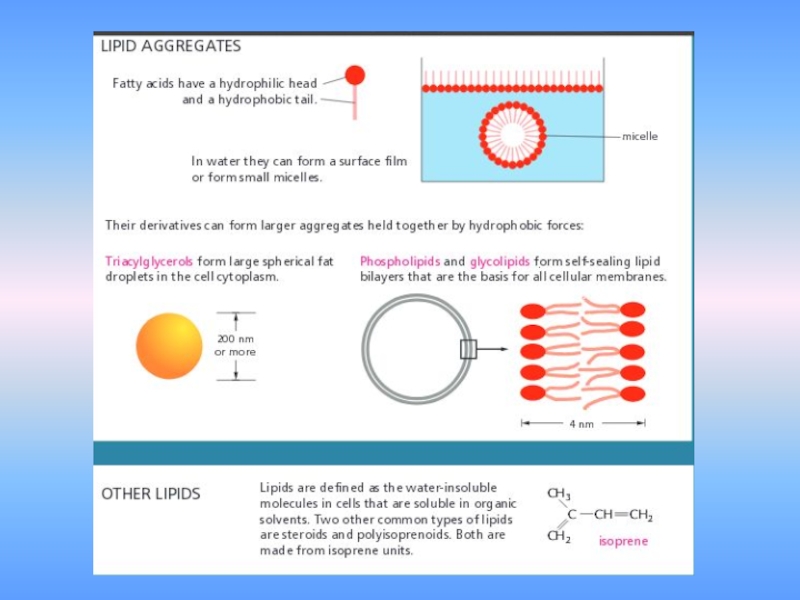
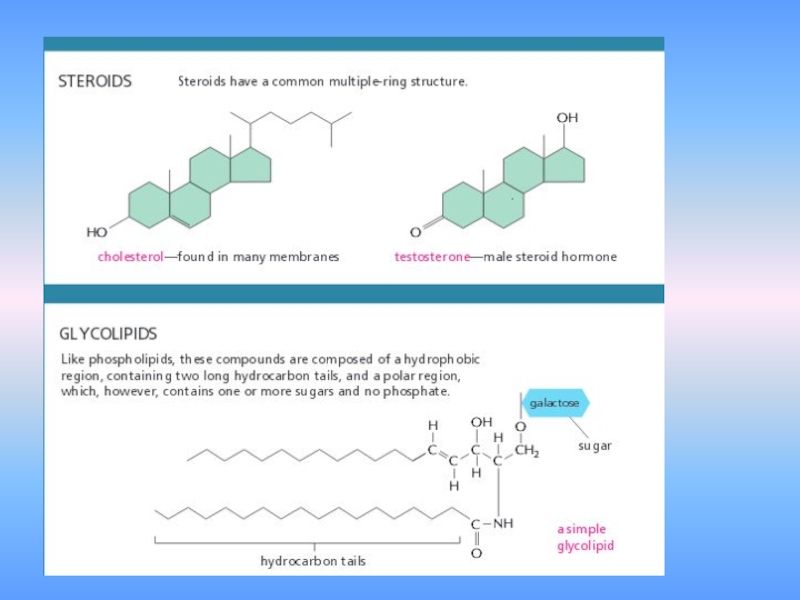
- 40. 4. жирные кислоты и другие липиды
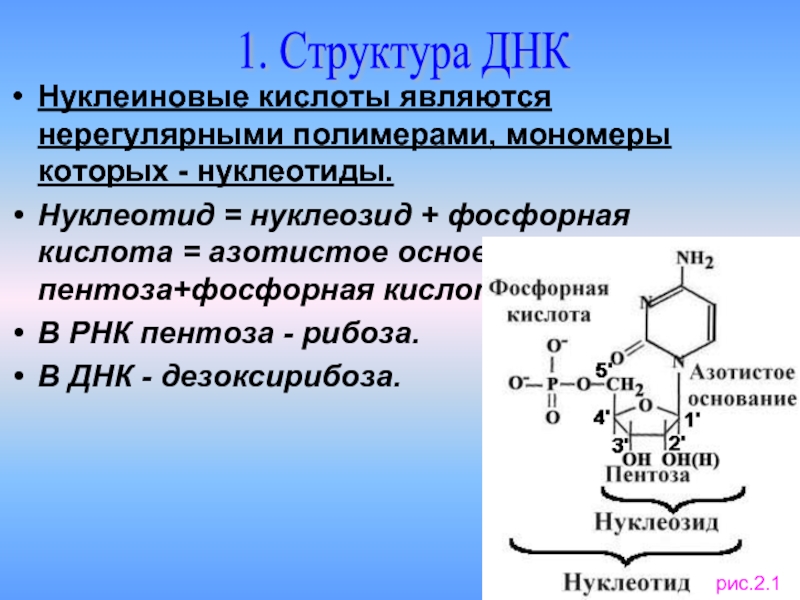
Слайд 3Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды.
Нуклеотид = нуклеозид
В РНК пентоза - рибоза.
В ДНК - дезоксирибоза.
Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды.
1. Структура ДНК
рис.2.1
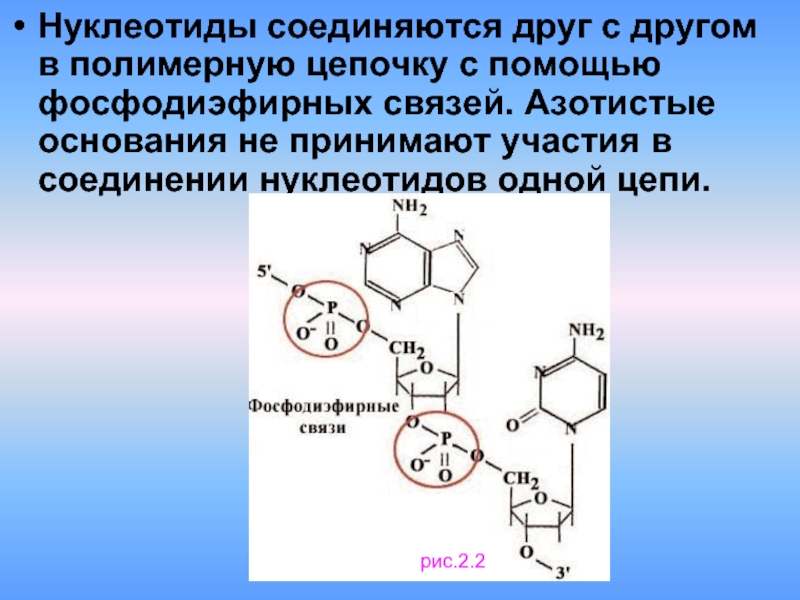
Слайд 4Нуклеотиды соединяются друг с другом в полимерную цепочку с помощью фосфодиэфирных
рис.2.2
Слайд 5Существует два класса азотистых оснований. Пурины: аденин (А) и гуанин (Г)
рис.2.3
Слайд 6Принципы строения ДНК
Нерегулярность.
Антипараллельность.
Комплементарность
Наличие регулярной вторичной структуры
рис.2.4
Слайд 9мРНК (матричная или информационная)
Одноцепочечная молекула, образующаяся на 1 из цепей ДНК
Слайд 10рРНК (рибосомная)
Кодируется особыми генами, находящимися в нескольких хромосомах и расположенными в
рРНК содержится в цитоплазме, где она связана с белковыми молекулами, образуя вместе с ними рибосомы.
Слайд 11тРНК (транспортная)
Для каждой аминокислоты имеется специфическая тРНК, и все они доставляют
Связующие звенья:
мРНК аминокислотная последовательность
Все тРНК имеют сходную структуру: «клеверный лист»
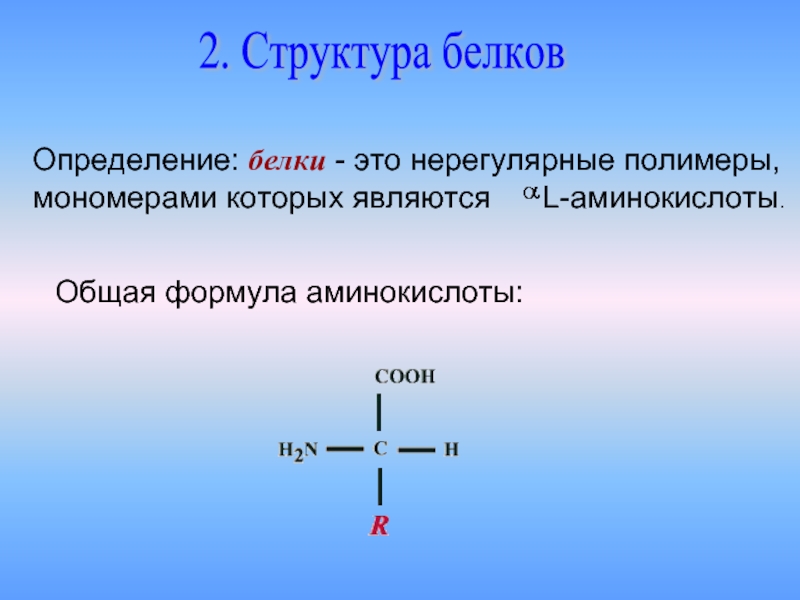
Слайд 162. Структура белков
Определение: белки - это нерегулярные полимеры,
мономерами которых
Общая формула аминокислоты:
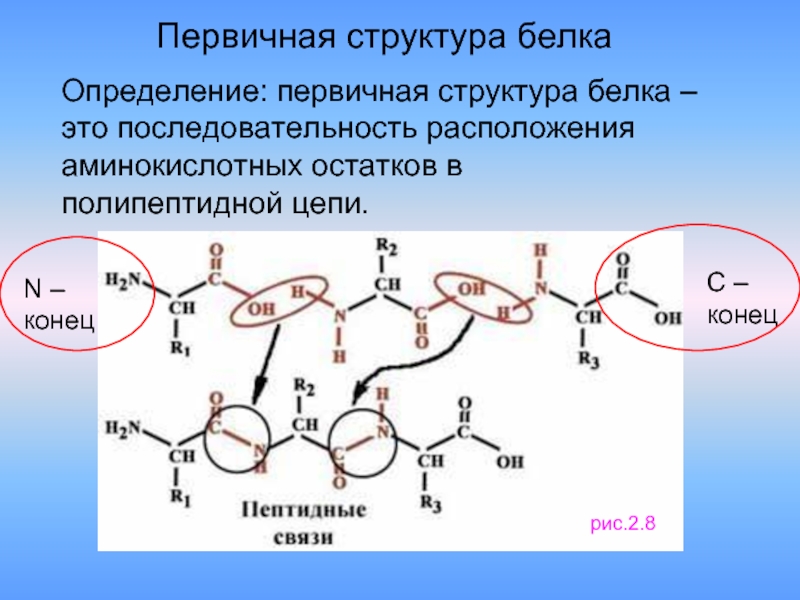
Слайд 18Первичная структура белка
Определение: первичная структура белка –
это последовательность расположения
аминокислотных остатков в
полипептидной цепи.
N –
конец
C –
конец
рис.2.8
Слайд 24Расшифровка первичной структуры белка
Ф. Сангер, 1953г. – аминокислотная последовательность инсулина
секвенирование
анализ нуклеотидной
сопоставление первичных структур нормального и аномального белков позволяют раскрыть основы патологических процессов, включая широко распространенные генетически детерминированные заболевания.
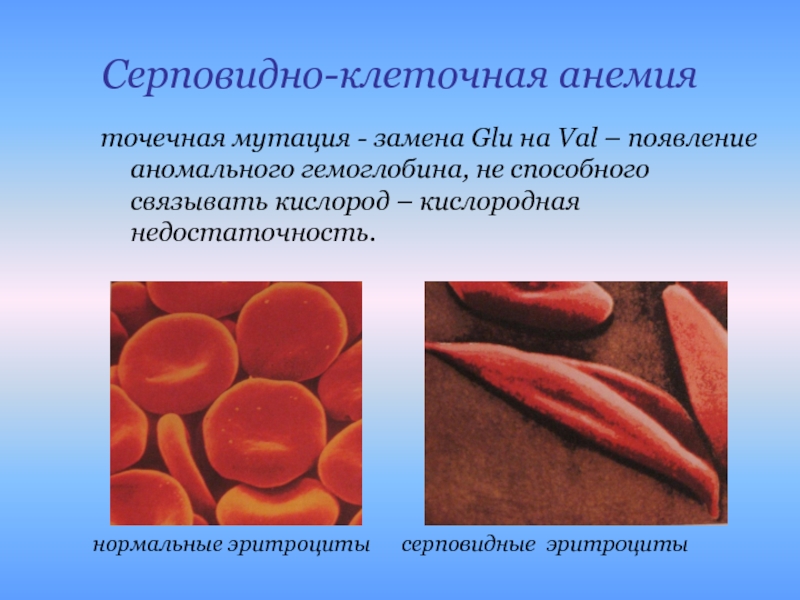
Слайд 25Серповидно-клеточная анемия
точечная мутация - замена Glu на Val – появление аномального
нормальные эритроциты
серповидные эритроциты
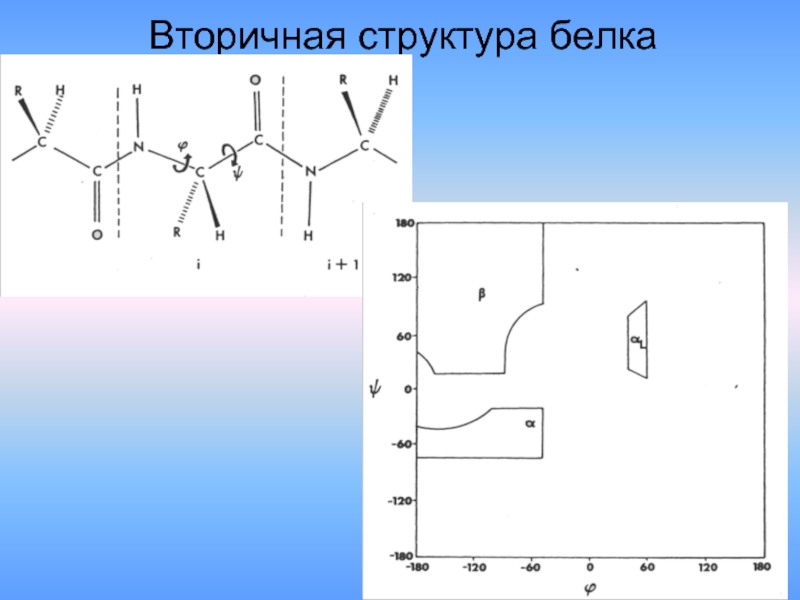
Слайд 26Вторичная структура белка
Определение: Вторичная структура белка –
это упорядоченное строение
обусловленное водородными связями между
группами С=О и N-H разных аминокислот.
Вторичная структура может быть регулярной
- спиралью и нерегулярной -складчатой
структурой. В -спирали NH группа n-ого
аминокислотного остатка взаимодействует с С=О
группой (n-4)-ого аминокислотного остатка.
На один виток -спирали с диаметром 10.1 A
приходится 3,6 аминокислотных остатков.
Период идентичности регулярной -спирали –
18 аминокислот (5 витков). Нарушителем
регулярной a-спирали в первую очередь является
пролин. Второе по значению влияние
оказывают одинаково заряженные, рядом
расположенные радикалы.
Слайд 29Третичная структура белка
Определение: третичная структура белка –
это пространственная конформация
имеющего вторичную структуру, и обусловленная
взаимодействиями между радикалами.
Слайд 30Существует четыре типа взаимодействий между радикалами:
Ковалентные связи между остатками
двух цистеинов(дисульфидные
2. Ионные (электростатические) взаимодействия
между противоположно заряженными аминокислотными
остатками (три радикала со знаком "+" и два со знаком "-").
3. Водородные связи.
Участвуют все аминокислоты, имеющие гидроксильные,
амидные или карбоксильные группы.
4. Гидрофобные взаимодействия .
Образуются между неполярными радикалами
в водной среде. Участвуют 8 аминокислот
(первый класс).
Слайд 33Четвертичная структура белка
Определение: четвертичная структура
белка - это агрегация двух
полипептидных цепей, имеющих третичную структуру,
в олигомерную функционально значимую композицию.
Связи, образующие и поддерживающие
четвертичную структуру, те же самые,
что и при образовании третичной структуры,
кроме гидрофобных.
Слайд 34Определение: Белок - это отдельный полипептид
или агрегат нескольких полипептидов, выполняющий
Полипептид - понятие химическое.
Белок - понятие биологическое.
Например, иммуноглобулин состоит из четырех полипептидных цепей, которые по отдельности не являются белками, белок - только их функциональный
агрегат.
Слайд 36Функции белков
1. Структурная функция
2. Каталитическая функция.
3. Защитная функция (пока уникальна).
4. Регуляторная функция.
5. Трансформация энергии.
6. Транспортная функция.
7. Энергетическая функция.
8. Питательная функция.
9. Буферная функция.