- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Радиационная биофизика. Детерминированные и стохастические, соматические и генетические эффекты облучения. (Лекция 3) презентация
Содержание
- 1. Радиационная биофизика. Детерминированные и стохастические, соматические и генетические эффекты облучения. (Лекция 3)
- 2. Детерминированные и стохастические, соматические и генетические эффекты облучения
- 3. Детерминированные и стохастические эффекты облучения. Определения Детерминированные
- 4. Детерминированные эффекты облучения. Примеры Детерминированные эффекты облучения
- 5. Стохастические эффекты облучения. Примеры Стохастические эффекты облучения
- 6. Соматические и генетические эффекты облучения. Определения Соматические
- 7. Как соотносятся между собой детерминированные и стохастические, соматические и генетические эффекты
- 8. Генетические эффекты облучения у человека До настоящего
- 9. Дозовые кривые выживаемости клеток. Теория мишени. Радиочувствительность разных стадий клеточного цикла
- 10. Кривые выживаемости клеток Кривые выживаемости культивируемых клеток
- 11. Какие клетки считаются выжившими? Выжившими считаются клетки,
- 12. Сравнение кривых выживаемости клеток при действии ядов
- 13. Кривая выживаемости клеток при действии ядов Кривые
- 14. Форма кривых выживаемости клеток при действии излучения
- 15. Теория «точечного тепла». Основные положения В основе
- 16. Форма кривых выживаемости клеток при действии излучения
- 17. Фридрих Дессауэр (Friedrich Dessauer, 1881-1963) – известный
- 18. Два фундаментальных положения в радиобиологии В 20‑30‑е
- 19. Принцип попадания Принцип попадания может быть сформулирован
- 20. Принцип мишени Принцип мишени может быть сформулирован
- 21. Мишени: какие они могут быть и сколько
- 22. Простейшие модели, описывающие кривые выживаемости Для описания
- 23. Имеет ли смысл использовать более сложные
- 24. Одноударная-многомишенная модель — чисто формальное использование На
- 25. Одноударная-многомишенная кривая (1) Исходные допущения для одноударной-многомишенной
- 26. Одноударная-многомишенная кривая (2) преобразуется в следующее: После
- 27. Одноударная-одномишенная кривая – частный случай одноударной-многомишенной кривой
- 28. Параметры, характеризующие кривые выживаемости с «плечом»
- 29. Взаимосвязь D0, Dq и n Параметры
- 30. Параметры, характеризующие кривые выживаемости без «плеча»
- 31. Форма кривой выживаемости клеток Итак, в общем
- 32. О чем говорит наличие плеча и величина
- 33. От чего зависит наличие «плеча» на кривых
- 34. Зависимость наличия «плеча» от вида ионизирующего излучения
- 35. Зависимость наличия плеча от облучаемого объекта
- 36. Молекулы ДНК – основная клеточная мишень для
- 37. Радиочувствительность разных стадий клеточного цикла
- 38. Клеточный цикл Пролиферирующие клетки эукариот в своем
- 39. Интерфаза S-фаза (от слова synthesis – синтез)
- 40. Продолжительность фаз клеточного цикла Митоз – наиболее
- 41. Продолжительность фаз клеточного цикла у 2-х часто
- 42. G0-фаза В медленно обновляющихся тканях большинство
- 43. Синхронизация клеток Обычная популяция пролиферирующих клеток
- 44. Радиочувствительность клеток на разных стадиях клеточного цикла
- 45. Исключения из общих закономерностей Описанные выше закономерности
- 46. Кривые выживаемости клеток на разных стадиях клеточного
- 47. Как сильно различается выживаемость клеток, облученных на
- 48. Вызванное облучением перераспределение клеток между фазами клеточного
- 49. Прямое и непрямое (косвенное) действие ионизирующих излучений. Радиолиз воды. Антиоксидантные защитные системы
- 50. Теория мишени - так ли всё в
- 51. В начале 1940-х гг. Уолтер Дейл (Walter
- 52. Прямое и непрямое (косвенное) действие ионизирующих излучений
- 53. При прямом действии излучения с ростом концентрации
- 54. При непрямом действии излучения лимитирующим параметром для
- 55. Непрямое действие преобладает только в разбавленных
- 56. Сравнение радиационных эффектов при облучении макромолекул
- 57. Обычно в растворенном в воде состоянии макромолекулы
- 58. Представления о вкладе непрямого действия излучения в
- 59. Рассмотрим теперь основные активные продукты, образующиеся при
- 60. Радиолиз воды (1) I. Если энергия кванта
- 61. Образовавшийся электрон может также стабилизироваться до относительно
- 62. Что такое свободные радикалы? Свободные радикалы
- 63. II. Если энергия кванта ионизирующего излучения менее
- 64. Вторичные продукты радиолиза воды, образовавшиеся при
- 65. В области рН от 3 до 10
- 66. При наличии в воде растворенного кислорода O2
- 67. В целом, наибольшее биологическое значение имеют следующие
- 68. Как видно из вышеприведенной схемы, среди основных
- 69. Продукты радиолиза воды могут диффундировать от места
- 70. Образовавшиеся в этих реакциях свободные радикалы биомолекул
- 71. Продукты радиолиза воды не являются чем-то необычным
- 72. Важность антиоксидантных систем Для предотвращения избыточного
- 73. В клетках можно выделить 3 уровня эндогенных
- 74. Антиоксидантные системы Ферментативные (белковые) антиоксидантные системы Низкомолекулярные
- 75. Общая схема взаимных превращений АФК
- 76. Низкомолекулярные антиоксиданты Одним из механизмов антиокислительного действия
- 77. Полиморфизм супероксиддисмутазы СОД Mn-СОД (в матриксе митохондрий)
- 78. Церулоплазмин Транспорт и запасание меди в организме
- 79. Каталаза Катализирует превращение перекиси водорода в воду:
- 80. Глутатионпероксидаза (GPx) Глутатионпероксидаза является одним из важнейших
- 81. Глутатионпероксидаза (GPx) осуществляет детоксикацию перекиси водорода
- 82. Селен-содержащие GPx Неселеновые GPx (глутатион-S-трансферазы
- 83. Глутатиопероксидаза гидроперекисей фосфолипидов (PhGPx) PhGPx (в отличие
- 84. Восстановленный глутатион – важнейший компонент антиоксидантной защиты
- 85. Основные функции глутатиона в клетке
- 86. Восстановленный глутатион – важнейший небелковый тиол в
- 87. Гемоксигеназа NADPH NADP+ O2 CO Fe2+ Heme
- 88. Полиморфизм гемоксигеназы
- 89. Почему гемоксигеназу относят к антиоксидантным ферментам? Для
- 90. Гем и его основные функции в организме
- 91. Свободный гем – сильный прооксидант Время жизни
- 92. Биливердин превращается в билирубин Biliverdin NADPH NADP+
- 93. Гемоксигеназа – антиоксидантный фермент Таким образом, гемоксигеназа
- 94. Внутриклеточная локализация основных антиоксидантных ферментов Catalase
Слайд 3Детерминированные и стохастические эффекты облучения. Определения
Детерминированные (нестохастические) эффекты облучения (детерминированный –
Стохастические эффекты облучения (стохастический – случайный, вероятностный; от греч. stochastikós – умеющий угадывать) – биологические эффекты, вызванные ионизирующим излучением в облученном организме или его потомстве, не имеющие дозового порога возникновения, вероятность появления которых увеличивается при повышении доз, а тяжесть проявления не зависит от дозы.
Слайд 4Детерминированные эффекты облучения. Примеры
Детерминированные эффекты облучения возникают, главным образом, в результате
К ним относятся, в частности, непосредственные проявления острого лучевого поражения, радиационные синдромы, нарушение репродуктивной функции, поражение кожи, возникновение катаракты.
Наблюдаются в основном в ближайшие сроки после облучения, реже – в отдаленные сроки (например, катаракта).
Порог для разных детерминированных эффектов может наблюдаться при дозах от 0,1 Гр до нескольких десятков грей.
Так, например, порог временной (обратимой) стерильности мужчин при однократном облучении семенников составляет около 0,15 Гр, а порог постоянной (необратимой) стерильности – 3,5‑6 Гр. Порог для постоянной стерильности женщин при остром облучении – 2,5‑6 Гр.
Порог возникновения катаракты у человека при остром воздействии γ- или рентгеновского излучения лежит в диапазоне 2‑6 Гр; для нейтронного излучения порог в 3-9 раз ниже.
Порог достоверного подавления кроветворения в красном костном мозге человека при остром облучении наблюдается при 0,15 Гр.
Слайд 5Стохастические эффекты облучения. Примеры
Стохастические эффекты облучения возникают в результате мутагенного действия
Стохастические эффекты облучения могут возникать как в самом облученном организме, так и у потомства облученного организма.
К стохастическим эффектам облучения относятся радиоиндуцированные опухоли, возникающие в различных тканях облученного организма. Наиболее часто встречаются злокачественные опухоли кожи, костей, молочной и щитовидной желез, яичников, легких, а также лейкозы.
Стохастические эффекты возникают через длительное время после облучения, т.е. являются отдаленными последствиями облучения.
Поскольку существуют механизмы клеточного восстановления, стохастические эффекты при малых дозах маловероятны, однако с увеличением дозы облучения их вероятность возрастает. Тяжесть же этих эффектов не зависит от дозы.
Лучевые изменения половых клеток могут привести к возникновению стохастических эффектов в виде наследственных болезней или уродств у потомства облученного организма.
Слайд 6Соматические и генетические эффекты облучения. Определения
Соматические эффекты облучения (от греч. sṓma
Могут быть как детерминированными, так и стохастическими, как ранними (проявления острой лучевой болезни и локальные лучевые повреждения), так и отдаленными (сокращение продолжительности жизни, возникновение опухолей, катаракты и др.).
Генетические (наследственные) эффекты облучения – вызванные ионизирующим излучением биологические эффекты, обусловленные повреждением генома (появление доминантных и рецессивных генных мутаций) половых клеток облученного организма и проявляющиеся у его потомства.
Относятся к стохастическим эффектам облучения. Могут быть как неблагоприятными (вредными), так и благоприятными (полезными). Полезные генетические эффекты используют для выведения более продуктивных штаммов микроорганизмов и сортов растений.
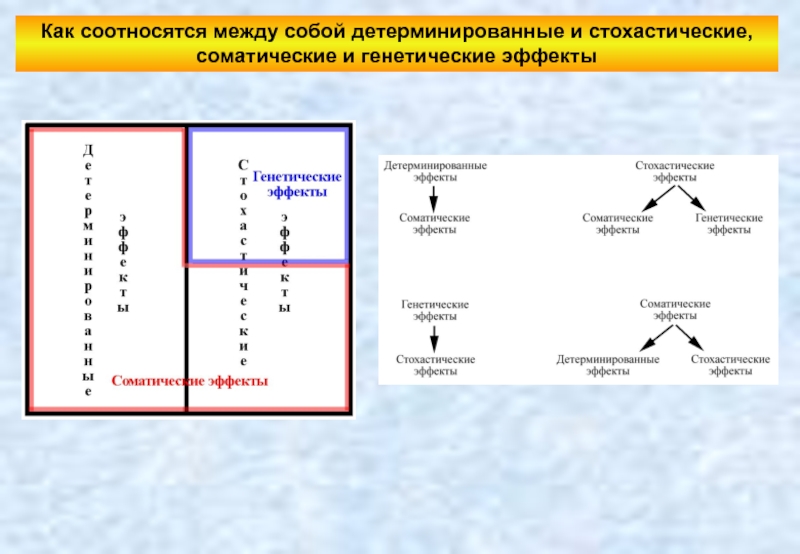
Слайд 7Как соотносятся между собой детерминированные и стохастические, соматические и генетические эффекты
Слайд 8Генетические эффекты облучения у человека
До настоящего времени не найдены радиационно-индуцированные наследственные
Весь прогноз наследственных заболеваний (т.н. генетического риска) у человека пока целиком основан на экстраполяции результатов опытов на животных.
В ряду дрозофила – мышь – человек выход мутаций на единицу дозы, максимально выраженный у дрозофилы, резко снижается у мыши и практически нивелируется у человека.
По-видимому, это связано с тем, что по мере эволюции степень эффективности механизма репарации повышалась и достигла максимума у человека.
Повышению эффективности репарационных процессов, вероятно, способствует и фактор времени – т.е. удлинение всех жизненных циклов у человека (в том числе, сперматогенеза и эмбрионального развития).
Слайд 9Дозовые кривые выживаемости клеток. Теория мишени. Радиочувствительность разных стадий клеточного цикла
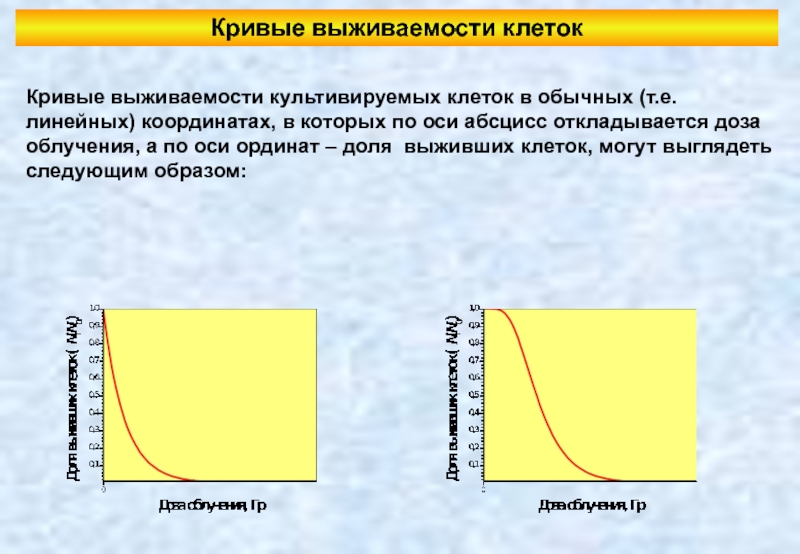
Слайд 10Кривые выживаемости клеток
Кривые выживаемости культивируемых клеток в обычных (т.е. линейных) координатах,
Слайд 11Какие клетки считаются выжившими?
Выжившими считаются клетки, непотерявшие клоногенной способности.
Под клоногенной (т.е.
Для образования такой колонии клетка должна совершить не менее 5-6 успешных делений, т.е. таких делений, в результате которых образуются дочерние клетки также способные к делению. (После 5 делений образуется 25=32 клеток, а после 6 делений – 26=64 клетки)
Учет выживаемости культивируемых клеток грызунов обычно проводят через 5-8 дней их роста после облучения, а для культивируемых клеток человека – через 2 недели. Разные сроки связаны с разной длительность клеточного цикла. Например, для часто используемых в экспериментах клеток HeLa (клетки карциномы шейки матки человека) длительность клеточного цикла – 24 часов, а для клеток V79 (фибробласты легких китайского хомячка) – 11 часов.
Слайд 12Сравнение кривых выживаемости клеток при действии ядов и ионизирующего излучения
Наличие подобного
При этом уже в то время было отмечено, что кривые выживаемости клеток после воздействия излучения отличаются от кривых выживаемости клеток после воздействия каких-либо токсических агентов химической природы, например ядов:
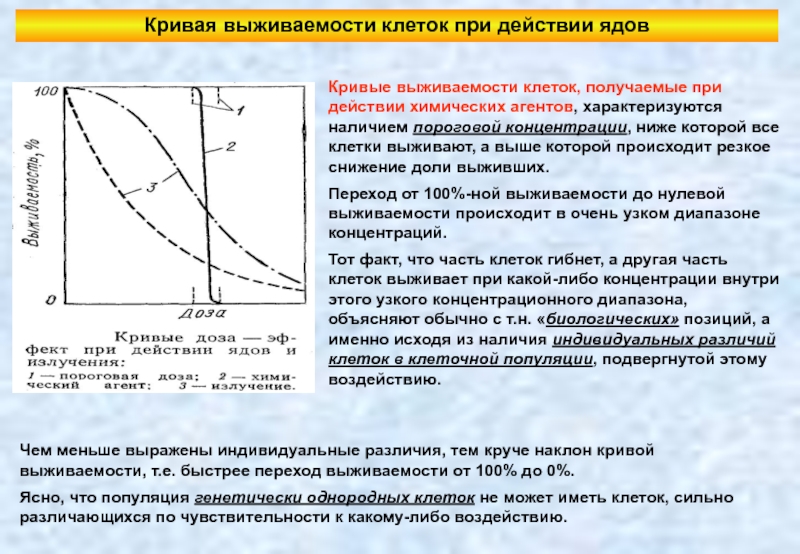
Слайд 13Кривая выживаемости клеток при действии ядов
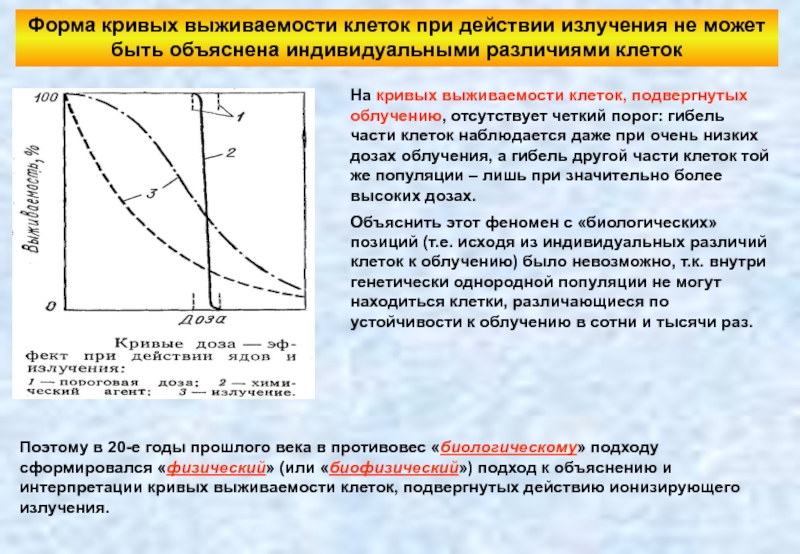
Кривые выживаемости клеток, получаемые при действии
Переход от 100%-ной выживаемости до нулевой выживаемости происходит в очень узком диапазоне концентраций.
Тот факт, что часть клеток гибнет, а другая часть клеток выживает при какой-либо концентрации внутри этого узкого концентрационного диапазона, объясняют обычно с т.н. «биологических» позиций, а именно исходя из наличия индивидуальных различий клеток в клеточной популяции, подвергнутой этому воздействию.
Чем меньше выражены индивидуальные различия, тем круче наклон кривой выживаемости, т.е. быстрее переход выживаемости от 100% до 0%.
Ясно, что популяция генетически однородных клеток не может иметь клеток, сильно различающихся по чувствительности к какому-либо воздействию.
Слайд 14Форма кривых выживаемости клеток при действии излучения не может быть объяснена
На кривых выживаемости клеток, подвергнутых облучению, отсутствует четкий порог: гибель части клеток наблюдается даже при очень низких дозах облучения, а гибель другой части клеток той же популяции – лишь при значительно более высоких дозах.
Объяснить этот феномен с «биологических» позиций (т.е. исходя из индивидуальных различий клеток к облучению) было невозможно, т.к. внутри генетически однородной популяции не могут находиться клетки, различающиеся по устойчивости к облучению в сотни и тысячи раз.
Поэтому в 20-е годы прошлого века в противовес «биологическому» подходу сформировался «физический» (или «биофизический») подход к объяснению и интерпретации кривых выживаемости клеток, подвергнутых действию ионизирующего излучения.
Слайд 15Теория «точечного тепла». Основные положения
В основе «биофизического» направления лежала «теория точечного
Несмотря на то, что плотность поглощенной энергии в облучаемом объекте в среднем очень низкая, энергия самих актов поглощения весьма велика и поэтому в микрообъемах вещества, в которых произошли акты поглощения энергии, происходит его локальное нагревание (т.е. появление т.н. «точечного тепла»), в результате чего вещество претерпевает значительные локальные изменения, обусловленные разрывом химических связей или активацией химических реакций.
Пространственное распределение мест локализации «точечного тепла» внутри облученной клетки имеет случайный характер, т.е является чисто статистической (т.е. вероятностной) функцией.
Клетка гетерогенна (т.е. неоднородна) по своему объему в отношении чувствительности к облучению и имеет как исключительно важные для жизни области, повреждение которых приводит клетку к гибели, так и области, относительно несущественные для выживания клетки.
Слайд 16Форма кривых выживаемости клеток при действии излучения объясняется вероятностным характером действия
Т.о. теория «точечного тепла» заявила, что конечный эффект в клетке (например, гибель) определяется вероятностью осуществления акта поглощения энергии (т.е. появления «точечного тепла») в жизненно важных областях (микрообъемах) клетки.
При увеличении дозы облучения вероятность осуществления акта поглощения энергии в этих клеточных областях возрастает, при снижении дозы – уменьшается.
Однако, даже при очень высокой дозе облучения существует определенная вероятность того, что в каком-то количестве клеток не произошло актов поглощения энергии в жизненно важных клеточных областях и поэтому эти клетки останутся неповрежденными облучением.
И наоборот – даже при очень низкой дозе существует вероятность того, что в каком-то количестве клеток произойдут акты поглощения энергии в жизненно важных клеточных областях, что вызовет гибель этих клеток.
Слайд 17Фридрих Дессауэр (Friedrich Dessauer, 1881-1963) – известный немецкий физик, биофизик, изобретатель,
В 1921 г. основал Институт физических основ медицины в г. Франкфурт-на-Майне. Главная цель института – изучение возможности медицинского применения излучений, в частности X‑лучей. Этот институт стал ведущим исследовательским центром в области исследования биологического действия ионизирующего излучения.
В 1922 г. сформулировал теорию «точечного тепла» (или «точечного нагрева»), объясняющую поражение клетки ионизирующим излучением, исходя из дискретной природы излучения и вероятностного характера взаимодействия излучения с веществом. Данную теорию рассматривают в качестве важной вехи в развитии радиобиологии, знаменующей начало второго этапа ее развития – этапа количественной радиобиологии.
Фридрих Дессауэр (1881-1963)
Слайд 18Два фундаментальных положения в радиобиологии
В 20‑30‑е годы прошлого столетия основные идеи
Дж. Кроутер (J.A. Crowther; в русскоязычной литературе встречаются также и другие варианты написания фамилии этого исследователя — Краузер, Кроузер),
Д. Ли (D.E. Lea),
К. Циммер (K.G. Zimmer)
Н.В. Тимофеев-Ресовский
В результате этих работ была сформулирована т.н. «теория мишени», в основе которой лежали два фундаментальных положения:
принцип попадания и
принцип мишени.
Слайд 19Принцип попадания
Принцип попадания может быть сформулирован следующим образом:
Поглощение энергии в облучаемом
Таким образом, «принцип попадания» отмечает дискретность и вероятностный (случайный) характер актов взаимодействия излучения с веществом.
Фактически попаданием считается возникновение акта ионизации каких-либо молекул в облучаемом объеме.
Слайд 20Принцип мишени
Принцип мишени может быть сформулирован следующим образом:
Клетка имеет в своем
Таким образом, «принцип мишени» отмечает биологическую гетерогенность различных областей (микрообъемов) внутри клетки в отношении чувствительности к облучению, а именно, наличие внутри клетки «мишеней» – чувствительных областей, радиационное повреждение которых приводит клетку к гибели.
Слайд 21Мишени:
какие они могут быть и сколько их может быть в клетке?
Чисто
одноударные мишени (когда мишень считается пораженной при одном попадании) и
многоударные мишени (когда мишень считается пораженной при 2, 3, 4, …, n попаданиях).
Можно также предположить наличие в клетке:
только одной мишени (одномишенная клетка)
или нескольких мишеней (многомишенная клетка)
Причем гибель многомишенной клетки может наступить лишь после того, как все мишени получат определенное число попаданий (при этом каждая из этих мишеней может отличаться по ударности).
Слайд 22Простейшие модели, описывающие кривые выживаемости
Для описания кривых пострадиационной выживаемости клеток используют
Двумя простейшими моделями, описывающими кривые пострадиационной выживаемости клеток и базирующимися на теории мишени, являются:
Многоударная-одномишенная модель
Одноударная-многомишенная модель
Слайд 23Имеет ли смысл использовать более сложные
многоударные-многомишенные модели?
Использовать другие более сложные
Так, например, кривая выживаемости для 10-ударных-16-мишенных объектов очень хорошо совпадает с кривой выживаемости для 48-ударных-1-мишенных объектов.
Кроме того, теория мишени не учитывает наличия в клетке репарационных процессов, которые существенно затрудняют интерпретацию кривых выживаемости только с позиций мишенности и ударности объекта.
Слайд 24Одноударная-многомишенная модель — чисто формальное использование
На практике во многих случаях для
Слайд 25Одноударная-многомишенная кривая (1)
Исходные допущения для одноударной-многомишенной модели:
Каждая клетка имеет n одинаковых
Для поражения каждой из n мишеней необходимо 1 попадание в эту мишень.
Клетка погибает при поражении всех n мишеней.
Кривая выживаемости для такой модели описывается следующим уравнением:
где N0 – исходное количество клеток;
N – количество клеток, выживших после облучения в дозе D;
k – коэффициент;
n – число мишеней.
Выживаемость клеток представляют обычно не в линейных координатах, а в полулогарифмических координатах (с использованием логарифмической шкалы ординат). По оси абсцисс – доза, а по оси ординат (в логарифмическом масштабе) – доля выживших клеток.
Кривая выживаемости
в общем виде имеет
плечо и прямолинейный
участок
Слайд 26Одноударная-многомишенная кривая (2)
преобразуется в следующее:
После логарифмирования получаем:
Т.о., при D → ∞
Значение ординаты n точки пересечения экстраполированного участка этой прямой с осью ординат называют экстраполяционным числом.
Как ясно видно из уравнения, описывающего эту прямую, экстраполяционное число равно числу мишеней.
При D → ∞ уравнение
То, что эта кривая выживаемости имеет прямолинейный участок, легко понять из следующих преобразований:
, т.е. уравнение прямой линии.
Слайд 27Одноударная-одномишенная кривая – частный случай одноударной-многомишенной кривой
Если число мишеней n=1, то
преобразуется в следующее:
После логарифмирования получаем:
Т.о., видно, что кривая выживаемости, не имеющая плеча, является частным случаем, для варианта, когда и число мишеней n=1, и ударность мишени тоже равна 1.
Ясно, что экстраполяционное число n для этого варианта равно 1.
Кривая выживаемости
без плеча (т.е.
представляет собой
прямую линию)
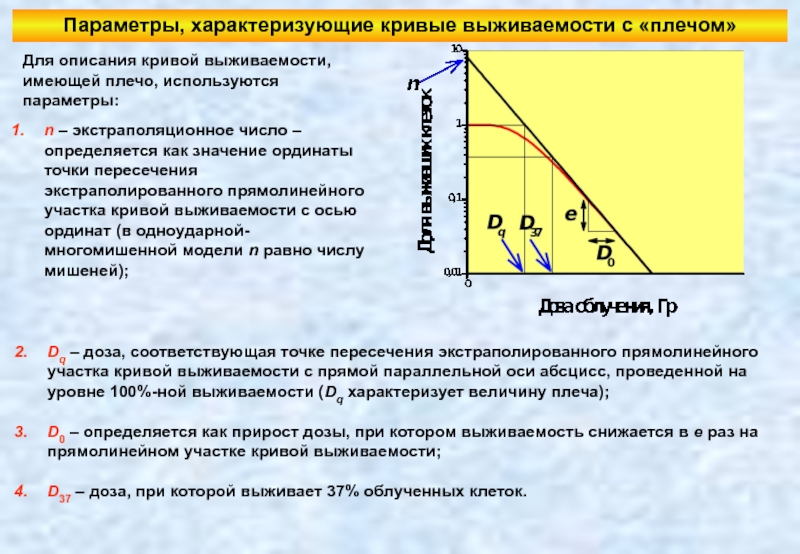
Слайд 28Параметры, характеризующие кривые выживаемости с «плечом»
n – экстраполяционное число – определяется
Для описания кривой выживаемости, имеющей плечо, используются параметры:
Dq – доза, соответствующая точке пересечения экстраполированного прямолинейного участка кривой выживаемости с прямой параллельной оси абсцисс, проведенной на уровне 100%-ной выживаемости (Dq характеризует величину плеча);
D0 – определяется как прирост дозы, при котором выживаемость снижается в е раз на прямолинейном участке кривой выживаемости;
D37 – доза, при которой выживает 37% облученных клеток.
Слайд 30Параметры, характеризующие кривые выживаемости без «плеча»
Для описания кривой выживаемости, не имеющей
Для кривых выживаемости, не имеющих плеча, D0 = D37, что следует из следующих расчетов:
доза D0, которая определяется как доза, при которой выживаемость уменьшается в e раз;
или доза D37 – доза, при которой выживает 37% облученных клеток.
Таким образом, при уменьшении выживаемости в e раз от исходного уровня (т.е. при облучении в дозе D0) выживаемость составит 37%, т.е. D0=D37.
уменьшение числа выживших клеток в e раз
D0
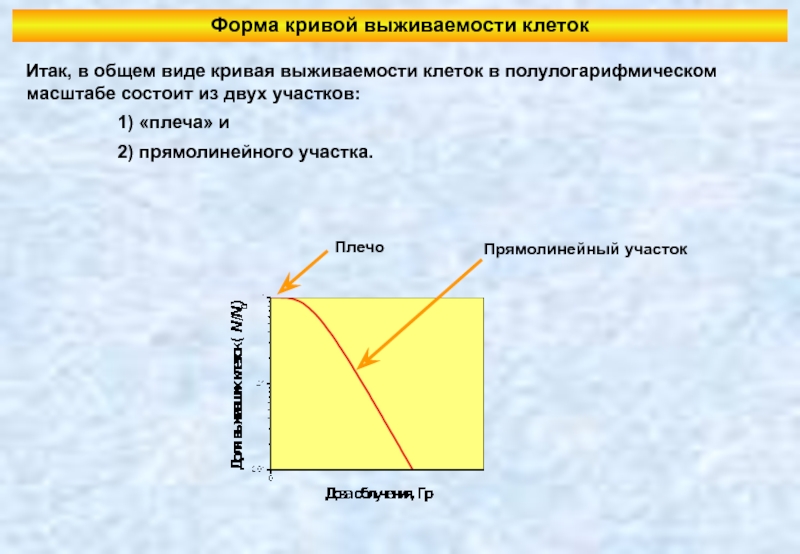
Слайд 31Форма кривой выживаемости клеток
Итак, в общем виде кривая выживаемости клеток в
1) «плеча» и
2) прямолинейного участка.
Плечо
Прямолинейный участок
Слайд 32О чем говорит наличие плеча и величина Dq?
В соответствии с теорией
либо объект является многомишенным,
либо мишень является многоударной.
Однако, в соответствии с современными представлениями наличие плеча трактуется не как наличие многоударности или многомишенности, а как свидетельство протекания в клетке восстановительных (репарационных) процессов.
При этом величину Dq используют в качестве показателя способности клетки осуществлять репарационные процессы: чем больше значение Dq (т.е. чем больше плечо), тем выше репарационная способность клетки.
Слайд 33От чего зависит наличие «плеча» на кривых выживаемости клеток?
В целом наличие
1) от облучаемого объекта (т.е. от наличия или отсутствия у него способности осуществлять репарацию), а также
2) от вида излучения.
Слайд 34Зависимость наличия «плеча» от вида ионизирующего излучения
Кривые выживаемости клеток, имеющие четко
При облучении плотноионизирующим излучением кривые выживаемости клеток имеют слабовыраженное плечо или вовсе его не имеют (например, в случае α-излучения). Это связано с тем, что при действии плотноионизирующего излучения образуются в основном двунитевые разрывы ДНК, которые являются нерепарабельными (или плохорепарабельными) повреждениями (даже при наличии в клетке репарационных процессов) и однозначно приводят клетку к гибели.
Слайд 35Зависимость наличия плеча от облучаемого объекта
Если кривые выживаемости клеток после облучения
Плечо не наблюдается при облучении редкоионизирующим излучением вирусов, а также макромолекул в простых модельных системах (например, растворов ферментов), т.к. они не обладают репарационной способностью.
Надо четко понимать, что:
Слайд 36Молекулы ДНК – основная клеточная мишень для ионизирующего излучения
Что же является
Основной мишенью в клетке является клеточное ядро (а точнее – молекулы ДНК). [Второй по значению мишенью в клетке, как считают некоторые исследователи, являются мембраны].
Тот факт, что ядро является основной мишенью было доказано в следующих экспериментах:
Эксперименты по определению размеров мишени в клетке
Эксперименты по локальному облучению различных областей клетки
Размер клеточной мишени совпадает с размером клеточного ядра
Облучение клеточного ядра приводит к гибели клетки; при облучении других клеточных областей гибель клетки происходит при значительно более высоких дозах
Слайд 38Клеточный цикл
Пролиферирующие клетки эукариот в своем развитии проходят несколько фаз, совокупность
Первая идентифицированная фаза клеточного цикла – митоз – фаза собственно деления клетки.
Временной интервал между окончанием одного митоза и началом следующего митоза получил название интерфазы. В интерфазе осуществляется подготовка клетки к последующему делению.
Слайд 39Интерфаза
S-фаза (от слова synthesis – синтез) – синтетическая фаза, в течение
G1-фаза (от англ. gap – промежуток, интервал) – предсинтетическая фаза, определяемая как интервал между митозом и S-фазой. В G1-фазе происходит синтез мРНК, белков и других компонентов клетки.
G2-фаза – постсинтетическая фаза, определяемая как интервал между S-фазой и митозом. G2-фаза является конечным этапом подготовки клетки к делению.
Слайд 40Продолжительность фаз клеточного цикла
Митоз – наиболее короткая фаза (от 0,5 до
G1-фаза – наиболее вариабельная по длительности фаза (часто является наиболее продолжительной и именно ее длительность определяет продолжительность клеточного цикла в целом).
S-фаза длится обычно 6-8 час. (довольно стабильная по длительности фаза; никогда не превышает 15 час.).
G2-фаза – обычно это самая короткая фаза в интерфазе, а в клеточном цикле – вторая по длительности после митоза.
Длительность клеточного цикла у активно пролиферирующих клеток млекопитающих обычно составляет от 10 до 24 час., но в некоторых тканях может достигать 200 и более часов.
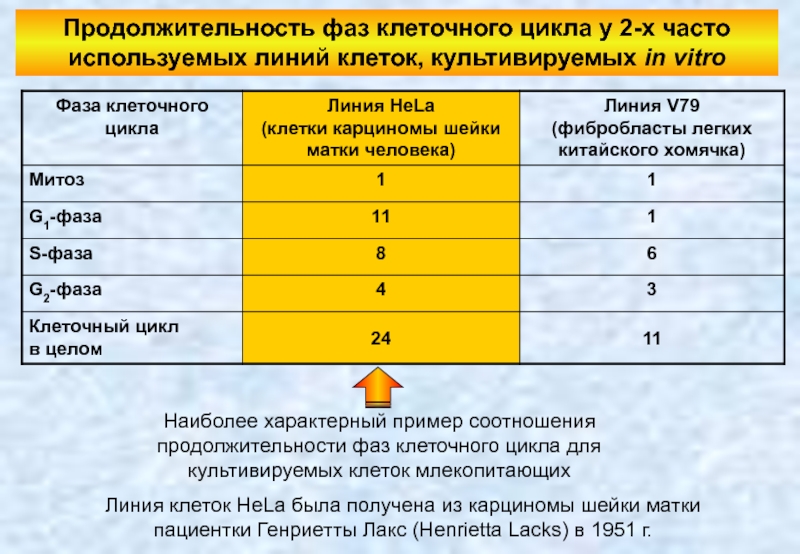
Слайд 41Продолжительность фаз клеточного цикла у 2-х часто используемых линий клеток, культивируемых
Наиболее характерный пример соотношения продолжительности фаз клеточного цикла для культивируемых клеток млекопитающих
Линия клеток HeLa была получена из карциномы шейки матки пациентки Генриетты Лакс (Henrietta Lacks) в 1951 г.
Слайд 42
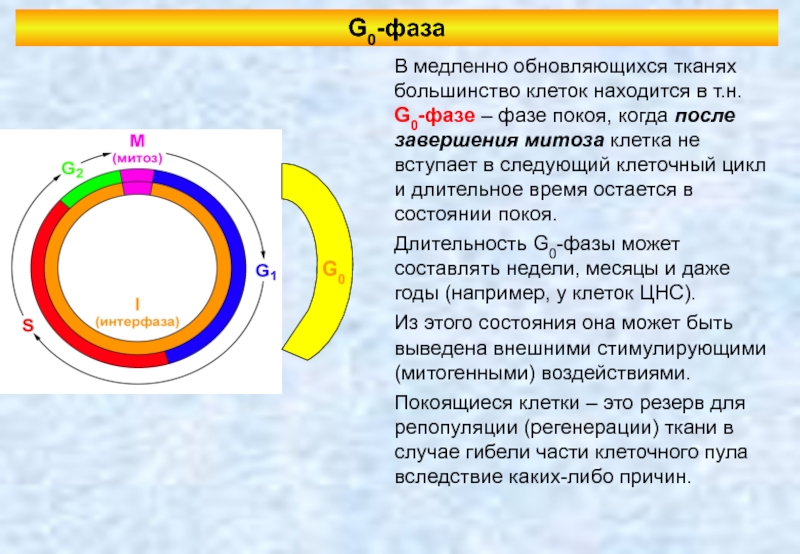
G0-фаза
В медленно обновляющихся тканях большинство клеток находится в т.н. G0-фазе –
Длительность G0-фазы может составлять недели, месяцы и даже годы (например, у клеток ЦНС).
Из этого состояния она может быть выведена внешними стимулирующими (митогенными) воздействиями.
Покоящиеся клетки – это резерв для репопуляции (регенерации) ткани в случае гибели части клеточного пула вследствие каких-либо причин.
G0
Слайд 43
Синхронизация клеток
Обычная популяция пролиферирующих клеток включает клетки, находящиеся на разных стадиях
Однако, для изучения радиочувствительности отдельных стадий клеточного цикла необходимо, чтобы все клетки популяции находились в момент облучения на одной и той же стадии цикла.
Для этого проводят т.н. синхронизацию культивируемых клеток.
Один из наиболее мягких и эффективных методов синхронизации был предложен Т.Терасимой и Л.Толмахом (T.Terasima, L.Tolmach) в 1963 г. Этот метод синхронизации может быть применен только для клеток, растущих в монослойных культурах. Он основан на том факте, что на стадии митоза клетки округляются и становятся хуже прикреплены к поверхности ростовой среды. Эти округленные клетки можно легко смыть с поверхности путем легкого встряхивания культурального сосуда и концентрировать последующим центрифугированием.
Так можно получить клеточную массу, в которой 90-95% клеток находится на стадии митоза.
После посева такие клетки будут синхронно проходить все три фазы первого клеточного цикла.
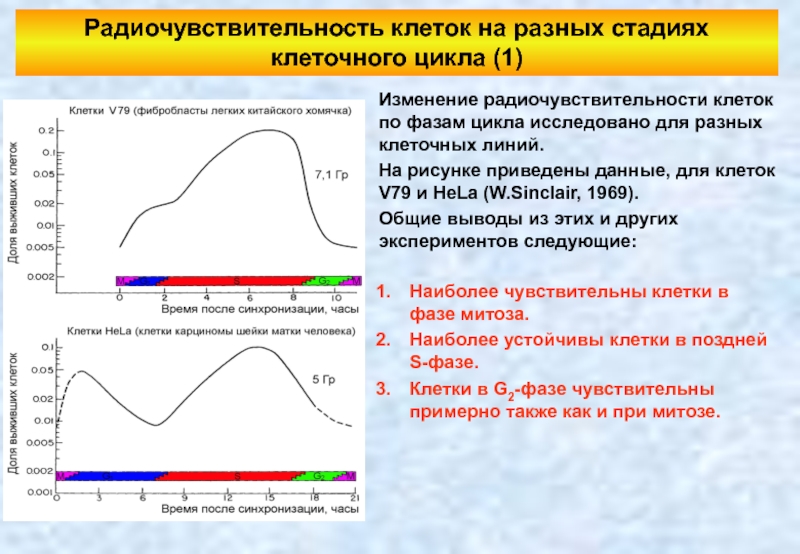
Слайд 44Радиочувствительность клеток на разных стадиях клеточного цикла (1)
Изменение радиочувствительности клеток по
На рисунке приведены данные, для клеток V79 и HeLa (W.Sinclair, 1969).
Общие выводы из этих и других экспериментов следующие:
Наиболее чувствительны клетки в фазе митоза.
Наиболее устойчивы клетки в поздней S-фазе.
Клетки в G2-фазе чувствительны примерно также как и при митозе.
Слайд 45Исключения из общих закономерностей
Описанные выше закономерности о радиочувствительности разных стадий клеточного
Слайд 46Кривые выживаемости клеток на разных стадиях клеточного цикла (Sinclair, 1968, 1970)
Варьирование
Кривая выживаемости клеток в S-фазе имеет наиболее выраженное плечо и наибольшие значения D0 и экстраполяционного числа n. – Это означает, что клетки, находящиеся в S-фазе обладают наиболее высокой способностью к репарации.
Клетки в М-фазе и G2-фазе не имеют плеча на кривых выживаемости и характеризуются наименьшими значениями D0.
Слайд 47Как сильно различается выживаемость клеток, облученных на разных стадиях клеточного цикла?
Из
примерно в 3 раза при дозе 3 Гр;
примерно в 20 раз при дозе 8 Гр;
примерно в 35 раз при дозе 12 Гр.
Это означает, что в результате облучения асинхронных популяций преимущественно выживают клетки, находившиеся в момент облучения в S-фазе. Таким образом, облучение выступает в качестве синхронизирующего агента, вызывающего перераспределение клеток между фазами клеточного цикла.
Таким образом, с увеличением дозы облучения возрастают и отличия в выживаемости клеток, облученных на разных стадиях клеточного цикла.
Слайд 48Вызванное облучением перераспределение клеток между фазами клеточного цикла можно использовать в
Эффект перераспределения клеток между фазами клеточного цикла очень важен для выбора оптимального режима фракционирования дозы при радиотерапии опухолей.
Наиболее эффективно применять повторное облучение опухоли через такой интервал времени, который соответствует временному промежутку, необходимому для перехода клеток, облученных в резистентной S-фазе, в наиболее чувствительные к облучению фазы G2 и митоза.
Клетки же, находившиеся в момент первого облучения в наиболее чувствительных к облучению фазах G2 и митоза, в значительной степени погибнут уже после первой фракции облучения.
Таким образом, можно существенно сенсибилизировать популяцию опухолевых клеток к повторной фракции облучения.
При этом такая сенсибилизация будет иметь место только в отношении быстро пролиферирующих клеток – т.е. опухолевых клеток, и не будет происходить в отношении медленно пролиферирующих клеток – т.е. клеток нормальной ткани, окружающей опухоль.
Слайд 49Прямое и непрямое (косвенное) действие ионизирующих излучений. Радиолиз воды. Антиоксидантные защитные
Слайд 50Теория мишени - так ли всё в действительности?
В 30-е гг. прошлого
Однако, уже в эти же 30-е годы и особенно в 40-е годы в научной литературе стали появляться результаты экспериментов, которые не находили объяснения с позиций теории мишени, а именно с позиций принципа попадания, т.е. идеи о том, что для поражения какой-либо молекулы необходимо осуществление акты взаимодействия (т.е. попадания) с ней ионизирующей частицы или кванта.
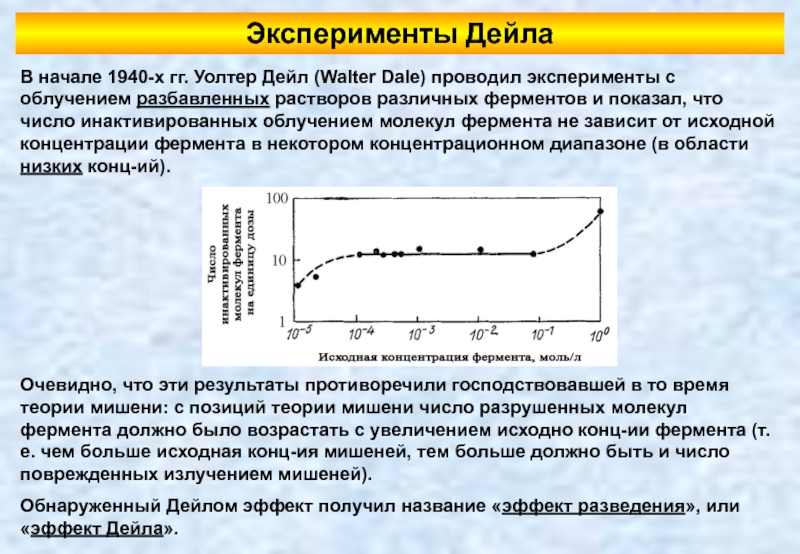
Слайд 51В начале 1940-х гг. Уолтер Дейл (Walter Dale) проводил эксперименты с
Эксперименты Дейла
Очевидно, что эти результаты противоречили господствовавшей в то время теории мишени: с позиций теории мишени число разрушенных молекул фермента должно было возрастать с увеличением исходно конц-ии фермента (т.е. чем больше исходная конц-ия мишеней, тем больше должно быть и число поврежденных излучением мишеней).
Обнаруженный Дейлом эффект получил название «эффект разведения», или «эффект Дейла».
Слайд 52Прямое и непрямое (косвенное) действие ионизирующих излучений
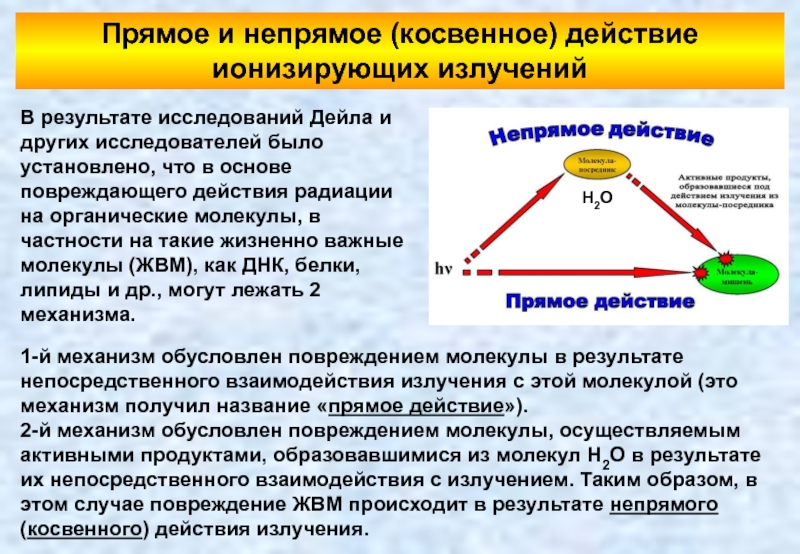
В результате исследований Дейла
1-й механизм обусловлен повреждением молекулы в результате непосредственного взаимодействия излучения с этой молекулой (это механизм получил название «прямое действие»).
2-й механизм обусловлен повреждением молекулы, осуществляемым активными продуктами, образовавшимися из молекул H2O в результате их непосредственного взаимодействия с излучением. Таким образом, в этом случае повреждение ЖВМ происходит в результате непрямого (косвенного) действия излучения.
H2O
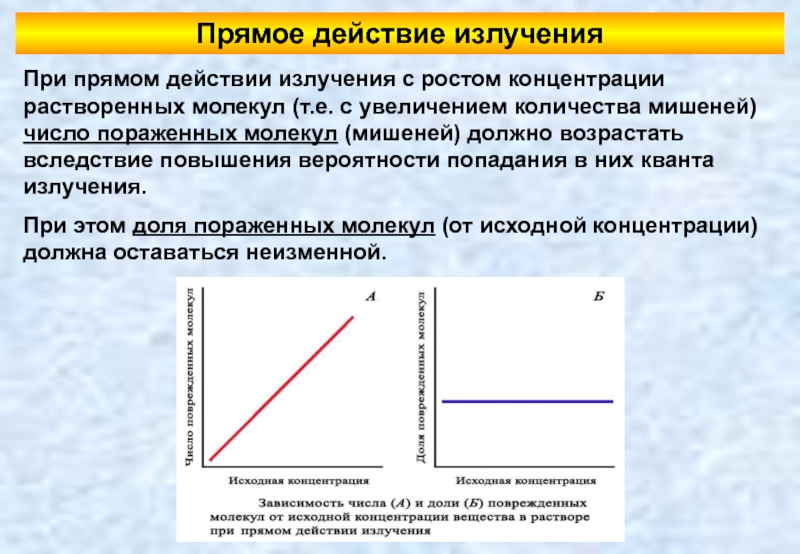
Слайд 53При прямом действии излучения с ростом концентрации растворенных молекул (т.е. с
При этом доля пораженных молекул (от исходной концентрации) должна оставаться неизменной.
Прямое действие излучения
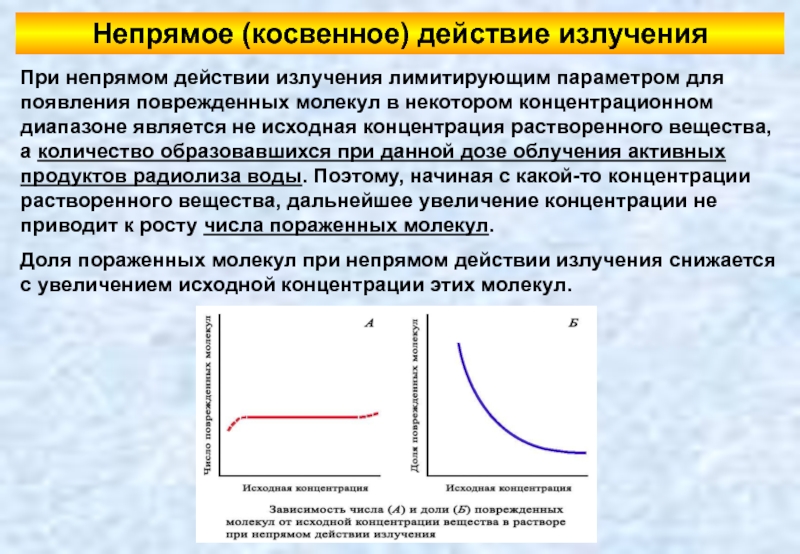
Слайд 54При непрямом действии излучения лимитирующим параметром для появления поврежденных молекул в
Доля пораженных молекул при непрямом действии излучения снижается с увеличением исходной концентрации этих молекул.
Непрямое (косвенное) действие излучения
Слайд 55Непрямое действие преобладает только
в разбавленных растворах
Иными словами отсутствие зависимости числа
Повышение же числа поврежденных молекул при больших исходных концентрациях растворенных молекул (изображено на рисунке пунктиром) связано с тем, что здесь заметный вклад в их повреждение начинает вносить прямое действие излучения.
Таким образом, непрямое действие излучения преобладает только в разбавленных растворах.
Слайд 56Сравнение радиационных эффектов
при облучении макромолекул в растворенном и сухом состоянии
В
Если в растворенном состоянии эти объекты становятся значительно более чувствительными к облучению, то считают, что существенный вклад в их повреждение вносят продукты радиолиза воды.
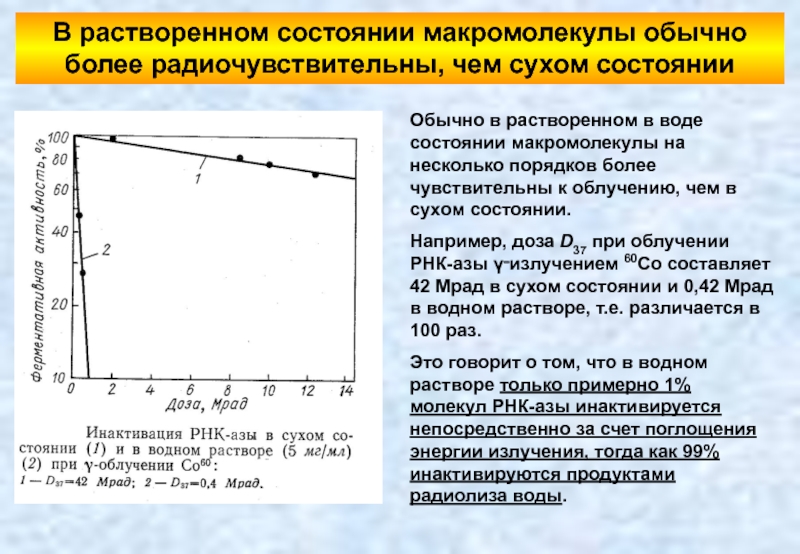
Слайд 57Обычно в растворенном в воде состоянии макромолекулы на несколько порядков более
Например, доза D37 при облучении РНК-азы γ‑излучением 60Со составляет 42 Мрад в сухом состоянии и 0,42 Мрад в водном растворе, т.е. различается в 100 раз.
Это говорит о том, что в водном растворе только примерно 1% молекул РНК-азы инактивируется непосредственно за счет поглощения энергии излучения, тогда как 99% инактивируются продуктами радиолиза воды.
В растворенном состоянии макромолекулы обычно более радиочувствительны, чем сухом состоянии
Слайд 58Представления о вкладе непрямого действия излучения в лучевое поражение клетки существенно
В настоящее время считается, что на уровне клетки во многих радиобиологических эффектах непрямое действие радиации играет столь же существенную роль, как и прямое действие.
И даже более того, вклад непрямого действия ионизирующего излучения в отношении появления радиационных повреждений таких критических клеточных структур, как молекулы ДНК, достигает 70-90%.
Открытие непрямого действия излучения стало очень важной вехой в понимании механизмов биологического действия ионизирующих излучений и стало основой для становления новых направлений радиобиологических исследований, в частности такого важного раздела радиобиологии, как химическая противолучевая защита.
Соотношение прямого и непрямого действия излучения в клетке
Слайд 59Рассмотрим теперь основные активные продукты, образующиеся при радиолизе воды и обеспечивающие
Слайд 60Радиолиз воды (1)
I. Если энергия кванта ионизирующего излучения составляет более 12,56 эВ,
т.е. из молекулы воды выбивается электрон.
Образовавшийся положительный ион воды взаимодействует с молекулой воды с образованием иона гидроксония и гидроксильного радикала:
а электрон взаимодействует с молекулой воды с образованием гидроксильного иона и радикала водорода:
Слайд 61Образовавшийся электрон может также стабилизироваться до относительно долгоживущего состояния, известного под
Первая гидратная оболочка гидратированного электрона состоит из 6 молекул воды, расположенных в вершинах октаэдра и повернутых в сторону электрона одним из своих атомов водорода.
Гидратированный электрон может диффундировать на значительно более далекие расстояния, чем свободный электрон, и взаимодействует с растворенными биологическими молекулами уже вдали от места своего появления в результате радиолиза воды.
Гидратированный электрон
Слайд 62Что такое свободные радикалы?
Свободные радикалы – это нейтральные частицы (молекулы или
Имея неспаренный электрон, такие частицы стремятся заполнить электронную оболочку еще одним электроном, отняв его у других молекул.
Именно поэтому свободные радикалы являются обычно очень реакционноспособными.
Слайд 63II. Если энергия кванта ионизирующего излучения менее 12,56эВ, но более 7
Радиолиз воды (2)
Слайд 64
Вторичные продукты радиолиза воды, образовавшиеся при рекомбинации радикалов
При рекомбинации радикалов Н•
Слайд 65В области рН от 3 до 10 радиационно-химический выход G (т.е.
Радиационно-химический выход основных продуктов радиолиза воды
Слайд 66При наличии в воде растворенного кислорода O2 количество возможных продуктов, образующихся
Так, например, могут возникать:
- супероксиданионрадикал по реакции:
- перекисный радикал H―O―O• по реакции:
Дополнительные продукты радиолиза воды, образующиеся в присутствии кислорода
Слайд 67В целом, наибольшее биологическое значение имеют следующие весьма химически активные продукты
Наиболее важные продукты радиолиза воды (1)
Слайд 68Как видно из вышеприведенной схемы, среди основных продуктов радиолиза воды есть
Гидроксильный радикал является мощным окислителем и считается наиболее активным продуктом радиолиза воды.
Гидратированный электрон также обладает высокой реакционной способностью, однако, уже в качестве восстановителя.
Перекись водорода представляет собой очень неустойчивое соединение и распадается с образованием различных радикальных продуктов (в первую очередь, гидроксильного радикала).
В присутствии ионов Fe2+ скорость распада перекиси водорода с образованием гидроксильного радикала (реакция Фентона) значительно возрастает (примерно на 3 порядка):
Наиболее важные продукты радиолиза воды (2)
Слайд 69Продукты радиолиза воды могут диффундировать от места образования к жизненно важным
MH + H• → M• + H2,
MH + H• → MH2•,
MH + OH• → M• + H2O,
MH + OH• → MHOH•,
MH + HO2• → MOOH + H•
и многих других реакций.
Основные реакции продуктов радиолиза воды
с жизненно важными молекулами
Слайд 70Образовавшиеся в этих реакциях свободные радикалы биомолекул могут привести:
к внутримолекулярным перестройкам
к взаимодействию этих молекул с другими имеющимися в клетке соединениями (например, с кислородом или какими-либо другими органическими молекулами).
В результате этих изменений биомолекулы могут изменить свои физико-химические свойства и потерять функциональную активность.
Последствия модификации жизненно важных молекул продуктами радиолиза воды
Слайд 71Продукты радиолиза воды не являются чем-то необычным для клетки!
И радикальные,
Такие же продукты образуются и в различных метаболических процессах, протекающих в клетке в норме в отсутствие облучения. В нормальных условиях, однако, их уровень существенно ниже.
Большинство из этих радикальных продуктов имеют в своем составе кислород и поэтому получили название активных форм кислорода (АФК, Reactive Oxygen Species – ROS).
Повышенный уровень АФК может наблюдаться и при многих других патологических состояниях, а не только при облучении.
Слайд 72Важность антиоксидантных систем
Для предотвращения избыточного накопления АФК и интенсификации деструктивных
В связи с тем, что гидроксильный радикал OH• является наиболее сильной АФК, действие антиокислительных защитных систем фактически направлено (либо непосредственно, либо косвенно) на предотвращение его образование или на его удаление.
В свете вышесказанного понятна исключительно важная роль эндогенных антиоксидантных систем как в нормальном клеточном метаболизме, так и при различных патологиях, сопровождающихся накоплением АФК.
Слайд 73В клетках можно выделить 3 уровня эндогенных защитных ресурсов, предназначенных для
Три уровня эндогенной защиты клетки в условиях радиационного воздействия
1-й уровень защиты – антиоксидантные системы и факторы, обеспечивающие инактивацию активных форм кислорода (АФК), а также других продуктов радиолиза воды и радикалов и предотвращающие их деструктивное действие на жизненно важные молекулы и структуры клетки;
2-й уровень защиты – системы репарации молекул ДНК, осуществляющие репарацию (восстановление) поврежденных молекул ДНК;
3-й уровень защиты – системы клеточного апоптоза, обеспечивающие удаление из популяции клеток, в которых не удалось осуществить репарацию поврежденных молекул ДНК.
Слайд 74Антиоксидантные системы
Ферментативные (белковые) антиоксидантные системы
Низкомолекулярные антиоксиданты
Водорастворимые (восст. глутатион, аскорбат и др.)
Липорастворимые
Каталаза, глутатионпероксидазная система (удаление H2O2 и органических гидроперекисей)
Ферритин (связывает ионы Fe2+), церулоплазмин (окисляет Fe2+ в Fe3+), трансферрин (связывает ионы Fe3+)
Супероксиддисмутаза, церулоплазмин (удаление супероксиданион-радикала O2•–)
Гемоксигеназа (множественное антиоксидантное действие
Слайд 76Низкомолекулярные антиоксиданты
Одним из механизмов антиокислительного действия низкомолекулярных антиоксидантов является перехват активных
R• + InH → RH + In•
где R• – любой активный свободный радикал (H•, OH•, HO2•, L•, LO•, LOO• и др.),
InH – антиоксидант (в восстановленной форме),
In• – радикал антиоксиданта (малоактивный).
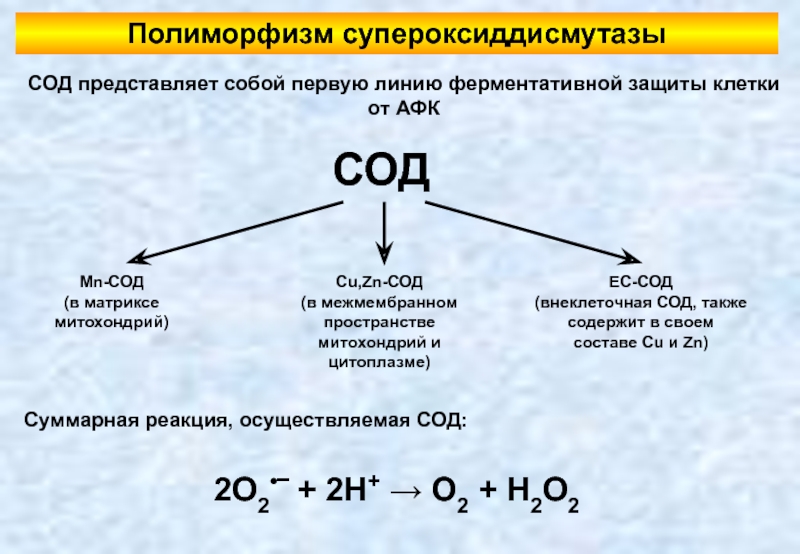
Слайд 77Полиморфизм супероксиддисмутазы
СОД
Mn-СОД
(в матриксе митохондрий)
Cu,Zn-СОД
(в межмембранном пространстве митохондрий и цитоплазме)
EC-СОД
(внеклеточная СОД, также
2O2•‾ + 2H+ → O2 + H2O2
Суммарная реакция, осуществляемая СОД:
СОД представляет собой первую линию ферментативной защиты клетки от АФК
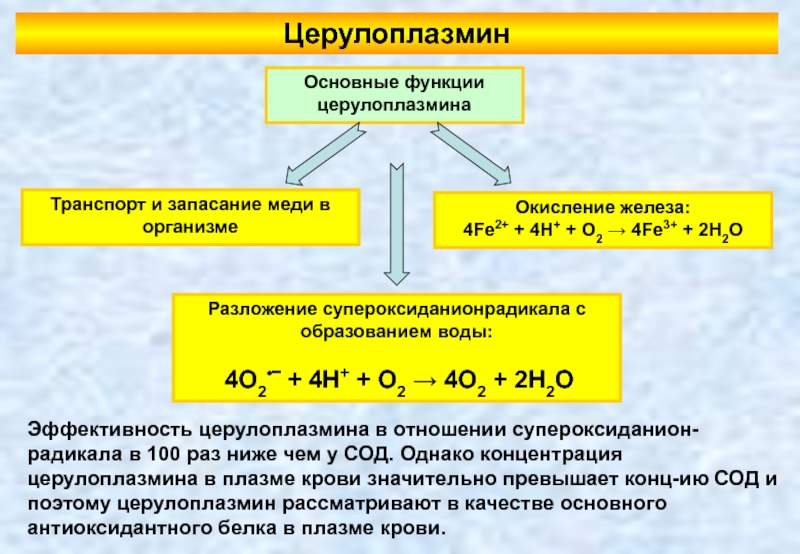
Слайд 78Церулоплазмин
Транспорт и запасание меди в организме
Окисление железа:
4Fe2+ + 4H+ + O2
Разложение супероксиданионрадикала с образованием воды:
4O2•‾ + 4H+ + O2 → 4O2 + 2H2O
Основные функции церулоплазмина
Эффективность церулоплазмина в отношении супероксиданион-радикала в 100 раз ниже чем у СОД. Однако концентрация церулоплазмина в плазме крови значительно превышает конц-ию СОД и поэтому церулоплазмин рассматривают в качестве основного антиоксидантного белка в плазме крови.
Слайд 79Каталаза
Катализирует превращение перекиси водорода в воду:
В клетках каталаза локализована, главным образом,
Слайд 80Глутатионпероксидаза (GPx)
Глутатионпероксидаза является одним из важнейших антиоксидантных ферментов, т.к. осуществляет детоксикацию
Считают, что глутатионпероксидаза играет более важную роль в удалении перекиси водорода, чем каталаза, т.к.:
глутатионпероксидаза локализована в тех же внутриклеточных компартментах (митохондриях и цитозоле), что и СОД – основной производитель перекиси водорода в клетке;
по сравнению с каталазой глутатионпероксидаза характеризуется более низкими значениями KM (константы Михаэлиса) в отношении перекиси водорода, т.е. действует в отношении низких концентраций перекиси водорода гораздо более эффективно, чем каталаза.
Глутатионпероксидаза осуществляет детоксикацию H2O2 и органических перекисей действуя совместно с восстановленным глутатионом (GSH), глутатионредуктазой (GRed) и восстановленным НАДФ, образуя т.н. глутатионпероксидазную систему.
Слайд 81
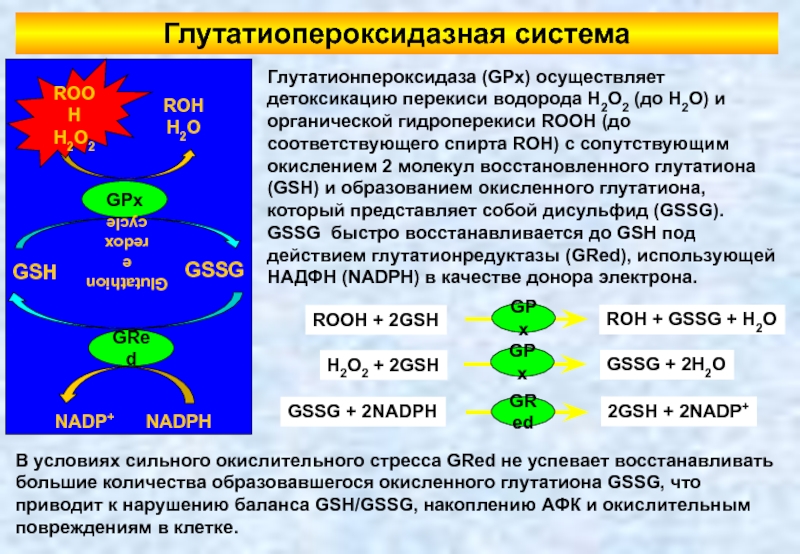
Глутатионпероксидаза (GPx) осуществляет детоксикацию перекиси водорода H2O2 (до H2O) и органической
В условиях сильного окислительного стресса GRed не успевает восстанавливать большие количества образовавшегося окисленного глутатиона GSSG, что приводит к нарушению баланса GSH/GSSG, накоплению АФК и окислительным повреждениям в клетке.
ROH
H2O
GSH
GSSG
GPx
GRed
NADP+
NADPH
ROOH + 2GSH
ROH + GSSG + H2O
H2O2 + 2GSH
GSSG + 2H2O
GSSG + 2NADPH
2GSH + 2NADP+
GPx
GPx
GRed
Glutathione
redox cycle
ROOH
H2O2
Глутатиопероксидазная система
Слайд 82Селен-содержащие
GPx
Неселеновые GPx
(глутатион-S-трансферазы [GSTs])
Цитозольная (клеточная) GPx (cGPx или GPx-1)
GPx
Внеклеточная (плазматическая) GPx (pGPx или GPx-3)
Желудочно-кишечная GPx (giGPx или GPx-2)
Полиморфизм глутатиопероксидазы
Слайд 83Глутатиопероксидаза гидроперекисей фосфолипидов (PhGPx)
PhGPx (в отличие от других форм) способна восстанавливать
Сравнение субстратной специфичности cGPx и PhGPx:
PhGPx оказалась также способна восстанавливать гидроперекиси тимина, которые образуются при действии АФК на тиминовые остатки ДНК (константа скорости для PhGPx на 4 порядка выше, чем для cGPx).
Слайд 84Восстановленный глутатион – важнейший компонент антиоксидантной защиты
В глутатионпероксидазной системе вторым по
GSH представляет собой трипептид γ-глутамилцистеинилглицин (т.е. состоит из 3-х аминокислотных остатков), в котором, однако аминогруппа (—NH2) цистеина соединена с глутаматом через карбоксильную группу (—СООН) боковой цепи глутамата, а не через α-карбоксильную группу как должно быть при обычной пептидной связи.
GSH играет исключительно важную роль в клетке, осуществляя различные защитные и регуляторные функции.
Слайд 85Основные функции глутатиона в клетке
Антиоксидантная
защита
Редокс-регуляция активности тиол- или дисульфид-содержащих низкомолекулярных регуляторных
Участие в детоксикации ксенобиотиков, осуществляемой глутатион-S-трансферазой
Неферментативная
антиоксидантная
защита
Ферментативная
антиоксидантная
защита
Перехват
свободных
радикалов
Детоксикация перекиси водорода H2O2 и
органических гидроперекисей ROOH глутатионпероксидазной системой
Слайд 86Восстановленный глутатион – важнейший небелковый тиол в клетке
Внутриклеточные концентрации восстановленного глутатиона
Восстановленый глутатион – это основной небелковый тиол в клетке. Его доля составляет 75-90% от общего содержания небелковых тиолов в клетке.
Среди других небелковых тиолов наибольшие концентрации имеют цистеин и коэнзим А.
Большая часть внутриклеточного глутатиона представлена восстановленным глутатионом (ориентировочно 95%).
Слайд 87Гемоксигеназа
NADPH
NADP+
O2
CO
Fe2+
Heme
oxygenase
Biliverdin
Гемоксигеназа – это фермент, который окисляет гем (тип b).
При этом образуется
Heme
(type b)
M = methyl (-CH3), V = vinyl (-CH=CH2),
P = propionic acid (-CH2-CH2-COOH)
Side chains of pyrrole rings
in type b heme
Слайд 89Почему гемоксигеназу относят к антиоксидантным ферментам?
Для ответа на этот вопрос рассмотрим
Слайд 90Гем и его основные функции в организме
Гем является составной частью –
ПРОСТЕТИЧЕСКАЯ ГРУППА (от греч. prosthetikos - прибавляющий) – это небелковая часть молекул сложных белков, в т.ч. ферментов.
ГЕМОПРОТЕИНЫ (т.е. белки, в состав которых входит гем) выполняют в организме множество исключительно важных функций, таких как:
связывание и перенос кислорода (гемоглобин, миоглобин);
клеточное дыхание и перенос электронов (цитохромы a, b, c);
биотрансформация ксенобиотиков и стероидов (цитохром P-450);
инактивация перекиси водорода и органических гидроперекией (каталаза и глутатионпероксидаза);
окисление различных субстратов, опосредованное перекисью водорода (миелопероксидаза, лактопероксидаза и др. пероксидазы);
синтез простагландинов (циклооксигеназа);
сигнальная трансдукция (гуанилатциклаза, синтаза оксида азота)
и другие функции.
У позвоночных встречается несколько типов гема, различающихся боковыми цепями пиррольных колец. Гем типа b наиболее распространен и является простетической группой всех гемопротеинов за исключением цитохромов c и a, в состав которых входит гем типа c и гем типа a, соответственно.
Слайд 91Свободный гем – сильный прооксидант
Время жизни молекул белков (в том числе
Высвобождающийся при распаде гемопротеинов гем также подвергается дальнейшей утилизации. Единственный физиологически значимый путь утилизации свободного гема в организме – это его окисление гемоксигеназой.
Свободный гем имеет в своем составе ион Fe и поэтому является как и свободный ион Fe мощным прооксидантом, вызывая распад органических гидроперекисей ROOH с образованием радикалов RO• и ROO• и распад перекиси водорода H2O2 с образованием гидроксильного радикала OH• (по реакции Фентона):
H2O2 + гем(Fe2+) → OH- + OH• + гем(Fe3+).
Благодаря своим гидрофобным свойствам и, соответственно хорошей растворимости в липидах, свободный гем является эффективным промотором перекисного окисления липидов, которое очень вредно для липидного слоя биомембран и клетки в целом.
Слайд 92Биливердин превращается в билирубин
Biliverdin
NADPH
NADP+
Biliverdin
reductase
Bilirubin
Conjugation
Excretion
Oxygen free radicals
(OFR)
БИЛИФЕРДИН – основной продукт окисления гема
БИЛИРУБИН, как оказалось, является сильным перехватчиком кислород-содержащих свободных радикалов, сравнимым по эффективности с известным мощным антиоксидантом α–токоферолом (витамином E). Под действием этих радикалов билирубин окисляется в биливердин.
Слайд 93Гемоксигеназа – антиоксидантный фермент
Таким образом, гемоксигеназа участвует в превращении гема (сильного
Именно поэтому гемоксигеназу рассматривают как антиоксидантный фермент.
Высвобождающееся железо (в форме Fe2+) при окислении свободного гема гемоксигеназой, конечно, является прооксидантом. Однако, под действием избыточных количеств ионов Fe2+ в клетке быстро индуцируется железо-запасающий белок ФЕРРИТИН, который связывает свободные ионы Fe2+ и окисляет их до Fe3+. Каждая молекула ферритина связывает до 4500 ионов железа!!!
Ферритин представляет собой глобулярный белок, состоящий из 24 субъединиц (2-х типов), образующих полую сферическую оболочку, внутри которой запасается железо.
Поскольку ферритин удаляет из цитозоля клетки избыточные количества двухвалентного железа Fe2+ (являющегося сильным прооксидантом), он также рассматривается как антиоксидантный белок.
Слайд 94
Внутриклеточная локализация основных антиоксидантных ферментов
Catalase
Mitochondrion
Matrix:
Mn-SOD
Intermembrane
space:
PhGPx (long form)
Cu,Zn-SOD
Cytosol
PhGPx (short form)
non-Se GPx
Cu,Zn-SOD
Heme oxygenase
Extracellular fluids
and interstitium:
ECSOD



























































![Селен-содержащие GPxНеселеновые GPx (глутатион-S-трансферазы [GSTs])Цитозольная (клеточная) GPx (cGPx или GPx-1) GPx гидроперекисей фосфолипидов (PhGPx или](/img/tmb/5/437108/75d4447921fb48a71d6e05ad28c70199-800x.jpg)