- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Обмен аминокислот. Синтез и распад нуклеиновых кислот презентация
Содержание
- 1. Обмен аминокислот. Синтез и распад нуклеиновых кислот
- 2. Биологическая ценность аминокислот
- 3. СН3
- 4. Н О
- 5. Н О
- 6. Дни болезни Активность ферментов 1 2
- 7. Декарбоксилирование аминокислот (образование биологически-активных аминов)
- 8. N -CH2-CH-COOH NH2
- 9. N -CH2-CH2 NH2
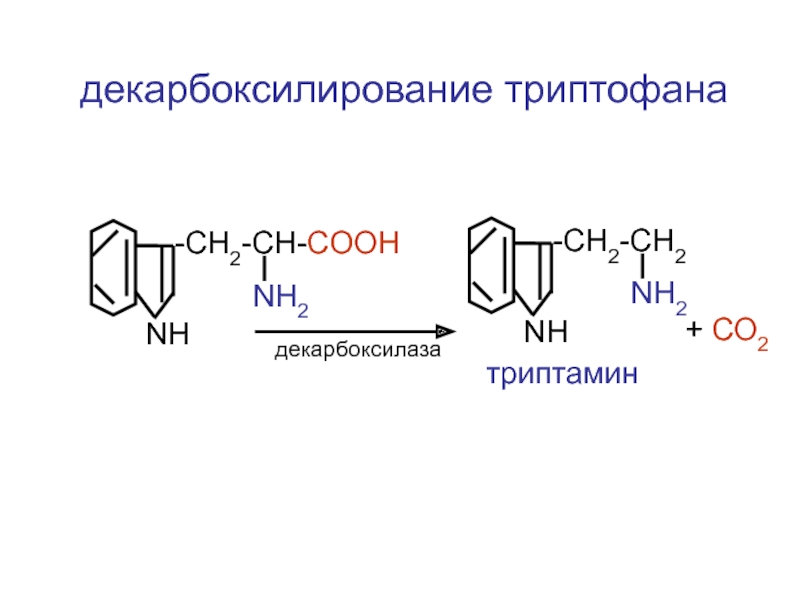
- 10. -CH2-CH-COOH NH2 NH -CH2-CH2 NH2 NH триптамин декарбоксилаза + СО2 декарбоксилирование триптофана
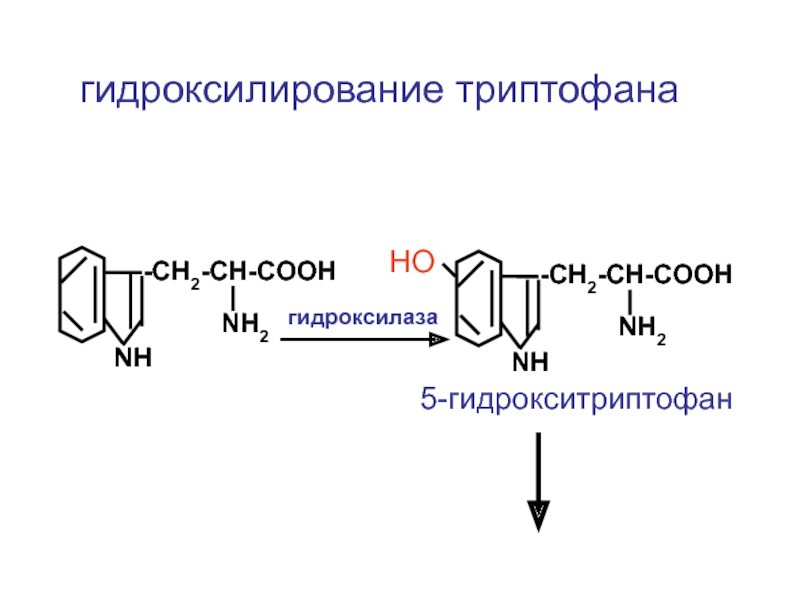
- 11. -CH2-CH-COOH NH2 NH гидроксилирование триптофана -CH2-CH-COOH NH2 NH НО гидроксилаза 5-гидрокситриптофан
- 12. -CH2-CH-COOH NH2 NH НО -CH2-CH2
- 13. СOOH CH-NH2 CH2 CH2 COOH CH2-NH2
- 14. CH2-CH-COOH NH2 ОН
- 15. CH2-CH-COOH NH2 ОН ОН
- 16. CH2-CH2 NH2 ОН ОН Синтез
- 17. CH-CH2 ОН NH2 ОН ОН
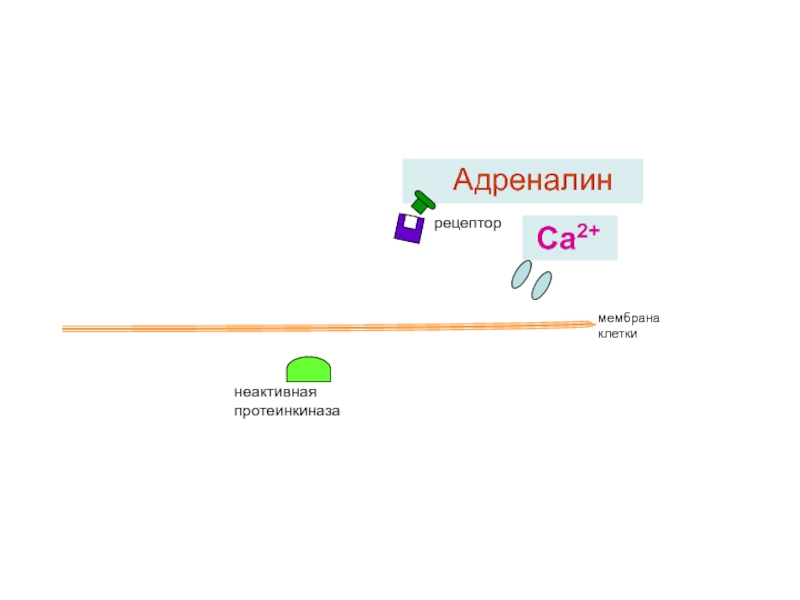
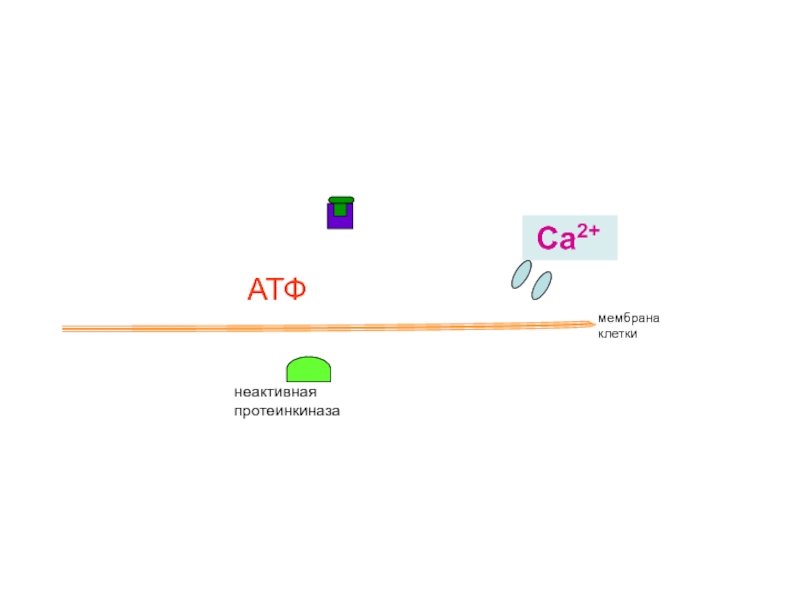
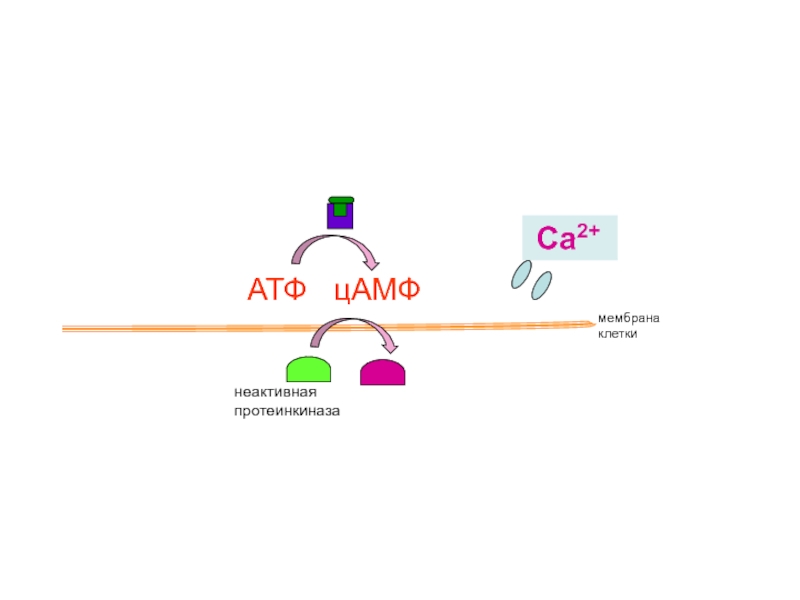
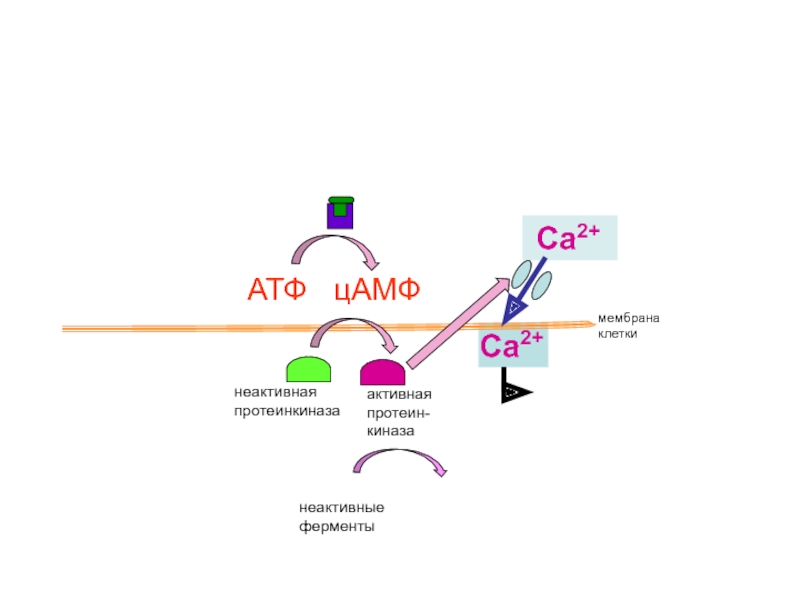
- 18. Активация адреналином сокращений сердца и обмена веществ
- 19. рецептор неактивная протеинкиназа мембрана клетки Са2+
- 25. рецептор
- 26. рецептор
- 27. рецептор
- 28. рецептор
- 29. рецептор
- 30. рецептор
- 32. неактивная
- 33. неактивная
- 34. неактивная
- 35. неактивная
- 43. Окислительное дезаминирование аминокислот
- 44. Реакция окислительного дезаминирования глутаминовой кислоты СООН
- 45. Реакция окислительного дезаминирования аспарагиновой кислоты СООН
- 46. аланин серин цистеин
- 47. СН3 СООН
- 48. окислительное дезаминирование глутаминовой кислоты + Н2О
- 49. NH3 окислительное
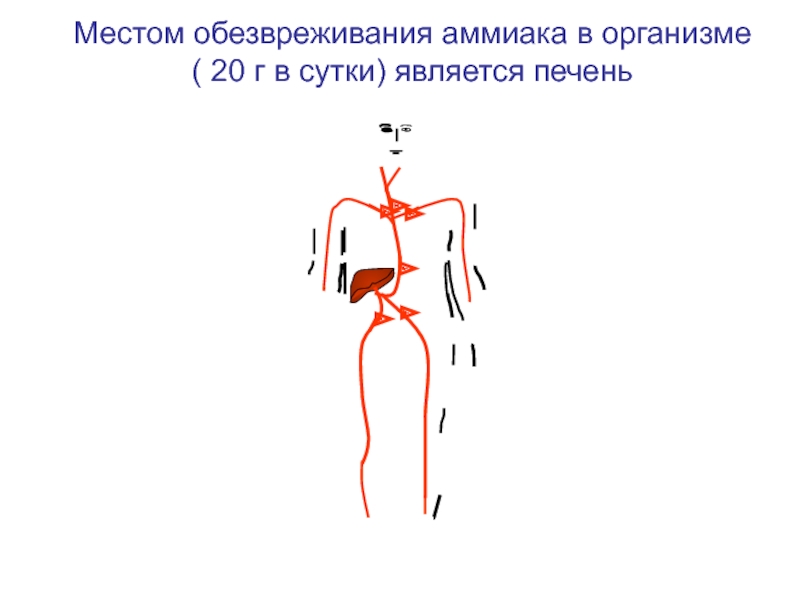
- 50. главный механизм обезвреживания аммиака в организме
- 52. НО – С – ОН
- 53. синтез мочевины
- 54. NH3 + CO2 +
- 55. образование карбамоилфосфата ГЛУ α-кетоглута-ровая
- 56. NH2 C=O O
- 57. NH2 C=NH NH CH2 CH2 CH2
- 58. NH2 CH2 CH2 CH2
- 59. Вспомогательный, быстрый механизм связывания аммиака
- 60. СООН СН2 СН2 CH-NH2 COOH NH3 СОNH2
- 62. Содержание мочевины в крови 2,5 – 8,3
- 63. Регуляция обмена белков
- 64. синтез белка концентрация и состав
- 65. Влияние некоторых факторов на концентрацию и состав
- 66. Влияние некоторых факторов на активность АРС-аз
- 67. Факторы, влияющие на скорость синтеза и-РНК и
- 68. Гормональная регуляция скорости синтеза белка Соматотропин, половые
- 69. На скорость дезаминирования аминокислот влияют: Соотношение НАДН2
- 70. Взаимосвязь между обменом белков, углеводов и липидов.
- 71. триглицериды
- 72. фосфоглицериновая кислота фосфоенол-пируват пируват ацетил-КоА Цикл
- 73. СН2-ОН СН -ОН СН2-ОН СН2-ОН
- 74. СООН С = О СН2-ОН СООН СH-NH2
- 75. Обмен нуклеиновых кислот
- 76. регенерация апоптоз Динамические равновесие между процессом запрограммированной смерти клетки и ее клонированием
- 77. Продукты, наиболее богатые нуклеиновыми кислотами икра дрожжи лекарственные препараты (нуклеинат натрия)
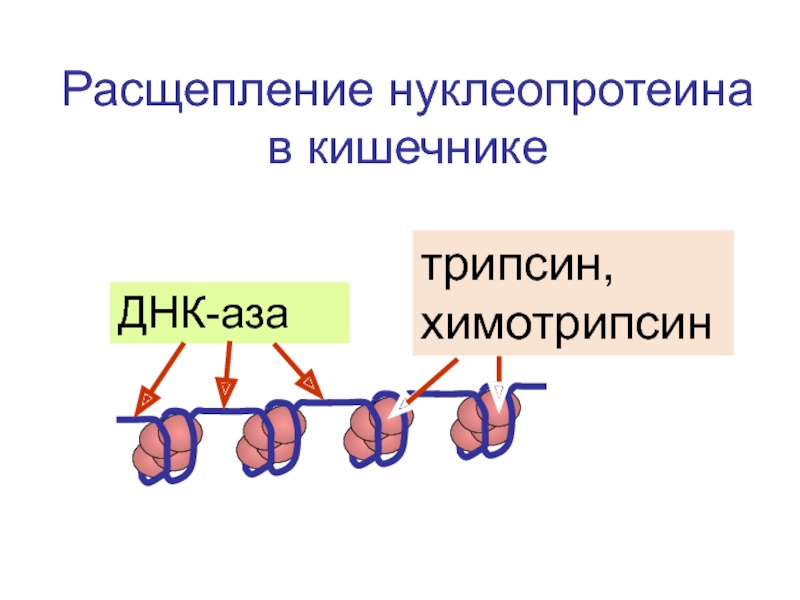
- 79. Расщепление РНК в кишечнике РНК-аза РНК
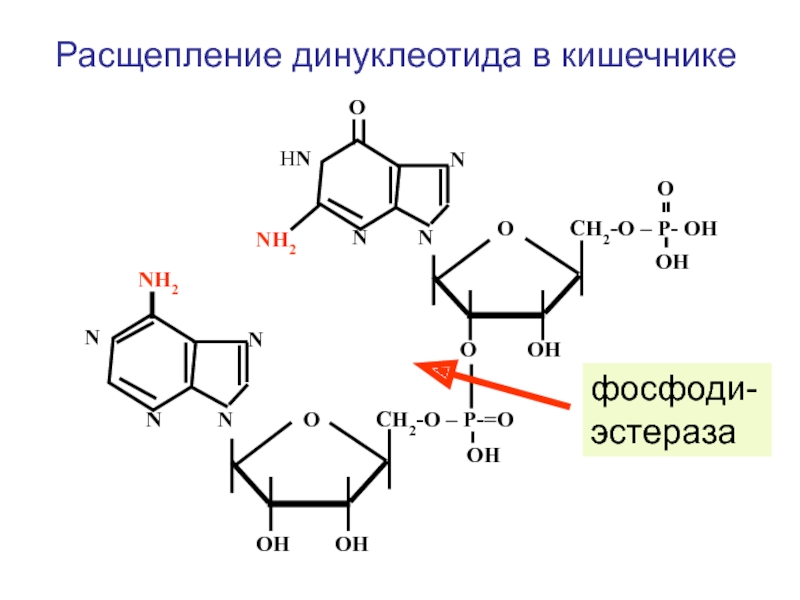
- 80. N N
- 81. Распад пуриновых нуклеотидов
- 82. N N
- 83. N N
- 84. N N
- 85. N N
- 86. N NН NН
- 87. NH N N
- 88. Содержание мочевой кислоты в крови 0,24 +0,06 ммоль/л
- 89. Распад пиримидиновых нуклеотидов
- 90. N
- 91. N
- 92. NН
- 93. NН
- 94. Биосинтез пуриновых нуклеотидов
- 95. СН2ОРО3H2 NH2 CH2 COOH NH2 -глутамин
- 96. H2C
- 97. NН2 N НN
- 98. N N
- 99. N N
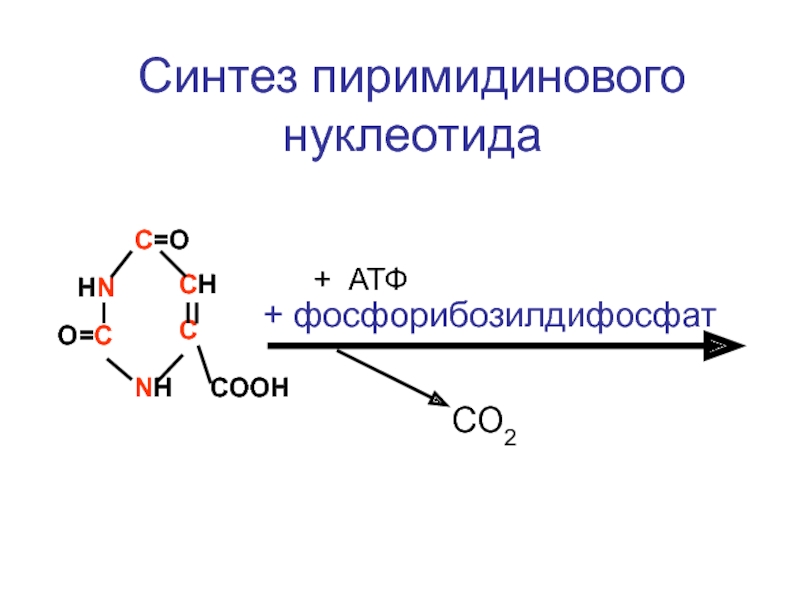
- 100. Биосинтез пиримидиновых нуклеотидов
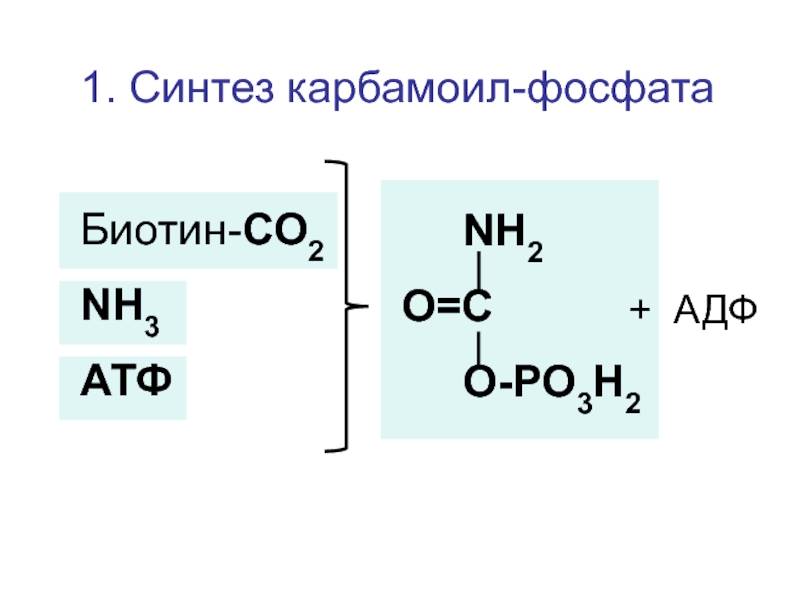
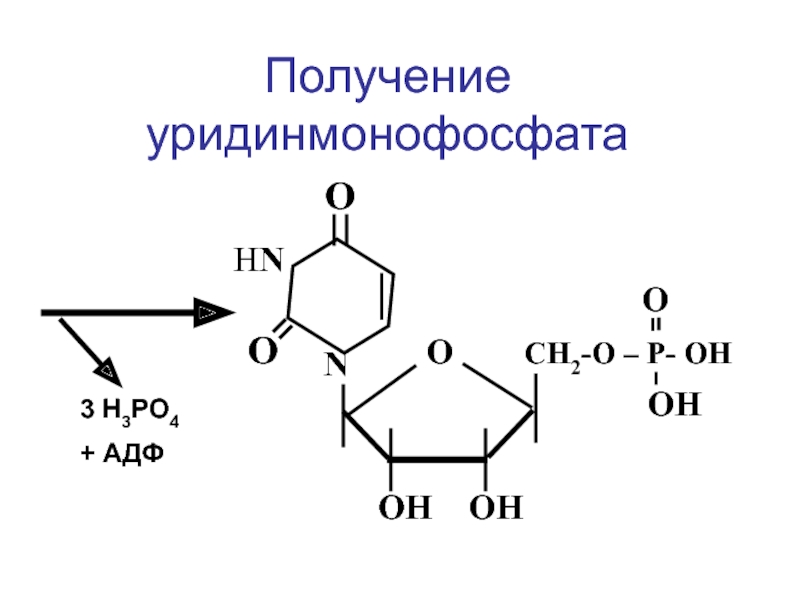
- 101. 1. Синтез карбамоил-фосфата
- 103. СН2ОРО3H2 ОH ОН
- 104. HN O=C
- 105. N
- 106. О
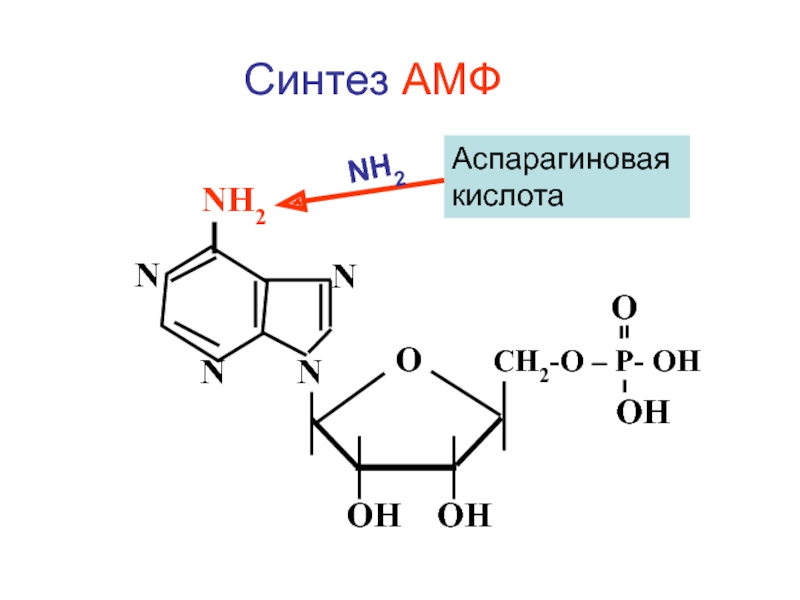
- 107. Энергизация нуклеотидов 1) АМФ + АТФ =
Слайд 2Биологическая ценность аминокислот
пируват ----------------------→ аланин
глицерин- ---------------------→ серин
серин -------------------------→ глицин
аланин-----------------------→ цистеин
щук ---------------→ аспарагиновая к-та
оксоглутаровая → глутаминовая к-та
глутаминовая к-та -----→ пролин
глутаминовая к-та ----→ гистидин
фенилаланин --------------→ тирозин
незаменимые
треонин
метионин
валин
лейцин
изолейцин
лизин
фенилаланин
триптофан
аргинин
Слайд 3
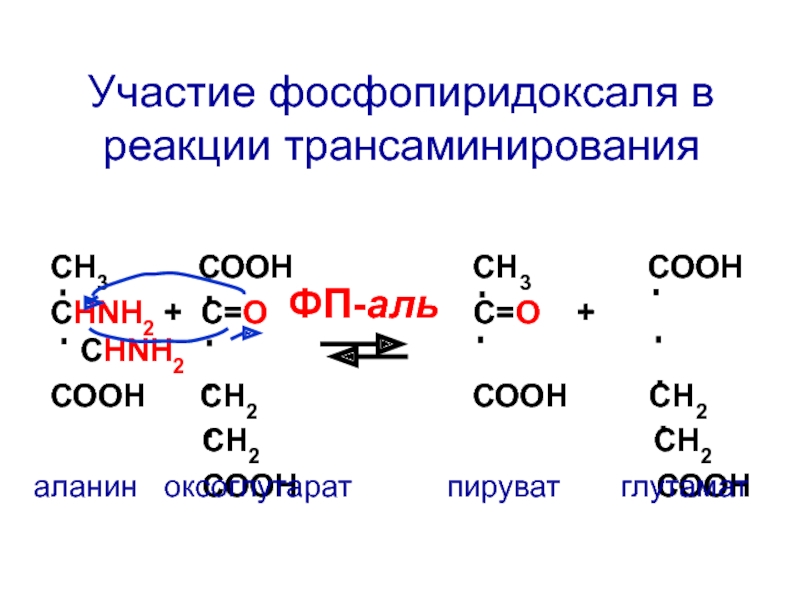
СН3 СООН
СНNH2 + C=О С=О + СНNH2
СООН СН2 СООН СН2
СН2 СН2
СООН СООН
ФП-аль
аланин оксоглутарат пируват глутамат
Участие фосфопиридоксаля в реакции трансаминирования
Слайд 4Н О
С
СН2О-РО3Н2
НО
Н3С
N
СН2-NH2
СН2О-РО3Н2
НО
Н3С
N
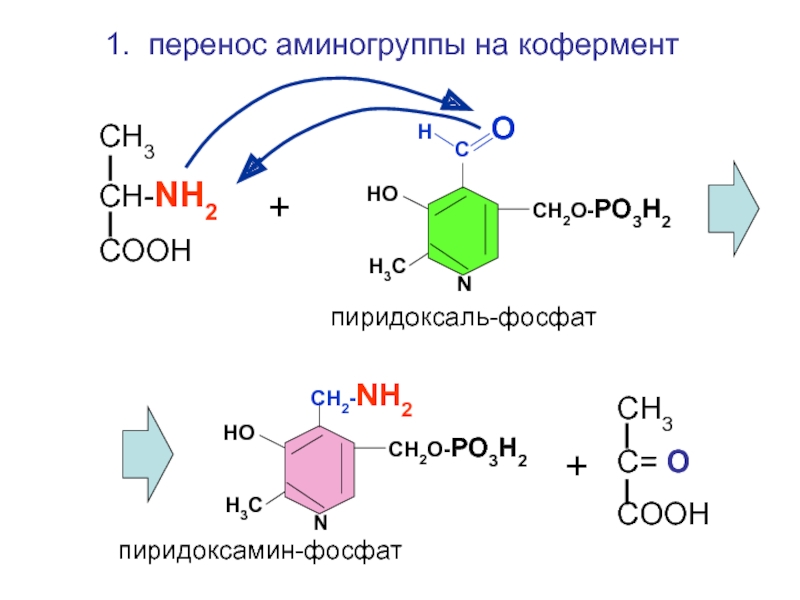
пиридоксаль-фосфат
пиридоксамин-фосфат
СН3
СН-NH2
COOH
+
СН3
С= O
COOH
+
1. перенос аминогруппы на кофермент
Слайд 5Н О
С
СН2О-РО3Н2
НО
Н3С
N
СН2-NH2
СН2О-РО3Н2
НО
Н3С
N
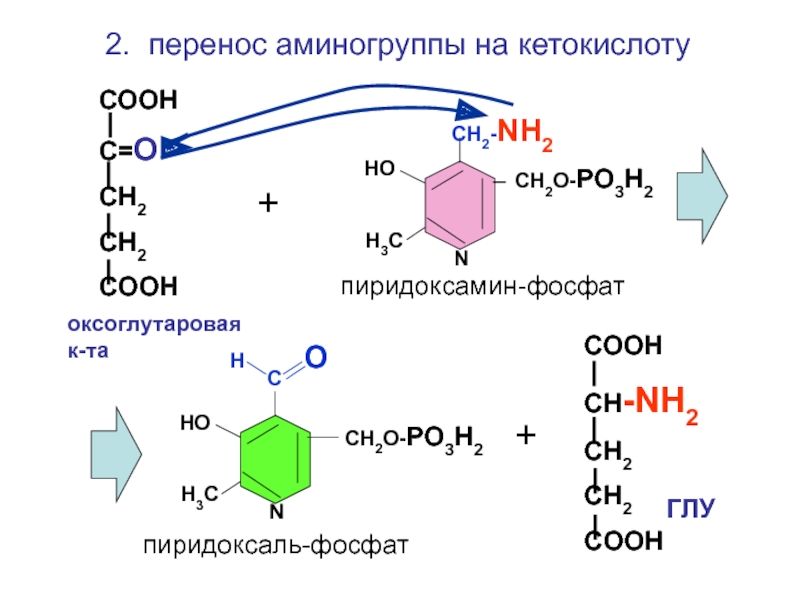
пиридоксаль-фосфат
пиридоксамин-фосфат
СООН
С=О
СН2
СН2
COOH
+
+
2. перенос аминогруппы на кетокислоту
СООН
СН-NH2
СН2
СН2
COOH
оксоглутаровая к-та
ГЛУ
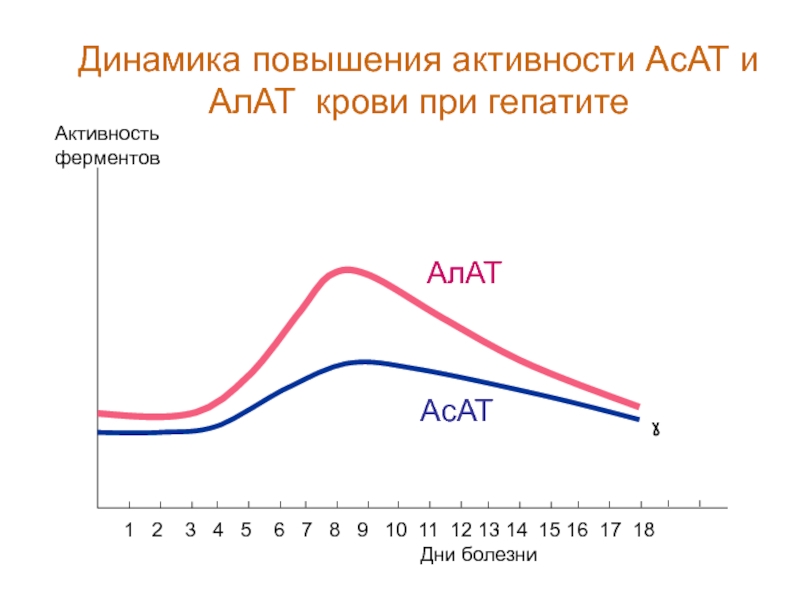
Слайд 6Дни болезни
Активность ферментов
1 2 3 4 5
АлАТ
Динамика повышения активности АсАТ и АлАТ крови при гепатите
АсАТ
Слайд 9N -CH2-CH2
NH2
NH
N -CH2-C=О
NH
моноамино-оксидаза
гистамин имидазолацетальдегид
Окисление гистамина
NH3
O2
Слайд 11
-CH2-CH-COOH
NH2
NH
гидроксилирование триптофана
-CH2-CH-COOH
NH2
NH
НО
гидроксилаза
5-гидрокситриптофан
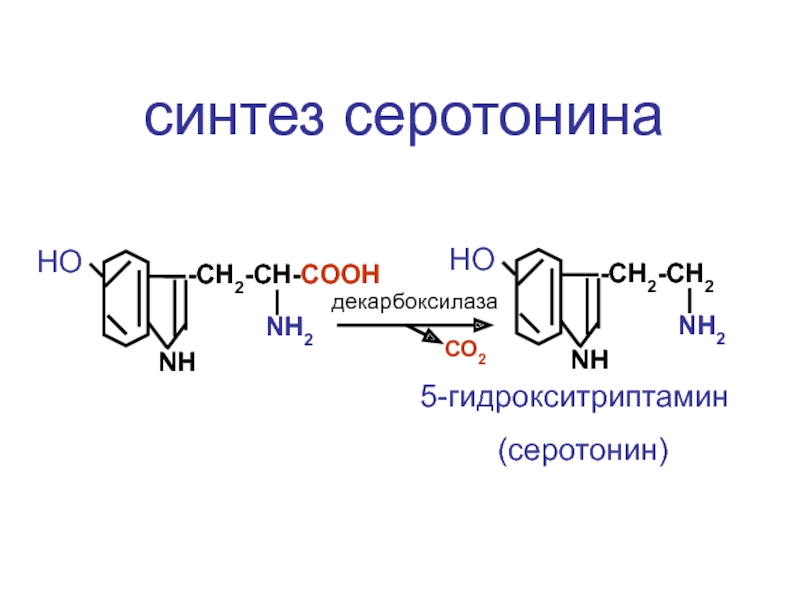
Слайд 12
-CH2-CH-COOH
NH2
NH
НО
-CH2-CH2
NH2
NH
НО
5-гидрокситриптамин
(серотонин)
декарбоксилаза
синтез серотонина
СО2
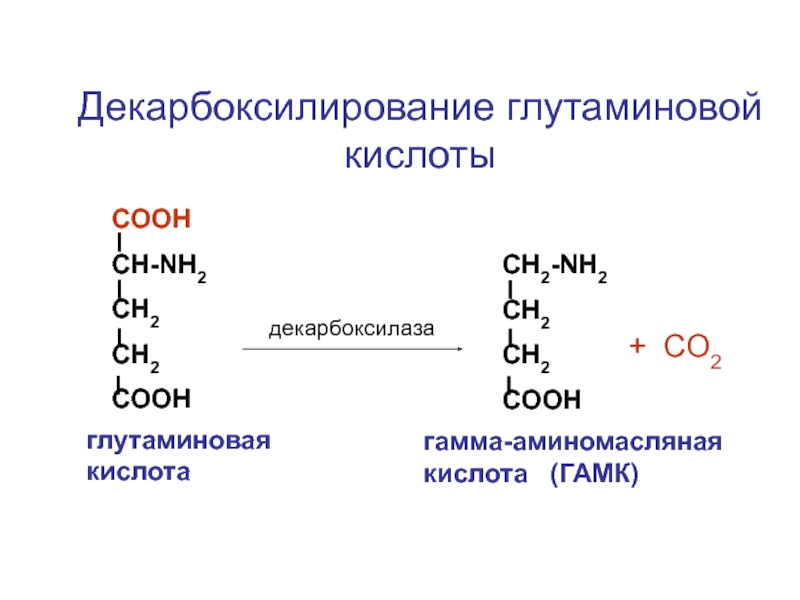
Слайд 13СOOH
CH-NH2
CH2
CH2
COOH
CH2-NH2
CH2
CH2
COOH
декарбоксилаза
+ CO2
глутаминовая кислота
гамма-аминомасляная кислота (ГАМК)
Декарбоксилирование глутаминовой кислоты
Слайд 14
CH2-CH-COOH
NH2
ОН
CH2-CH-COOH
NH2
ОН
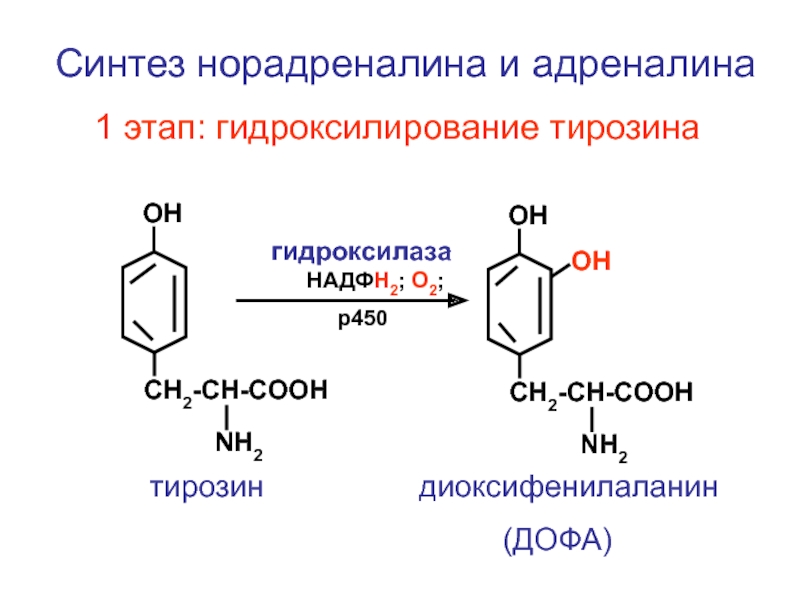
Синтез норадреналина и адреналина
1 этап: гидроксилирование тирозина
НАДФН2;
р450
ОН
тирозин диоксифенилаланин
(ДОФА)
гидроксилаза
Слайд 15
CH2-CH-COOH
NH2
ОН
ОН
CH2-CH2
NH2
ОН
ОН
+ СО2
декарбоксилаза
Синтез норадреналина и адреналина
2 этап: декарбоксилирование диоксифенилаланина
диоксифенилэтиламин (дофамин)
Слайд 16
CH2-CH2
NH2
ОН
ОН
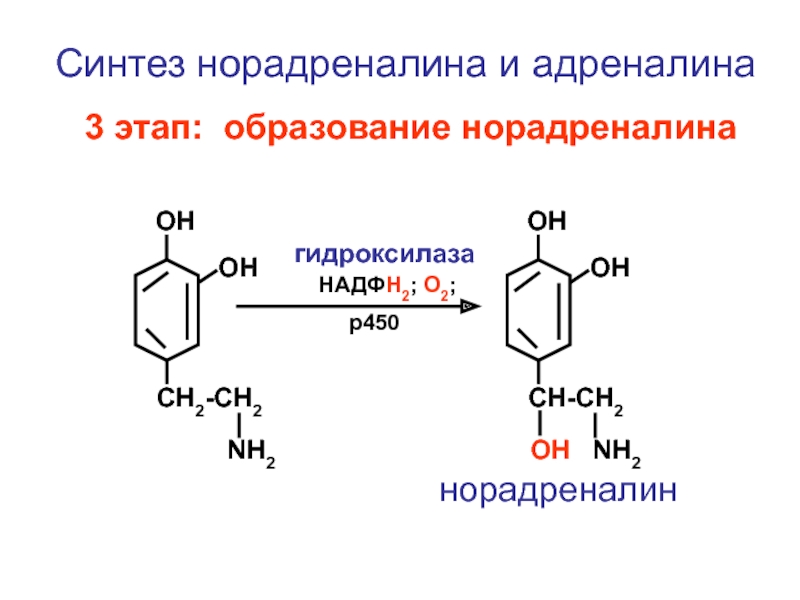
Синтез норадреналина и адреналина
3 этап: образование норадреналина
CH-CH2
ОН
ОН
ОН
НАДФН2; О2;
р450
гидроксилаза
норадреналин
Слайд 17
CH-CH2
ОН NH2
ОН
ОН
норадреналин
CH-CH2
ОН NH – СН3
ОН
ОН
адреналин
метил-фолиевая кислота; вит. В12
метионин
Синтез адреналина
Слайд 40
неактивная протеинкиназа
активная
протеин-киназа
неактивные
ферменты
мембрана
клетки
АТФ цАМФ
Са2+
Са2+
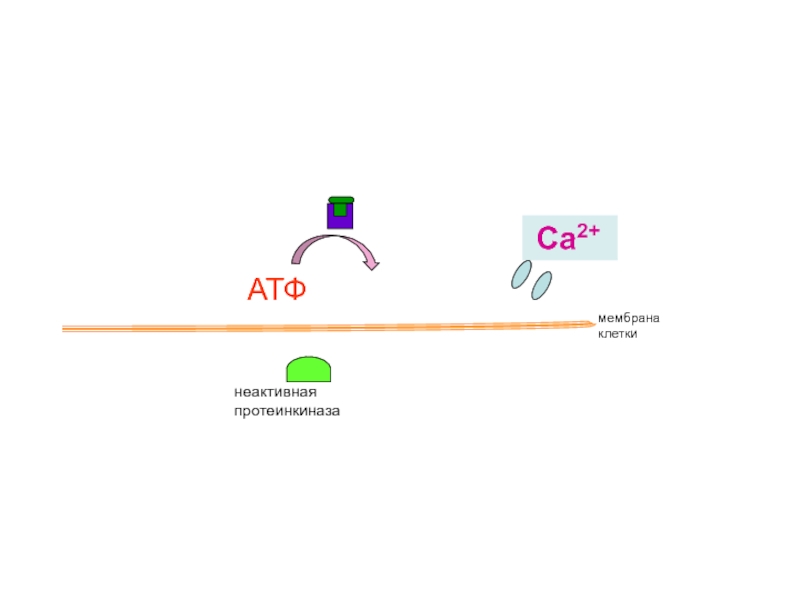
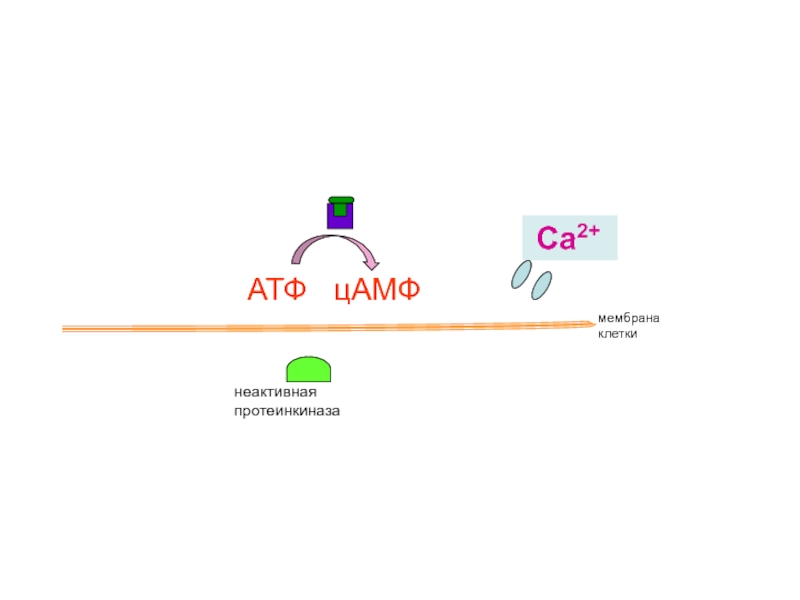
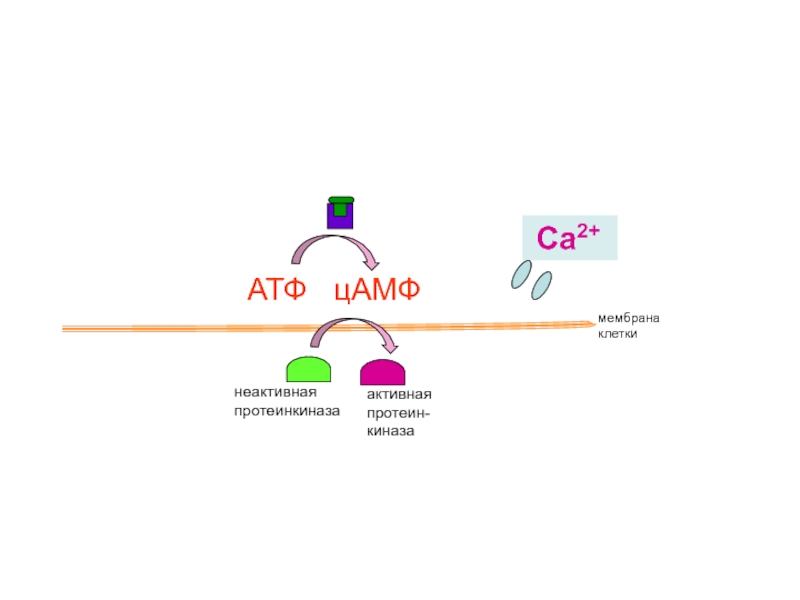
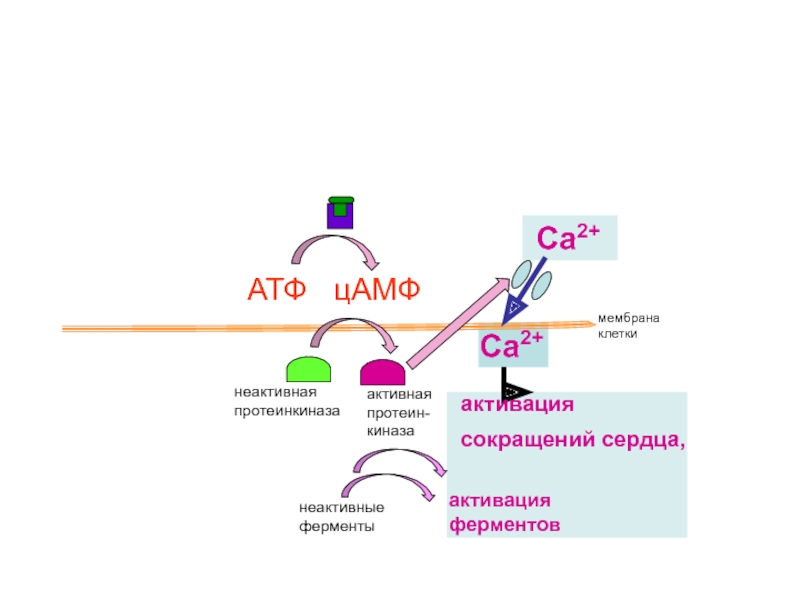
Слайд 41
неактивная протеинкиназа
активная
протеин-киназа
неактивные
ферменты
мембрана
клетки
АТФ цАМФ
Са2+
Са2+
активация сокращений сердца,
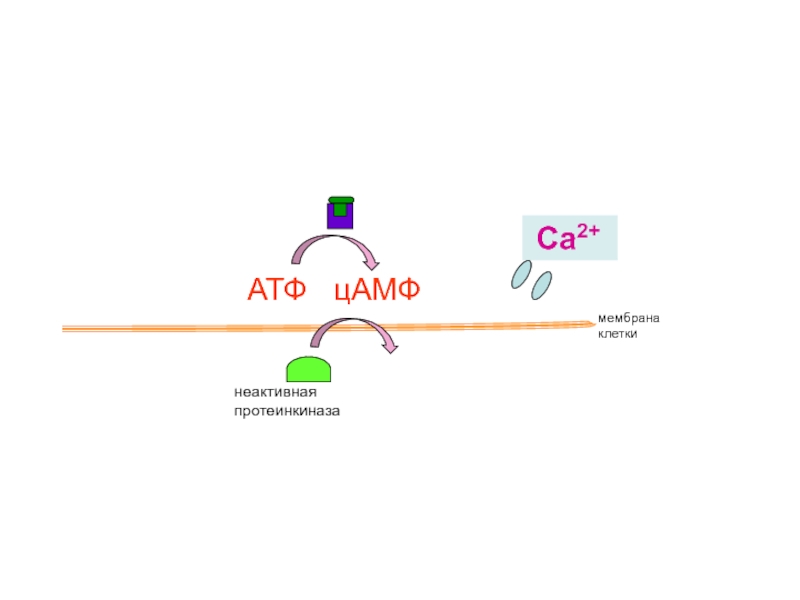
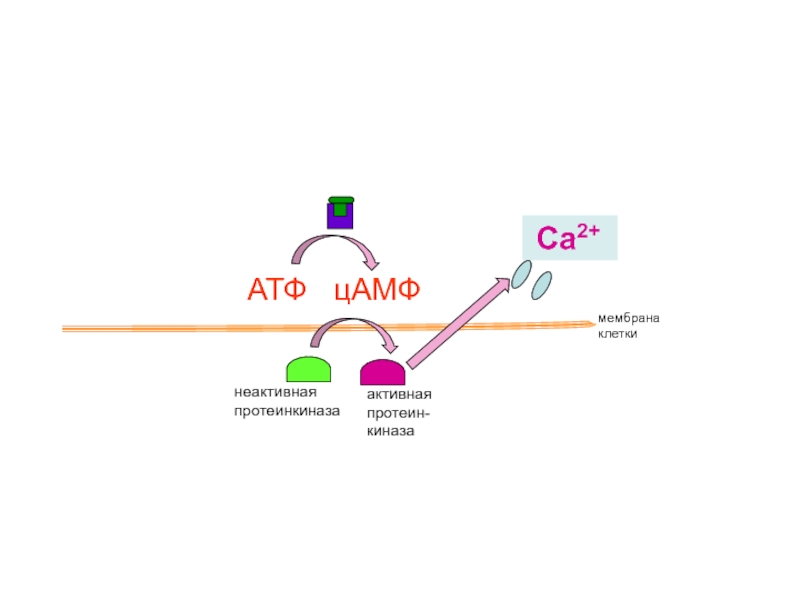
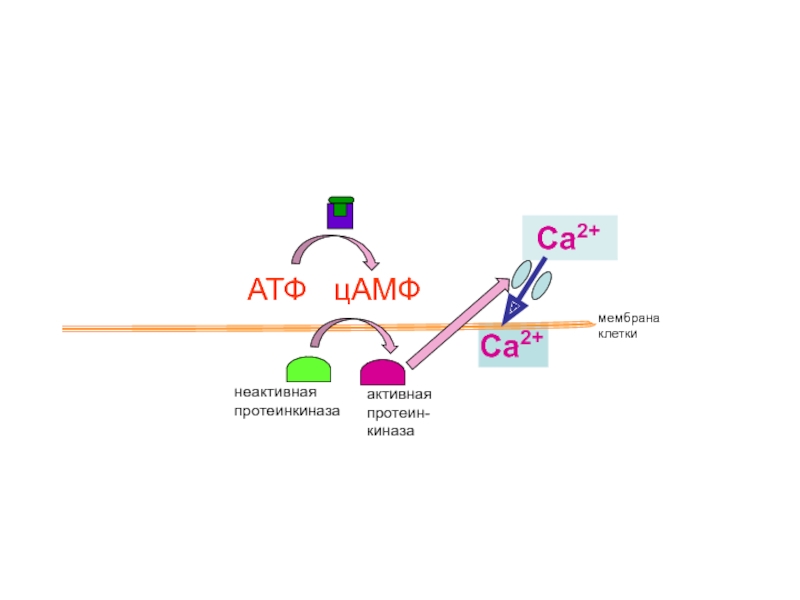
Слайд 42
неактивная протеинкиназа
активная
протеин-киназа
неактивные
ферменты
активация
ферментов
мембрана
клетки
АТФ цАМФ
Са2+
Са2+
активация сокращений сердца,
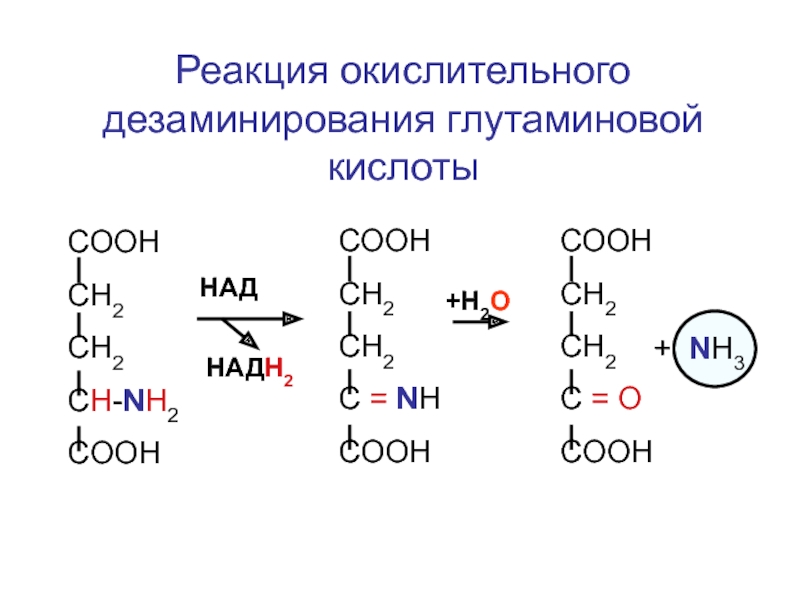
Слайд 44
Реакция окислительного дезаминирования глутаминовой кислоты
СООН
СН2
СН2
CH-NH2
COOH
HАД
HАДН2
+Н2О
СООН
СН2
СН2
C = NH
COOH
СООН
СН2
СН2
C = О
COOH
+ NH3
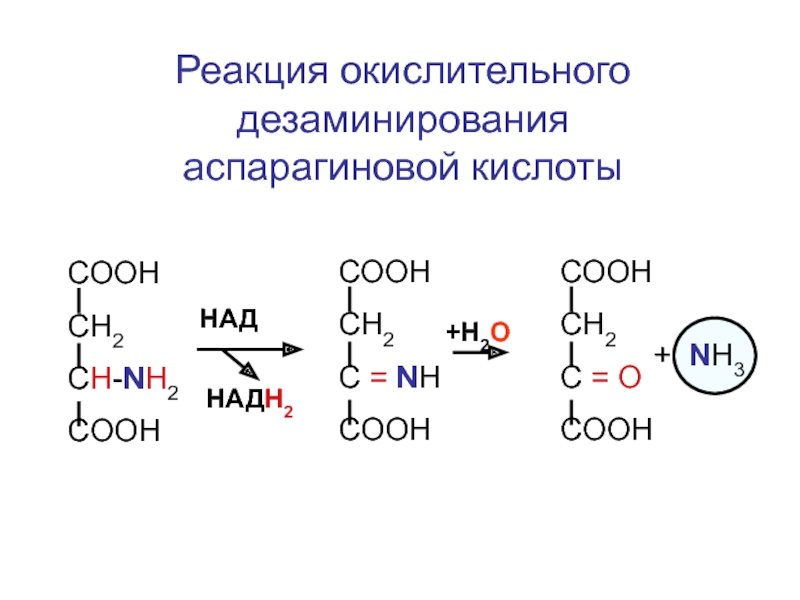
Слайд 45
Реакция окислительного дезаминирования аспарагиновой кислоты
СООН
СН2
CH-NH2
COOH
HАД
HАДН2
+Н2О
СООН
СН2
C = NH
COOH
СООН
СН2
C = О
COOH
+ NH3
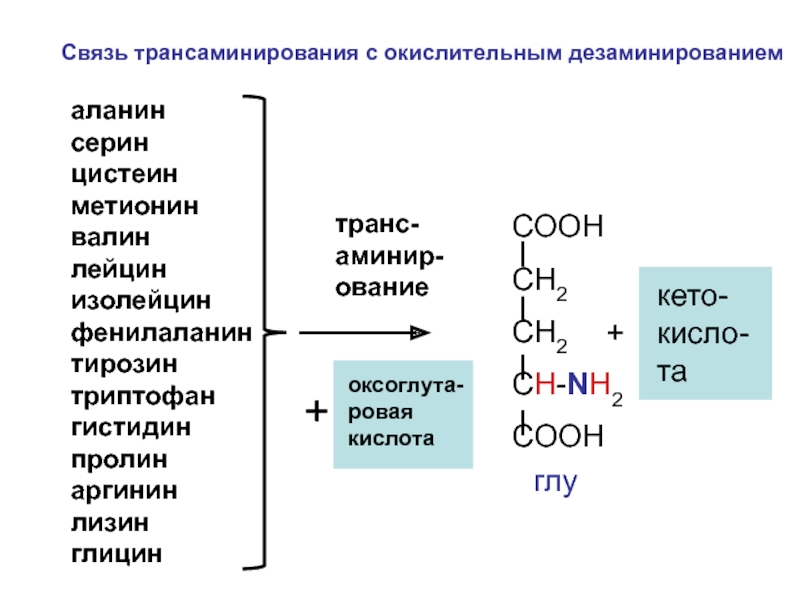
Слайд 46
аланин серин цистеин метионин валин лейцин изолейцин
транс-аминир-ование
оксоглута-ровая кислота
+
СООН
СН2
СН2
CH-NH2
COOH
+
кето-кисло-та
Связь трансаминирования с окислительным дезаминированием
глу
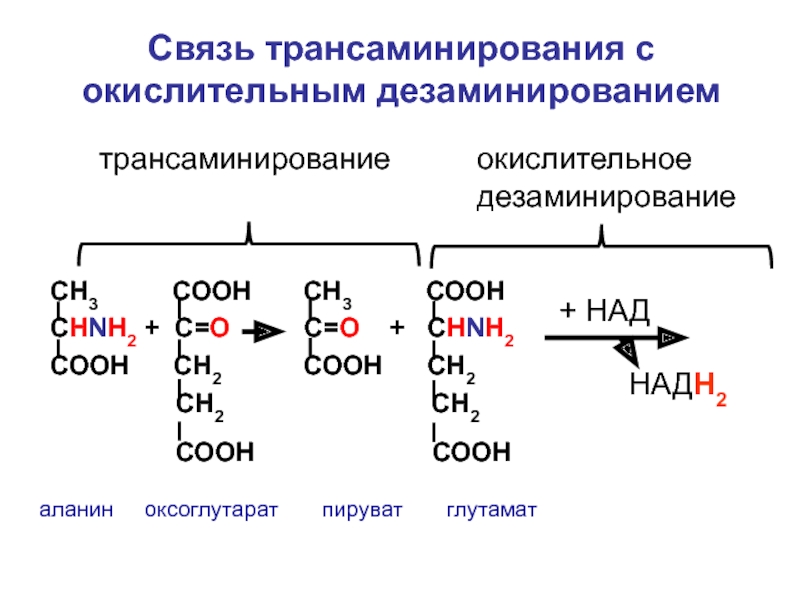
Слайд 47
СН3 СООН СН3
СНNH2 + C=О С=О + СНNH2
СООН СН2 СООН СН2
СН2 СН2
СООН СООН
аланин оксоглутарат пируват глутамат
+ НАД
НАДН2
трансаминирование
окислительное дезаминирование
Связь трансаминирования с окислительным дезаминированием
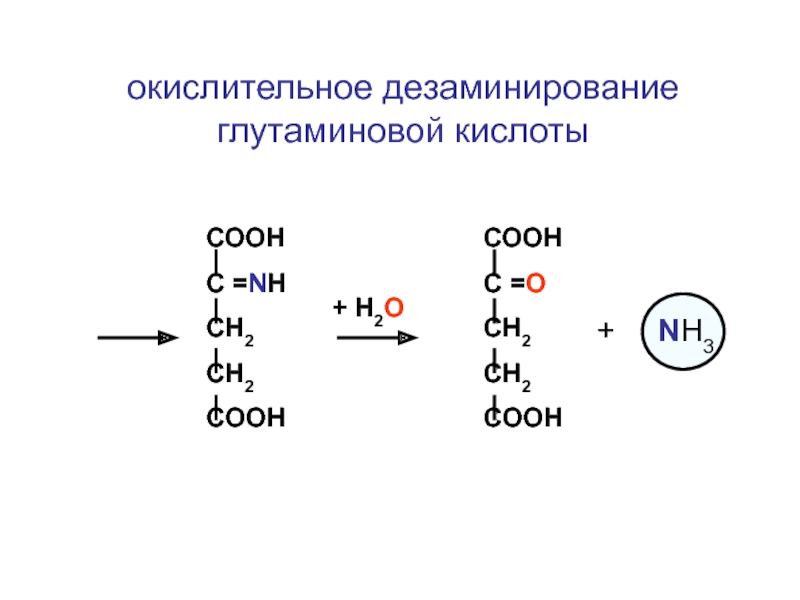
Слайд 48
окислительное дезаминирование глутаминовой кислоты
+ Н2О
СООН
С =NH
СН2
CH2
COOH
СООН
С =O
СН2
CH2
COOH
+ NH3
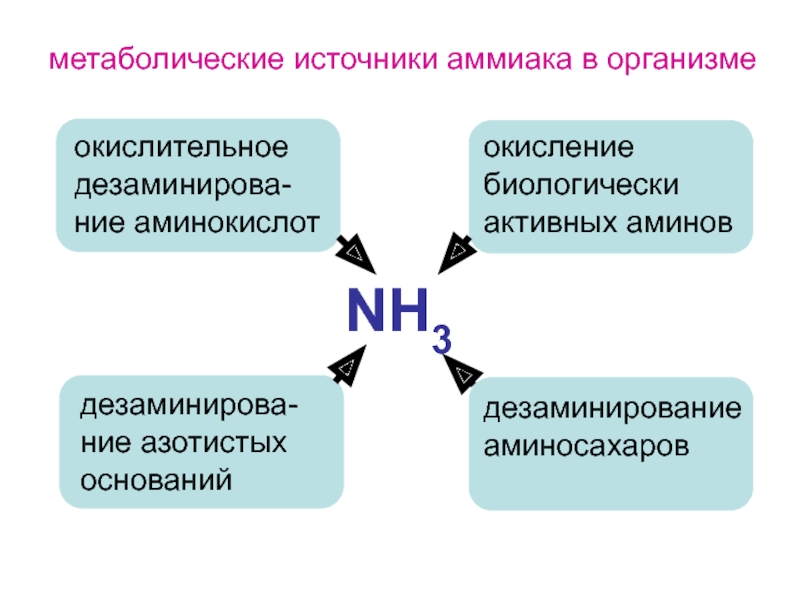
Слайд 49
NH3
окислительное дезаминирова-ние аминокислот
дезаминирова-ние азотистых оснований
окисление биологически активных аминов
дезаминирование аминосахаров
метаболические источники аммиака
Слайд 54
NH3 + CO2 + 2 АТФ
NH2-C-O~P=O
O
OH
OH
орнитин
цитруллин
аспарагино-вая кислота
аргинин
фумаро-вая к-та
мочевина
Орнитиновый цикл
карбамоилфосфат
Слайд 55
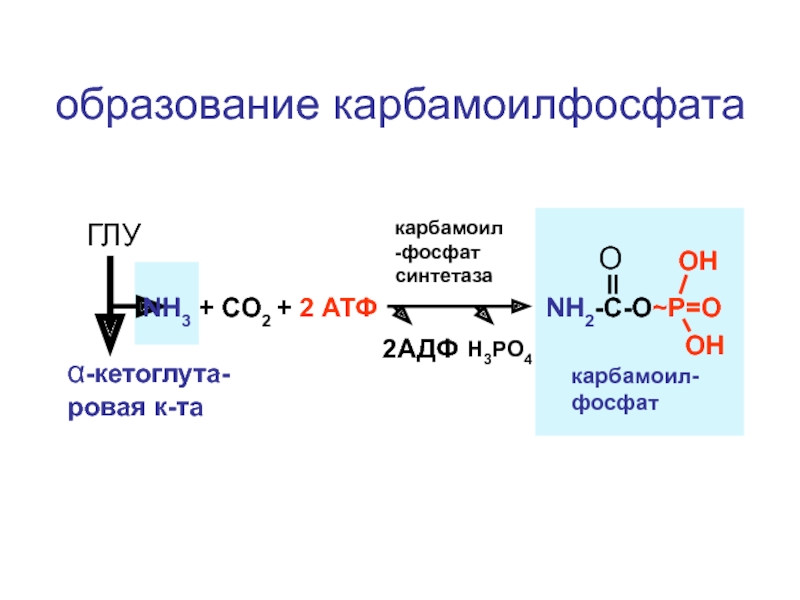
образование карбамоилфосфата
ГЛУ
α-кетоглута-ровая к-та
NH3 + CO2 + 2 АТФ
карбамоил-фосфат синтетаза
2АДФ
H3PO4
NH2-C-O~P=O
O
OH
OH
карбамоил-фосфат
Слайд 56
NH2
C=O
O
P=O
OH
OH
+
NH2
CH2
CH2
CH2
CHNH2
COOH
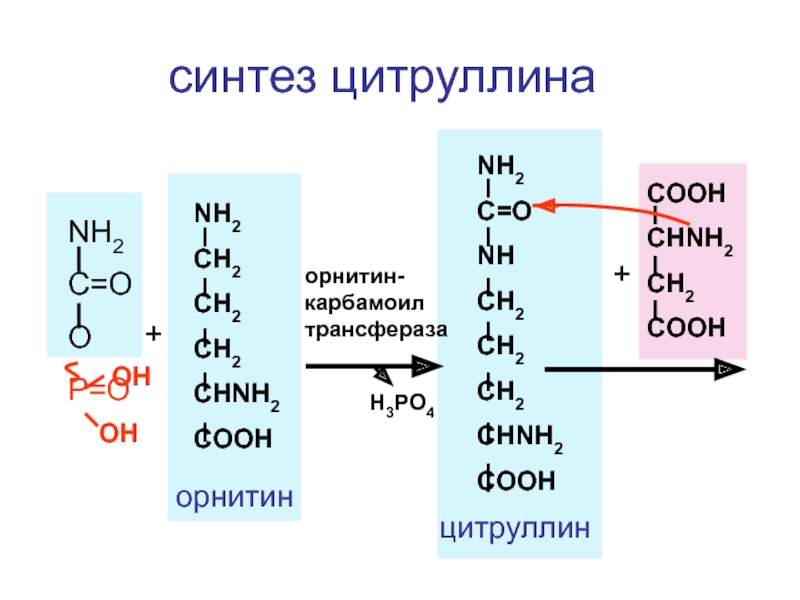
орнитин
орнитин-карбамоил трансфераза
H3PO4
NH2
C=O
NH
CH2
CH2
CH2
CHNH2
COOH
цитруллин
COOH
CHNH2
CH2
COOH
+
синтез цитруллина
Слайд 57
NH2
C=NH
NH
CH2
CH2
CH2
CHNH2
COOH
COOH
CH
CH
COOH
фумаровая к-та
+ АТФ
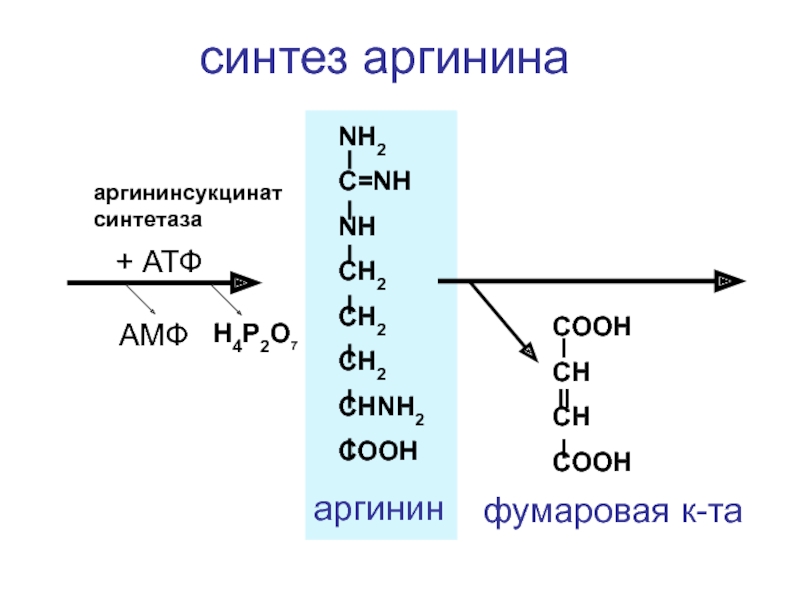
аргининсукцинатсинтетаза
АМФ
H4P2O7
аргинин
синтез аргинина
Слайд 58
NH2
CH2
CH2
CH2
CHNH2
COOH
C=O
NH2
NH2
мочевина
NH2
C=NH
NH
CH2
CH2
CH2
CHNH2
COOH
аргинин
орнитин
аргиназа
+
образование мочевины
Н2О
Слайд 59
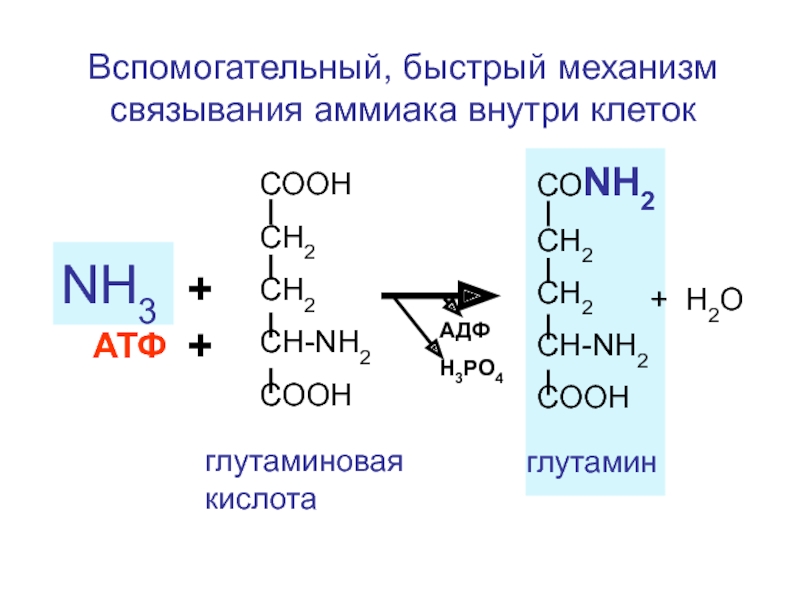
Вспомогательный, быстрый механизм связывания аммиака внутри клеток
СООН
СН2
СН2
CH-NH2
COOH
NH3
+
СОNH2
СН2
СН2
CH-NH2
COOH
АТФ
+
+ H2O
глутаминовая кислота
АДФ
Н3РО4
глутамин
Слайд 60СООН
СН2
СН2
CH-NH2
COOH
NH3
СОNH2
СН2
СН2
CH-NH2
COOH
+ H2O
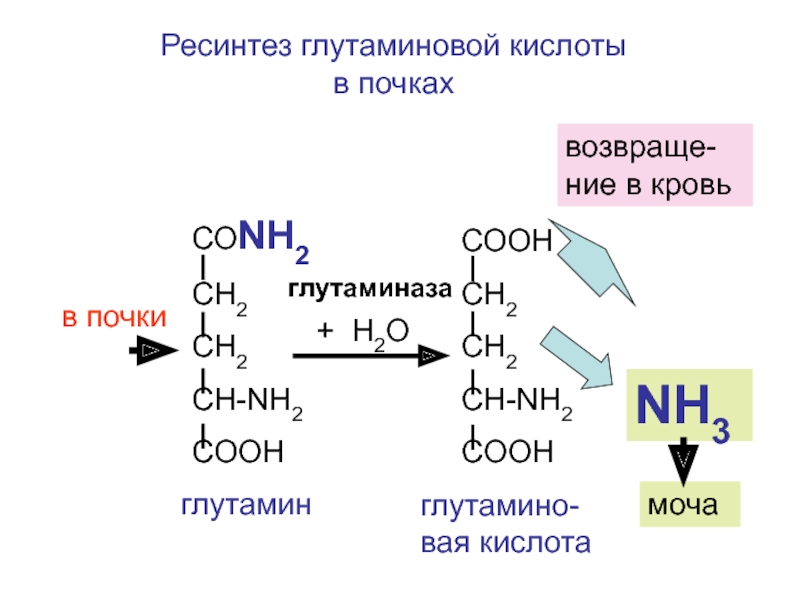
глутамино-вая кислота
глутамин
глутаминаза
моча
возвраще-ние в кровь
в почки
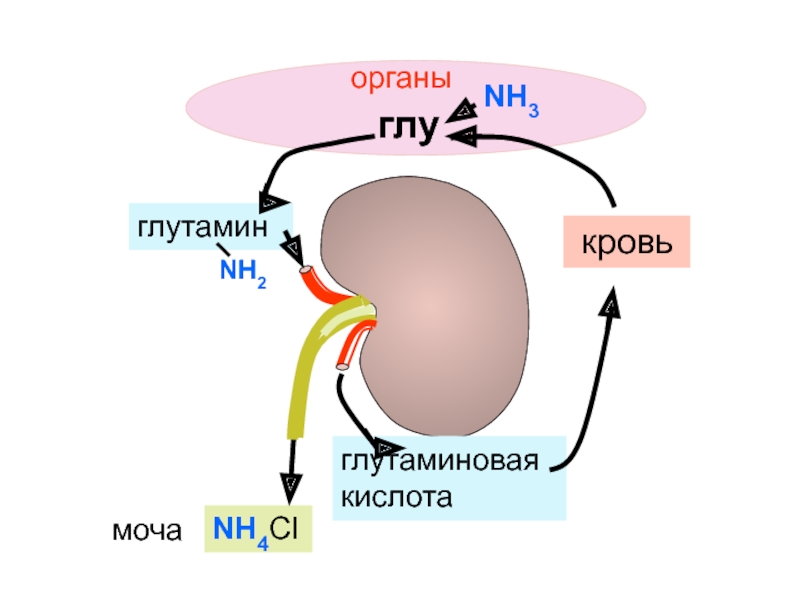
Ресинтез глутаминовой кислоты в почках
Слайд 64
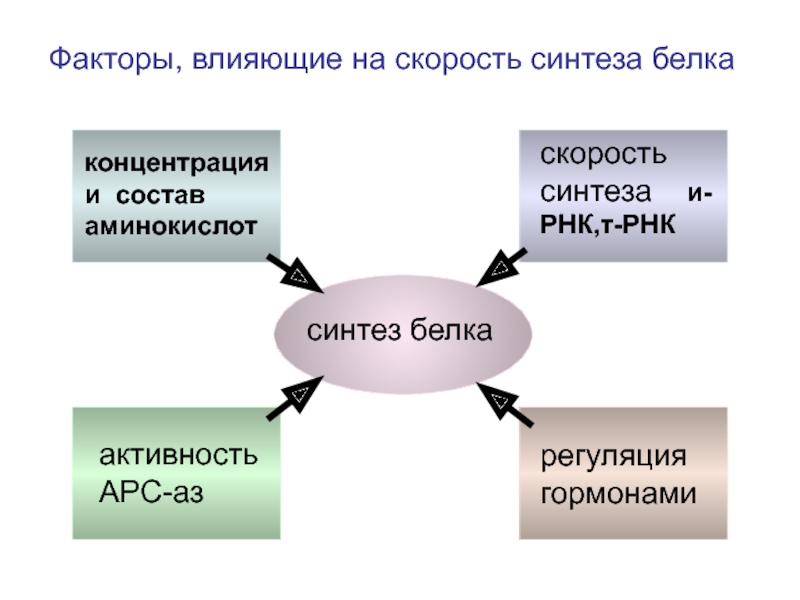
синтез белка
концентрация и состав аминокислот
скорость синтеза и-РНК,т-РНК
активность АРС-аз
регуляция гормонами
Факторы, влияющие
Слайд 65Влияние некоторых факторов на концентрацию и состав аминокислот
Доступность в белковой диете;
2. Наличие полноценных белков в продуктах;
2. Содержание альбумина в крови;
3. Заболевания органов пищеварения;
4. Нарушения всасывания аминокислот;
5. Заболевания почек, печени, поджелудочной железы;
6. Гиповитаминоз (В6; фолиевой кислоты, В12)
Слайд 66
Влияние некоторых факторов на активность АРС-аз
Активность белково-синтезирующей системы;
2. Кислотно-основное состояние в
3. Состояние биоэнергетических процессов.
Слайд 67Факторы, влияющие на скорость синтеза и-РНК и т-РНК
Наличие нуклеотидного фонда;
3. Влияние факторов роста на процесс транскрипции (индукция и репрессия генов).
Слайд 68Гормональная регуляция скорости синтеза белка
Соматотропин, половые гормоны (индукторы транскрипции и биосинтеза
2. Тироксин (активатор транскрипции ферментов, осуществляющих липолиз и протеолиз);
3. Инсулин (активатор транскрипции ферментов, участвующих в углеводном обмене);
4. Глюкокортикоиды (репрессоры транскрипции генов, контролирующие синтез белков и липидов. Индукторы транскрипции и биосинтеза ферментов глюконеогенеза).
Слайд 69На скорость дезаминирования аминокислот влияют:
Соотношение НАДН2 /НАД. При гипоксии увеличивается концентрация
2. Концентрация NH3. Увеличение концентрации аммиака замедляет процесс дезаминирования.
3. Снижение концентрации глутаминовой кислоты или аспарагиновой кислоты понижает скорость окислительного дезаминирования.
Слайд 71
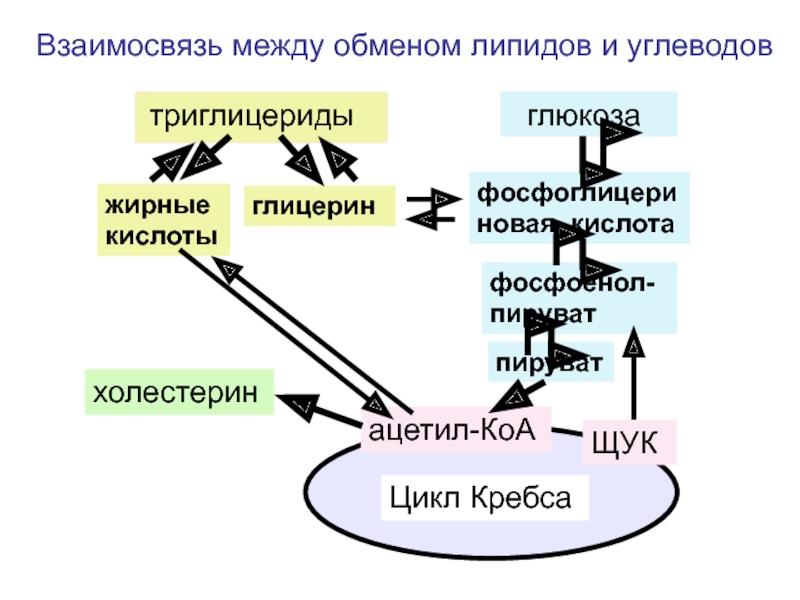
триглицериды глюкоза
жирные
глицерин
фосфоглицериновая кислота
фосфоенол-пируват
пируват
ацетил-КоА
холестерин
Цикл Кребса
ЩУК
Взаимосвязь между обменом липидов и углеводов
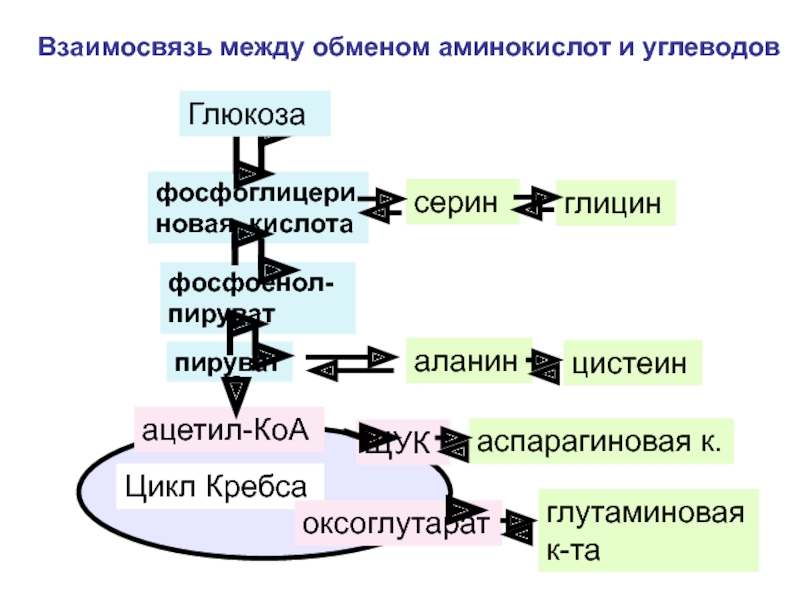
Слайд 72фосфоглицериновая кислота
фосфоенол-пируват
пируват
ацетил-КоА
Цикл Кребса
ЩУК
Взаимосвязь между обменом аминокислот и углеводов
Глюкоза
оксоглутарат
серин
глицин
аланин
цистеин
аспарагиновая к.
глутаминовая
Слайд 73
СН2-ОН
СН -ОН
СН2-ОН
СН2-ОН
СН -ОН
СН2-ОРО3Н2
СН2-ОН
С = О
СН2-ОРО3Н2
АТФ
НАД
НАДН2
С = О
СН -ОН
СН2-ОРО3Н2
Н
СООН
С = О
СН2-ОРО3Н2
СООН
С =
СН2-ОН
НАД
НАДН2
Н3РО4
Превращение глицерина в фосфоглицериновый альдегид
глицерин фосфоглицерин фосфодиоксиацетон
фосфоглицериновый гидроксипируват альдегид
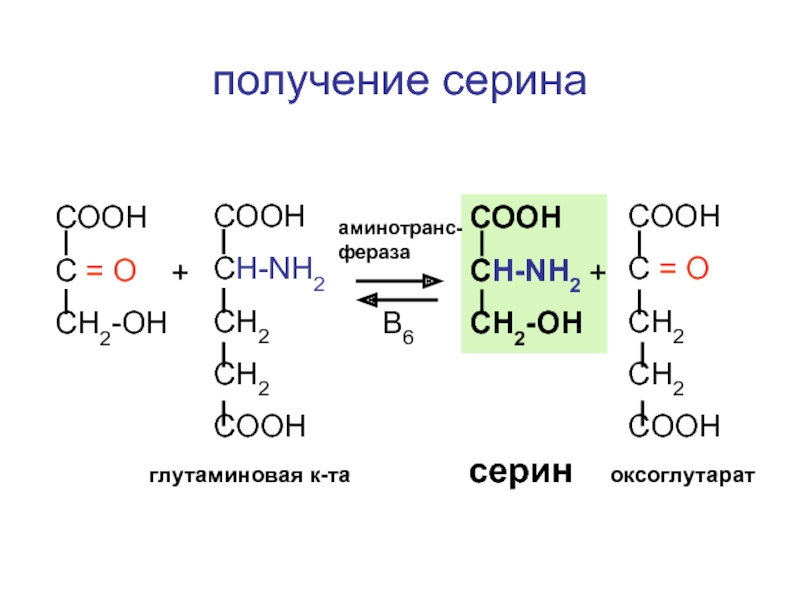
Слайд 74СООН
С = О
СН2-ОН
СООН
СH-NH2
CH2
CH2
COOH
СООН
СH-NH2
СН2-ОН
СООН
С = O
CH2
CH2
COOH
+
+
аминотранс-фераза
В6
глутаминовая к-та
получение серина
Слайд 76
регенерация
апоптоз
Динамические равновесие между процессом запрограммированной смерти клетки и ее клонированием
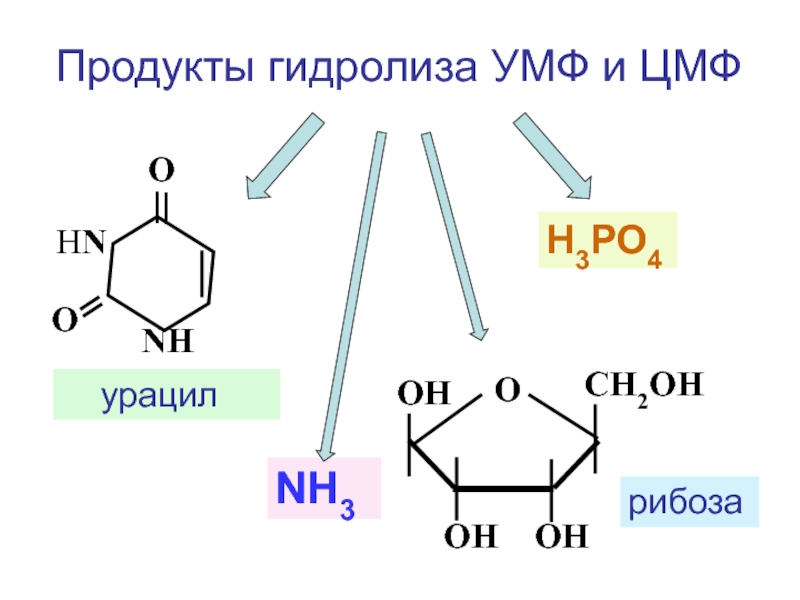
Слайд 77Продукты, наиболее богатые нуклеиновыми кислотами
икра
дрожжи
лекарственные препараты (нуклеинат натрия)
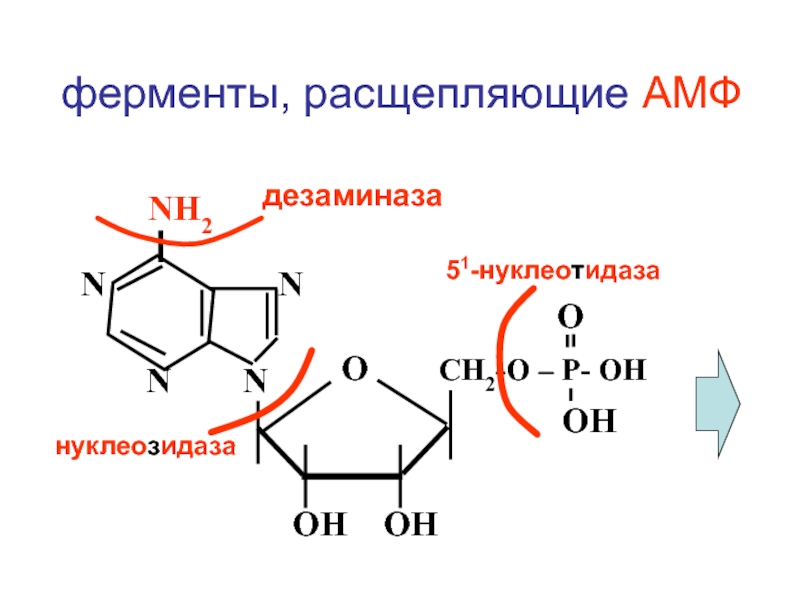
Слайд 82 N
N N
NH2
N
ОH ОН
О
ОН
дезаминаза
51-нуклеотидаза
нуклеозидаза
ферменты, расщепляющие АМФ
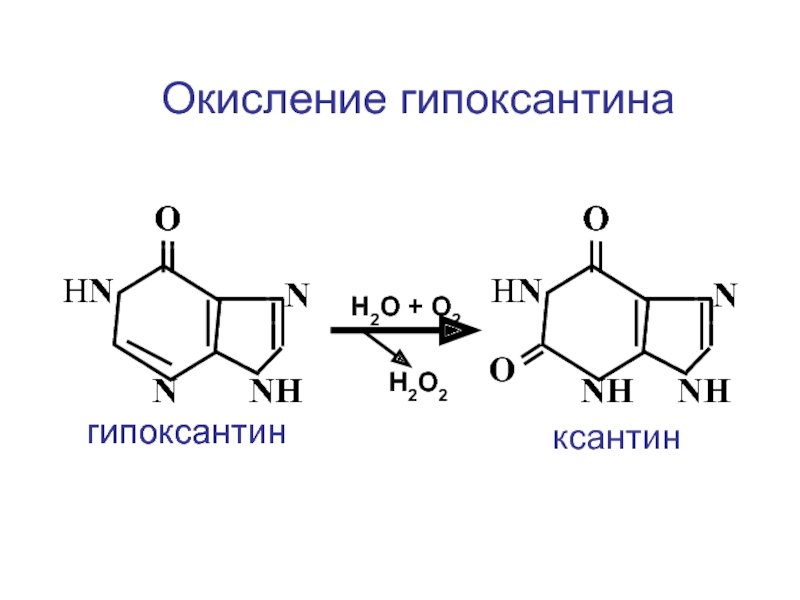
Слайд 84 N
N NН
О
НN
гипоксантин
N
О
НN
гипоксантин
N
N NН
О
НN
N
NH
О
НN
ксантин
О
Н2О + О2
Н2О2
Окисление гипоксантина
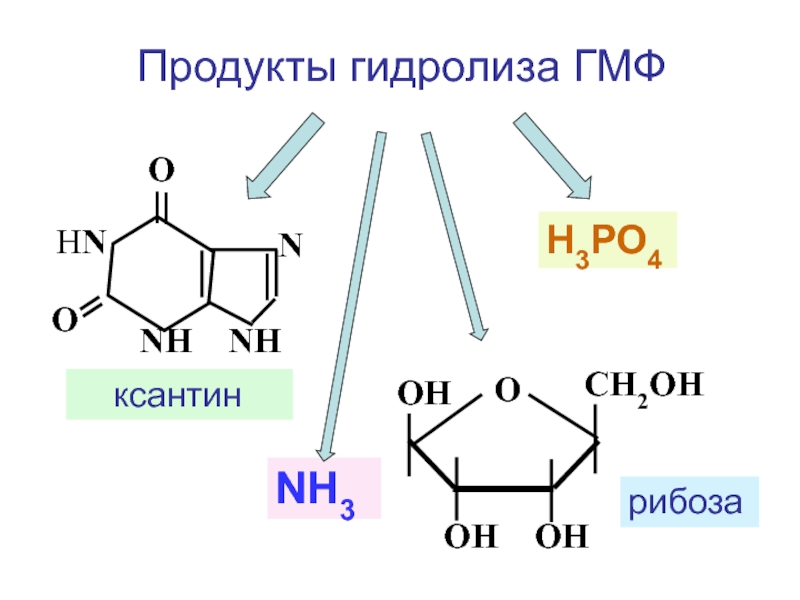
Слайд 85 N
N N
NH2
НN
ОH ОН
О
ОН
дезаминаза
51-нуклеотидаза
нуклеозидаза
ферменты, расщепляющие ГМФ
О
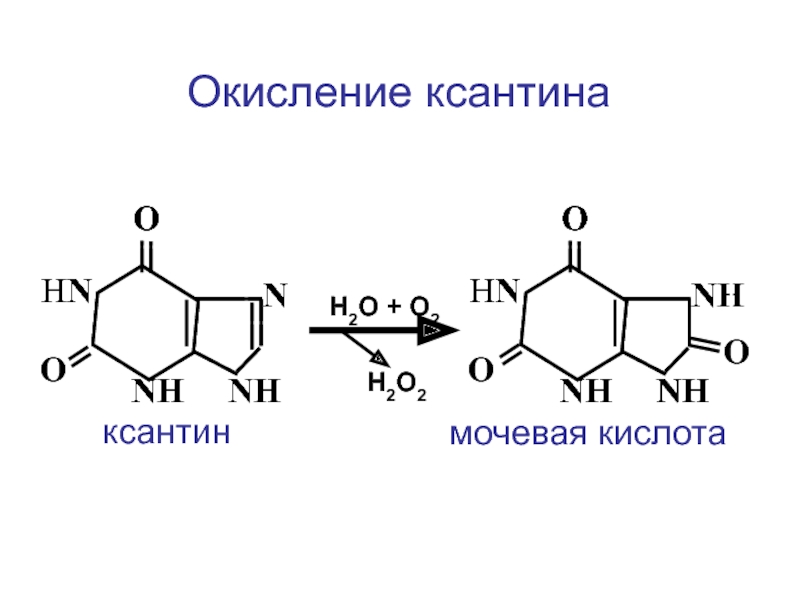
Слайд 87 NH
N
N NН
О
НN
О
НN
О
мочевая кислота
О
N
N NН
О
НN
ксантин
N
NН
О
НN
Н2О + О2
Н2О2
Окисление ксантина
О
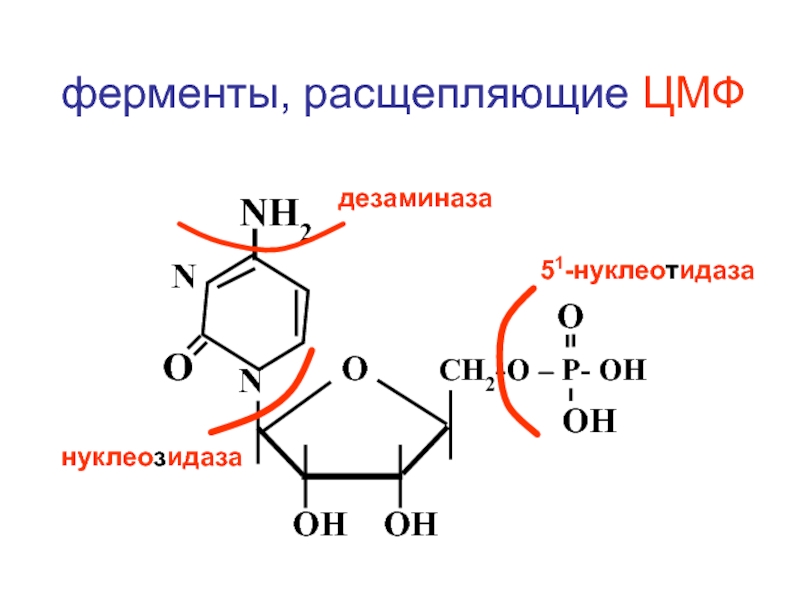
Слайд 90 N
N
О
ОH ОН
О
ОН
51-нуклеотидаза
нуклеозидаза
ферменты, расщепляющие ЦМФ
NH2
О
дезаминаза
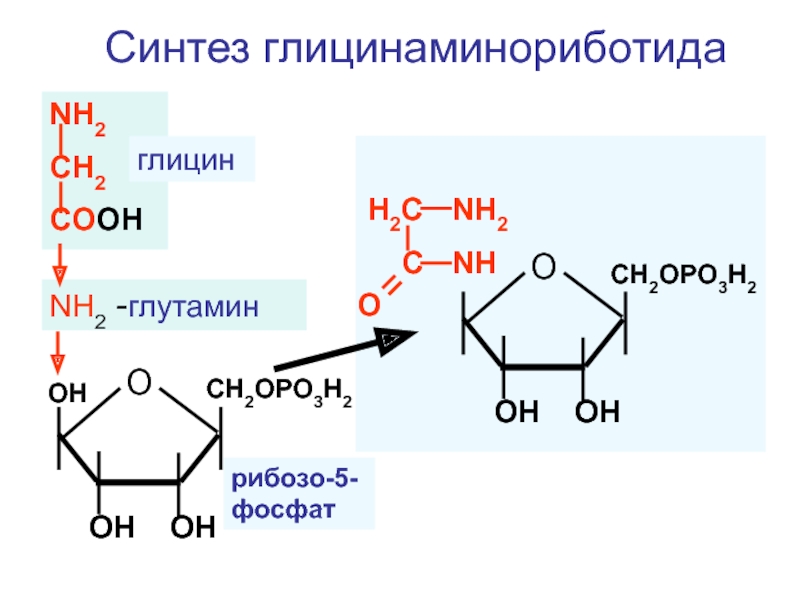
Слайд 95
СН2ОРО3H2
NH2
CH2
COOH
NH2 -глутамин
ОH ОН
О
ОН
СН2ОPO3H2
H2C
C
ОH ОН
О
NH2
NH
O
Синтез глицинаминориботида
глицин
рибозо-5-фосфат
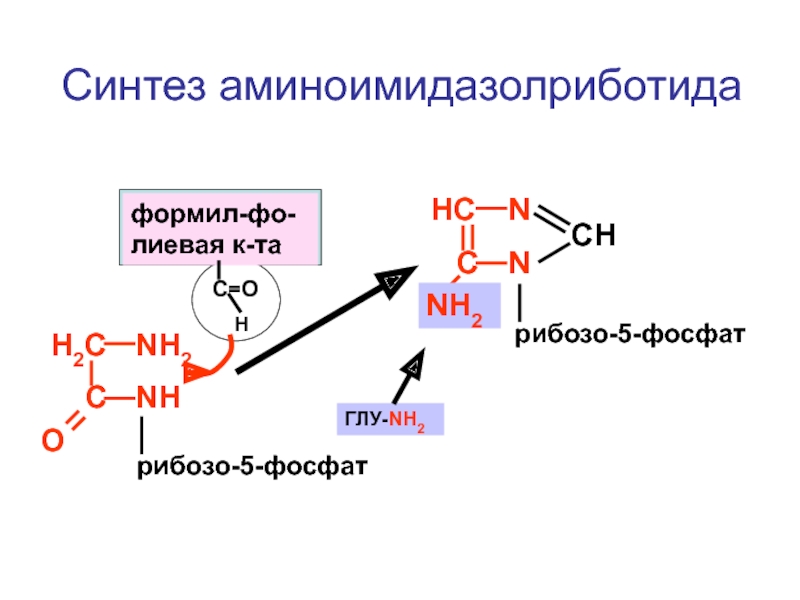
Слайд 96
H2C
C
NH2
NH
O
HC
C
N
N
NH2
СН
формил-фо-лиевая к-та
С=О
ГЛУ-NH2
рибозо-5-фосфат
рибозо-5-фосфат
Синтез аминоимидазолриботида
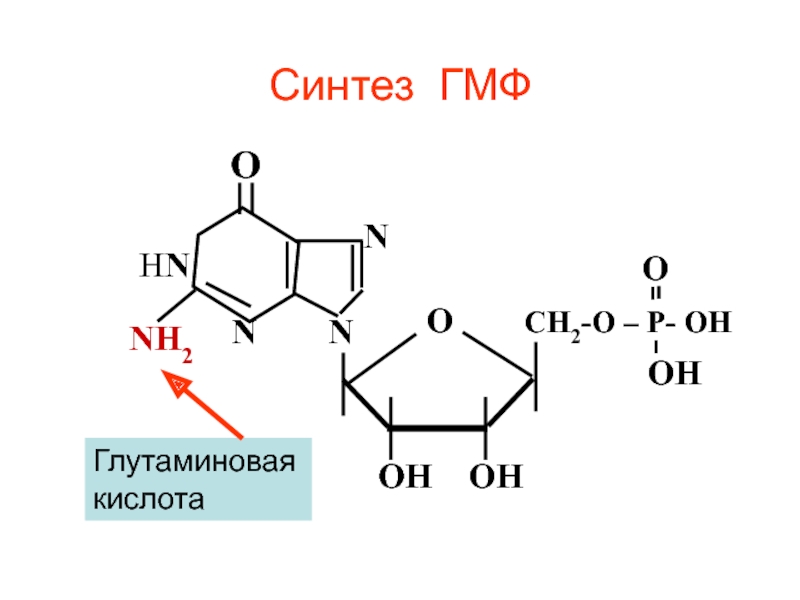
Слайд 97 NН2
N
НN
N
С=О
О=С
рибозо-5-фосфат
биотин-СО2
аспарагиновая к-та
формил-фолиевая к-та
Построение пиримидинового кольца в пуриновом
Слайд 102
NH2
O=C
O-PO3H2
СООН
СН2
СН
NH2
HN
O=C
С=O
СН
С
NH COOH
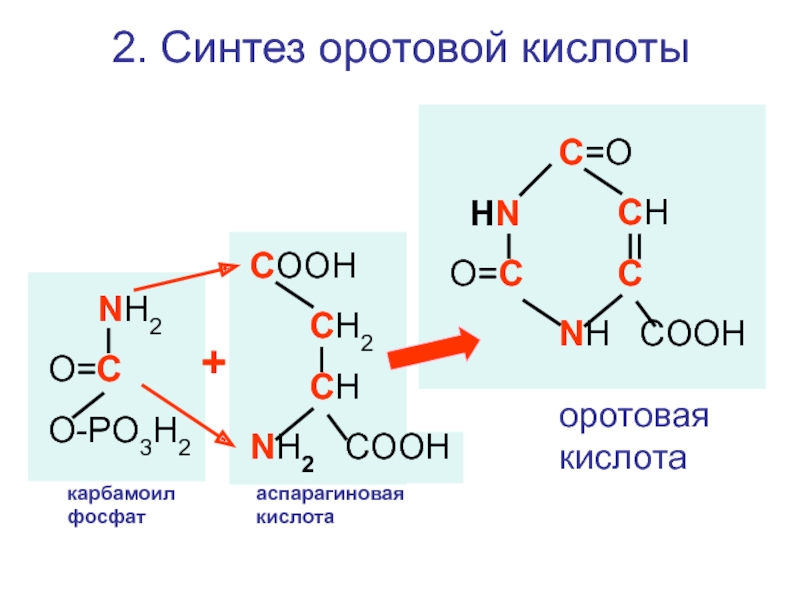
оротовая кислота
карбамоил фосфат
аспарагиновая кислота
2. Синтез оротовой кислоты
+
Слайд 103
СН2ОРО3H2
ОH ОН
О
ОН
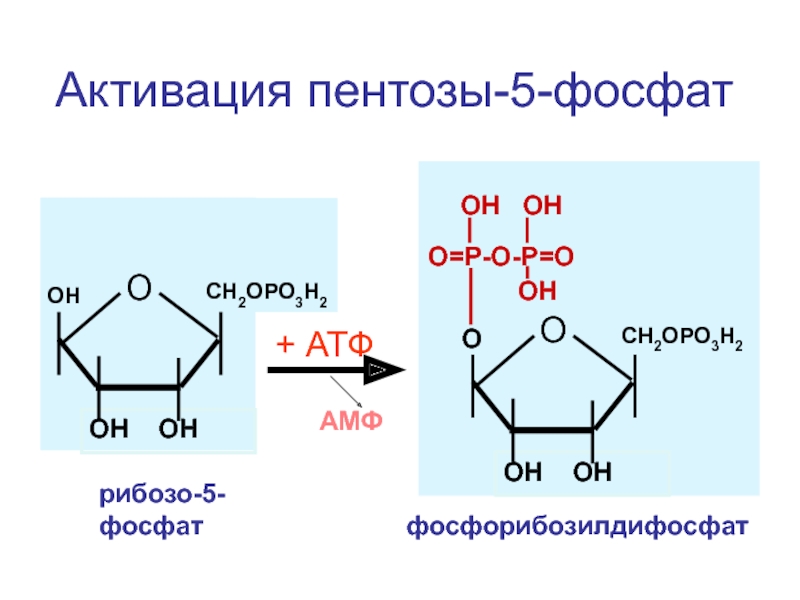
рибозо-5-фосфат
СН2ОРО3Н2
ОH ОН
О
О
+ АТФ
АМФ
фосфорибозилдифосфат
Активация пентозы-5-фосфат
О=Р-О-Р=О
ОН ОН
ОН
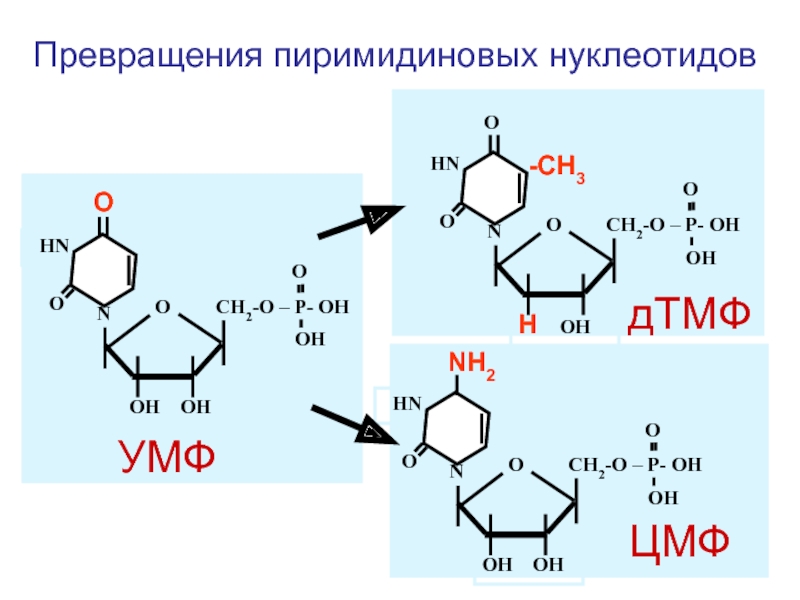
Слайд 106
О СН2-О – Р-
N
НN
ОH ОН
О
ОН
О
О
О СН2-О – Р- ОН
N
НN
H ОН
О
ОН
О
О
О СН2-О – Р- ОН
N
НN
ОH ОН
О
ОН
NH2
О
-СН3
УМФ
дТМФ
ЦМФ
Превращения пиримидиновых нуклеотидов
Слайд 107Энергизация нуклеотидов
1) АМФ + АТФ = 2 АДФ
ГМФ + 2 АТФ = ГТФ + 2 АДФ
УМФ + 2 АТФ = УТФ + 2 АДФ
ТМФ + 2 АТФ = ТТФ + 2 АДФ
ЦМФ + 2 АТФ = ЦТФ + 2 АДФ