- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Молекулярная биология гена. (Лекция 1) презентация
Содержание
- 1. Молекулярная биология гена. (Лекция 1)
- 2. Лекция 1. Введение.
- 3. Что мы знали вчера о своем геноме?
- 4. Геном человека У взрослого человека примерно 1014
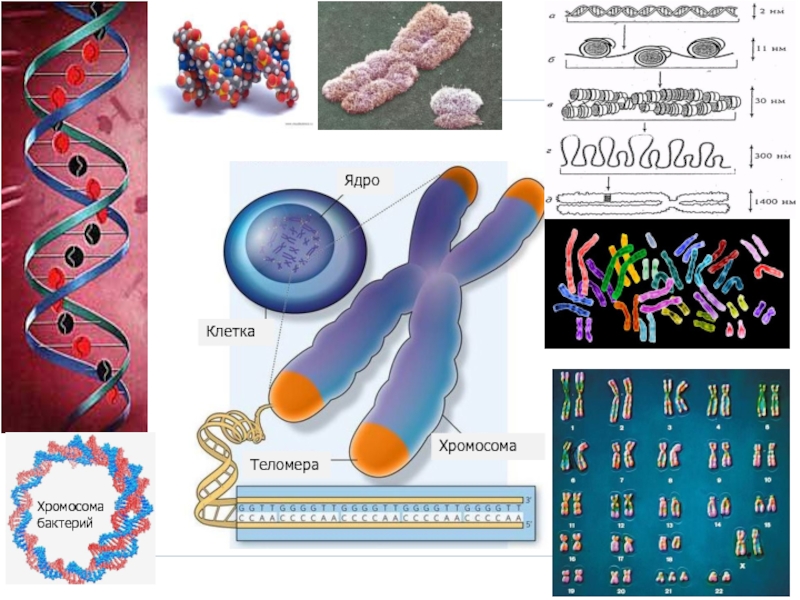
- 5. Ядро Клетка Теломера Хромосома Хромосома бактерий
- 6. Что знаем сегодня:
- 7. Исследователи надеются, что дальнейшее изучение этой структуры
- 8. Ученые выявили новый тип клеточной ДНК
- 9. Началось детальное исследование "мусорной ДНК" Большая
- 10. Ученые обнаружили смысл в "мусорной" ДНК человека
- 11. Хотя функции микроРНК весьма разнообразны, основная их
- 12. Роль микроРНК в ходе онтогенеза Например,
- 13. Ученые из Йельского университета смогли остановить рост
- 14. Специфические микроРНК (например, микроРНК-122) контролируют размножение вируса
- 15. МикроR214 отвечает за выработку инсулина поджелудочной железой.
- 16. В декабре 2008 г. фармацевтическая компания Regulus
- 17. Ироничный афоризм "Ты – есть то, что
- 18. Еще одно открытие! Прорыв в науке
- 19. 1. Пересадка ядер, взятых
- 20. Перепрограммирование ядра клетки эпителия лягушки. Гердон использовал
- 21. 1958 First cloned animal Xenopus laevis Джон Гордон
- 22. Неоплодотворенная яйцеклетка Инактивация ядра ультрафиолетом Клетки кишечника головастика Пересадка ядра в яйцеклетку Микропипетка Клонирование лягушки
- 23. Ian Wilmut Долли …и ее потопство 1994, 1996
- 24. На седьмом году её жизни Долли пришлось
- 25. 3. Модификация соматической клетки, приводящая к её
- 26. Способ перепрограммирования специализированной клетки в стволовую
- 27. Команда ученых из Университета Киото добилась
- 28. С ооцитами сложнее – тут пришлось использовать
- 29. Данная технология позволит производить человеческие эмбрионы из
- 30. Ученые отмечают, что сам процесс превращения эпителиальных
- 31. Из стволовых клеток выращены клетки мозга
- 32. Японцы предложили выращивать человеческие органы в животных
- 33. Из тканей пациентов (1), страдающих различными заболеваниями,
- 34. ИПСК уже получены для таких заболеваний как:
- 35. В Японии созданы фрагменты почки человека из
- 36. ИПСК (индуцированные плюрипотентные стволовые клетки) прочно вошли
- 37. С помощью стволовых клеток отечественные специалисты
- 38. В 2013 г. в Минске откроется клиника
- 39. У нас мало генов, но это не мешает быть нам самыми умными! Почему?
- 40. Анализ 400 млн фрагментов РНК из разных
- 41. Сплайсинг это довольно простое и важное биологическое
- 42. Пре-мРНК Зрелая мРНК Экзоны (последовательности, которые кодируют
- 43. Альтернативный сплайсинг В ходе созревания пре-мРНК
- 44. Альтернативный сплайсинг мРНК м м
- 45. Альтернативный сплайсинг — процесс, в ходе которого
- 46. После трансляции дает белок – гормон щитовидной
- 47. Какова роль альтернативного сплайсинга в эволюции
- 48. 20 мая 2010 года навсегда войдет в
- 49. Альтернативная энергетика. В 2009 г. принадлежащая
- 50. Успехи в клонировании животных
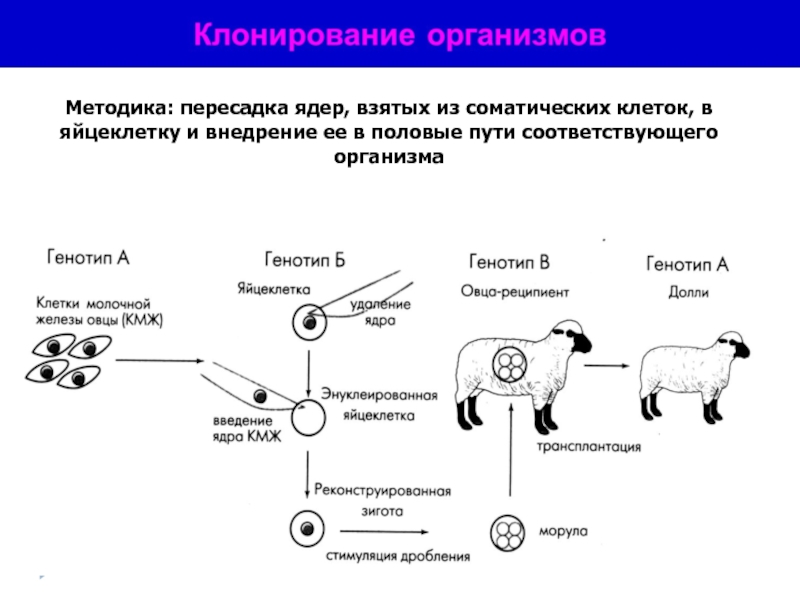
- 51. Методика: пересадка ядер, взятых из соматических клеток,
- 53. Затем появилась трансгенная Полли и ее сестры
- 54. 2002 – кролик 2003 – мул по
- 55. 2003 – бентанг
- 56. 2005 – собака - африканская борзая Снаппи
- 57. 2006 – индийский буйвол
- 58. К настоящему времени клонированы и другие млекопитающие
- 59. Аргентинские генетики вывели трансгенную корову, которая имеет
- 60. Корову, которая дает молоко, не вызывающее аллергию,
- 61. Трансгенные козы, живут в Жодино. Они стали настоящей сенсацией в мировой науке.
- 62. Лактоферрин является уникальным и многофункциональным белком,
- 63. Первые в мире фантастические обезьяны словно сошли
- 64. Клонированы светящиеся собаки Ученые из Южной Кореи
- 65. У трансгенной лягушки Xenopus laevis зеленым светятся
- 67. В Израиле изобрели курицу без перьев
- 68. Ноги вместо плавников – новый эксперимент генетиков
- 69. В 2013 году может родиться первый "гибридный"
- 70. Расшифровка генома человека Основной метод расшифровки геномов
- 71. В 1998 г. аналогичный проект был запущен
- 72. Секвенирование генома человека сегодня (а точнее на
- 73. Расшифрован геном сперматозоида Объектом исследования 91
- 74. Геном человека разнообразнее, чем считалось раньше
- 75. В данном случае секвенирование (определение нуклеотидной
- 76. Планируется, что проект по секвенированию генома
- 77. В Калифорнийском университете запущен масштабный проект для
- 78. 270 бактерий, 46 эукариот, из
- 79. Расшифровка генома мини-пигов (миниатюрных свиней Wuzhishan) предоставила
- 80. Расшифрован геном мыши: отличие от человека -
- 81. Прочитан геном шимпанзе Люди отличаются от
- 82. Ученые: человека от зверя отделяет только один
- 83. Использование ДНК-технологий в: ДНК-генеалогии человека Палеонтологии Криминалистике
- 84. ДНК-технологии
- 85. Развитие нового направления – ДНК-генеалогии человека ДНК-генеалогия
- 86. Наиболее распространенные генетические различия между людьми составляют
- 87. Коричневым цветом показана первая волна (75–62 тыс. лет
- 88. ГаплогруппаR1а Происходит от мутации гаплогруппы R1,
- 89. Гаплогруппа N1 Y-ДНК гаплогруппа N1 найдена повсюду
- 90. Гаплогруппа I2 Гаплогруппа I2 зародилась в Юго-Восточной
- 91. Гаплогруппа I1 Гаплогруппа I1 зародилась не более
- 92. Гаплогруппа E1b1b1 зародилась в верхнем палеолите примерно
- 93. Гаплогруппа J2 Гаплогруппа J2-M172 зародилась на Ближнем
- 94. Гаплогруппа R1b Гаплогруппа R1b возникла предположительно в
- 95. Гаплогруппа С3 Гаплогруппа, возникшая после того, как
- 96. Гаплогруппа Q Y-хромосомная гаплогруппа Q распространена у
- 97. Гаплогруппа G2a Гаплогруппа G2 предположительно возникла около
- 98. Галогруппа O3 Корейская диаспора. Гаплогруппа J1 Гаплогруппа L Гаплогруппа T Гаплогруппа G2c
- 99. Генетики: европейские мужчины оказались дальними родственниками египтян
- 100. Китайские ученые провели исследование генома прямого потомка
- 101. Снежный человек произошел от встречи женщины
- 102. Палеонтология
- 103. Скоро генетики смогут выяснить, какими генами обусловлены
- 104. Геном неандертальца прочтен, осталось в нем разобраться
- 105. Американские генетики ищут суррогатную мать для неандертальца
- 106. Генетическая паспортизация населения
- 107. В несколько упрощенном варианте генетические паспорта (или
- 108. Это получение, хранение и использование биологического материала
- 109. Криминалистика
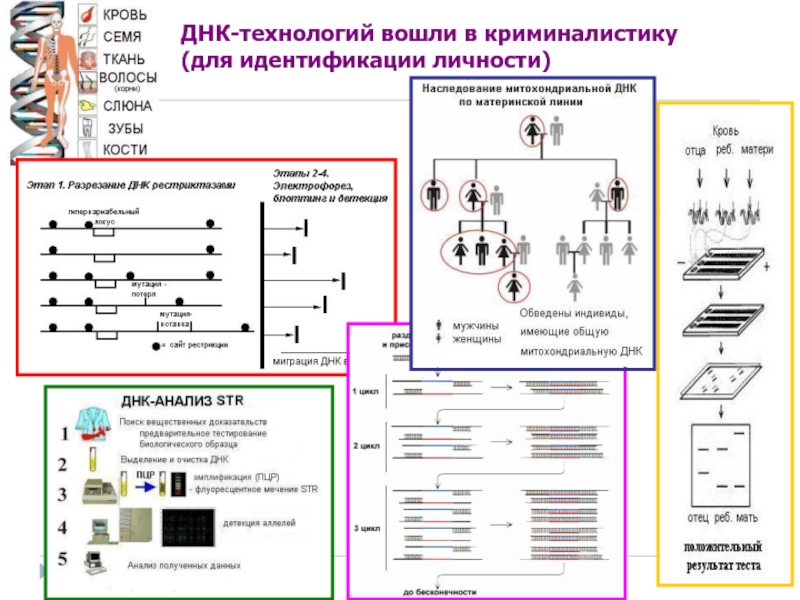
- 110. ДНК-технологий вошли в криминалистику (для идентификации личности)
- 112. Биочип для криминалистики Специалисты Института
- 113. В чем смысл генов?
- 114. Гены приносят счастье женщинам Ученые обнаружили ген,
- 115. Ученые: родители награждают ребенка 60 мутациями Впервые
- 116. Генетическая предрасположенность к курению Статьи, опубликованные
- 118. Медицина
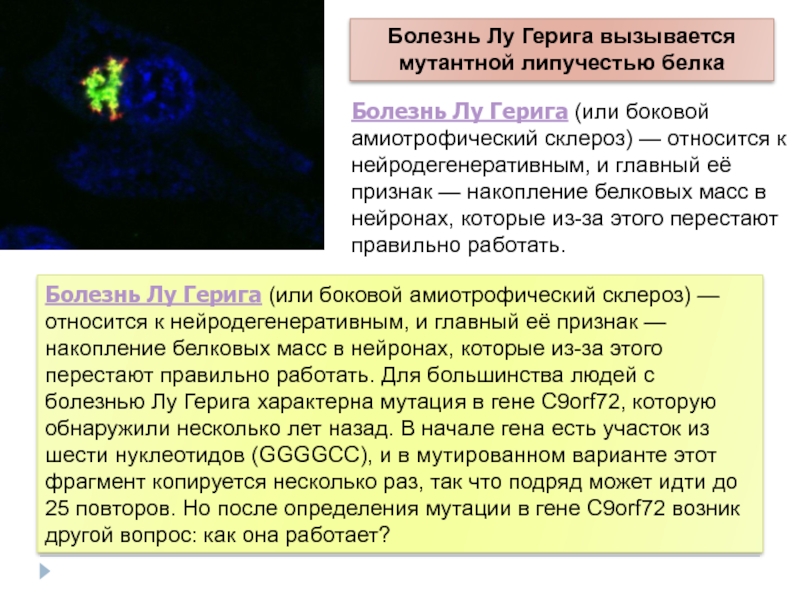
- 119. Болезнь Лу Герига (или боковой амиотрофический склероз)
- 120. В статье, опубликованной в Science показано, что,
- 122. Установлена молекулярная причина шизофрении В норме
- 123. У 30% малышей наблюдаются генетические нарушения
- 124. Трисомию можно лечить Вполне возможно, что, хотя
- 125. В нашем организме этанол превращается в ацетальдегид,
- 126. Американские ученые и предприниматели заявили о старте
- 127. Преимплантационная диагноститка Жительница Лондона родила первого в
- 128. Британцев будут проверять на генетические болезни перед
- 129. Обнаружен ген, отключение которого у мышей приводит к смерти,
- 130. Болезнь Паркинсона развивается при недостатке микроРНК
- 131. Алкоголь нарушает развитие мозга эмбриона, блокируя работу
- 132. Табакокурение снижает активность генома Обсуждение [0]
- 133. Управление синтезом тРНК может помочь в лечении раковых
- 134. Больных с нарушением свертываемости крови будут лечить
- 135. Трансгенные комары помогут в борьбе с малярией
- 136. Найден распространенный ген гипертензии Американские ученые
- 137. Сельское хозяйство
- 139. Генные инженеры открыли способ увеличения урожайности путем
- 140. Употребление нового сорта помидоров препятствует развитию рака
- 141. Выведена сверхполезная морковь Американские ученые вывели
- 142. ГМО: без вариантов? Витаминизированная кукуруза Трансгенная
- 143. Спорт и генетика
- 144. Феноменальные возможности элитных спортсменов зависят от уникальных
- 145. Британские ученые обнаружили зависимость успеха восхождения на
- 146. Определены генетические маркеры предрасположенности к занятиям футболом
- 147. В США вырастили супермышей Помещенный в
- 148. Опубликована новая версия карты генов человека, ассоциированных
- 149. 1. Фосфор - ключевой компонент ДНК, но
- 150. Завтра:
- 151. 2020 год На рынке появляются лекарства от диабета, гипертонии и других
- 152. 2040 год Все общепринятые меры здравоохранения основаны на геномике.
Слайд 1
Молекулярная биология гена
Наталья Павловна Максимова
зав. кафедрой генетики, д.б.н., профессор
Курс лекций 40
Слайд 4Геном человека
У взрослого человека примерно 1014 клеток, так что общая длина
ДНК в организме 1011 км (почти в тысячу раз больше расстояния от Земли
до Солнца).
В молекулах ДНК одной клетки человека 3 млрд пар нуклеотидов. Как представить себе 3 млрд оснований зримо? Чтобы воспроизвести информацию, содержащуюся в ДНК единственной клетки, даже самым
мелким шрифтом (как в телефонных справочниках), понадобится тысяча
1000-страничных книг!
Сколько же всего генов, то есть последовательностей нуклеотидов, кодирующих белки, в ДНК человека?
В 1990 г. полагали, что около 100 тыс., затем решили, что не более 80 тыс.
В конце 1998 г. пришли к выводу, что в геноме человека 50-60 тыс. генов.
По последним данным – генов у человека примерно 22-25 тыс.
На их долю приходится только 1,5-2% от общего количества ДНК.
Остальная ДНК – некодирующая – «мусорная».
В любой соматической клетке человека 23 пары хромосом.
В каждой из них по одной молекуле ДНК. Длина всех 46-и молекул почти 2 метра.
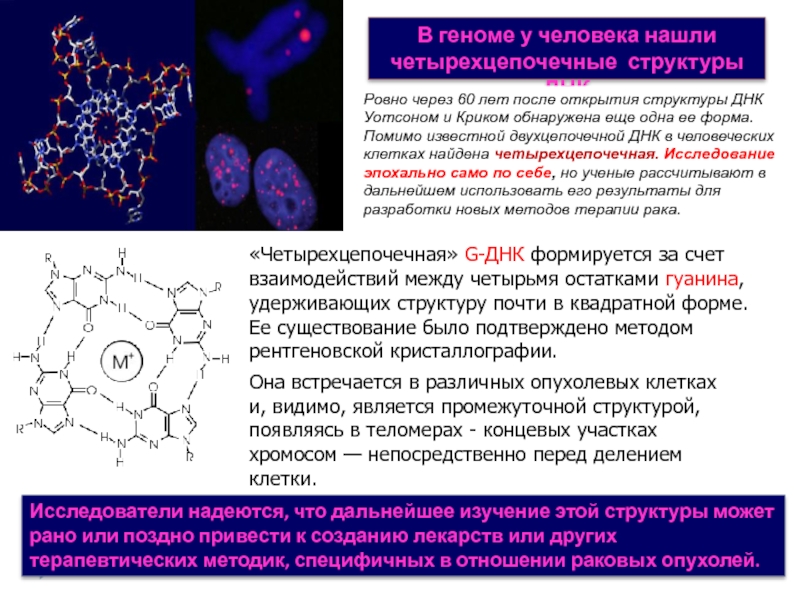
Слайд 7Исследователи надеются, что дальнейшее изучение этой структуры может рано или поздно
В геноме у человека нашли четырехцепочечные структуры ДНК
Она встречается в различных опухолевых клетках и, видимо, является промежуточной структурой, появляясь в теломерах - концевых участках хромосом — непосредственно перед делением клетки.
Ровно через 60 лет после открытия структуры ДНК Уотсоном и Криком обнаружена еще одна ее форма. Помимо известной двухцепочечной ДНК в человеческих клетках найдена четырехцепочечная. Исследование эпохально само по себе, но ученые рассчитывают в дальнейшем использовать его результаты для разработки новых методов терапии рака.
«Четырехцепочечная» G-ДНК формируется за счет взаимодействий между четырьмя остатками гуанина, удерживающих структуру почти в квадратной форме. Ее существование было подтверждено методом рентгеновской кристаллографии.
Слайд 8
Ученые выявили новый тип клеточной ДНК
Обычно ДНК в клетках организована в
После этого исследователи проводили определение состава и последовательности обнаруженных кольцевых молекул, которым они дали название микроДНК.
Оказалось, что выявленная микроДНК является результатом делеции (или иными словами вырезания) небольших участков генома, содержащих как гены, так и участки, которые влияют на работу генов.
МикроДНК - это не первый обнаруженный вид кольцевой ДНК, образующейся после делеции участков генома. Наследственная информация, которая кодируется в ДНК, хранится не только в хромосомах. Клетки человека так же, как и всех представителей животного и растительного мира, помимо основной, хромосомной ДНК, содержат еще кольцевую митохондриальную ДНК, несущую гены, важные для работы митохондрий. Данная ДНК наследуется исключительно по материнской линии и очень часто используется биологами для того, чтобы определить происхождение человека.
Ученые выявили в клетках мышей и человека новый тип кольцевой нехромосомной ДНК, имеющей в составе от 200 до 400 пар оснований. Результаты проведенной ими работы опубликованы в последнем номере журнала Science.
Слайд 9Началось детальное исследование "мусорной ДНК"
Большая часть человеческого генома представлена так
Установлено, что 8% генетического материала человека — от вирусов. Было известно, что из них - 1% человеческого генома представлен эндогенными
ретровирусами.
Недавно было показано, что в геноме людей и других млекопитающих содержится ДНК, появившееся в результате вставки борнавируса (это РНК соде6ржащий вирус, чья репликация и транскрипция происходит внутри ядра).
Ассимиляция вирусных последовательностей в геноме хозяина называется эндогенизацией. Это происходит когда вирусная ДНК встраивается в хромосомы репродуктивных клеток и последовательно передается от родителей детям. Ранее единственными вирусами, способными создавать эндогенные копии себя в позвоночных, считались ретровирусы. Но ученым удалось обнаружить множественную эндогенизацию борнавируса (не являющегося ретровирусом) в млекопитающих в процессе эволюции.
При попадании в организм человека он вызывает заболевание называемое болезнью Борна. Вирус поражает только нейроны головного мозга, создавая перманентный очаг инфекции в голове носителя. Тайваньские генетики показали, что в семьях людей, пораженных вирусом Борна, велик процент больных шизофренией и другими психическими расстройствами. Кроме того, генетики обнаружили механизм, позволяющий этим РНК-элементам вируса Борна внедряться в хромосомы человека, перенесшего это заболевание, что ведет к последующим мутациям нервной клетки и провоцирует появление психических отклонений в последующих поколениях.
Слайд 10Ученые обнаружили смысл в "мусорной" ДНК человека
Ученым удалось выяснить, что «некодирующая
Главную роль в регуляции этого типа играют малые РНК, считываемые с участков ДНК, находящихся в некодирующей части генома («мусорной ДНК»), которые считываются (транскрибируются) с образованием коротких молекул РНК (19-25 нуклеотидов). Эти РНК получили название микроРНК.
Важность открытия этого нового механизма регуляции активности генов так велика, что оно было названо «малой РНК - революцией» (small RNA revolution).
Слайд 11Хотя функции микроРНК весьма разнообразны, основная их роль состоит в участии
В настоящее время известно более 8 тыс. типов микроРНК. Главная трудность — установить точную функцию конкретной микроРНК.
Один тип микроРНК может регулировать трансляцию мРНК более 100 различных генов.
Экспрессия более 50% белок-кодирующих генов человека регулируется микроРНК.
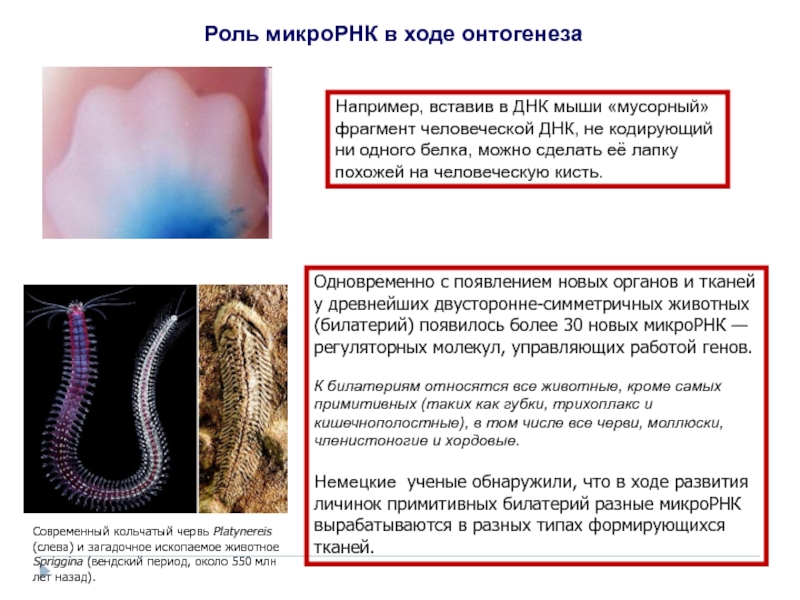
Слайд 12Роль микроРНК в ходе онтогенеза
Например, вставив в ДНК мыши «мусорный»
Современный кольчатый червь Platynereis (слева) и загадочное ископаемое животное Spriggina (вендский период, около 550 млн лет назад).
Одновременно с появлением новых органов и тканей у древнейших двусторонне-симметричных животных (билатерий) появилось более 30 новых микроРНК — регуляторных молекул, управляющих работой генов.
К билатериям относятся все животные, кроме самых примитивных (таких как губки, трихоплакс и кишечнополостные), в том числе все черви, моллюски, членистоногие и хордовые.
Немецкие ученые обнаружили, что в ходе развития личинок примитивных билатерий разные микроРНК вырабатываются в разных типах формирующихся тканей.
Слайд 13Ученые из Йельского университета смогли остановить рост опухоли в легких мышей
Эксперимент проводился на фоне контрольной группы мышей, которые не получали лекарства. У них опухоль продолжала развиваться, как и ранее. Введение в организм млекопитающего let-7 не привело к исчезновению опухоли, однако ее размер сократился на 66%.
Внедряется в практику терапевтическое применение микроРНК для целенаправленного подавления экспрессии генов при некоторых заболеваниях.
Слайд 14Специфические микроРНК (например, микроРНК-122) контролируют размножение вируса гепатита С в клетках
Датскими учеными создана субстанция, рабочее название которой SPC3649. Принцип действия у нее такой - это короткая искусственная ДНК, которая связывается с молекулой микроРНК-122 и не дает выполнять ей свою функцию. Новое лечение гепатита С начали испытывать на людях, но о результатах мы узнаем позже.
МикроРНК-122 отвечает также за обмен жиров в организме и поддержание уровня холестерина в крови. Заблокировав образование микроРНК-122 в клетках здоровой печени, можно снизить уровень холестерина в организме.
Слайд 15МикроR214 отвечает за выработку инсулина поджелудочной железой. Согласно работам профессора Гая
Сотрудники Института химической биологии и фундаментальной медицины (ИХБФМ) СО РАН под руководством академика В.Власова синтезировали 22-звенную двуцепочечную микроРНК, которая тормозит рост раковых клеток и стимулирует синтез интерферона.
Российские учёные синтезировали противоопухолевую микроРНК
Учёные также исследовали способность препарата вызывать синтез интерферона. Было показано, что в присутствии дцРНК клетки стали синтезировать интерферон-α в три раза активнее. При этом молекула, в отличие от других известных препаратов на основе РНК, почти не вызывает воспаления. Авторы исследования полагают, что полученный ими препарат окажется полезным в лечении опухолей.
Источник: strf.ru
Препараты на основе интерферона стимулируют работу иммунной системы и тем самым подавляют рост злокачественных опухолей. Однако применять их можно очень ограниченно, так как они вызывают у пациентов воспаление и аллергические реакции. Поэтому медики стараются использовать не сам интерферон, а препараты, стимулирующие его синтез в организме больного.
Показано, что использование этой дцРНК эффективно подавляет развитие эпидермоидной карциномы - скорость деления клеток падала в 3–3,5 раза.
Учёные предполагают, что «лечебная» дцРНК взаимодействует с клеточным ферментом дцРНК-зависимой протеинкиназой R. Этот фермент защищает организм млекопитающих от вирусов, геном которых представлен дцРНК, блокируя деление заражённых клеток. Когда в клетку попадает «лечебная» молекула, фермент реагирует на неё как на вирус и не позволяет этой клетке размножаться.
Слайд 16В декабре 2008 г. фармацевтическая компания Regulus Therapeutics объявила об успешных
С другой стороны, группа итальянских исследователей из Международного центра генной инженерии и биотехнологии в Триесте рассказала, как можно «подстегнуть» пролиферативную активность клеток сердца с помощью микроРНК. Особый тип микроРНК, которые способны индуцировать клетки сердечной мышцы к делению, вводили в сердце мышей после инфаркта, и спустя два месяца повреждённый участок выздоравливал наполовину, а функция сердца почти полностью восстанавливалась.
До сих пор никому не удавалось добиться такого результата на сердце млекопитающих. В ближайшем будущем исследователи хотят проверить свою методику на животных с более крупным сердцем, больше похожим на человеческое, передает Nature News.
Слайд 17Ироничный афоризм "Ты – есть то, что ты ешь" стал реальностью.
Последние исследования китайских ученых Чен Ю Янг и его коллеги из Нанкинского Университета, занимающиеся проблемами микроРНК животных и растений, обнаружили наличие микроРНК из сельскохозяйственных культур, таких как рис, пшеница, картофель и капуста в крови и клетках органов человека.
Результаты этой работы опубликованы в научно-исследовательском журнале «Cell Research». Поскольку эта информация вызывает новые опасения в отношении генетически модифицированных культур, так как прежде никто не изучал количественный и качественный состав их микроРНК, статью, содержащую во многом революционные результаты, не приняли для публикации такие солидные журналы как Science, Cell и Molecular Cell. Но теперь, когда «ящик Пандоры», наконец, открыт, можно ожидать роста интереса к микроРНК растений и вала публикаций в этой интригующей области.
Но можем лы мы верить этим результатам?
Слайд 18Еще одно открытие!
Прорыв в науке — перепрограммирование клеток
Лауреатами Нобелевской
Слайд 19
1. Пересадка ядер, взятых из соматических клеток, в оплодотворенную
2. слияние соматических клеток с плюрипотентными стволовыми клетками;
3. модификация соматической клетки, приводящая к её превращению в стволовую клетку, с помощью:
- генетического материала, кодирующего белковые репрограммирующие факторы;
- специальных рекомбинантных белков;
- микроРНК;
- низкомолекулярных биологически активных веществ.
В настоящее время существует три пути перепрограммирования соматических клеток в плюрипотентные стволовые клетки:
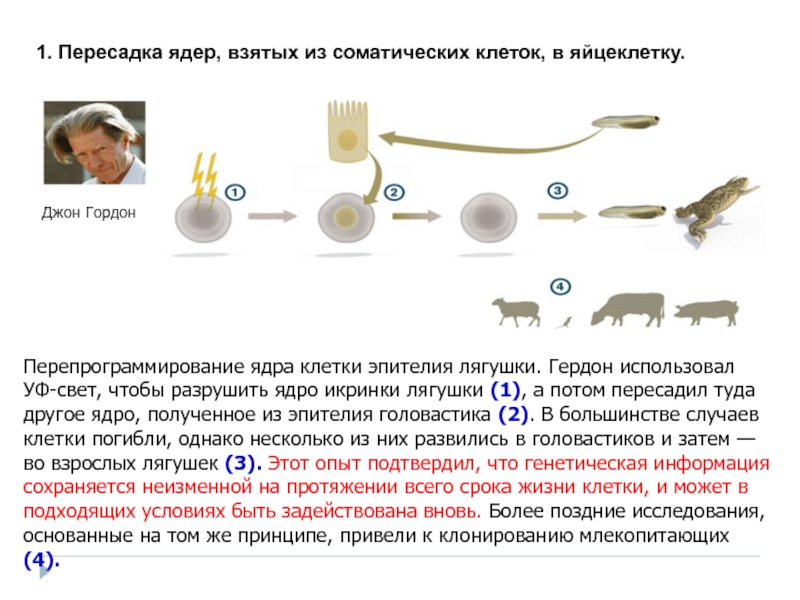
Слайд 20Перепрограммирование ядра клетки эпителия лягушки. Гердон использовал УФ-свет, чтобы разрушить ядро
1. Пересадка ядер, взятых из соматических клеток, в яйцеклетку.
Джон Гордон
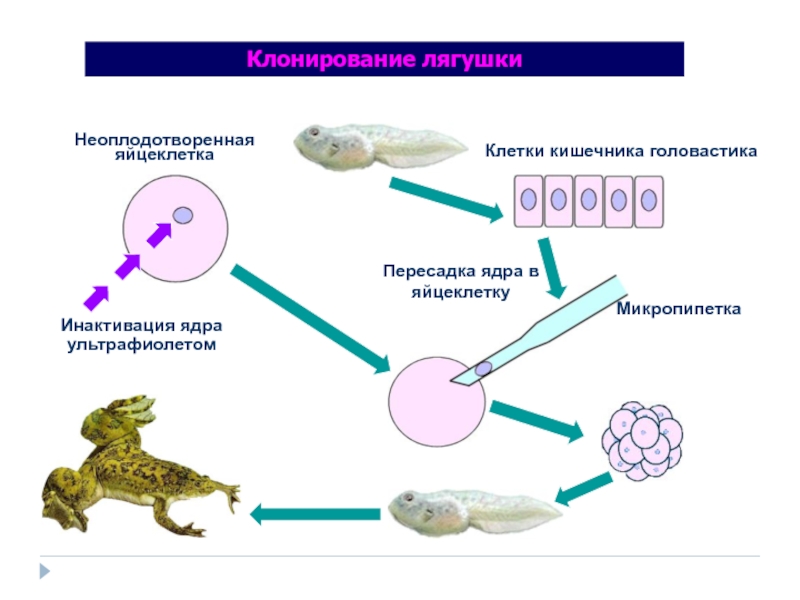
Слайд 22Неоплодотворенная
яйцеклетка
Инактивация ядра
ультрафиолетом
Клетки кишечника головастика
Пересадка ядра в
яйцеклетку
Микропипетка
Клонирование лягушки
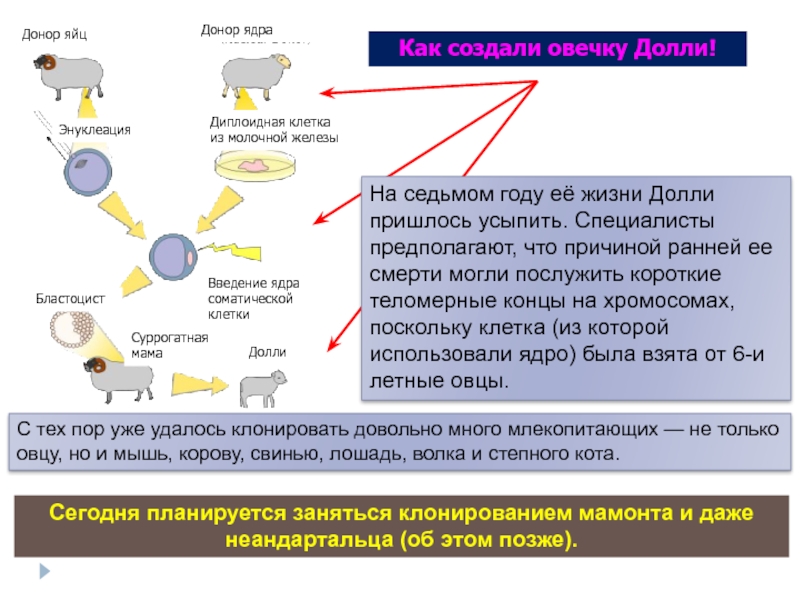
Слайд 24На седьмом году её жизни Долли пришлось усыпить. Специалисты предполагают, что
Донор яйц
Донор ядра
Энуклеация
Диплоидная клетка из молочной железы
Бластоцист
Введение ядра соматической клетки
Суррогатная мама
Долли
С тех пор уже удалось клонировать довольно много млекопитающих — не только овцу, но и мышь, корову, свинью, лошадь, волка и степного кота.
Как создали овечку Долли!
Сегодня планируется заняться клонированием мамонта и даже неандартальца (об этом позже).
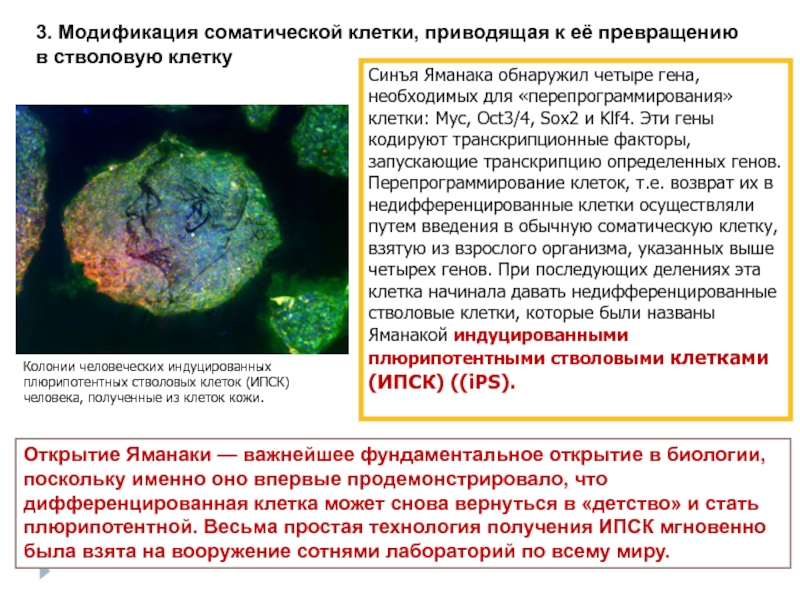
Слайд 253. Модификация соматической клетки, приводящая к её превращению в стволовую клетку
Колонии
Синъя Яманака обнаружил четыре гена, необходимых для «перепрограммирования» клетки: Myc, Oct3/4, Sox2 и Klf4. Эти гены кодируют транскрипционные факторы, запускающие транскрипцию определенных генов.
Перепрограммирование клеток, т.е. возврат их в недифференцированные клетки осуществляли путем введения в обычную соматическую клетку, взятую из взрослого организма, указанных выше четырех генов. При последующих делениях эта клетка начинала давать недифференцированные стволовые клетки, которые были названы Яманакой индуцированными плюрипотентными стволовыми клетками (ИПСК) ((iPS).
Открытие Яманаки — важнейшее фундаментальное открытие в биологии, поскольку именно оно впервые продемонстрировало, что дифференцированная клетка может снова вернуться в «детство» и стать плюрипотентной. Весьма простая технология получения ИПСК мгновенно была взята на вооружение сотнями лабораторий по всему миру.
Слайд 26Способ перепрограммирования специализированной клетки в стволовую
Яманака изъял фибробласт из тканей
Метод может быть использован для разработки новых способов лечения многих болезней. Например, основанных на внедрении в организм человека плюрипотентных стволовых клеток, генетически идентичных клеткам самого организма и способных заменять поврежденные болезнью клетки и ткани.
Слайд 27
Команда ученых из Университета Киото добилась сенсационного успеха: из стволовых клеток
Таким образом, впервые из индуцированных плюрипотентных стволовых клеток фактически вырастили взрослую особь. Мышь-донор стала одновременно отцом и матерью своих детей, что для здоровых двуполых млекопитающих в естественных условиях невозможно.
Метод Гордона и Яманаки в действии
Под впечатлением от работ Яманаки ученые быстро нашли способ превратить экзокринные клетки поджелудочной железы в эндокринные, а фибробласты — в кардиомиоциты. Есть даже пример превращения друг в друга клеток разных зародышевых листков — мезодермальных фибробластов в эктодермальные нейроны.
Слайд 28С ооцитами сложнее – тут пришлось использовать следующую процедуру: смесь эмбриональных
Для получения сперматозоидов ученые выращивали плюрипотентные стволовые клетки в коктейле из белков и получали клетки-зародыши (предшественники половых), которые превращались в сперматозоиды.
Слайд 29Данная технология позволит производить человеческие эмбрионы из клеточных линий и тканей
Ученые полагают, что смогут разобраться в молекулярных механизмах, участвующих в формировании половых клеток, и впоследствии обойтись без промежуточного этапа пересадки зародышевых клеток, то есть выращивать полноценные сперматозоиды и яйцеклетки непосредственно «в пробирке».
Слайд 30Ученые отмечают, что сам процесс превращения эпителиальных клеток в ИПСК занимал
Проведя серию экспериментов на крысах, авторы исследования показали, что инъецированные в мозг клетки становятся нормальными нейронами и не вызывают образования опухолей. Пока метод имеет прежде всего исследовательскую ценность, поскольку позволяет относительно просто получить большое количество индуцированных стволовых клеток мозга.
Ученые из Китая разработали метод, с помощью которого можно получить индуцированные стволовые клетки мозга из содержащихся в моче клеток почечного эпителия.
Слайд 31Из стволовых клеток выращены клетки мозга
Исследователи из Висконсинского университета вживили
Этот эксперимент показывает, что в дальнейшем поврежденный нейрон в мозге больных людей может быть заменен на новый.
Американские ученые изобрели эффективный метод борьбы с болезнями, которые связаны с нейрогенетивными нарушениями, например, болезнь Паркинсона.
Слайд 32Японцы предложили выращивать человеческие органы в животных
Для проведения эксперимента исследователи из
Когда мыши родились и выросли, у них не наблюдалось признаков диабета, который неминуемо возник бы в отсутствие поджелудочной железы, вырабатывающей инсулин. Оказалось, что все они обладают функционирующей железой, практически полностью состоящей из клеток крыс.
Причем, "крысиный" орган вырос именно в том месте, где должна была находиться отсутствующая у мышей поджелудочная железа.
В настоящее время исследователи ожидают разрешения на эксперимент со стволовыми клетками человека, чтобы с помощью разработанной методики вырастить человеческие органы в организме свиньи. Если этот эксперимент окажется успешным, методика в будущем сможет стать источником органов для трансплантации.
Новая методика получила название
Бластоцистная комплементация
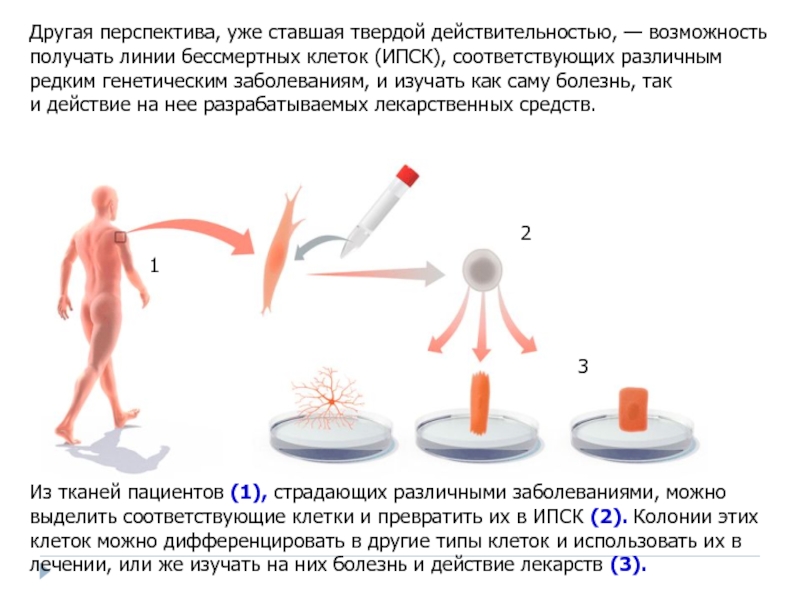
Слайд 33Из тканей пациентов (1), страдающих различными заболеваниями, можно выделить соответствующие клетки
1
2
3
Другая перспектива, уже ставшая твердой действительностью, — возможность получать линии бессмертных клеток (ИПСК), соответствующих различным редким генетическим заболеваниям, и изучать как саму болезнь, так и действие на нее разрабатываемых лекарственных средств.
Слайд 34ИПСК уже получены для таких заболеваний как:
амиотрофический латеральный склероз (болезнь
синдром Ретта - психоневрологическое заболевание. Дети с синдромом Ретта после 1-1,5 лет начинают терять все приобретенные навыки, включая речевой, двигательный и предметно-ролевой. Заболевание обусловлено мутацией гена MECP2 и практически не поддается лечению.
спинальная мышечная атрофия (СМА) - нарушение работы поперечнополосатой мускулатуры нижних конечностей, а также головы и шеи.
недостаточность антитрипсина α1,
семейная гиперхолестеринемия,
различные кардиологические заболевания,
имеется прогресс в изучении заболеваний со сложной генетикой, таких как шизофрения.
Слайд 35В Японии созданы фрагменты почки человека из ИПСК
Ученые вырастили из ИПСК
Успех японских ученых может стать первым шагом для выращивания органов.
Примечательно, что летом прошлого года ученые из другого японского университета - Университета Иокогама первыми в мире смогли вырастить ткани печени при использовании стволовых клеток неэмбрионального происхождения.
Ученые университета Киото Япония впервые в мире смогли создать фрагменты ткани почки человека из индуцированных плюрипотентных стволовых клеток (ИПСК).
Слайд 36ИПСК (индуцированные плюрипотентные стволовые клетки) прочно вошли в лабораторную практику и
В частности, на модели наследственной вегетативной дистонии проведен скрининг ряда химических веществ и найден прототип лекарства кинетин, который способен частично облегчить состояние больных с болезнью Альцгеймера.
Слайд 37
С помощью стволовых клеток отечественные специалисты планируют научиться лечить в первую
Стволовые клетки помогают специалистам реализовывать еще один уникальный проект – формировать банк пуповинной крови. Человек, кровь которого попадает в такую базу, на протяжении десятилетий может рассчитывать на то, что его собственный биоматериал при необходимости поможет ему устранить проблемы со здоровьем.
Некоторые заболевания в стране уже лечатся стволовыми клетками, пока эти работы проводятся на уровне клинической апробации. Однако ученые уверены, что в скором времени такие методы лечения станут доступнее для белорусов.
Белорусские ученые и медики планируют освоить технологию лечения заболеваний центральной и периферической нервной системы человека стволовыми клетками
Слайд 38В 2013 г. в Минске откроется клиника по лечению некоторых заболеваний
Помимо лечения планируется организовать совместное производство стволовых клеток. Для этого будет создано совместное предприятие "Международный научно-медицинский центр - клеточные технологии". Производство стволовых клеток будет сертифицировано по мировым стандартам.
На базе 9-й ГКБ Минска в ближайшее время будет создан первый в Беларуси банк стволовых клеток, полученных из пуповинной и плацентарной крови.
Находящиеся в нем образцы послужат для лечения онкологических и гематологических заболеваний.
Слайд 40
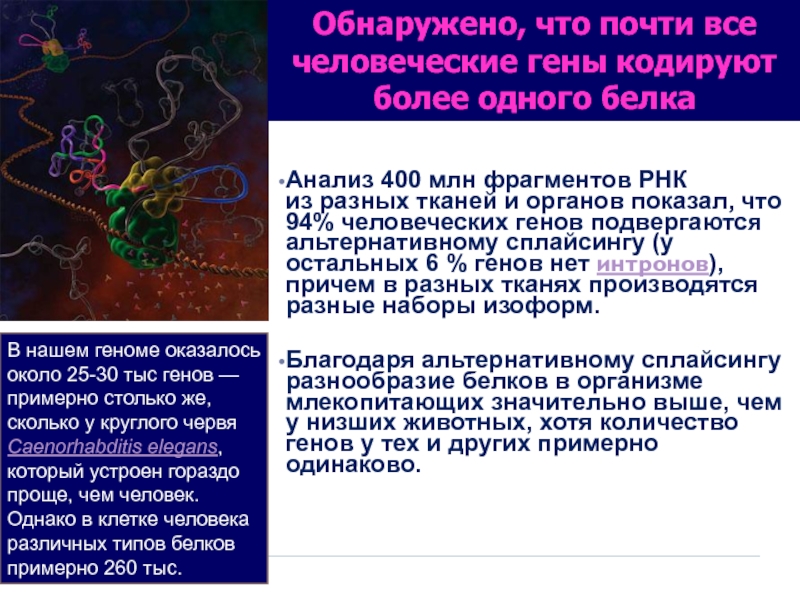
Анализ 400 млн фрагментов РНК из разных тканей и органов показал, что 94% человеческих
Благодаря альтернативному сплайсингу разнообразие белков в организме млекопитающих значительно выше, чем у низших животных, хотя количество генов у тех и других примерно одинаково.
Обнаружено, что почти все человеческие гены кодируют более одного белка
В нашем геноме оказалось около 25-30 тыс генов — примерно столько же, сколько у круглого червя Caenorhabditis elegans, который устроен гораздо проще, чем человек. Однако в клетке человека различных типов белков примерно 260 тыс.
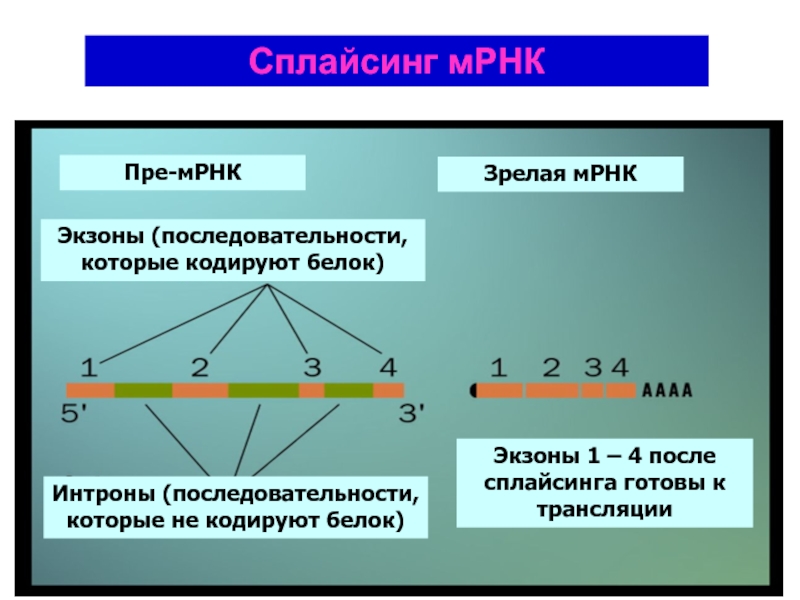
Слайд 41Сплайсинг это довольно простое и важное биологическое явление. Его суть состоит
Слайд 42Пре-мРНК
Зрелая мРНК
Экзоны (последовательности, которые кодируют белок)
Интроны (последовательности, которые не кодируют белок)
Экзоны
Сплайсинг мРНК
Слайд 43
Альтернативный сплайсинг
В ходе созревания пре-мРНК в ядре сшиваться могут не все
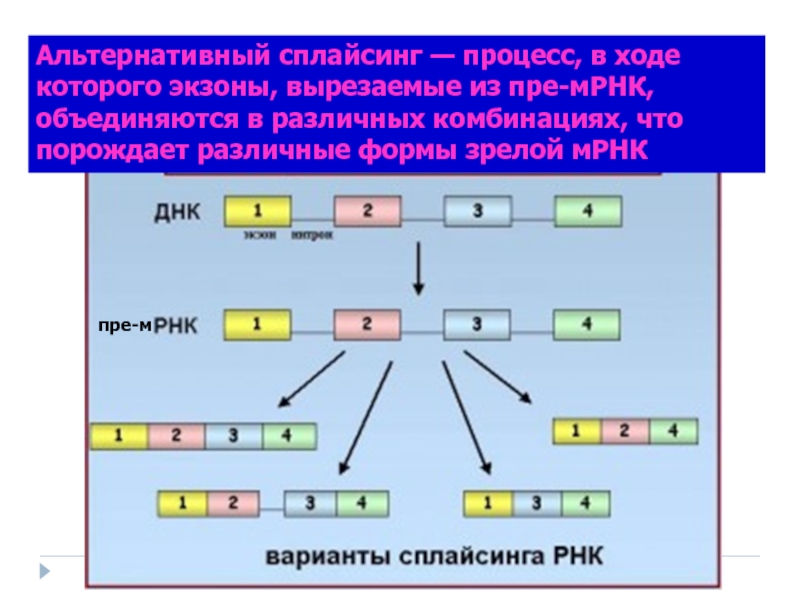
Слайд 45Альтернативный сплайсинг — процесс, в ходе которого экзоны, вырезаемые из пре-мРНК,
пре-м
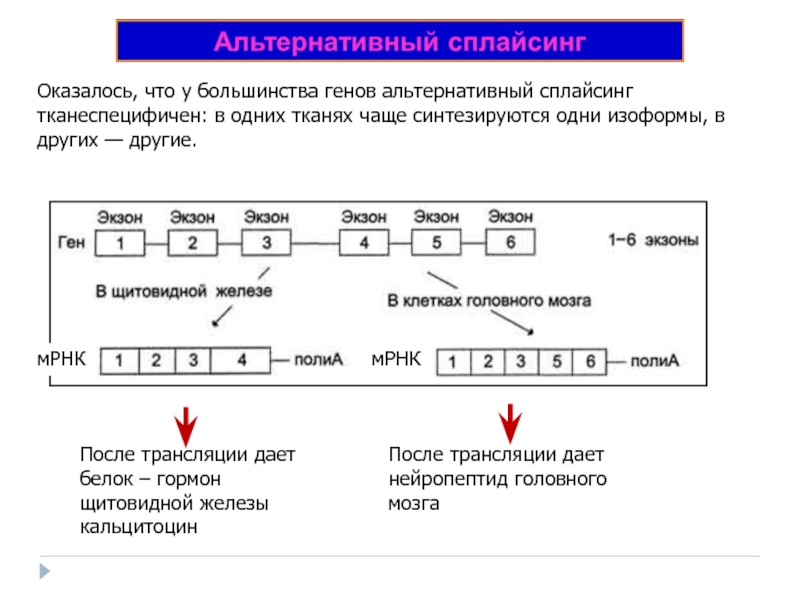
Слайд 46После трансляции дает белок – гормон щитовидной железы кальцитоцин
мРНК
После трансляции дает
мРНК
Оказалось, что у большинства генов альтернативный сплайсинг тканеспецифичен: в одних тканях чаще синтезируются одни изоформы, в других — другие.
Слайд 47
Какова роль альтернативного сплайсинга в эволюции живого?
К альтернативному сплайсингу начинают приглядываться
Большая группа ученых сравнила разнообразие и частоту сплайсинговых вариантов у представителей разных позвоночных. Они обнаружили, что у всех приматов, а не только у человека, частота сплайсинга примерно в полтора-два раза выше, чем у мыши и других четвероногих.
Какую бы ткань мы ни взяли, разнообразие альтернативных вариантов сплайсинга у приматов будет выше, чем у мыши, а у мыши будет выше, чем у лягушки. То есть особенности картины сплайсинга определяются не типом ткани, а биологическим видом.
Авторы исследования заключают, что разнообразие альтернативных вариантов накапливается по ходу эволюционного развития организмов.
Слайд 4820 мая 2010 года навсегда войдет в историю как день, в
Автор проекта - Крейг Вентер.
Создан первый организм с искусственным геномом
Схема создания организма с синтетическим геномом заключалась в следующем:
(1) ученые получили полную геномную последовательность ДНК Mycoplasma mycoides;
(2) затем на основании этих данных воссоздали геном этой бактерии химическим путем;
(3) полученную ДНК специалисты помещали в клетки бактерии Mycoplasma capricolum, из которой предварительно был удален собственный геном;
(4) Анализ свойств полученного организма показал, что он обладает свойством M. mycoides. Размер синтезированного генома генома - 1,08 млн. пар нуклеотидов.
Крейг Вентер потратил 15 лет на то, что бы оживить мертвую материю.
Еще одна сенсация -
синтетическая биология в действии !!!
Слайд 49 Альтернативная энергетика. В 2009 г. принадлежащая Крейгу Вентеру компания Synthetic
Будущее синтетической биологии
2. Живой компьютер. Создание из клеток аналогов электронных устройств. В декабре 2010 года ученые из Гетеборгского университета модифицировали клетки дрожжей таким образом, что их можно программировать на решение логических задач. Под влиянием разнообразных раздражителей они способны передавать свое состояние собратьям, выделяя в питательную среду молекулы различных типов, каждый из которых соответствует определенному раздражителю. Комбинируя реакцию на два разных раздражителя, клетки могут производить сигналы, «складывая» и «перемножая» посылки, как это делает процессор.
3. Органический синтез. Колонии искусственных микроорганизмов смогут синтезировать сложные органические молекулы тоннами, а их применение будет самым разнообразным - производство лекарств и пищевых продуктов, промышленная химия и т.д. Поскольку биомасса бактерий способна увеличиваться по экспоненте, производство может быть сколь угодно масштабным, а затратность - минимальной. В ближайших планах конструкторов - получение бактерий, способных обнаруживать ядовитые вещества и взрывчатку по «запаху» (крохотным частицам вещества, распространяющегося в воздухе), микробов, очищающих экосистему от пластикового мусора, и т.д., и т.п. и пр.
Слайд 51Методика: пересадка ядер, взятых из соматических клеток, в яйцеклетку и внедрение
Слайд 53Затем появилась трансгенная Полли и ее сестры
В геноме Полли содержится человеческий
Фото www.roslin.ac.uk/
Слайд 562005 – собака - африканская борзая Снаппи
2005 – африканская кошка
2006 –
Слайд 572006 – индийский буйвол
2007 - собака
2008 - коммерческое клонирование собаки -
Начато массовое коммерческое клонирование собак
2009 - верблюд – Инджас
2009 – пиринейский горный козел
2011 - восемь клонированных щенков койота
трансгенные козы
В геноме этих коз содержится человеческий ген антитромбина III, препятствующего свертыванию крови. Белок выделяется с молоком.
Фото http://news.bbc.co.uk/1/hi/sci/tech/329107.stm
Слайд 58К настоящему времени клонированы и другие млекопитающие – корова, свинья, мышь,
Слайд 59Аргентинские генетики вывели трансгенную корову, которая имеет ряд человеческих генов и
Зовут ее Розита.
Слайд 60Корову, которая дает молоко, не вызывающее аллергию, вырастили ученые в Новой
Для выведения генно-модифицированной коровы специалисты сначала внедрились в геном животного и «выключили» работу гена, ответственного за производство бета-лактоглобулина. Известно, что это вещество способно у многих людей вызывать аллергию, в частности, у маленьких детей от него может появиться высыпание на коже.
Новорожденную трансгенную корову назвали Дейзи. Она родилась на четыре недели раньше срока и... без хвоста.
Ученые пока не знают, способна ли Дейзи к размножению, к тому же оказалось, что вкус у гипоаллергенного молока немного отличается от обычного.
.
Слайд 62 Лактоферрин является уникальным и многофункциональным белком, который содержится в том числе
Для этого белка характерно большое количество биологических активностей, он обладает иммуномодулирующими свойствами, проявляет противовирусную, антибактериальную, антигрибковую активность. Кроме того, данный белок обладает противовоспалительным действием. Именно поэтому полученный в молоке трансгенных коз лактоферрин может быть применим и в фармацевтике, и в косметологии, а также в пищевой промышленности и даже в спорте. Но прежде всего лактоферрин может стать спасением для детей, лишенных материнского молока. Годовой объем мирового производства лактоферрина из коровьего молока оценивается в 60 т, а в стоимостном выражении - в $6 млрд.
Слайд 63Первые в мире фантастические обезьяны словно сошли со страниц научно-фантастического произведения.
Учёные брали по нескольку четырёхклеточных эмбрионов макаки, соединили их вместе и имплантировали «смешанные» эмбрионы суррогатной матери, которая родила здоровое потомство. Макак назвали Chimero, Roku и Hex.
Слайд 64Клонированы светящиеся собаки
Ученые из Южной Кореи клонировали четырех щенков породы Бигль,
Это первые трансгенные собаки с генами флуоресценции. Все «трансгенные» собаки являются клонами от одного донора.
Ученые под руководством Ли взяли клетки кожи, затем в них были добавлены гены флуоресценции, все это имплантировано в яйцеклетку и подсажено суррогатной матери, в роли которой выступила собака смешанной породы. Родилось шесть щенков, но лишь четверо из них выжили.
Эти светящиеся собаки доказывают возможность успешной имплантации генов, ответственных за определенное свойство, что дает надежду на имплантацию необходимых генов для лечения болезней. Кстати, по заявлениям профессора, его группа сейчас именно этим и занимается, пытаясь найти способы лечения генетических заболеваний. Ранее ученому удалось клонировать светящихся мышей и свиней, но с собаками это первый удачный опыт.
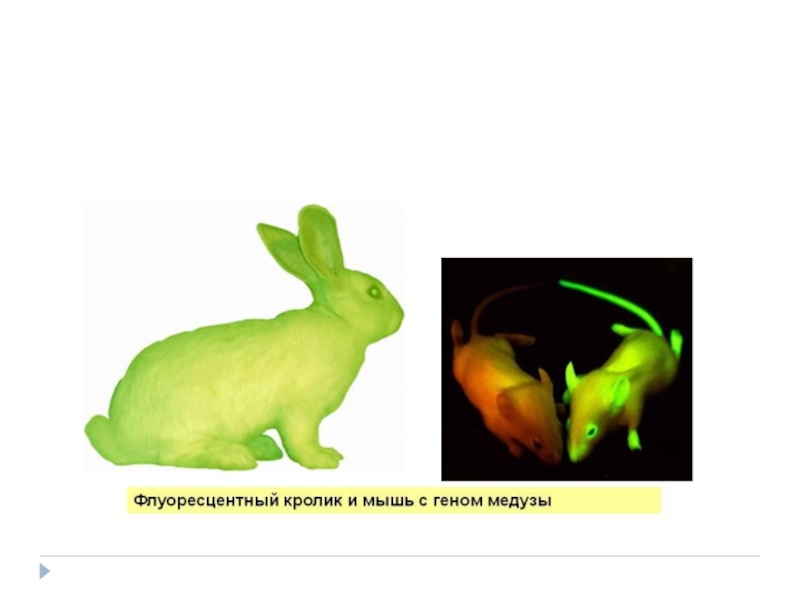
Слайд 65У трансгенной лягушки Xenopus laevis зеленым светятся только глаза
Трансгенные светящиеся рыбки предназначены для того, чтобы украшать аквариум.
www.glofish.com/ photos.asp
Слайд 67В Израиле изобрели курицу без перьев
В скором времени нужда в ощипывании
Это полностью естественная курица, которая никакими заболеваниями не страдает, – утверждает он. Первые курицы без перьев появились в Израиле еще в 2002 году, однако потребовалось почти 9 лет, чтобы закрепить новую породу. На длительность работы
также повлияло и отсутствие финансирования – ученые из Реховотского аграрного института делали все за свой счет.
Слайд 68Ноги вместо плавников – новый эксперимент генетиков
Ученые не перестают экспериментировать на
Для достижения желаемого эффекта группа исследователей в Севилье решили немного изменить поведение гена Hoxd13, активность которого, как известно, крайне низка у зародышей рыб и высока у четвероногих. В ходе эксперимента рыбам-зебрам (Danio rerio) была введена в геном вторая копия Hoxd13. В результате у зародышей с измененным геном вместо обычных плавников стали формироваться не плоские, а округлые конечности. Данная конструкция стала уже довольно сильно напоминать лапы животного.
По всей вероятности, примерно таким образом произошло сотни миллионов лет назад превращение рыб в амфибий.
Предположения подтвердились после введения в геном рыбы-зебры гена CsС, который управляет работой Hoxd13 в зародыше мыши, плавники стали превращаться уже в примитивный аналог лап.
Это указывает на присутствие клеточных механизмов, которые могут запускать программу преобразования в геноме общего предка рыб и наземных животных.
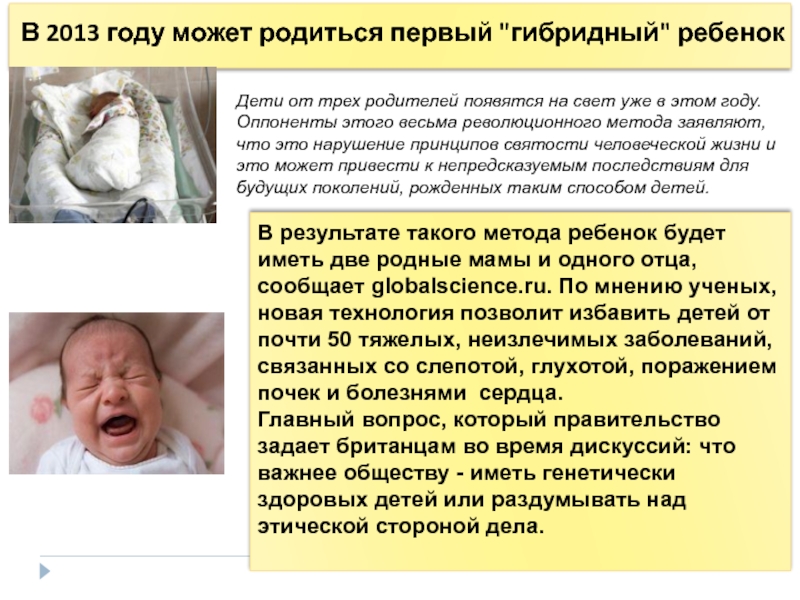
Слайд 69В 2013 году может родиться первый "гибридный" ребенок
В результате такого метода
Главный вопрос, который правительство задает британцам во время дискуссий: что важнее обществу - иметь генетически здоровых детей или раздумывать над этической стороной дела.
Дети от трех родителей появятся на свет уже в этом году. Оппоненты этого весьма революционного метода заявляют, что это нарушение принципов святости человеческой жизни и это может привести к непредсказуемым последствиям для будущих поколений, рожденных таким способом детей.
Слайд 70Расшифровка генома человека
Основной метод расшифровки геномов – секвенирование (определение нуклеотидных по
Метод был разработан в 1977 году, а сегодня - это уже технологичная рутина.
В 1990 г. при поддержке США, а также ряда других стран, был запущен 3 млрд. проект «Геном человека». Возглавил его Фрэнсис Коллинз, глава International Human Genome Sequencing Consortium. Целями проекта являлись:
- определение последовательности 3 млрд. пар оснований, составляющих ДНК человека, и сохранение этой информации в базе данных;
- идентификация генов человека;
- усовершенствование приборов для анализа данных;
- исследование этических, правовых и социальных вопросов, возникающих при расшифровке генома.
Слайд 71В 1998 г. аналогичный проект был запущен Крейгом Вентером (фирма «Celera
6 июня 2000 г. было объявлено о расшифровке человеческого генетического генома. На это ушло около 15 лет. На самом деле это был рабочий черновик человеческого генома, и лишь к 2003 г. он был расшифрован практически полностью, хотя и сегодня все еще проводят дополнительный анализ некоторых участков генома.
Сегодня скорость секвенирования стала стремительно расти, а само секвенирование — столь же стремительно дешеветь.
Например, в период 2007—2010 годов она упала в сто раз — с миллиона долларов до десяти тысяч.
В 2011 – 2012 гг. – секвенировать геном уже можно было за 5 тыс. долларов. В настоящее время технологии секвенирования позволяют секвенировать свой геном за 1 тыс. долларов.
В настоящее время около одного миллиона человек уже заказали полный анализ своего генома.
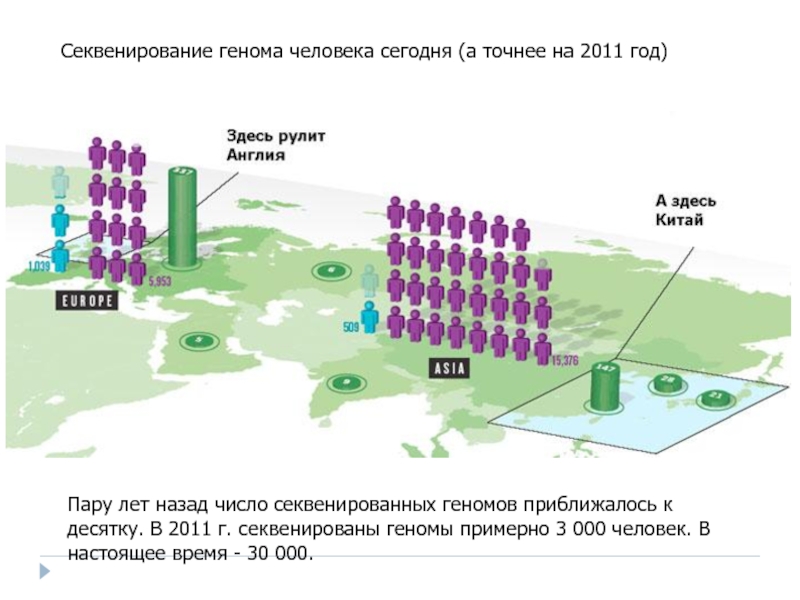
Слайд 72Секвенирование генома человека сегодня (а точнее на 2011 год)
Пару лет назад
Слайд 73Расшифрован геном сперматозоида
Объектом исследования 91 мужская гамета, которая была выделена из
Было определено, что каждый сперматозоид абсолютно уникален по степени и частоте случаев мутаций и рекомбинаций генов, причем это отличие оказалось несколько более выраженным, чем ожидалось.
Полученные данные, в особенности касающиеся уровня мутаций в мужских гаметах, дают возможность по-новому взглянуть на проблему мужского бесплодия. «Мы готовы побиться об заклад, что вскоре будет доказана связь между числом и типом мутаций в сперматозоидах и мужской фертильностью, - заявили ученые. - Все это само по себе вносит гигантский вклад в понимание причин мужского бесплодия, о которых известно значительно меньше, чем о причинах женского бесплодия".
Впервые расшифрован геном человеческой половой клетки. Об успешном завершении длившегося почти десятилетие процесса расшифровки полного генома сперматозоида объявила группа ученых из Стэнфордского университета. Результаты их работы опубликованы 20 июля 2012 г. в журнале Cell.
Слайд 74Геном человека разнообразнее, чем считалось раньше
И вот учёные Европейской лаборатории молекулярной
Во время удвоения ДНК могут возникать различные ошибки: не только замена одного нуклеотида на другой, но и перенос, удвоение или потеря участка ДНК. Большинство таких изменений не затрагивает жизненно важные гены и поэтому не отсеивается естественным отбором. В результате в любой крупной популяции (например, человеческой) обнаруживается много структурных вариантов генома (СВГ).
Слайд 75
В данном случае секвенирование (определение нуклеотидной последовательности молекулы ДНК) было проведено
Сравнивая ДНК опухоли поджелудочной железы и нормальных клеток, исследователи обнаружили генетические изменения (мутации), которые имеют важное значение для разработки оптимального способа лечения. В будущем все онкобольные смогут надеяться на такой индивидуальный подход.
«Мы пока не обладаем полным знанием обо всех наблюдаемых генетических мутациях, о том, как они согласуются с препаратами, применяемыми для лечения, — поясняет Джеффри Трент, президент и директор по исследованиям Исследовательского института трансляционной геномики. — То, чем мы занимаемся, — всего лишь прототип медицины будущего».
Секвенирование поможет лечить и предотвращать раковые заболевания
Американские ученые успешно завершили секвенирование полного генома онкологического пациента — с учётом как нормальных, так и раковых клеток.
Слайд 76
Планируется, что проект по секвенированию генома 100 тысяч пациентов продлится от
В Великобритании стартовал масштабный проект секвенирования генома 100 тысяч пациентов, у которых диагностирован рак или одно из редко встречающихся заболеваний
Авторы проекта обещают, что благодаря результатам их работы уже через пять-десять лет все онкологические больные смогут получать персонализированную терапию, что в корне изменит нынешнюю ситуацию в этой области и фактически сделает рак если не полностью излечимым, то контролируемым заболеванием.
В настоящее время генетическое профилирование новообразований применяется лишь при некоторых видах рака. Так, при метастатическом раке молочной железы определяют наличие опухолевой гиперэкспрессии гена HER2 – только в этом случае возможна терапия препаратом герцептин. Препарат вемурафениб увеличивает выживаемость только тех пациентов с метастатической меланомой, у которых имеется мутация BRAF V600.
Слайд 77В Калифорнийском университете запущен масштабный проект для быстрого тестирования микробных инфекций
Наряду
Становится все яснее и яснее тот факт, что живучесть микробных патогенов и их способность проникать в пищевую цепь обусловлены генетической пластичностью, которая позволяет им приспосабливаться к любому окружению. Отсутствие информации о геномах бактерий, имеющих отношение к продуктам питания, лишает ученых возможности обеспечить людей безопасным питанием.
В результате выполнения проекта "100 тысяч геномов" диагностические тесты сделаются быстрыми, точными и экономичными.
Секвенирование будет проводиться в Калифорнийском университете совместно с м выполнении крупных работ по расшифровке ДНК и функциональной геномике с Пекинским институтом геномики (BGI).
Реализация проекта предполагает чтение геномов целевых микроорганизмов. Большая часть собранных бактериальных геномов будет представлена в виде черновых вариантов, которые будут сопоставляться с избранными полногеномными референсными последовательностями.
Слайд 78
270 бактерий, 46 эукариот, из них 12 протистов, 19 грибов, 2
Человек
Нематоды Caenorhabditis briggsae,
Дрозофилы,
Малярийного комара,
Шелкопряда,
Асцидии,
Рыб Tetraodon nigroviridis, Danio rerio и Takifugu rubripes,
Крысы, мыши,
Домашней собаки,
Шимпанзе,
Макаки-резус,
Кенгуру,
Курицы,
Кошки,
Опоссум и др.
25 архебактерий,
В ближайшем будущем планировалось секвенировать и расшифровать еще 905 прокариотических и 569 эукариотических геномов. Работа продолжается!
В качестве примера – данные 3-4 летней давности:
Секвенировано:
Расшифровка геномов различных организмов
Слайд 79Расшифровка генома мини-пигов (миниатюрных свиней Wuzhishan) предоставила ценную медицинскую информацию.
Опубликована полная
Работа выполнена китайскими учеными из Пекинского геномного института (BGI), Пекинского института ветеринарии и Китайской академии сельскохозяйственных наук в сотрудничестве с коллегами из Дании.
Появление генома мини-свиньи, или мини-пига, предоставляет генетические инструменты для изучения животного, у которого наблюдаются те же сложные заболевания, что и у человека, в частности, ишемическая болезнь сердца. В исследовании выявлено 20326 общих с человеком генов.
Слайд 80Расшифрован геном мыши: отличие от человека - не более процента
С точки
По словам ученых, в процессе расшифровки генома мыши, было открыто около 1200 человеческих генов.
Как сообщается, на 20 хромосомах у мыши "записано" 2,5 млрд пар нуклеотидов - "букв" генетического кода. Количество генов оценивается на уровне 30 тыс., что сравнимо с числом генов у человека.
Слайд 81
Прочитан геном шимпанзе
Люди отличаются от шимпанзе не тем, чем мы хотели
В попытках
Видимо, скачок в умственных способностях человека обусловлен изменениями в очень малом числе генов, которые сложно детектировать.
Напротив, гены, участвующие в функционировании семенников, демонстрируют массовое и быстрое накопление благоприятных мутаций как у человека, так и у шимпанзе.
Недавно прочтен и полный геном шимпанзе — нашего самого близкого современного родственника.
Слайд 82Ученые: человека от зверя отделяет только один ген
Этот ген активен
Международная группа ученых обнаружила ген, присущий только людям, но не приматам и другим животным. По всей видимости, именно этот ген сыграл ключевую роль в быстрых эволюционных изменениях в человеческом мозге.
Благодаря этому гену мы научились пользоваться сложными инструментами и разговаривать. Этот ген называется miR-941. Он кодирует микроРНК.
Слайд 83Использование ДНК-технологий в:
ДНК-генеалогии человека
Палеонтологии
Криминалистике
Генетической паспортизации населения
Медицине
Сельском хозяйстве
Спорте и др.
Слайд 85Развитие нового направления – ДНК-генеалогии человека
ДНК-генеалогия использует ДНК-тесты совместно с традиционными
В процессе теста специальных ДНК-маркеров последовательность оснований в них повторяется множество раз (это называется «коротким тандемным повтором» (англ. Short Tandem Repeat)). Например, специальное оборудование читает последовательность ДНК так:
… CTGT TCTA TCTA TCTA TCTA TCTA TCTA TCTA TCTA TCTA TCTGCC …
Можно заметить, что TCTA повторяется 9 раз, а поскольку этот STR маркер называется DYS391 (DNA Y-chromosome Segment № 391) делается запись: DYS391 = 9.
Слайд 86Наиболее распространенные генетические различия между людьми составляют единичные замены (SNP) пар
Информацию о единичных изменениях исследователи систематизируют, находят общие мутации ДНК у различных людей. Можно рассчитать частоту определенных типов изменений в конкретном месте на земле и их распространение.
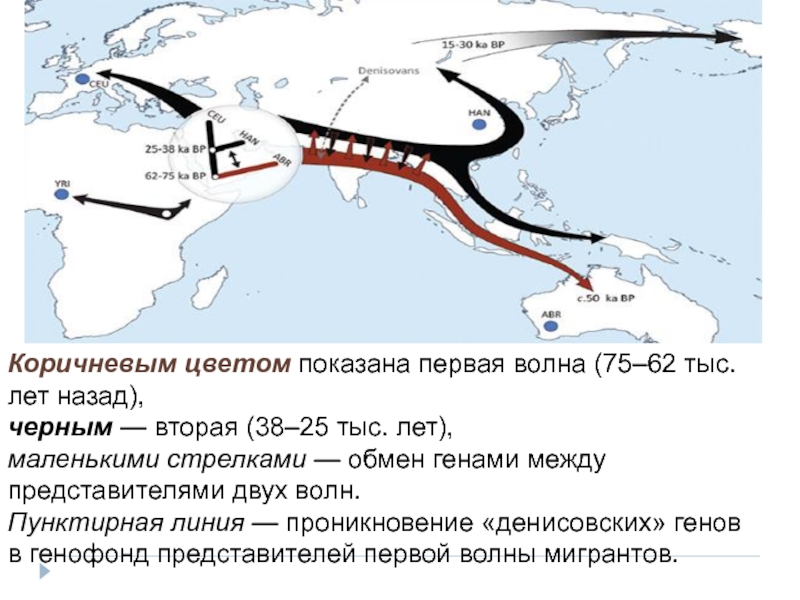
Слайд 87Коричневым цветом показана первая волна (75–62 тыс. лет назад),
черным — вторая (38–25 тыс.
маленькими стрелками — обмен генами между представителями двух волн.
Пунктирная линия — проникновение «денисовских» генов в генофонд представителей первой волны мигрантов.
Слайд 88ГаплогруппаR1а
Происходит от мутации гаплогруппы R1, произошедшей у мужчины, жившего ок. 15
Больше всего данная гаплогруппа распространена среди славян, северных индийцев (потомки ведийских ариев) и среднеазиатских народов.
Наибольшее распространение имеет в Северо-Западной Индии, Пакистане, Центральной и Восточной Европе: среди лужичан (63 %), поляков (ок. 56 %), украинцев (54 %), русских (52—53 %), белорусов (60 %), литовцев (45 %), латышей (41 %), татар (33—34 %), башкир (26 %)и в Центральной Азии.
Умеренное распространение в скандинавских странах (23 % в Исландии, 18—19 % в Швеции и ок. 27 % в Норвегии), в Иране (от 4 до 25 %).
Слайд 89Гаплогруппа N1
Y-ДНК гаплогруппа N1 найдена повсюду в Северной Евразии.
Гаплогруппа распространена
Слайд 90Гаплогруппа I2
Гаплогруппа I2 зародилась в Юго-Восточной Европе более 15 тыс. лет
Слайд 91Гаплогруппа I1
Гаплогруппа I1 зародилась не более 5000 лет на территории современной
Слайд 92Гаплогруппа E1b1b1 зародилась в верхнем палеолите примерно 15000-20000 лет назад на
Слайд 93Гаплогруппа J2
Гаплогруппа J2-M172 зародилась на Ближнем Востоке примерно 18 тыс. лет
Слайд 94Гаплогруппа R1b
Гаплогруппа R1b возникла предположительно в Передней Азии 15-20 тыс. лет
Слайд 95Гаплогруппа С3
Гаплогруппа, возникшая после того, как современные люди покинули Африку. Миграционное
Слайд 96Гаплогруппа Q
Y-хромосомная гаплогруппа Q распространена у некоторых сибирских народов, а так
Слайд 97Гаплогруппа G2a
Гаплогруппа G2 предположительно возникла около 30 тыс. лет назад на
Слайд 99Генетики: европейские мужчины оказались дальними родственниками египтян
Швейцарские генетики пришли к
Ученые полагают, что их общий предок жил на Кавказе примерно 9,5 тысячи лет назад.
В ходе исследования специалисты взяли образец ДНК из мумифицированных останков фараона, на египетском троне более трех тысяч лет назад, и сравнили с современным европейцем. Результаты исследования показали, что Тутанхамон принадлежал известной группе р1Б1А2, к которой относятся примерно 50% всего мужского населения Западной Европы.
Также ученые пришли к выводу, что к одной генетической группе с Тутанхамоном относятся около 70% испанцев и 60% французов. По итогам пройденной работы, стало известно, что у половины мужского населения Швейцарии в венах течет египетская кровь.
Слайд 100Китайские ученые провели исследование генома прямого потомка Чингисхана.
Это первое исследование ДНК
Считается, что у нег было около 3 тысяч жен, и до половины процента населения Земли сегодня могут являться его потомками. Ученые намерены продолжать исследования, и проведут секвенирование геномов еще 199 монголов. Таким образом, будет создана база данных
генома этой этнической группы. Это, вероятно, поможет выявить особенности эволюции монголов, а также исследовать ряд болезней.
Ученые исследуют геном потомка Чингисхана
Слайд 101Снежный человек произошел от
встречи женщины с обезьяной
Секвенирование генома из 20
Изучение ДНК привело экспертов в областях генетики, судебной медицины, патанатомии к выводу, что снежный человек зародился около 15 000 лет назад в результате встречи женщины с самцом неизвестного ныне вида приматов. По результатам исследования Кетчам обратилась к официальным лицам с просьбой признать бигфута одним из коренных обитателей своего региона, наделенного всеми соответствующими правами.
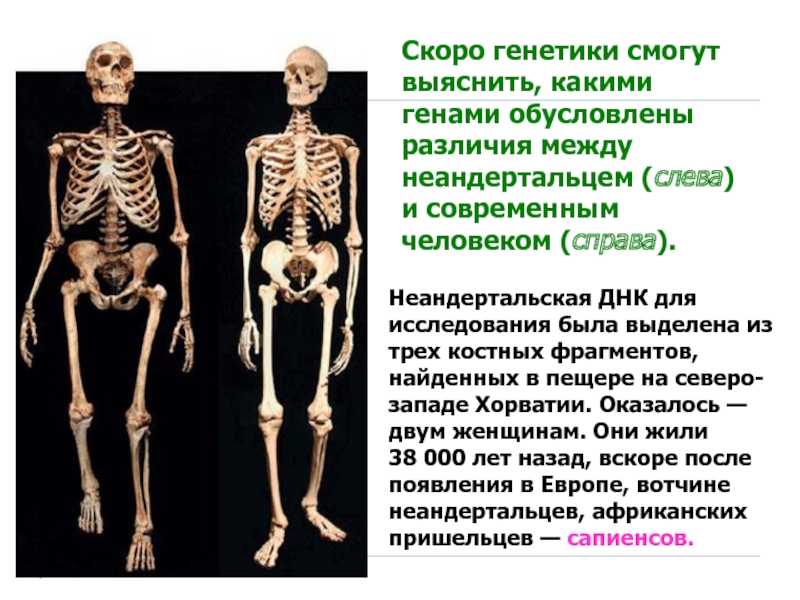
Слайд 103Скоро генетики смогут выяснить, какими генами обусловлены различия между неандертальцем (слева)
Неандертальская ДНК для исследования была выделена из трех костных фрагментов, найденных в пещере на северо-западе Хорватии. Оказалось — двум женщинам. Они жили 38 000 лет назад, вскоре после появления в Европе, вотчине неандертальцев, африканских пришельцев — сапиенсов.
Слайд 104Геном неандертальца прочтен, осталось в нем разобраться
Важнейшие вехи в развитии палеогеномики
1997 — отсеквенирован первый фрагмент митохондриальной ДНК неандертальца.
2006 — начало проекта «геном неандертальца».
2007 — установлено, что неандертальцы были рыжими и светлокожими.
2007 — показано, что ген FOXP2 (ген речи) идентичен у неандертальца и современного человека.
2008 — показано, что у неандертальцев встречалась группа крови 0.
2009 — черновое прочтение ядерного генома неандертальца.
Слайд 105Американские генетики ищут суррогатную мать для неандертальца
Вид неандертальцев вымер 33 000
На первом этапе планируется ввести искусственно воссозданную ДНК неандертальца в стволовые клетки человека. Образовавшийся эмбрион можно будет имплантировать в матку суррогатной матери.
Ученый считает, что древних людей ошибочно изображают глупыми и примитивными, так как объем мозга неандертальца был чуть меньше, чем у современного человека.
Отметим, что именно при участии этого ученого был запущен проект по исследованию генома человека.
Руководитель группы ученых из Высшей школы медицины при Гарвардском университете Джордж Черч ищет женщину, которая готова выносить в плод неандертальца.
По словам профессора ему удалось полностью расшифровать геном древнего предка современного человека, а для завершения эксперимента необходимо найти женщину, которая согласится выносить клон неандертальца.
Слайд 107В несколько упрощенном варианте генетические паспорта (или карты) уже существуют на
Правоохранительные органы США используют результаты идентификационных исследований ДНК осужденных преступников, пробы биологического материала с мест происшествий и неопознанных человеческих останков.
В Великобритании обязательному ДНК-тестированию подвергаются не только преступившие закон, но и подозреваемые в совершении правонарушений.
В Западной Европе, США и Канаде «генетическая паспортизация» проводится по различным медицинским показаниям и просто по личному желанию граждан. Формируются индивидуальные и семейные базы генетических данных — процесс начался.
Генетическая паспортизация
Слайд 108Это получение, хранение и использование биологического материала и содержащейся в нем
Цель геномной регистрации - идентификация личности человека.
С 1 января 2009 г. в России введена обязательная и добровольная геномная регистрация граждан
Слайд 111 Совершенству нет предела
Финская
Обнаружив угнанную машину, полицейские увидели в салоне комара и предположили, что он может стать важной уликой. Образцы ДНК, полученные экспертами при анализе крови, которую выпило насекомое, совпали с данными, которые уже значились в полицейской картотеке.
Подозреваемый отрицает свою вину, утверждая, что ехал автостопом и случайно остановил машину, которая оказалась в розыске.
Это первый случай в истории криминалистики, когда дело раскрывают при помощи насекомого.
Слайд 112
Биочип для криминалистики
Специалисты Института молекулярной биологии им. В. А. Энгельгардта РАН и Московского физико-технического
Биочип содержит характерные последовательности ДНК трёх генов: ABO, AMEL и HLA-DQA1. Первый ген (ABO) определяет группу крови человека, HLA-DQA1, ген главного комплекса гистосовместимости, имеет 34 варианта. Ген AMEL кодирует белок, который участвует в развитии зубной эмали. Он расположен на половых хромосомах, причём последовательности на Х и Y-хромосомах несколько отличаются, что помогает определить пол человека.
Идентифицировать человека можно по окуркам сигарет с фильтром, на котором осталась слюна, смятым в руке бумажным салфеткам со следами пота. Участников эксперимента также просили выпить воды из одноразового стакана, после чего смоченной в стерильной воде салфеткой с его края снимали отпечатки губ. Из этого материала выделяли ДНК нужных генов и наносили её на биочип для идентификации.
Слайд 114Гены приносят счастье женщинам
Ученые обнаружили ген, который делает женщин счастливыми. На
Ученые заявили, что слабовыраженная форма гена моноаминоксидазы А (МАОА) у женщин связана с повышенным ощущением счастья. "Это первый женский ген счастья", - комментирует руководитель исследования ХеньянЧен, профессор эпидемиологии и биостатистики Флоридского колледжа общественного здравоохранения во Флориде.
Низкую активность гена МАОА ранее связывали с такими негативными последствиями, как алкоголизм, агрессивность, асоциальное поведение. Некоторые ученые даже называют его "геном воина". Однако, как показала наша работа, он имеет "светлую" сторону, по крайней мере для женщин", - говорит Х.Чен.
Ген МАОА регулирует ферменты, которые расщепляют серотонин, дофамин и другие нейромедиаторы в головном мозге ("гормоны настроения", которые являются мишенями для антидепрессантов, поскольку их снижение связано с депрессией). Как выяснилось в ходе исследования, снижение экспрессии гена МАОА повышает количество моноаминов, благодаря которым нейромедиаторы остаются на высоком уровне, что в свою очередь положительно влияет на настроение.
Ученые объясняют гендерное отличие работой гормона тестостерона, который содержится у женщин в меньшем количестве, чем у мужчин. Именно он блокирует положительный эффект гена МАОА у представителей сильной половины человечества. Возможная выгода от гена у мальчиков снижается при росте уровня тестостерона в период полового созревания. "Мужчины счастливее до полового созревания, поскольку их уровень тестостерона в это время ниже", - полагает Х.Чен
Слайд 115Ученые: родители награждают ребенка 60 мутациями
Впервые ученые смогли ответить на вопросы:
Каждый из людей получает от родителей около 60 новых мутаций. Это поразительное открытие было сделано в ходе прямых сравнений геномов отца и матери с геномами их детей.
Слайд 116Генетическая предрасположенность к курению
Статьи, опубликованные на прошедших выходных в журнале «Nature
Начало курения оказалось связано с вариантом гена в 11 хромосоме, а изменения в 9 хромосоме чаще встречались у бросивших курить.
Люди с вариантами генов в 8 и 19 хромосомах обычно курили больше сигарет (в среднем на полсигареты в день) и были на 10% более подвержены риску заболевания раком легких, чем люди без этих изменений.
Все эти исследования не только добавили новые факты к списку связей между генами и курением, но и сделали свой вклад в разработку диагностических средств для выявления людей подверженных более серьезному риску при курении.
Несколько исследований, проведенных в последнее время, показали, что начало курения и пристрастие к этой привычке может во многом быть связано с генами человека.
Слайд 119Болезнь Лу Герига (или боковой амиотрофический склероз) — относится к нейродегенеративным,
Болезнь Лу Герига вызывается мутантной липучестью белка
Болезнь Лу Герига (или боковой амиотрофический склероз) — относится к нейродегенеративным, и главный её признак — накопление белковых масс в нейронах, которые из-за этого перестают правильно работать.
Слайд 120В статье, опубликованной в Science показано, что, когда с такого участка
Слайд 122Установлена молекулярная причина шизофрении
В норме соединение ацетильных групп с гистонами (ацетилирование
По мнению авторов исследования, которое опубликовано в журнале Translational Psychiatry, именно недостаточное ацетилирование гистонов в головном мозге является молекулярной причиной шизофрении.
Для устранения этого эпигенетического эффекта ученые предлагают начать разрабатывать лекарства на основе веществ, которые подавляют активность определенного фермента – гистон-деацетилазы. Этот фермент лишает гистоны необходимых для последующего считывания ДНК ацетильных групп.
Биологи из Исследовательского института Скриппса в Калифорнии обнаружили, что некоторые участки ДНК в клетках головного мозга больных шизофренией постоянно пребывают в "упакованном" и недоступном для считывания генетической информации состоянии, сообщает ScienceDaily.
Слайд 123У 30% малышей наблюдаются генетические нарушения
Как оказалось, каждый год количество бесплодных
По этой причине уменьшается количество новорожденных. Если в стране в 1990 г. жили 40 млн. детей, то в 2015-м в России их количество не превысит 28 миллионов. Здоровыми при этом рождаются лишь 18–20% детей, а у 30% врачи наблюдают нарушения генетического характера. Ученые говорят, что во многом причиной данного явления есть так называемый синдром мегаполиса: загрязнение пищи и окружающей среды токсическими продуктами , постоянное присутствие иммунно-депрессивных и аллергенных факторов, а также отсутствие условий , в которых ребенок может полноценно развиваться и формироваться.
Согласно сведениям академии наук России, в Российской Федерации бесплодием страдают 10 млн. человек. При этом из тех малышей, которые рождаются, количество здоровых составляет менее 25%, а у 30% есть генетические нарушения.
Слайд 124Трисомию можно лечить
Вполне возможно, что, хотя и не сегодня, и не
средство для лечения синдрома Дауна. Американские исследователи-микробиологи сумели изъять копии 21-й хромосомы из клеток человека, который болеет этим тяжелым, неизлечимым врожденным заболеванием. Конечно, этот единичный успех еще не значит, что вот-вот уже совсем скоро появятся эффективные
, общедоступные методы лечения этого сложнейшего генетического заболевания. Ученые не спешат делать заявления и говорят о том
, до времени, когда можно будет лечить больных с этим синдромом еще нужно ждать и ждать. Однако, их работа
уже сегодня сможет существенно помочь диагностировать и лечить рак крови у этих больных – а ведь очень и очень многие люди с синдромом Дауна подвержены этому страшному заболеванию. Ученые считают, что при помощи их открытия уже совсем скоро можно будет практически полностью “очистить” (это дословное цитирование слов одного из исследователей) пресловутые стволовые клетки пациента от этой так называемой Хромосомы “Дауна”. Конечно, понять, что именно и как делают ученые для подобной “очистки” мы не сможем, но в общих чертах напомним, что всего у здорового человека имеется 24 пары хромосом. Однако, есть некоторые виды генетических заболеваниях, при которых отдельные хромосомы мутируют из “дуэта” в “трио”. Эта мутация называется трисомией. Трисомии бывают разных видов, но в самом распространенном случае это мутация касается именно 21-й хромосомы. Трисомия 21-й хромосомы и является первопричиной такого заболевания синдром как Дауна. Американские исследователи разработали методику, позволяющую удалить лишнюю хромосому у 21-й пары. Все существовавшие до этого исследования приводили только к полному разрушению 21-й лишней хромосомы.
Слайд 125В нашем организме этанол превращается в ацетальдегид, который ведёт себя довольно
В 2011 г. Установлено, что алкоголь вызывает мутации в нашей ДНК
Как пишут в журнале Nature, ацетальдегид —может приводить к катастрофическим повреждениям ДНК. И умирать бы нам от первой же рюмки, если бы у клеток не было двухступенчатой системы защиты: первая ступень включает в себя ферменты, нейтрализующие собственно ацетальдегид, вторая — набор белков, берущих на себя экстренный ремонт повреждённой ДНК. Учёные экспериментировали с беременными мышами, у которых были отключены обе системы: у таких животных даже небольшая однократная доза алкоголя приводила к гибели плода; более того, у самих взрослых мышей наблюдалась гибель кровяных стволовых клеток.
Проверить влияние алкоголя на ДНК учёных побудили две группы сведений. Во-первых, к алкоголю крайне чувствительны люди, страдающие от синдрома Фанкони, тяжёлого наследственного недуга. У этих больных не работают белки, ответственные за репарацию ДНК, вследствие чего ацетальдегид наносит необратимые повреждения генам, и это приводит болезням крови и онкозаболеваниям. С другой стороны, люди с врождённой непереносимостью алкоголя весьма подвержены раку пищевода, при этом у них не работает система нейтрализации ацетальдегида. В обоих случаях последствия приёма алкоголя выражены в заболеваниях, затрагивающих молекулярно-генетический аппарат клетки.
Действие этих защитных систем может не справляться при регулярном употреблении алкоголя. Это часто можно наблюдать в виде пороков развития, объединяемых общим названием плодного алкогольного синдрома, которыми родители-алкоголики награждают своих детей.
Слайд 126Американские ученые и предприниматели заявили о старте нового исследовательского проекта. «Индивидуальный
Организаторы приглашают к сотрудничеству добровольцев, расшифрованные геномы и медицинские данные которых будут опубликованы в открытом доступе в Интернете. На данный момент к публикации готовятся геномы и медицинские карты десяти первых участников. Сейчас в очередь на расшифровку генома записались более пяти тысяч человек, а в будущем их число планируется довести до 100 тысяч.
Беспрепятственный доступ к гигантской базе проекта различных ученых значительно ускорит изучение причин наследственных заболеваний и поиск новых методов их лечения. На данный момент ни у кого из добровольцев не было обнаружено серьезных генетических аномалий, но если в результате расшифровки генома у кого-то из добровольцев будут обнаружены дефекты, то участник может в любой момент отказаться от участия в проекте и публикации своих данных.
Желающие пополнить базу данных проекта могут зарегистрироваться в качестве участника на сайте Personal Genome Project.
Слайд 127Преимплантационная диагноститка
Жительница Лондона родила первого в Великобритании ребенка, которого на ранней
Генетический анализ был произведен на клетках зародыша, полученного после искусственного оплодотворения перед имплантацией в организм матери. Для этого понадобилось изъять одну из восьми клеток, из которых состоит эмбрион на третьем дне развития. Как было известно ранее, на дальнейшее развитие организма такая процедура не влияет. Подобная диагностика уже достаточно широко используется для обнаружения генетических дефектов, обязательно приводящих к развитию заболевания, такого как, например, муковисцидоз.
В связи с этим ценность произошедшего события скорее не научная, а юридическая. Как и любое достижение в области генетики и эмбриологии оно вызвало неоднозначную реакцию: в то время как одни видят в этом начало новой эпохи в развитии медицины и здоровья общества, другие опасаются перспектив вырождения «селекционного» человечества или кары за «вмешательство в божий промысел».
Слайд 128Британцев будут проверять на генетические болезни перед зачатием
Жители Великобритании смогут свободно
В настоящее время генетическое обследование бесплатно могут пройти лишь британцы с высоким риском развития наследственных болезней, например, чьи родственники страдают такими заболеваниями. Согласно отчету HGC, внедрение общей скрининговой программы обеспечит жителям Соединенного Королевства равноправный доступ к указанным медицинским услугам.
Одним из главных преимуществ такой программы является возможность предоставления британцам, у которых в ходе тестирования будут выявлены наследственные болезни, вспомогательных репродуктивных технологий. В частности, использования донорских яйцеклеток и спермы, а также проведение генетических анализов экстракорпорально оплодотворенных яйцеклеток.
Рекомендации HGC по внедрению генетического тестирования были представлены на рассмотрение британского Национального скринингового комитета (UK NationalScreeningCommittee). Комитету предстоит определить перечень медицинских учреждений страны, в которых будут проводиться соответствующие анализы.
Слайд 129Обнаружен ген, отключение которого у мышей приводит к смерти, а у человека — к
Этот ген (SCN9A) находится на второй хромосоме и кодирует белок, участвующий в транспорте ионов натрия через мембраны нейронов, отвечающих за болевые ощущения.
Открытие дает возможность фармакологам разработать новые высокоэффективные анальгетики.
Чтобы никогда не чувствовать боли, человеку достаточно отключить один ген
Слайд 130Болезнь Паркинсона развивается при недостатке микроРНК
Группа американских ученых исследовала ансамбли
Слайд 131Алкоголь нарушает развитие мозга эмбриона, блокируя работу фактора роста
Выяснилось, что
Слайд 132Табакокурение снижает активность генома
Обсуждение [0]
К многочисленным предостережениям медиков о том,
Слайд 133Управление синтезом тРНК может помочь в лечении раковых заболеваний
Американские ученые открыли
Слайд 134Больных с нарушением свертываемости крови будут лечить препаратом из молока генно-инженерных
Американские эксперты признали эффективность и безопасность препарата человеческого белка антитромбина, полученного из молока генноинженерных коз.
Планируется наладить производство препаратов для лечения гемофилии, ангионевротического отека, дефицита альфа-1 антитрипсина и других заболеваний, связанных с недостаточностью какого-либо белка. Для большей части подобных болезней мировая потребность в соответствующем белке может быть удовлетворена одним стадом из 50 коров или 100 коз.
Слайд 135Трансгенные комары помогут в борьбе с малярией
Американские ученые вывели трансгенную
Слайд 136Найден распространенный ген гипертензии
Американские ученые обнаружили ген STK39, увеличивающий риск
Слайд 139Генные инженеры открыли способ увеличения урожайности путем увеличения транспорта фитогормонов.
Как
Генетики совершили открытие, которое может решить многие проблемы сельского хозяйства
Слайд 140Употребление нового сорта помидоров препятствует развитию рака и увеличивает продолжительность жизни
Антоцианины – натуральные пигменты, относящиеся к классу флавоноидов. Обладают антиоксидантными свойствами, содержатся в ежевике, чернике и клюкве. Предположили, что продукты, богатые антоцианинами, могут препятствовать развитию злокачественных опухолей, а также оказывать благоприятное действие на сердечно-сосудистую систему.
Ученые выделили два гена из растений львиного зева, отвечающих за синтез антоцианина, и встроили их в геном обычных помидоров. В результате им удалось получить темно-фиолетовые томаты с высоким содержанием полезного антиоксиданта.
Затем новый продукт испытали на мышах, лишенных важного противоракового гена p53 и, соответственно, склонных к развитию опухолей. Выяснилось, что употребление фиолетовых помидоров в виде порошка увеличило среднюю продолжительность жизни грызунов почти в три раза – со 142 до 182 дней.
Слайд 141Выведена сверхполезная морковь
Американские ученые вывели морковь, содержание кальция в которой
Для этого они внесли в геном растения модифицированный ген, регулирующий транспорт кальция через клеточные мембраны.
Эксперимент с участием 30 взрослых добровольцев показал, что из генетически модифицированной моркови они получали на 41% больше кальция, чем из обычных овощей.
Слайд 142ГМО: без вариантов?
Витаминизированная кукуруза
Трансгенная папайя
Трансгенная морковь – в ней вдвое больше
Трансгенный золотой рис (справа)
Слайд 144Феноменальные возможности элитных спортсменов зависят от уникальных генетических комбинаций
Молекулярная генетика
Слайд 145Британские ученые обнаружили зависимость успеха восхождения на восьмитысячники от наличия благоприятного
Проведено генетическое тестирование 139 высококвалифицированных альпинистов с целью выявления полиморфизмов генов, которые обуславливают индивидуальные различия в способности к восхождению на восьмитысячники.
Ученые обнаружили, что частота встречаемости длинной (I аллель) копии гена АПФ (ангиотензин-превращающий фермент) преобладает в группе альпинистов, которые смогли успешно преодолеть 8000-метровый барьер по сравнению с теми, кому не удалось это сделать.
Кроме того, носители генотипа II (наличие двух длинных копий гена) в среднем достигали 8559 метров, в то время как наличие двух коротких копий гена АПФ (генотип DD) “останавливало” альпинистов в среднем на 8079-метровой отметке.
Слайд 146Определены генетические маркеры предрасположенности к занятиям футболом
Известно, что среди испанских
Ранее уже было показано, что наличие этого генотипа ассоциируется с выдающимися скоростно-силовыми возможностями, чем не преминула воспользоваться Австралийская футбольная лига в отборе детей для занятий футболом еще 2 года тому назад.
Слайд 147В США вырастили супермышей
Помещенный в колесо, грызун с модифицированным геном
Генетически модифицированная по гену PEPCK (фосфоенолпируват –карбоксикиназа) супермышь, способная пробегать вдвое большие дистанции, чем ее сородичи, выведена американскими учеными.
Слайд 148Опубликована новая версия карты генов человека, ассоциированных с физической активностью
Идентифицировано
Во-первых, это гены, отвечающие за развитие быстроты, силы, выносливости, мышечной массы, восстановление после физических нагрузок, энергетику.
Во-вторых, это гены, связанные с профессиональными патологиями у спортсменов.
И наконец, гены, чувствительные к пищевым веществам.
Пожалуй, на первое место нужно поставить те гены, которые влияют на здоровье спортсменов. Например, для тех, кто занимается бегом на длинные дистанции, лыжными гонками, велоспортом, хоккеем и футболом, важно определить гены, которые отвечают за работу сердца. У гимнастов определяют склонность к травмам, у боксеров – риск повреждения головного мозга.
Слайд 1491. Фосфор - ключевой компонент ДНК, но в прошлом году, команда
Источник: globalscience.ru
12 фактов о ДНК, которые мы еще не знали
Слайд 1512020 год
На рынке появляются лекарства от диабета, гипертонии и других заболеваний, разработанные на основе геномных данных.
Разрабатывается терапия рака.
Фармакогеномика становится общепринятым подходом для создания многих лекарств.
Изменение способа диагностики психических заболеваний, появление новых способов их лечения, изменение отношения общества к таким заболеваниям.
Практические приложения геномики все еще доступны далеко не везде.
Слайд 1522040 год
Все общепринятые меры здравоохранения основаны на геномике.
Определяется предрасположенность к большинству заболеваний (ещё
Болезни определяются на ранних стадиях путем молекулярного мониторинга.
Для многих заболеваний доступна генная терапия.
Замена лекарств продуктами генов, вырабатываемыми организмом при ответе на терапию.
Средняя продолжительность жизни достигнет 90 лет благодаря улучшению социо-экономических условий.
Проходят серьезные дебаты о возможности человека контролировать собственную эволюцию.







































































































![Табакокурение снижает активность генома Обсуждение [0] К многочисленным предостережениям медиков о том, что курение ведет](/img/tmb/3/250353/7a691adcfb0b361d4bc228e2ad38f79b-800x.jpg)