Слайд 1МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКИЙ
ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ – МСХА ИМЕНИ К.А. ТИМИРЯЗЕВА
(ФГБОУ ВО РГАУ - МСХА ИМЕНИ К.А. ТИМИРЯЗЕВА)
Факультет зоотехнии и биологии
Метаболические пути
Выполнил студент 405 группы
Гарбузов С.Г.
Москва, 2017
Слайд 2ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
Характер метаболизма в тканях во многом определяется питанием. У
человека и ряда других млекопитающих метаболическим превращениям подвергаются продукты, абсорбируемые после переваривания содержащихся в пище углеводов, липидов и белков. Это главным образом глюкоза, триацилглицерол и, аминокислоты. У жвачных животных (и в меньшей степени у других травоядных) целлюлоза переваривается симбиотическими микроорганизмами с образованием низших гомологов органических кислот (уксусной, пропионовой, масляной); тканевый метаболизм у этих животных адаптирован к утилизации в качестве основного субстрата низших жирных кислот. (Марри Р., Греннер Д., Мейес П., Родуэлл В.)
Слайд 3Тканевое дыхание
Это процесс потребление клетками тканей организма кислорода, который участвует в
биологическом окислении. Такой вид окисления называют аэробным окислением. Если конечным акцептором в цепи переноса водорода выступает не кислород, а другие вещества (например пировиноградная кислота), то такой тип окисления называют анаэробным.
Т.о. биологическое окисление - это дегидрирование субстрата с помощью промежуточных переносчиков водорода и его конечного акцептора.
Дыхательная цепь (ферменты тканевого дыхания) - это переносчики протонов и электронов от окисляемого субстрата на кислород. Окислитель - это соединение, способное принимать электроны. Такая способность количественно характеризуется окислительно-восстановительным потенциалом по отношению к стандартному водородному электроду, рН которого равен 7,0. Чем меньше потенциал соединения, тем сильнее его восстанавливающие свойства и наоборот.
Т. о. любое соединение может отдавать электроны только соединению с более высоким окислительно-восстановительным потенциалом. В дыхательной цепи каждое последующее звено имеет более высокий потенциал, чем предыдущее.
(Кнорре Д. Г., Мызина С. Д.)

Слайд 4Дыхательная цепь состоит из:
1. НАД - зависимой дегидрогеназы;
2.
ФАД- зависимой дегидрогеназы;
3. Убихинона (КоQ);
4. Цитохрмов b, c, a+a3 .
НАД-зависимые дегидрогеназы. В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.
ФАД и ФМН-зависимые дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 (ФАД).
Убихинон (КоQ) отнимает водород у флавопротеидов и превращается при этом в гидрохинон.
Цитохромы - белки хромопротеиды, способные присоединять электроны, благодаря наличию в своем составе в качестве простетических групп железопорфиринов. Они принимают электрон от вещества, являющегося немного боле сильным восстановителем, и передают его более сильному окислителю. Атом железа связан с атомом азота имидазольного кольца аминоксилоты гистидина с одной стороны от плоскости порфиринового цикла, а с другой стороны с атомом серы метионина. Поэтому потенциальная способность атома железа в цитохромах к связыванию кислорода подавлена.
В цитохроме с порфириновая плоскость ковалентно связана с белком через два остатка цистеина, а в цитохромах b и а, она ковалентно не связано с белком.
В цитохроме а+а3 (цитохромоксидазе) вместо протопорфирина содержатся порфирин А, который отличатся рядом структурных особенностей. Пятое координационное положение железа занято аминогруппой, принадлежащей остатку аминосахара, входящего в состав самого белка. (Кнорре Д. Г., Мызина С. Д. )

Слайд 5Механизм работы электронтранспортной цепи
Наружная мембрана митохондрии (рис. 4.8.1)проницаема для большинства мелких
молекул и ионов, внутренняя почти для всех ионов (кроме протонов Н) и для большинства незаряженных молекул.
Все вышеперечисленные компоненты дыхательной цепи встроены во внутреннюю мембрану. Транспорт протонов и электронов по дыхательной цепи обеспечивается разностью потенциалов между ее компонентами. При этом каждое увеличение потенциала на 0,16 В освобождает энергию, достаточную для синтеза одной молекулы АТФ из АДФ и Н3РО4. При потреблении одной молекулы О2 образуется 3 АТФ. (Ленинджер А., Скулачев В. П. )
Слайд 6
Механизм работы электронтранспортной цепи
Процессы окисления и образования АТФ из АДФ и
фосфорной кислоты т.е. фосфорилирования протекают в митохондриях. Внутренняя мембрана образует множество складок - крист. Пространство органиченное внутренней мембраной - матриксом. Пространство между внутренней и наружной мембранами называется межмембранным.
Такая молекула содержит в себе три макроэргических связи. Макроэргической или богатой энергией называют химическую связь, при разрыве которой высвобождается более 4 ккал/моль. При гидролитическом расщеплении АТФ до АДФ и фосфорной кислоты высвобождается 7,3 ккал/моль. Ровно столько же тратится для образования АТФ из АДФ и остатка фосфорной кислоты и это один из основных путей запасания энергии в организме.
В процессе транспорта электронов по дыхательной цепи высвобождается энергия, которая тратится на присоединение остатка фосфорной кислоты к АДФ с образованием одной молекулы АТФ и одной молекулы воды. В процессе переноса одной пары электронов по дыхательной цепи высвобождается и запасается в виде трех молекул АТФ 21,3 ккал/моль. Это составляет около 40 % высвободившейся при электронном транспорте энергии.
Такой способ запасания энергии в клетке называется окислительным фосфорилированием или сопряженным фосфорилированием.
Молекулярные механизмы этого процесса наиболее полно объясняет хемоосмотическая теория Митчелла, выдвинутая в 1961 году. (Ленинджер А. Скулачев В. П. )

Слайд 7Метаболизм углеводов
У всех млекопитающих глюкоза в клетках превращается в пируват и
лактат по метаболическому пути, который называется гликолизом. Для вступления на этот путь необходимо предварительное фосфорилирование. Гликолиз может протекать в отсутствие кислорода (анаэробно), если конечным продуктом является лактат. Ткани, которые потребляют кислород (аэробные условия), способны осуществлять превращение пирувата в ацетил-СоА, который далее может вступать в цикл лимонной кислоты; в этом цикле ацетил-СоА полностью окисляется до большая часть потенциальной свободной энергии процесса запасается в форме АТР в результате окислительного фосфорилирования. (Марри Р., Греннер Д., Мейес П., Родуэлл В.)
Рис. 2 Общая схема метаболизма углеводов с указанием главных конечных продуктов.
Слайд 8Метаболизм углеводов
Таким образом, глюкоза служит главным видом топлива для многих тканей,
однако она (а также ее метаболиты) участвует и в других процессах.
Глюкоза превращается в полимер гликоген, который
запасается в ряде тканей, в особенности в скелетных мышцах и в печени.
Субстрат пентозофосфатного пути является одним из промежуточных продуктов гликолиза. Этот путь служит источником восстановительных эквивалентов используемых в процессах биосинтеза, например в биосинтезе жирных кислот; кроме того, он является источником рибозы, необходимой для синтеза нуклеотидов и нуклеиновых кислот.
Трнозофосфат, образующийся на одной из стадий гликолиза, является источником глицерола, используемого в синтезе ацилглицеролов (жиров).
Пируват и ряд промежуточных соединений цикла лимонной кислоты—это источники углеродных скелетов, используемых в синтезе аминокислот, а ацетил-СоА служит основным строительным блоком в синтезе длинноцепочечных жирных кислот и холестерола—предшественника всех синтезируемых в организме стероидов (Марри Р., Греннер Д., Мейес П., Родуэлл В.).
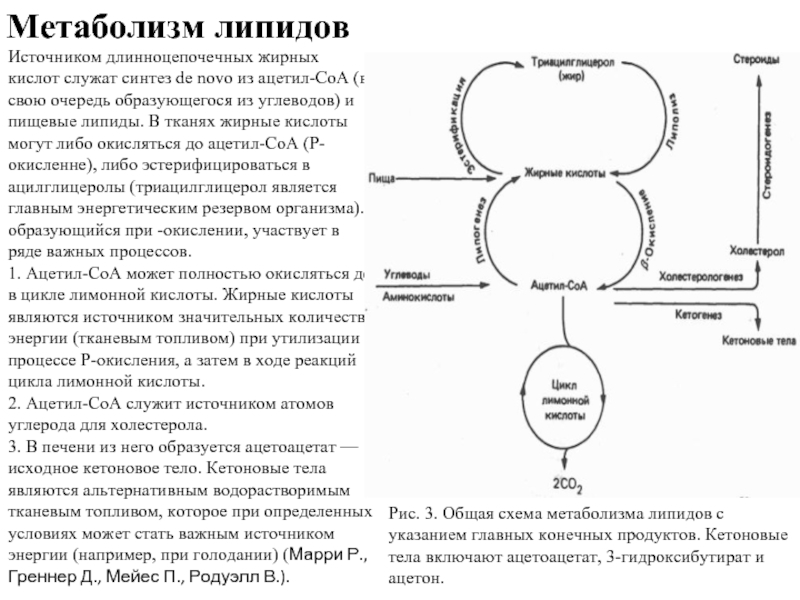
Слайд 9Метаболизм липидов
Источником длинноцепочечных жирных кислот служат синтез de novo из ацетил-СоА
(в свою очередь образующегося из углеводов) и пищевые липиды. В тканях жирные кислоты могут либо окисляться до ацетил-СоА (Р-окисленне), либо эстерифицироваться в ацилглицеролы (триацилглицерол является главным энергетическим резервом организма). образующийся при -окислении, участвует в ряде важных процессов.
1. Ацетил-СоА может полностью окисляться до в цикле лимонной кислоты. Жирные кислоты являются источником значительных количеств энергии (тканевым топливом) при утилизации в процессе Р-окисления, а затем в ходе реакций цикла лимонной кислоты.
2. Ацетил-СоА служит источником атомов углерода для холестерола.
3. В печени из него образуется ацетоацетат — исходное кетоновое тело. Кетоновые тела являются альтернативным водорастворимым тканевым топливом, которое при определенных условиях может стать важным источником энергии (например, при голодании) (Марри Р., Греннер Д., Мейес П., Родуэлл В.).
Рис. 3. Общая схема метаболизма липидов с указанием главных конечных продуктов. Кетоновые тела включают ацетоацетат, 3-гидроксибутират и ацетон.
Слайд 10Метаболизм аминокислот
Аминокислоты необходимы для синтеза белков. Некоторые из них должны обязательно
поступать с пищей (незаменимые аминокислоты), поскольку ткани не способны их синтезировать. Остальные аминокислоты (заменимые) также поступают с пищей, но могут образовываться и из промежуточных метаболитов путем переаминировання, т. е. переноса аминогрупп от других аминокислот, присутствующих в избыточном количестве. После дезаминирования избыточный аминный азот удаляется в составе мочевины; остающийся после переаминировання углеродный скелет либо окисляется до в цикле лимонной кислоты, либо превращается в глюкозу (глюконеогенез) или кетоновые тела.
Помимо использования в синтезе белков аминокислоты служат предшественниками ряда важных соединений — пуринов, пиримидинов, гормонов (например, адреналина и тироксина) (Марри Р., Греннер Д., Мейес П., Родуэлл В.).
Рис. 4. Общая схема метаболизма аминокислот с указанием главных конечных продуктов.
Слайд 11Список литературы
Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия
человека: В 2-х томах. Т. 1. Пер. с англ.: — М.: Мир, 1993. - 384 с
Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.: Мир, 1974, 956 с.;
Скулачев В. П. Энергетика биологических мембран // М.: Наука, 1989, 565 с.;
Карякин А. В., Арчаков А. И. Межмембранный перенос электронов // Успехи современной биологии, 1981, Т. 91, вып. 1, с. 74-89;