доктор медицинских наук, профессор
Цапок Петр Иванович
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Конечные продукты азотистого обмена. Биосинтез мочевины презентация
Содержание
- 1. Конечные продукты азотистого обмена. Биосинтез мочевины
- 2. КОНЕЧНЫЕ ПРОДУКТЫ : АММИАК
- 4. ТОКСИЧНОСТЬ АММИАКА Аммиак - NH3 является клеточным
- 5. Токсичность аммиака В опытах на кроликах концентрация
- 6. Нейтр. мол. своб. NH3 легко
- 7. Причины токсичности 2. NH3 + а-КГ +
- 8. Токсичность аммиака Аммиак настолько токсичен, что должен
- 9. Механизмы детоксикации аммиака 1. Синтез глутамина: Глн,
- 10. Механизмы детоксикации аммиака 5.Синтез пурин. и пиримид.
- 11. Восстановительное аминирование Большинство организмов обладает способностью реутилизировать
- 12. Восстановительное аминирование
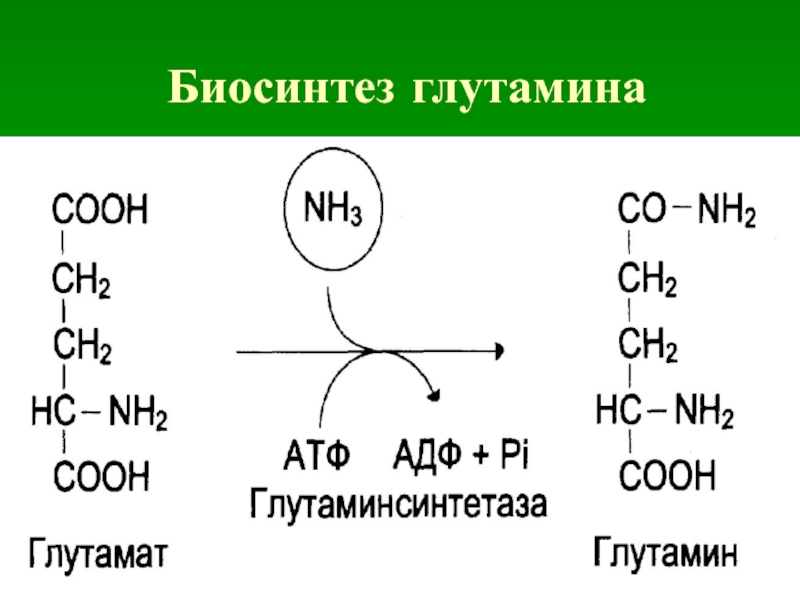
- 13. Биосинтез глутамина
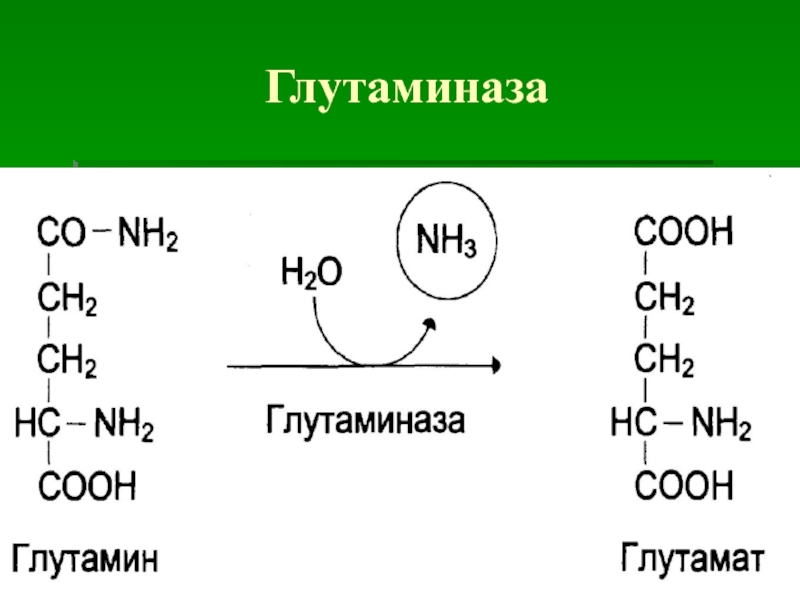
- 14. Глутаминаза
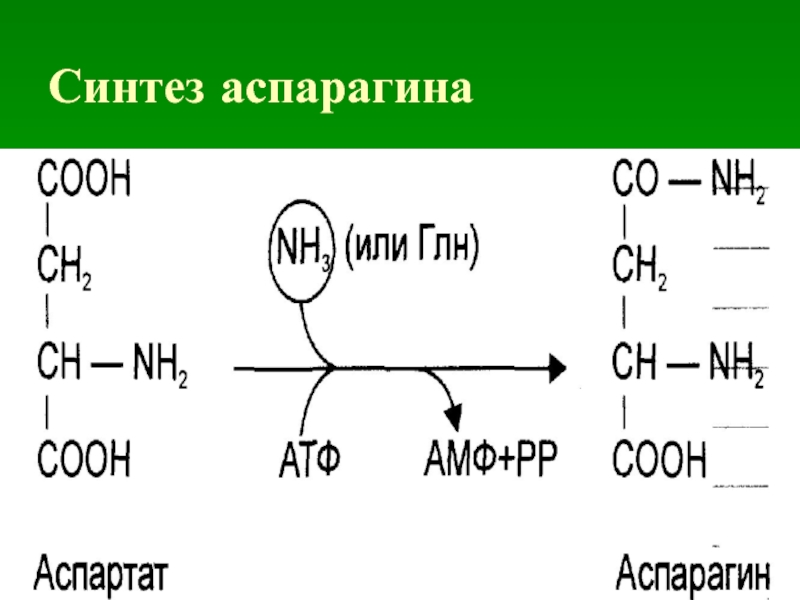
- 17. Синтез аспарагина
- 18. МОЧЕВИНА У человека инактивация NH3
- 19. Синтез мочевины Мочевина
- 20. СТАДИИ СИНТЕЗА МОЧЕВИНЫ Мочевина образуется в результате
- 21. Первая реакция На первой стадии из гидрокарбоната
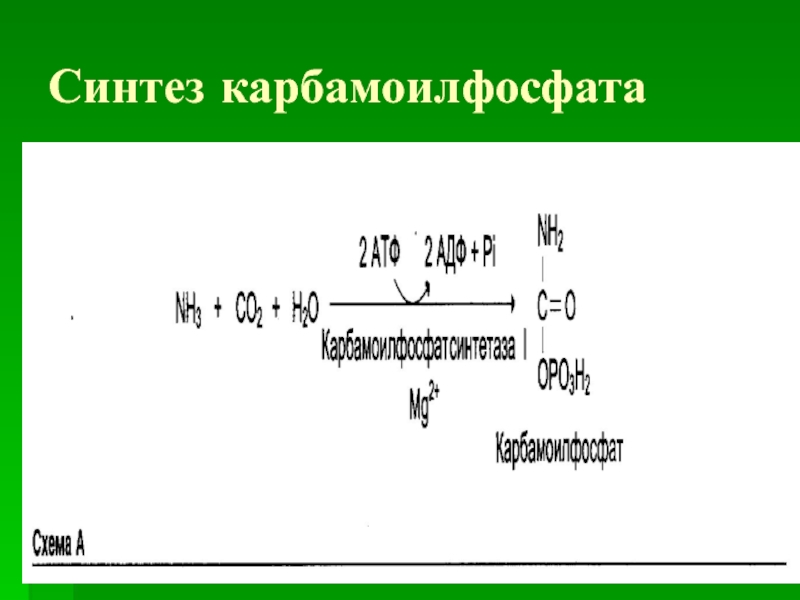
- 22. Синтез карбамоилфосфата
- 23. Вторая стадия Карбамоильный остаток переносится на
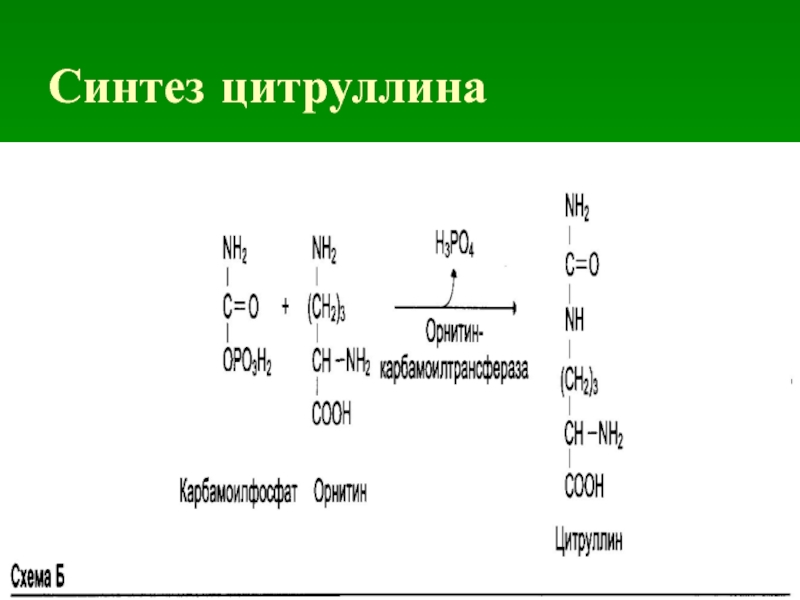
- 24. Синтез цитруллина
- 25. Третья стадия Вторая аминогруппа молекулы мочевины поставляется за счет реакции аспартата с цитруллином.
- 26. Синтез аргининосукцината
- 27. Для обеспечения необратимости реакции дифосфат
- 28. Четвертая стадия
- 29. Пятая стадия из которого в результате
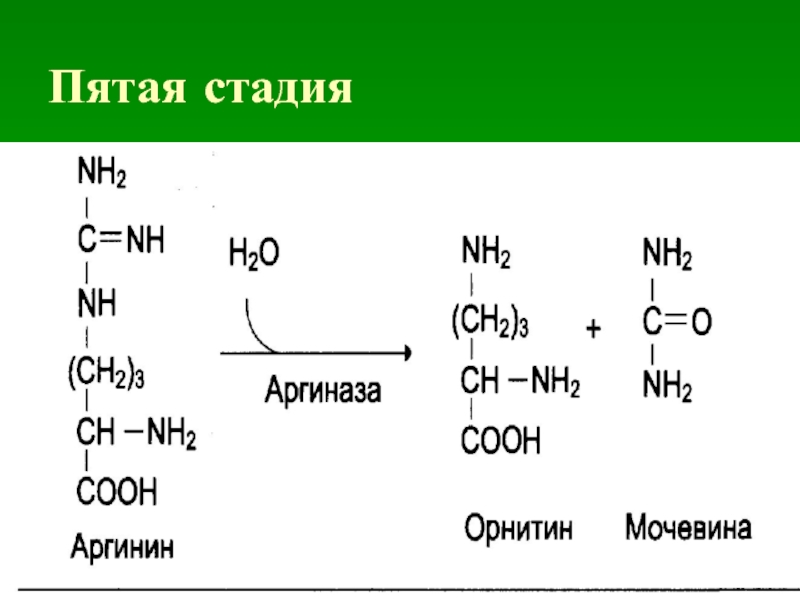
- 30. Пятая стадия
- 32. ВЕЛОСИПЕД КРЕБСА Фумарат, образующийся в цикле мочевины,
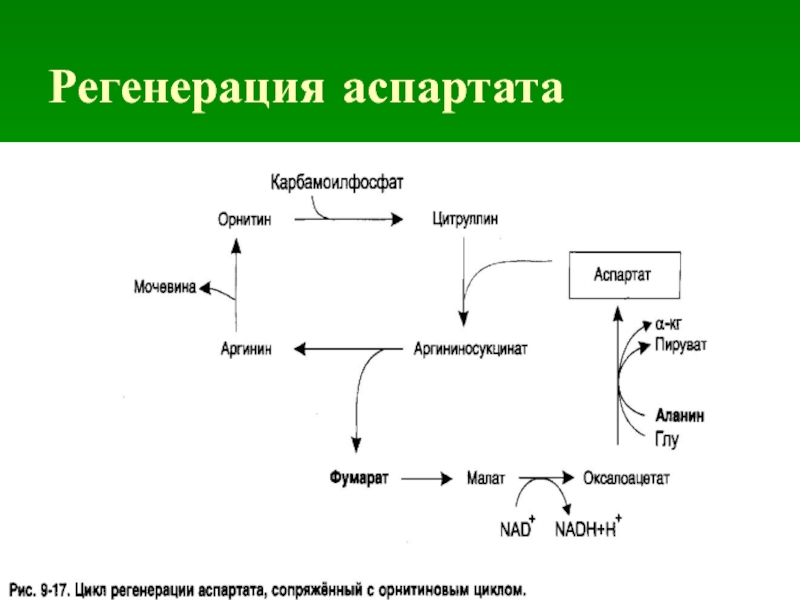
- 33. Регенерация аспартата
- 35. Взаимосвязь цикла мочевинообразования и ЦТК
- 36. ЭНЕРГОЗАВИСИМЫЙ ПРОЦЕСС Биосинтез мочевины требует больших затрат
- 37. КОМПАРТМЕНТАЛИЗАЦИЯ Цикл мочевины протекает исключительно в печени.
- 38. АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ СИНТЕЗА МОЧЕВИНЫ Скорость
- 39. Наследственные нарушения орнитинового цикла и их симптомы
- 41. Включение безазотистого остатка АК в ЦТК
- 42. Пути биосинтеза заменимых АК
- 43. Глюкозо-аланиновый цикл
Слайд 1Кировская государственная медицинская академия
Кафедра химии
Лекция:
КОНЕЧНЫЕ ПРОДУКТЫ АЗОТИСТОГО ОБМЕНА.
БИОСИНТЕЗ МОЧЕВИНЫ
Зав. кафедрой:
Слайд 2 КОНЕЧНЫЕ ПРОДУКТЫ : АММИАК
Деградация аминокислот происходит преимущественно в печени.
При этом освобождается аммиак. Значительные количества аммиака образуются при распаде пуринов и пиримидинов.
Слайд 4ТОКСИЧНОСТЬ АММИАКА
Аммиак - NH3 является клеточным ядом. При высоких концентрациях он
повреждает главным образом нервные клетки (гепатаргическая кома).
В норме распад 70 г АК в сутки ведет к концентрации NH3 в крови 60 мкмоль/л.
В норме распад 70 г АК в сутки ведет к концентрации NH3 в крови 60 мкмоль/л.
Слайд 5Токсичность аммиака
В опытах на кроликах концентрация
NH3 3 ммоль/л
вызывала смерть!
Причины токсичности:
1. при рН крови в виде NH4+, проникает через плазм. и МХ мембраны с большим трудом.
Причины токсичности:
1. при рН крови в виде NH4+, проникает через плазм. и МХ мембраны с большим трудом.
Слайд 6
Нейтр. мол. своб. NH3 легко проходят эти мембраны. При
рН 7,4 только 1% NH3 от общего количества аммиака проникает в клетки мозга и МХ.
Слайд 7Причины токсичности
2. NH3 + а-КГ + НАДФН2 -?
Глу + НАДФ+ Н2О
Отток альфа- КГ из фонда ЦТК и как следствие – снижение скорости окисления глюкозы
Отток альфа- КГ из фонда ЦТК и как следствие – снижение скорости окисления глюкозы
Слайд 8Токсичность аммиака
Аммиак настолько токсичен, что должен быть немедленно удален посредством экскреторного
механизма, либо путем включения в другое азотсодержащее соединение - менее токсичное.
Слайд 9Механизмы детоксикации аммиака
1. Синтез глутамина: Глн, аспарагина: Асн.
2. Синтез мочевины.
3. Аминирование
а-КГ --> Глу.
4. Амидирование белков.
4. Амидирование белков.
Слайд 10Механизмы детоксикации аммиака
5.Синтез пурин. и пиримид. структур.
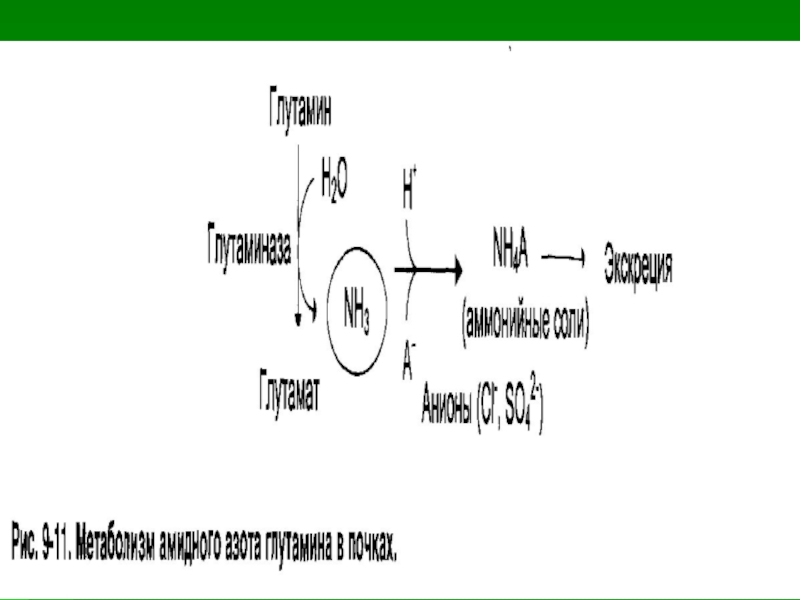
6. Нейтрализация в почках кислотами
и выделение с мочой аммонийных солей.
Слайд 11Восстановительное аминирование
Большинство организмов обладает способностью реутилизировать аммиак за счет реакции, катализируемой
глутаматдегидрогеназой.
А-Кетоглутарат + NH3 + НАДФН.Н+ ?
Глутамат + НАДФ+.
Это восстановительное аминирование.
А-Кетоглутарат + NH3 + НАДФН.Н+ ?
Глутамат + НАДФ+.
Это восстановительное аминирование.
Слайд 18 МОЧЕВИНА
У человека инактивация NH3 осуществляется за счет синтеза мочевины,
часть NH3 выводится почками.
Слайд 19Синтез мочевины
Мочевина - это нейтральное и нетоксичное соединение. Молекула
мочевины может проходить через мембраны, из-за ее хорошей растворимости в воде мочевина легко переносится кровью и выводится с мочой.
Слайд 20СТАДИИ СИНТЕЗА МОЧЕВИНЫ
Мочевина образуется в результате циклической последовательности реакций, протекающих в
печени.
Оба атома азота берутся из свободного аммиака и за счет дезаминирования аспартата, карбонильная группа — из гидрокарбоната.
Оба атома азота берутся из свободного аммиака и за счет дезаминирования аспартата, карбонильная группа — из гидрокарбоната.
Слайд 21Первая реакция
На первой стадии из гидрокарбоната (НСО3-) и аммиака с потреблением
2 молекул АТФ образуется карбамоилфосфат.
Слайд 23 Вторая стадия
Карбамоильный остаток переносится на орнитин с образованием цитруллина. Вновь
необходима энергия в форме АТФ, который при этом расщепляется на АМФ и дифосфат.
Слайд 25Третья стадия
Вторая аминогруппа молекулы мочевины поставляется за счет реакции аспартата с
цитруллином.
Слайд 27
Для обеспечения необратимости реакции дифосфат гидролизуется полностью. Отщепление фумарата от
аргининосукцината приводит к аргинину,
Слайд 29Пятая стадия
из которого в результате гидролиза образуется мочевина. Остающийся орнитин
вновь включается в цикл мочевины.
Слайд 32ВЕЛОСИПЕД КРЕБСА
Фумарат, образующийся в цикле мочевины, может в результате двух стадий
цитратного цикла [6, 7] через малат переходить в оксалоацетат, который за счет трансаминирования [9] далее прекращается в аспартат. Последний также вновь вовлекается в цикл мочевины.
Слайд 36ЭНЕРГОЗАВИСИМЫЙ ПРОЦЕСС
Биосинтез мочевины требует больших затрат энергии. Энергия поставляется за счет
расщепления четырех высокоэнергетических связей: двух при синтезе карбамоилфосфата и двух (!) при образовании аргининосукцината (АТФ → АМФ + PPi, РРi → 2Pi).
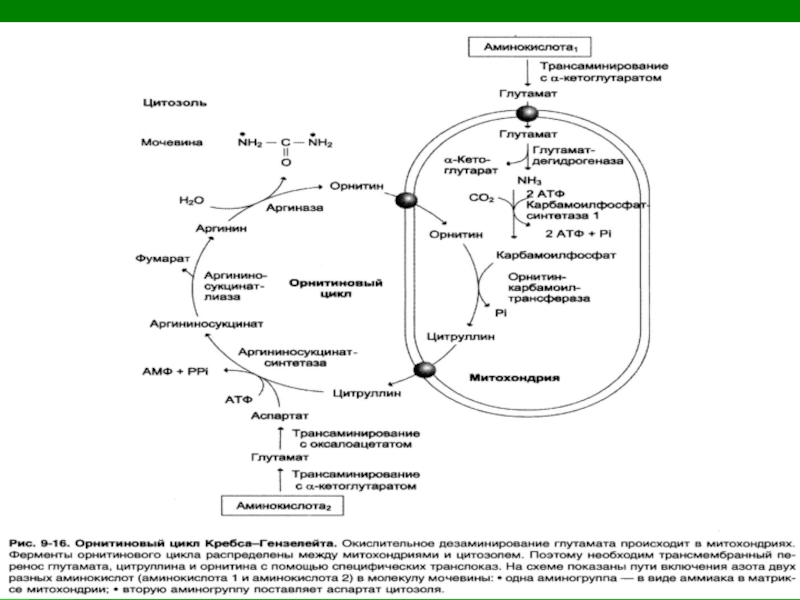
Слайд 37КОМПАРТМЕНТАЛИЗАЦИЯ
Цикл мочевины протекает исключительно в печени. Он разделен на два компартмента:
митохондрии и цитоплазму. Прохождение через мембрану промежуточных соединений цитруллина и орнитина возможно только с помощью переносчиков.
Слайд 38АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ СИНТЕЗА МОЧЕВИНЫ
Скорость синтеза мочевины определяется первой реакцией
цикла. Карбамоилфосфатсинтаза активна только в присутствии N-ацетилглутамата. Уровень аргинина и энергоснабжение сильно зависят от концентрации этого аллостерического эффектора.























![ВЕЛОСИПЕД КРЕБСАФумарат, образующийся в цикле мочевины, может в результате двух стадий цитратного цикла [6, 7]](/img/tmb/4/321182/a1a8c4e5b2149da88d21a0d08209ebd8-800x.jpg)