- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химический состав клетки презентация
Содержание
- 1. Химический состав клетки
- 2. По количественному содержанию в клетке все химические
- 3. Макроэлементы составляют основную массу вещества клетка на
- 4. Микроэлементы – преимущественно ионы металлов (кобальта, меди,
- 5. Химические соединения в клетке Органические Неорганические
- 6. Неорганические вещества Вода Содержание воды в
- 7. Роль воды в клетке определяется ее свойствами:
- 8. Обладает высокой удельной теплоемкостью. Высокая
- 9. Биологическая роль воды в клетке Универсальный растворитель
- 10. Обладает высокой удельной теплоемкостью – поглощает большое
- 11. Биологическая роль воды в клетке Метаболическая –
- 12. Минеральные соли Анионы фосфорной кислоты создают фосфатную
- 13. Липиды
- 14. Органические вещества клетки Полимер – это
- 15. – это биополимеры, мономерами которых являются аминокислоты.
- 16. Сокращенное название Аминокислота Ала
- 17. Аминокислоты По способности человека синтезировать аминокислоты
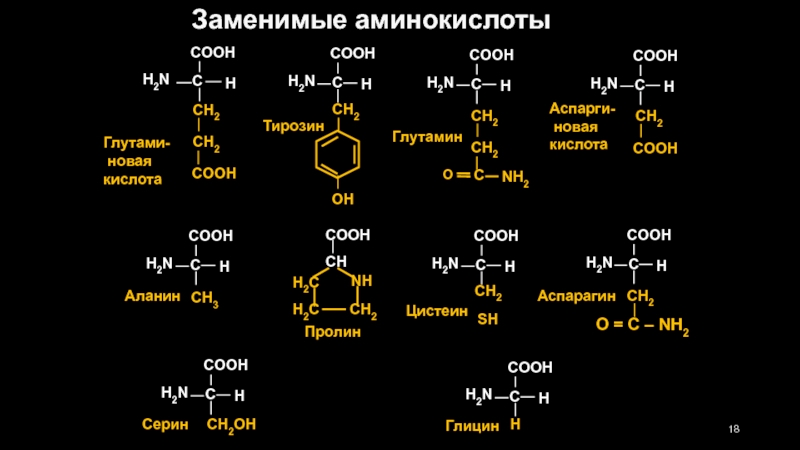
- 18. Заменимые аминокислоты
- 19. Полузаменимые аминокислоты Для детей они являются незаменимыми
- 20. Незаменимые аминокислоты
- 21. карбоксильная группа H +
- 22. Различают четыре уровня пространственной организации белков Строго
- 23. Вторичная структура белка – полипептидная цепь,
- 24. Третичная структура белка Третичная структура – сворачивание
- 25. Четвертичная структура белка Взаимное расположение в пространстве
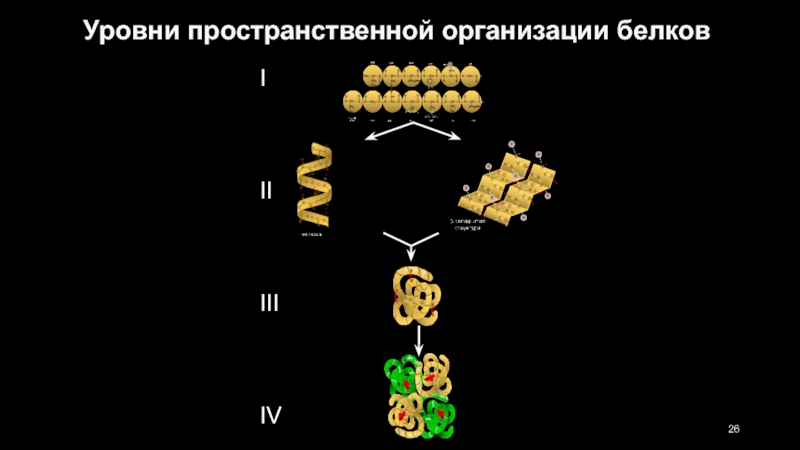
- 26. I II
- 27. Функции белков ферментативная: выступают в качестве
- 28. защитная: при попадании инородных тел
- 29. Углеводы – вещества, состоящие из углерода,
- 30. Моносахариды – в зависимости от числа углеродных
- 31. Олигосахариды – вещества, образованные несколькими моносахаридами (до
- 32. Полисахариды – образуются путем соединения многих моносахаридов
- 33. Функции углеводов энергетическая: при окислении 1г
- 34. Молекулы жиров образованы остатками трехатомного спирта (глицерина)
- 35. теплоизоляционная: у некоторых животных (тюлени, киты)
- 36. АТФ – аденозинтрифосфорная кислота АТФ
Слайд 2По количественному содержанию в клетке все химические элементы делят на 3
Химический состав клетки
Клетки состоят из тех же химических элементов, которые образуют неживую природу.
Из 112 химических элементов периодической системы
Д. И. Менделеева в клетках живых организмов обнаружено примерно 25.
Слайд 3Макроэлементы составляют основную массу вещества клетка на их долю приходится около
кислород – 65%
углерод – 18%
водород – 10%
азот – 3%
И еще 1% приходится на долю 8 элементов:
кальций, фосфор,
хлор, калий, сера,
натрий, магний,
железо
Содержатся в десятых или сотых долях процента
Химический состав клетки.
Макроэлементы
Органогенные элементы – входят в состав белков, нуклеиновых кислот, липидов, углеводов, воды
Слайд 4Микроэлементы – преимущественно ионы металлов (кобальта, меди, цинка и др.) и
и др.). Они содержатся в количествах от 0,001% до 0,000001%.
Входят в состав гормонов, ферментов, витаминов.
Например, цинк – необходимый элемент ДНК- и РНК- полимераз, гормона инсулина. Йод входит в состав тироксина – гормона щитовидной железы.
Ультрамикроэлементы – концентрация ниже 0,000001 %. К ним относят золото, уран, ртуть, селен и др.
Физиологическая роль большинства этих элементов в живых организмах не установлена
Химический состав клетки
Слайд 5Химические соединения в клетке
Органические
Неорганические
Белки
Жиры
Углеводы
Нуклеиновые
кислоты
АТФ
Вода
Минеральные соли
Слайд 6Неорганические вещества
Вода
Содержание воды в организмах составляет 60 – 90%.
Играет
В клетке находится в двух формах: свободной и связанной. Свободная (95% всей воды) используется как растворитель и как среда протоплазмы. Связанная вода (4-5%) благодаря своей дипольности (атомы водорода имеет частично положительный заряд, а атом кислорода – частично отрицательный) связана, как с положительно, так и с отрицательно заряженными белками. В результате образуется водная оболочка вокруг белков, которая препятствует склеиванию их друг с другом.
Слайд 7Роль воды в клетке определяется ее свойствами:
малые размеры молекул воды,
полярность молекул,
способность соединяться
друг с другом
водородными связями.
Неорганические вещества. Вода
Слайд 8Обладает высокой удельной теплоемкостью.
Высокая теплопроводность – обусловленная малыми размерами ее
Универсальный растворитель
Биологическая роль воды в клетке
Метаболическая
Слайд 9Биологическая роль воды в клетке
Универсальный растворитель
для полярных веществ: солей, сахаров, кислот
С неполярными веществами (гидрофобные – жиры) вода не образует Н-связи, а следовательно, не растворяет и не смешивается
с ними.
Структурная – цитоплазма клеток содержит 60%-95% воды.
обуславливает осмос и тургорное давление, т.е. физические свойства клетки;
Слайд 10Обладает высокой удельной теплоемкостью – поглощает большое количество тепловой энергии при
собственной температуры.
Обладает наивысшей теплоемкостью из всех известных жидкостей. При повышении температуры окружающей среды часть тепловой энергии затрачивается на разрыв водородных связей между молекулами воды, при этом поглощается тепло. При охлаждении вновь возникают водородные связи между молекулами воды и выделяется тепло. Этим обусловлена её способность обеспечивать терморегуляцию клетки.
Высокая теплопроводность – обусловленная малыми размерами ее молекул.
Биологическая роль воды в клетке
Слайд 11Биологическая роль воды в клетке
Метаболическая – служит средой протекания химических реакций,
В процессе фотосинтеза вода является источником электронов и атомов водорода.
Она же и источник свободного кислорода:
6H2O + 6CO2 = C6H12O6 + 6O2
Слайд 12Минеральные соли
Анионы фосфорной кислоты создают фосфатную буферную систему, поддерживающую рН внутриклеточной
Угольная кислота и ее анионы создают бикарбонатную буферную систему, которая поддерживает рН внеклеточной среды (плазма крови) на уровне 7,4.
Минеральные соли
Состав
Роль в клетке
В диссоциирован-ном состоянии:
- катионы
Состоят из катионов и анионов
С разностью концентрации ионов по разные стороны мембраны связывают активный перенос веществ через мембрану.
Обеспечивают постоянство осмотического давления в клетке.
В связанном с органическими веществами состоянием
Обеспечивают функциональную активность ферментов и др. макромолекул (например, анионы фосфорной кислоты входят в состав фосфолипидов, АТФ, нуклеотидов и др.; ион Fе2+ входит в состав гемоглобина, магний в состав хлорофилла и т. д.).
Слайд 13
Липиды
Нуклеиновые кислоты
Углеводы
АТФ
Белки
Органические вещества
Органические соединения – это соединения углерода
Слайд 14Органические вещества клетки
Полимер – это вещество с высокой молекулярной массой,
молекула которого состоит из большого количества
повторяющихся единиц – мономеров.
Биологические полимеры – органические соединения,
входящие в состав клеток живых организмов.
Биополимеры Мономеры органических веществ
Нуклеотиды
Основные органические соединения клетки
Полисахариды(целлюлоза,
гликоген, крахмал)
Спирт, глицерин и жирные кислоты
Липиды и липоиды
Аминокислоты
Белки
Нуклеиновые кислоты
Моносахариды (глюкоза, фруктоза)
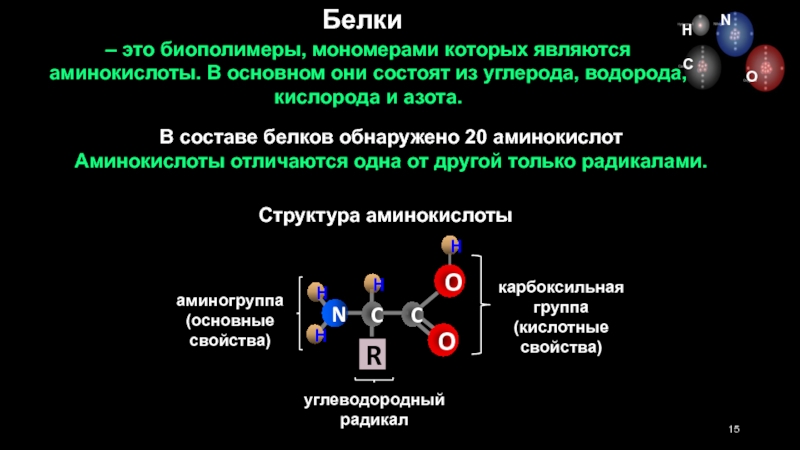
Слайд 15– это биополимеры, мономерами которых являются аминокислоты. В основном они состоят
Структура аминокислоты
аминогруппа
(основные свойства)
углеводородный
радикал
карбоксильная группа
(кислотные свойства)
В составе белков обнаружено 20 аминокислот
Аминокислоты отличаются одна от другой только радикалами.
Белки
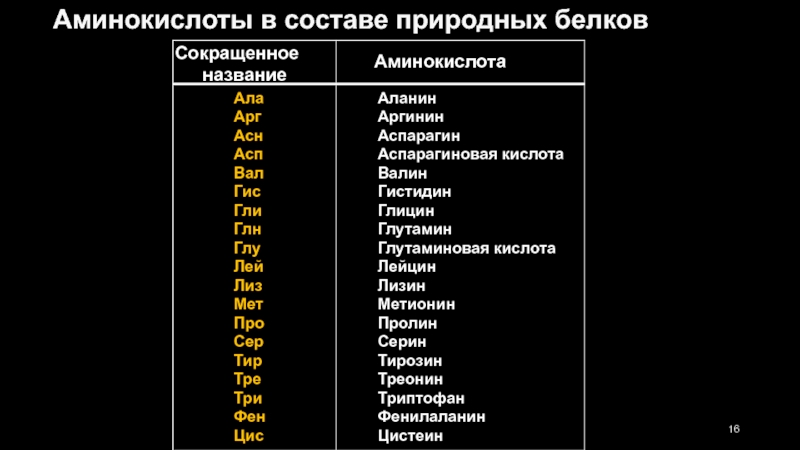
Слайд 16Сокращенное
название
Аминокислота
Ала
Арг
Асн
Асп
Вал
Гис
Гли
Глн
Глу
Лей
Лиз
Мет
Про
Сер
Тир
Тре
Три
Фен
Цис
Аланин
Аргинин
Аспарагин
Аспарагиновая кислота
Валин
Гистидин
Глицин
Глутамин
Глутаминовая кислота
Лейцин
Лизин
Метионин
Пролин
Серин
Тирозин
Треонин
Триптофан
Фенилаланин
Цистеин
Аминокислоты в составе природных белков
Слайд 17Аминокислоты
По способности человека синтезировать аминокислоты из предшественников, различают:
Заменимые аминокислоты –
глицин, аланин, серин, цистеин, тирозин, аспарагин, глутамин, аспарагиновая и глутаминовые кислоты.
Незаменимые аминокислоты –
не синтезируются в организме человека. Необходимо их поступление
в организм с пищей:
валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин.
Полузаменимые аминокислоты – аргинин, гистидин.
Образуются в недостаточном количестве.
Их недостаток должен восполняться с белковой пищей.
Слайд 21карбоксильная
группа
H
+
аминогруппа
аминогруппа
карбоксильная
группа
пептидная
связь
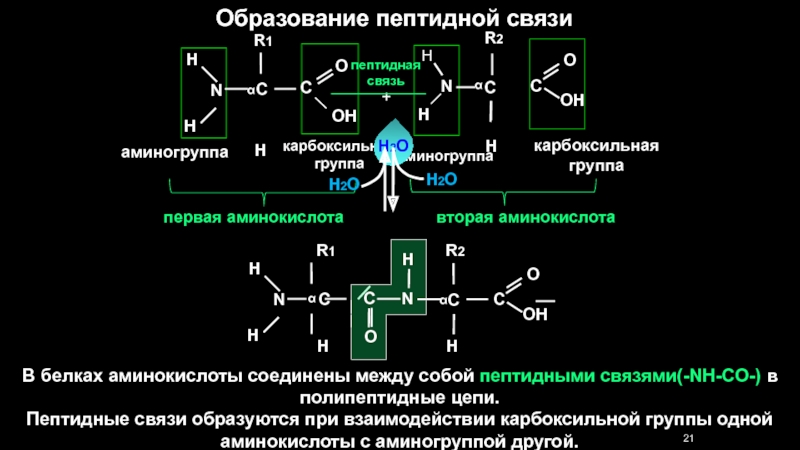
Образование пептидной связи
В белках аминокислоты соединены между собой пептидными связями(-NH-CO-) в
Пептидные связи образуются при взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой.
первая аминокислота вторая аминокислота
C
OH
O
N
H
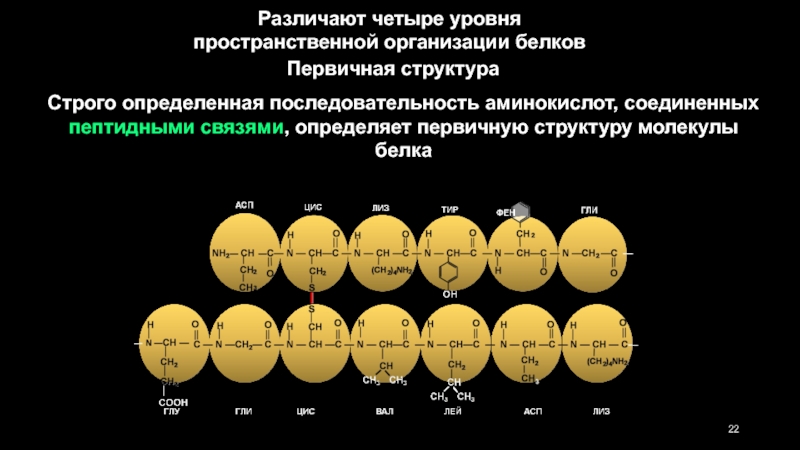
Слайд 22Различают четыре уровня пространственной организации белков
Строго определенная последовательность аминокислот, соединенных пептидными
Первичная структура
Слайд 23
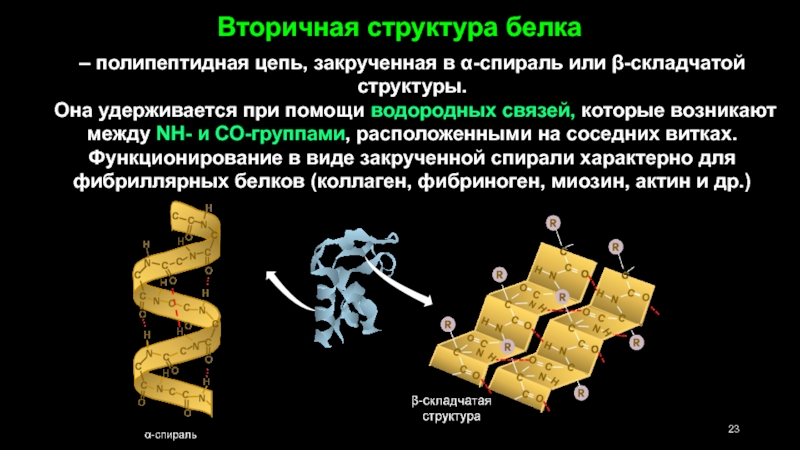
Вторичная структура белка
– полипептидная цепь, закрученная в α-спираль или β-складчатой структуры.
Она удерживается при помощи водородных связей, которые возникают между NH- и СО-группами, расположенными на соседних витках.
Функционирование в виде закрученной спирали характерно для фибриллярных белков (коллаген, фибриноген, миозин, актин и др.)
Слайд 24Третичная структура белка
Третичная структура – сворачивание спирали в сложную конфигурацию –
Многие белковые молекулы становятся функционально активными только после приобретения глобулярной (третичной) структуры.
Слайд 25Четвертичная структура белка
Взаимное расположение в пространстве нескольких одинаковых или разных полипептидных
Гемоглобин
в эритроцитах
Слайд 27Функции белков
ферментативная: выступают в качестве биологических
катализаторов,
строительная: белки являются обязательным компонентом всех
клеточных структур;
транспортная: перенос О2, гормонов в теле животных и человека;
двигательная: все виды двигательных реакций обеспечиваются
сократительными белками- актином и миозином;
Слайд 28
защитная: при попадании инородных тел в организме
энергетическая: при недостатке углевода и жиров могут окислиться
молекулы аминокислот (1 г белка-17,6 кДж энергии).
сигнальная: в мембрану встроены особые белки, способные
изменять свою третичную структуру на действие факторов внешней
среды. Так происходит прием сигналов из внешней среды и передача информации в клетку.
Функции белков
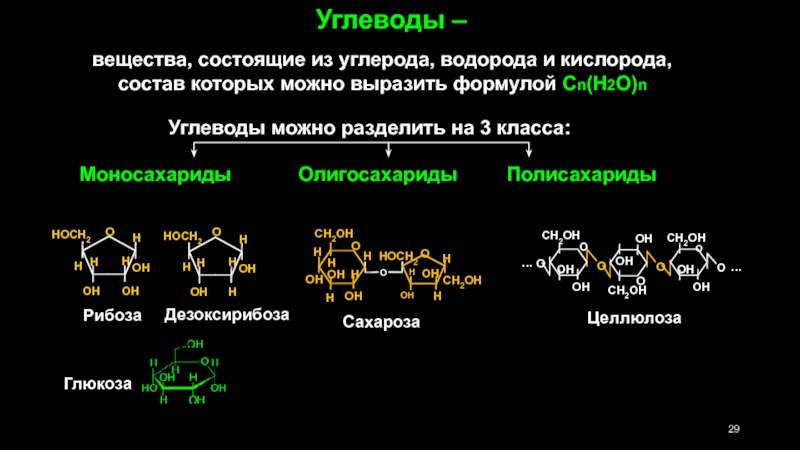
Слайд 29Углеводы –
вещества, состоящие из углерода, водорода и кислорода, состав которых
Углеводы можно разделить на 3 класса:
Полисахариды
Олигосахариды
Моносахариды
Целлюлоза
Слайд 30Моносахариды – в зависимости от числа углеродных атомов в их молекуле
Свойства: малые молекулы легко растворяются в воде. Представлены кристаллическими формами, сладкие на вкус.
Углеводы
Слайд 31Олигосахариды – вещества, образованные несколькими моносахаридами (до 10);
Дисахариды – объединяют в
Свойства: растворимы в воде. Кристаллизуются. Сладкий вкус.
Углеводы
Глюкоза + Фруктоза = Сахароза
Глюкоза + Глюкоза = Мальтоза
Глюкоза + Галактоза = Лактоза
Слайд 32Полисахариды – образуются путем соединения многих моносахаридов и имеют формулу (С6H10O5)n.
Наибольшее
Свойства:
макромолекулы нерастворимы или плохо растворимы в воде.
Не кристаллизуются. Не сладкие на вкус.
Углеводы
Целлюлоза
Слайд 33Функции углеводов
энергетическая: при окислении 1г углеводов (до СО2 и Н2О)
высвобождается 17,6 кДж энергии;
запасающая: запасается в клетках печени и мышц в виде гликогена;
строительная: в растительной клетке - прочная основа клеточных стенок (целлюлоза);
защитная: вязкие секреты (слизи) выделяемые различными
железами, богаты углеводами и их производными (гликопротеиды). Защищают стенки внутренних органов (пищевод, кишечник, желудок, бронхи) от механических повреждений и проникновения микроорганизмов;
рецепторная: входят в состав воспринимающей части
клеточных рецепторов.
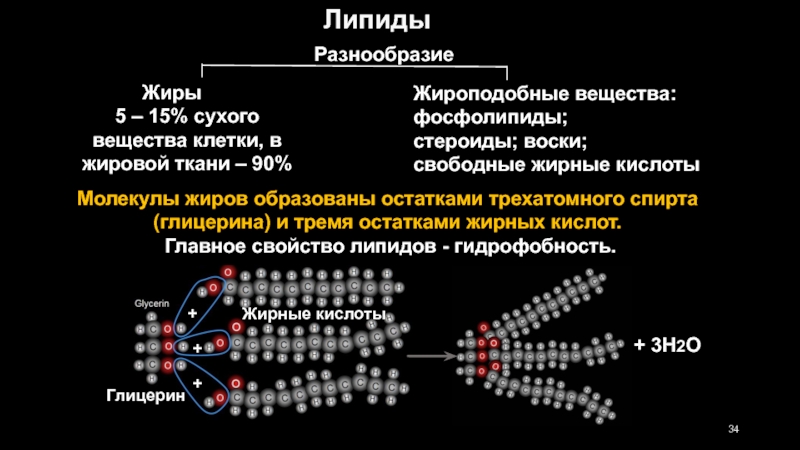
Слайд 34Молекулы жиров образованы остатками трехатомного спирта (глицерина) и тремя остатками жирных
Главное свойство липидов - гидрофобность.
Липиды
Разнообразие
Жиры
5 – 15% сухого
вещества клетки, в жировой ткани – 90%
Жироподобные вещества:
фосфолипиды;
стероиды; воски;
свободные жирные кислоты
Слайд 35 теплоизоляционная: у некоторых животных (тюлени, киты) он откладывается
запасающая: накапливаются в жировой ткани животных, в плодах и
семенах растений;
энергетическая: при полном расщеплении 1г жира выделяется 39 кДж энергии;
структурная: фосфолипиды служат составной частью клеточных мембран;
регуляторная: многие гормоны (например, коры надпочечников, половые) являются производными липидов.
Функции липидов
Слайд 36
АТФ – аденозинтрифосфорная кислота
АТФ – макроэргическое соединение, содержащее химические связи, при
Аденин
Рибоза
~
~
+
H3PO4
OH
O
АТФ + H2O → АДФ + H3PO4 + энергия (40кДж/моль)