- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристика іонізуючих випромінювань і взаємодія їх із речовиною презентация
Содержание
- 1. Характеристика іонізуючих випромінювань і взаємодія їх із речовиною
- 2. У сучасному уявленні атом складається з
- 3. Маса атома вимірюється в атомних одиницях маси,
- 4. Співвідношення Енштейна Е=mc Е – енергія, m
- 5. Процес передавання енергії ЕМВ 1. фотоелектричний ефект
- 6. Атоми, що мають надлишок енергії, називаються збудженими,
- 7. Атом без одного чи кількох електронів називається
- 8. Радіоактивні ізотопи - це атоми одного
- 9. Радіоактивні речовини – це речовини, до складу
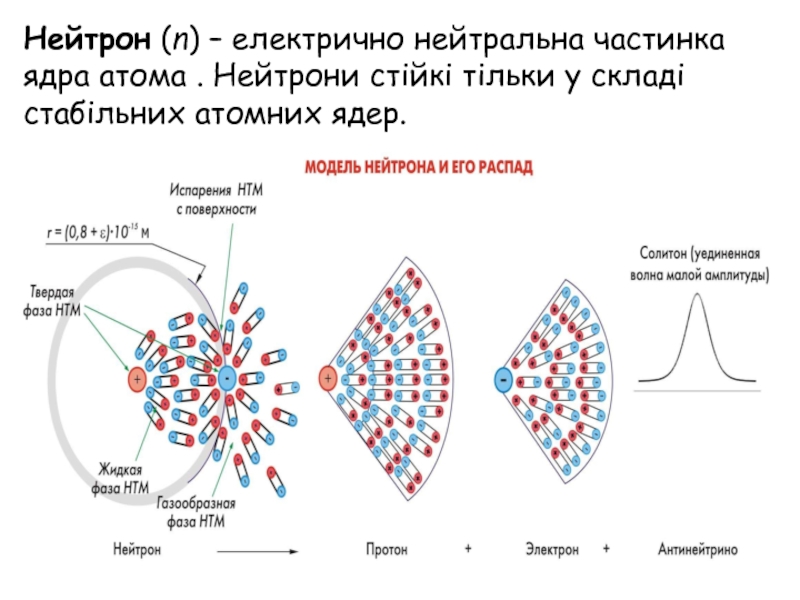
- 10. Нейтрон (n) – електрично нейтральна частинка ядра
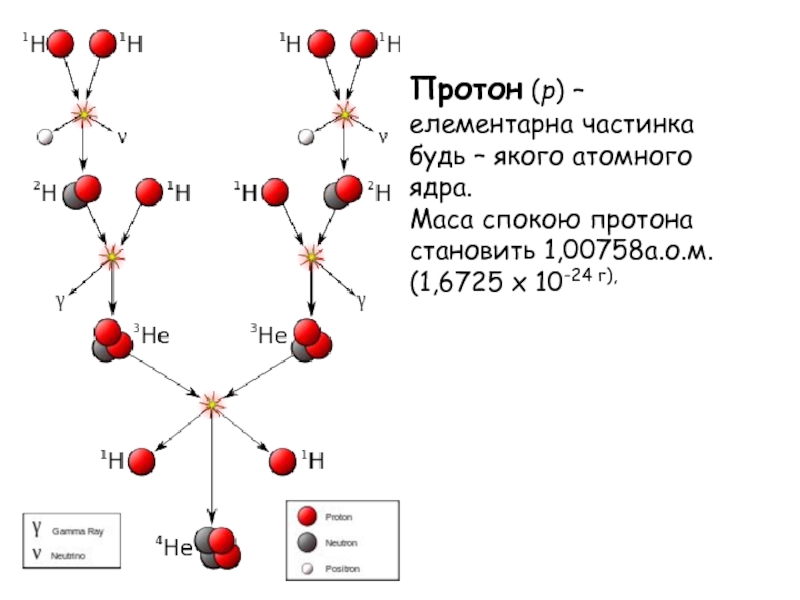
- 11. Протон (р) – елементарна частинка будь –
- 12. Радіонуклід – це нестійкий нуклід, що розпадається.
- 13. поверхнева – Кі/км2; Бк/м2; розп/хв. Зв 1
- 14. ОДИНИЦІ, ЩО ВИКОРИСТОВУЮТЬСЯ ДЛЯ ВИМІРЮВАННЯ ІОНІЗУЮЧОГО ВИПРОМІНЮВАННЯ
- 15. СПІВВІДНОШЕННЯ МІЖ ВЕЛИЧИНАМИ ОДИНИЦЬ РАДІАЦІЇ НАСТУПНЕ:
- 17. БЕТА-РОЗПАД. ЦЕ РАДІОАКТИВНИЙ РОЗПАД ЯДРА АТОМА, ЩО
- 18. Внутрішня конверсія Її суть полягає в
- 19. ЕЛЕКТРОННИЙ ЗАХВАТ. ПЕРЕТВОРЕННЯ ЯДРА МОЖЕ БУТИ ЗДІЙСНЕНО
- 20. ЗАКОН РАДІОАКТИВНОГО РОЗПАДУ
Слайд 1Характеристика іонізуючих випромінювань і взаємодія їх із речовиною
Радіоактивність значною мірою обумовлюється
Термін “атом” означає “неподільний”. Атом – елементарна, доцільна досконало збудована частинка елементу, що зберігає його хімічні властивості
Слайд 2 У сучасному уявленні атом складається з ядра, що має позитивний
Кількість електронів в атомі дорівнює сумарному позитивному заряду ядра, тому атоми нейтральні.
Маса атома вимірюється в атомних одиницях маси, а енергія частинок – в електронвольтах.
Слайд 3Маса атома вимірюється в атомних одиницях маси, а енергія частинок –
1000еВ =кеВ(кілоелектронвольт)
1000 000еВ=меВ(мегаелектронвольт)
Слайд 4Співвідношення Енштейна
Е=mc
Е – енергія, m – маса, c - швидкість світла
Оболонки атому позначають у порядку віддалення їх від ядра: K, L, M, N, O, P, Q
2
Слайд 5Процес передавання енергії ЕМВ
1. фотоелектричний ефект
2. непружне співударяння (ефект Комптона)
3. народження
При наданні електронам зовні додаткової енергії, меншої ніж енергія зв’язку електрона з ядром, вони будуть переходити з одного енергетичного рівня на інший. Такий атом залишається електрично нейтральним, але з надлишком енергії
Слайд 6Атоми, що мають надлишок енергії, називаються збудженими, а перехід електронів з
Коли атом зі збудженого стану переходить у початковий стан спокою, надлишкова енергія виділяється у вигляді квантів
Слайд 7Атом без одного чи кількох електронів називається позитивним іоном, а той,
Слайд 8Радіоактивні ізотопи -
це атоми одного елементу, що мають різну масу,
Радіоактивні ізотопи – нестійкі ізотопи хімічних елементів, які здатні самовільно розпадатися і перетворюватися в ізотопи інших елементів.
Наприклад, елемент калій складається з трьох ізотопів – 39К, 40К, 41К. Перший і третій ізотопу калію є стійкими, а 40К – радіоактивний.
Слайд 9Радіоактивні речовини – це речовини, до складу яких входять радіоактивні ізотопи
Радіоактивні речовини, як правило, випромінюють альфа- (позитивно заряджені атоми гелію) і бета- (електрони) частинки, гама- і гальмівне (електромагнітне високої енергії) випромінювання, нейрони, можуть бути протони і важкі ядра.
Слайд 10Нейтрон (n) – електрично нейтральна частинка ядра атома . Нейтрони стійкі
Слайд 11Протон (р) – елементарна частинка будь – якого атомного ядра. Маса спокою
Слайд 12Радіонуклід – це нестійкий нуклід, що розпадається. Термін “радіонуклід” застосовується для
Слайд 13поверхнева – Кі/км2; Бк/м2; розп/хв. Зв 1 см2
питома – Кі/кг; Бк/кг
об’ємна – Кі/л; Бк/л тощо
Радіоактивність (радіо – випомінюю + активність – дію) – явище спонтанного перетворення атомного ядра ізотопу одного хімічного елементу в ядро ізотопу того ж або іншого елементу і супроводжується іонізуючим випромінюванням.
Основний закон радіоактивного розпаду стверджує, що за одиницю часу розпадається однакова частка ядер, що є в наявності.
Розрізняють три види радіоактивності :
Слайд 14ОДИНИЦІ, ЩО ВИКОРИСТОВУЮТЬСЯ ДЛЯ ВИМІРЮВАННЯ ІОНІЗУЮЧОГО ВИПРОМІНЮВАННЯ НАСТУПНІ:
у системі
несистемні
- активність - Бк (бекерель)
- поглинута доза - Гр. (грей)
- еквівалентна доза - Зв (зіверт)
- експозиційна доза - Кл/кг (кулон на кг)
- ефективна еквівалентна доза – Зв (зіверт)
Кі (кюрі)
Рад (рад)
Бер (бер)
Р (рентген)
Бер.
Слайд 15СПІВВІДНОШЕННЯ МІЖ ВЕЛИЧИНАМИ ОДИНИЦЬ РАДІАЦІЇ НАСТУПНЕ: 1 БК = 1 РОЗПАД/СЕК
Слайд 16 ТИПИ ЯДЕРНИХ ПЕРЕТВОРЕНЬ
Альфа-розпад супроводжується
У процесі альфа – розпаду розрізняють дві стадії:
Слайд 17БЕТА-РОЗПАД. ЦЕ РАДІОАКТИВНИЙ РОЗПАД ЯДРА АТОМА, ЩО СУПРОВОДЖУЄТЬСЯ ВИДІЛЕННЯМ З ЯДРА
При бета – розпаді енергія може бути розподілена між трьома частинками: електроном (або позитроном), антинейтрино (чи нейтрино) і ядром
Слайд 18Внутрішня конверсія
Її суть полягає в тому, що ядро передає енергію
Слайд 19ЕЛЕКТРОННИЙ ЗАХВАТ. ПЕРЕТВОРЕННЯ ЯДРА МОЖЕ БУТИ ЗДІЙСНЕНО ШЛЯХОМ ЕЛЕКТРОННОГО ЗАХВАТУ, КОЛИ
Слайд 20 ЗАКОН РАДІОАКТИВНОГО РОЗПАДУ
фізичний закон, що описує залежність
Існує кілька формулювань закону, наприклад, у вигляді диференціального рівняння:
яке означає, що число розпадів -dN, яке відбулося за короткий інтервал часу dt, пропорційнo числу
атомів у зразку N