- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Генетика микроорганизмов. Основы биотехнологии презентация
Содержание
- 1. Генетика микроорганизмов. Основы биотехнологии
- 2. План лекции Особенности генетики бактерий. Плазмиды, транспозоны,
- 3. Особенности генетики бактерий Хромосома находится в cуперспирализованной
- 4. Модули генома бактерий Хромосома (нуклеоид). Плазмиды. Умеренные бактериофаги. Траспозоны. Is-элементы.
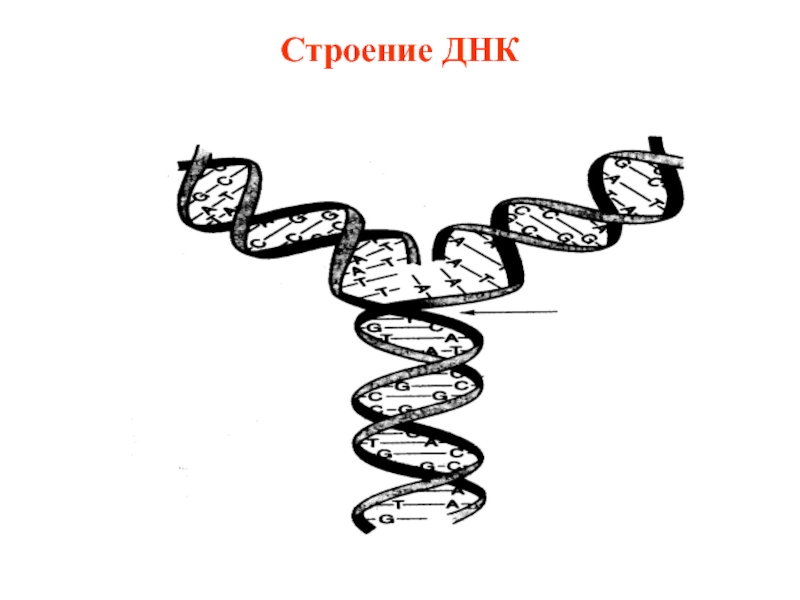
- 5. Строение ДНК
- 6. Плазмиды и свойства бактерий - носителей
- 7. Свойства плазмид Саморегулируемая репликация. Явление поверхностного исключения.
- 8. Транспозоны – участки ДНК, свободно перемещающиеся вдоль
- 9. Is-последовательности – простейший тип мигрирующих элементов (фрагменты
- 10. Формы изменчивости микроорганизмов Фенотипическая (модификации) 1. Кратковременные 2. Длительные Генотипическая 1. Мутации 2. Рекомбинации
- 11. Классификация мутаций 1. По происхождению: 1) спонтанные;
- 12. Классификация рекомбинаций по молекулярному механизму. Гомологичные –
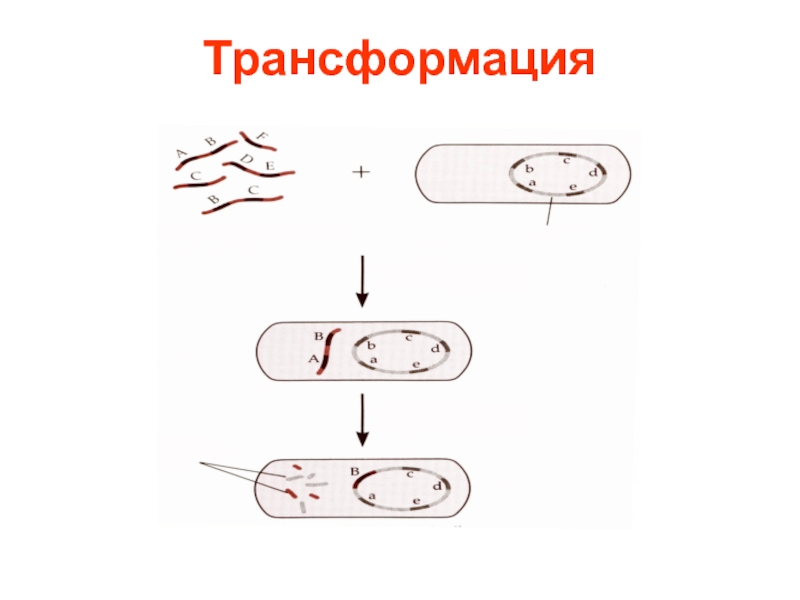
- 13. Трансформация
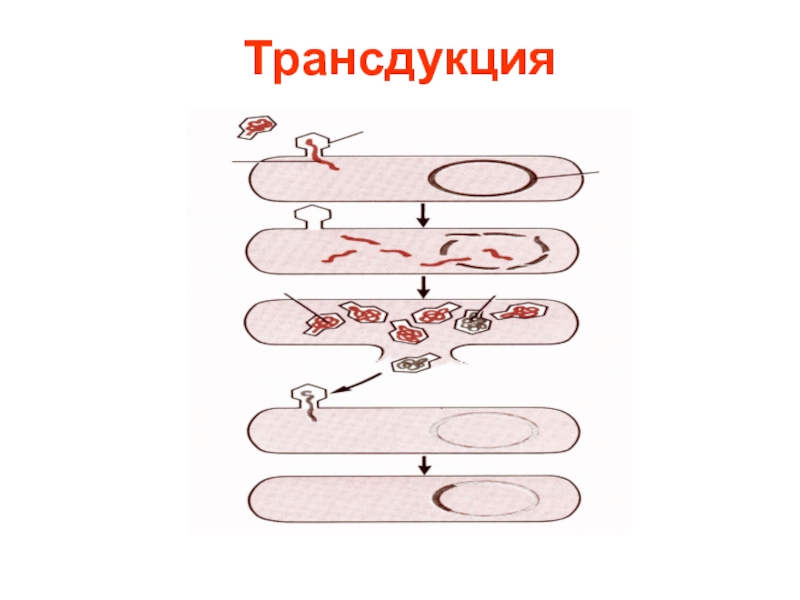
- 14. Трансдукция
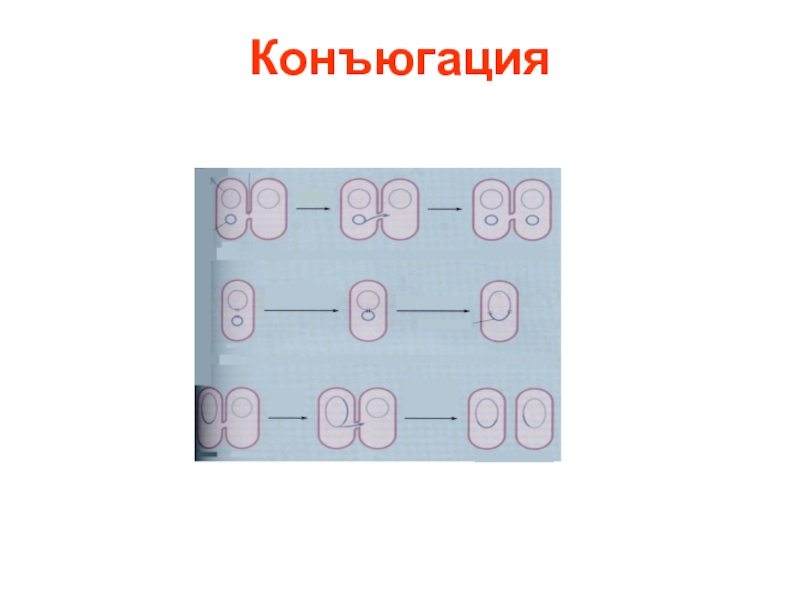
- 15. Конъюгация
- 16. Формы изменчивости вирусов. Генетическая рекомбинация. Генетическая реактивация. Комплементация. Фенотипическое смешивание.
- 17. Генетические методы, применяемые в диагностике инфекционных болезней. Рестрикционный анализ. Генетическая карта E.coli
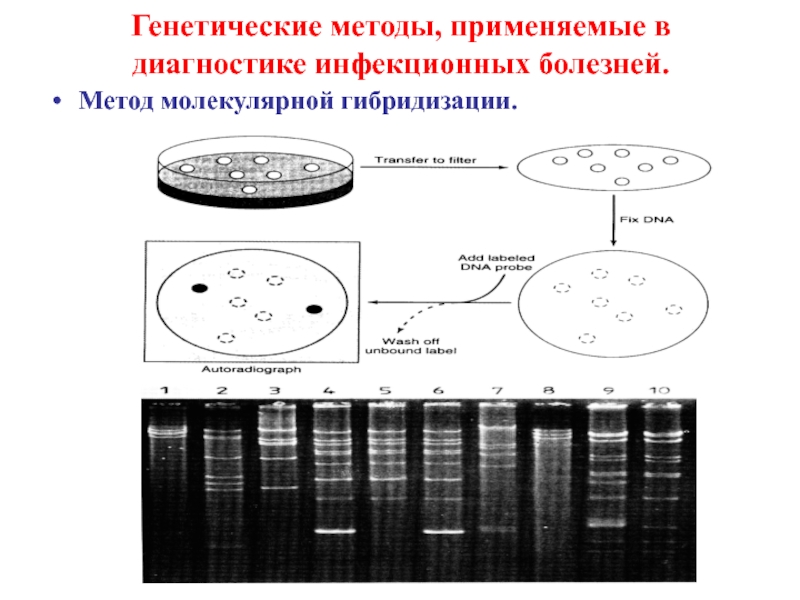
- 18. Генетические методы, применяемые в диагностике инфекционных болезней. Метод молекулярной гибридизации.
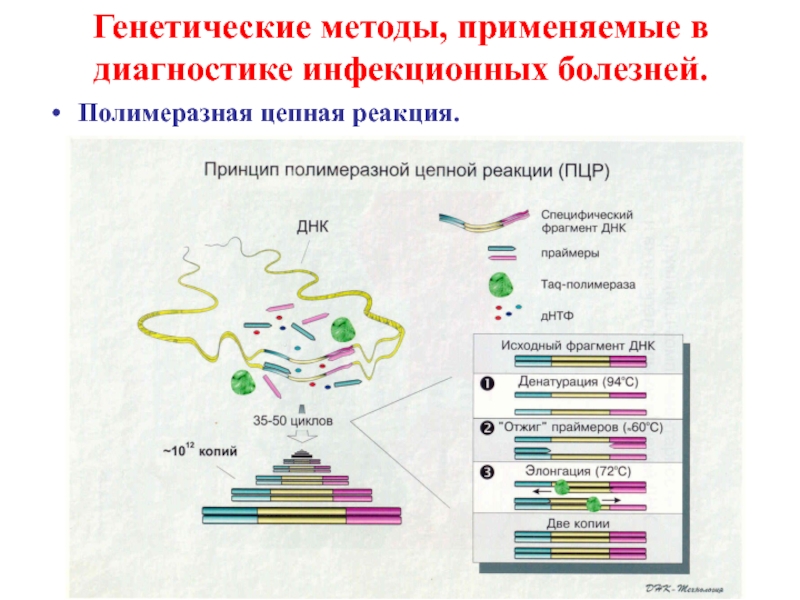
- 19. Генетические методы, применяемые в диагностике инфекционных болезней. Полимеразная цепная реакция.
- 20. Генетические методы, применяемые в диагностике инфекционных болезней.
- 21. Разделы биотехнологии. Фундаментальная биотехнология. Медицинская биотехнология.
- 22. Медицинские технологии. Создание новых технологий производства вакцин
- 23. Этапы генетической инженерии. Получение гена, кодирующего необходимый
- 24. Способы получения генов. Фрагментация всей хромосомы с
- 25. Векторы должны обладать свойствами: обеспечить проникновение гена
- 26. Способы введения рекомбинантной ДНК в клетку: трансформация;
- 27. Перспективные направления медицинской биотехнологии Онко- препараты Терапев-
- 28. Наномедицина «Наука и технология диагностики, лечения и
- 29. Наномедицина включает в себя пять перекрывающихся субтем:
- 30. Декларируемая «конечная цель» наномедицины: создание нанороботов-лекарей
- 31. Программа действий нанороботов-лекарей. Поиск клеток-мишеней. Доставки к
- 32. В наибольшей степени к нанороботам продвинулись в
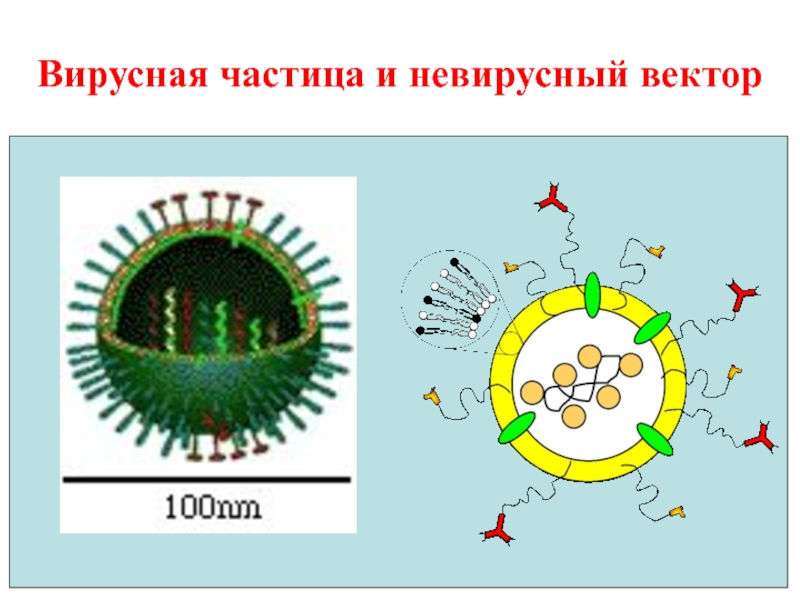
- 33. Вирусная частица и невирусный вектор
- 34. Проблемы вирусных векторов. Наработка вирусных частиц. Загрузка
- 35. Проблемы невирусных векторов. Механизмы эффективной загрузки. Присоединение
- 36. Схема нанолекарства недалекого будущего
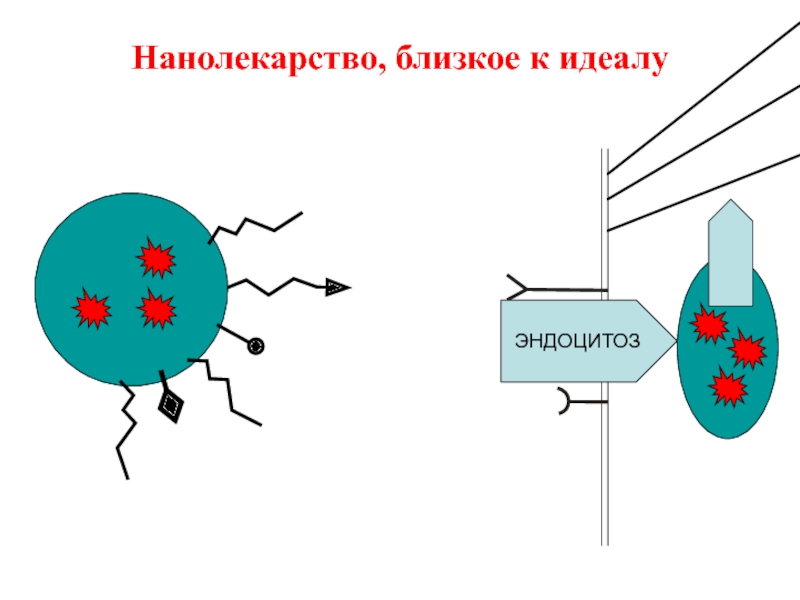
- 37. Нанолекарство, близкое к идеалу
- 38. Реализованный уровень современной наномедици-ны - контейнерная доставка
Слайд 2План лекции
Особенности генетики бактерий.
Плазмиды, транспозоны, Is-элементы.
Формы изменчивости микроорганизмов.
Типы рекомбинаций и их
Особенности генетики вирусов.
Генетические методы, применяемые в диагностике инфекционных болезней.
Биотехнология: разделы, достижения и перспективы.
Слайд 3Особенности генетики бактерий
Хромосома находится в cуперспирализованной форме и свободно располагается в
Бактерии имеют гаплоидный набор, но содержание ДНК у них непостоянно.
Передача генетической информации происходит как по вертикали, так и горизонтали.
Очень часто помимо хромосомного гена имеется дополнительный плазмидный геном.
Слайд 4Модули генома бактерий
Хромосома (нуклеоид).
Плазмиды.
Умеренные бактериофаги.
Траспозоны.
Is-элементы.
Слайд 6Плазмиды и свойства
бактерий - носителей плазмид
Категории
F-плазмиды
R-плазмиды
Col-плазмиды
Ent-плазмиды
Hly-плазмиды
Биодеградивные
плазмиды
Криптические плазмиды
Свойства
Донорные функции
Антибиотикоустойчивость
Синтез колицинов
Синтез
Синтез гемолизинов
Расщепление органических
и неорганических соединений
Неизвестны
Слайд 7Свойства плазмид
Саморегулируемая репликация.
Явление поверхностного исключения.
Явление несовместимости.
Контроль числа копий плазмид.
Контроль стабильного поддержания.
Контроль
Способность к самопереносу.
Способность к мобилизации на перенос.
Способность наделять клетку хозяина дополнительными биологическими свойствами.
Слайд 8Транспозоны – участки ДНК, свободно перемещающиеся вдоль хромосомы бактерий и способные
Характеристика транспозонов.
Состоят из 2000 – 25000 пар нуклеотидов.
При включении в ДНК вызывают в ней дупликацию, а при перемещении – делеции и инверсии.
Могут находиться в свободном состоянии в виде коль-цевой молекулы.
Реплицируются только в составе хромосомы бактерий.
Способны к перемещению с хромосомной ДНК в плаз-миду и наоборот.
Слайд 9Is-последовательности – простейший тип мигрирующих элементов (фрагменты ДНК длиной 1000 пар
Is-последовательности самостоятельно не реплицируются и содержат информацию, необходимую только для их транспозиции.
Основные функции Is-последовательностей.
Координация взаимодействия транспозонов, плазмид и умеренных бактериофагов как между собой, так и с хромосомой бактериальной клетки.
«Выключение» гена или функция промотора.
Индуцирование мутаций типа делеций или инверсий при перемещении и дупликации при встраивании в хромосому.
Слайд 10Формы изменчивости микроорганизмов
Фенотипическая (модификации)
1. Кратковременные
2. Длительные
Генотипическая
1. Мутации
2. Рекомбинации
Слайд 11Классификация мутаций
1. По происхождению:
1) спонтанные;
2) индуцированные.
2. По протяжённости изменений повреждения ДНК:
1)
2) протяжённые (аберрации).
3. По количеству мутировавших генов:
1) генные (чаще всего точечные):
а) прямые;
б) обратные;
2) хромосомные:
а) делеции;
б) инверсии;
в) дупликации.
3. По фенотипическим последствиям:
1) нейтральные;
2) условно-летальные;
3) летальные.
Слайд 12Классификация рекомбинаций по молекулярному механизму.
Гомологичные – обмен между участками ДНК, обладающими
Сайт-специфические – происходят в опреде-лённых участках генома и не требуют высокой степени гомологии ДНК.
Незаконные или репликативные – не зависят от функционирования генов recA, B, C, D (REC-системы).
Слайд 16Формы изменчивости вирусов.
Генетическая рекомбинация.
Генетическая реактивация.
Комплементация.
Фенотипическое смешивание.
Слайд 17Генетические методы, применяемые в диагностике инфекционных болезней.
Рестрикционный анализ.
Генетическая карта E.coli
Слайд 18Генетические методы, применяемые в диагностике инфекционных болезней.
Метод молекулярной гибридизации.
Слайд 19Генетические методы, применяемые в диагностике инфекционных болезней.
Полимеразная цепная реакция.
Слайд 20Генетические методы, применяемые в диагностике инфекционных болезней.
Рестрикционный анализ.
Метод молекулярной гибридизации.
Полимеразная цепная
Риботипирование и опосредованная транскрипцией амплификация рибосомальной РНК.
Слайд 21Разделы биотехнологии.
Фундаментальная биотехнология.
Медицинская биотехнология.
Сельскохозяйственная биотехнология.
Пищевая биотехнология.
Промышленная биотехнология.
Экологическая биотехнология.
Слайд 22Медицинские технологии.
Создание новых технологий производства вакцин и других иммунологических препаратов для
Создание новых молекулярно-генетических методов диагностики и лечения врождённых патологий и наследственных заболеваний;
Разработка новых методов диагностики и лечения онкологических заболеваний.
Новые методологические подходы к лечению, диагностике и профилактике «соматических» заболеваний.
Слайд 23Этапы генетической инженерии.
Получение гена, кодирующего необходимый признак вместе со структурами, обеспечи-вающими
Подбор необходимого проводника (вектора).
Соединение гена с вектором.
Введение рекомбинантной ДНК в подходя-щую клетку-реципиент.
Отбор клеток, получивших дополнительный ген и обеспечивших его функционирование.
Слайд 24Способы получения генов.
Фрагментация всей хромосомы с помощью ферментов-рестриктаз.
Синтез нужных генов
Синтез ДНК-копий на матриксных мРНК данного гена с помощью РНК-зависимых ДНК-полимераз.
Слайд 25Векторы должны обладать свойствами:
обеспечить проникновение гена в клетку;
обеспечить репликацию рекомбинантной
защищать рекомбинантную ДНК от рестрик-таз клетки;
кодировать один или несколько признаков, которые позволяют отобрать клетки, получившие рекомбинантную ДНК.
Слайд 26Способы введения рекомбинантной ДНК в клетку:
трансформация;
трансдукция;
инфекция вирусами;
с помощью липосом
слияние протопластов;
слияние клеток животных.
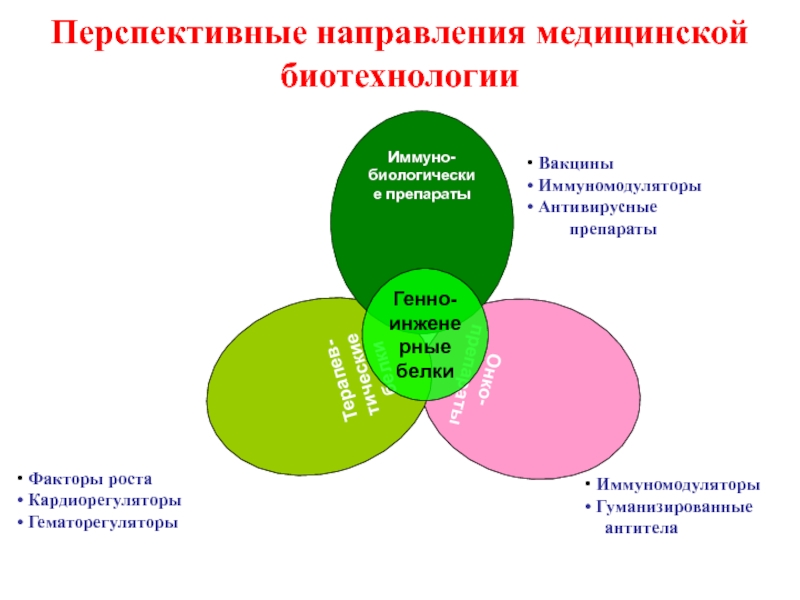
Слайд 27Перспективные направления медицинской биотехнологии
Онко-
препараты
Терапев-
тические
белки
Иммуно-
биологические препараты
Генно-
инженерные
белки
Иммуномодуляторы
Гуманизированные
антитела
Вакцины
Иммуномодуляторы
Антивирусные
препараты
Факторы роста
Кардиорегуляторы
Гематорегуляторы
Слайд 28Наномедицина
«Наука и технология диагностики, лечения и преду-преждения болезни и травматического повреждения,
«Forward Look on Nanomedicine», The European Science Foundation (ESF) 2005
Слайд 29Наномедицина
включает в себя пять перекрывающихся субтем:
аналитические методики и инструменты для диагностики
визуализация нанообъектов (от субмолекулярных событий до болезней пациентов);
нанолекарства для лечения болезней, включая биологически активные вещества и системы доставки лекарств;
поддержка химии и технологии, которые создают наноматериалы и наномашины;
перенос от лаборатории к клинике, включая промышленное масштабирование, аттестацию, регуляцию и оценку безопасности и эффективности.
Слайд 30Декларируемая «конечная цель» наномедицины:
создание нанороботов-лекарей для адресной доставки:
лекарственной субстанции,
устройств
создание нанороботов-чистильщиков.
Слайд 31Программа действий нанороботов-лекарей.
Поиск клеток-мишеней.
Доставки к ним субстанции для лечения или обнаружения
Проникновение в клетки-мишени.
Выгрузка содержимого.
Разборка на безвредные части.
Часто требуется, чтобы доставка происходила в опреде-лённые компартменты клетки (ядро, митохондрии и др.).
Слайд 32В наибольшей степени к нанороботам продвинулись в генной терапии.
Вирусные векторы -
Эти недостатки стимулируют разработку невирусных векторов.
Слайд 34Проблемы вирусных векторов.
Наработка вирусных частиц.
Загрузка вирионов лекарственной субстанцией.
Модификация генов поверхностных белков
Принципы безопасного конструирования.
Слайд 35Проблемы невирусных векторов.
Механизмы эффективной загрузки.
Присоединение к поверхности:
ПЭГ;
молекулярного адреса;
ТАТ-пептида;
ядерного (митохондриального) сигнала.
Сигнал для
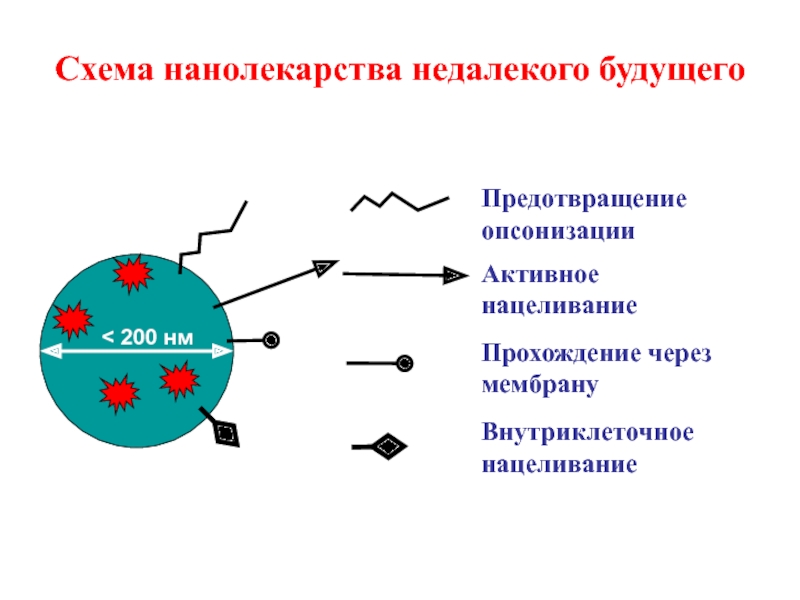
Слайд 36Схема нанолекарства недалекого будущего
Предотвращение опсонизации
Активное нацеливание
Прохождение через мембрану
Внутриклеточное нацеливание
< 200
Слайд 38Реализованный уровень современной наномедици-ны - контейнерная доставка лекарственных и диагностических субстанций
вирусные векторы для генной терапии;
продвинутые нанокапсулы (стелс-липосомы).
Более скромная, но востребованная сегодня цель - солюбилизация плохо растворимых субстанций.