- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Физиология растений. Фотоиндуцированное окисление воды презентация
Содержание
- 1. Физиология растений. Фотоиндуцированное окисление воды
- 2. ФС II
- 3. Поток электронов в
- 4. Поток электронов по
- 5. Поток электронов по
- 6. строма лумен тиллакоидная мембрана
- 8. ФС II и ФС I размещаются последовательно
- 9. Поток электронов (продолжение):
- 10. Поток электронов (продолжение):
- 11. Поток электронов (продолжение):
- 12. 4. Работа комплекса
- 13. Поток электронов (продолжение):
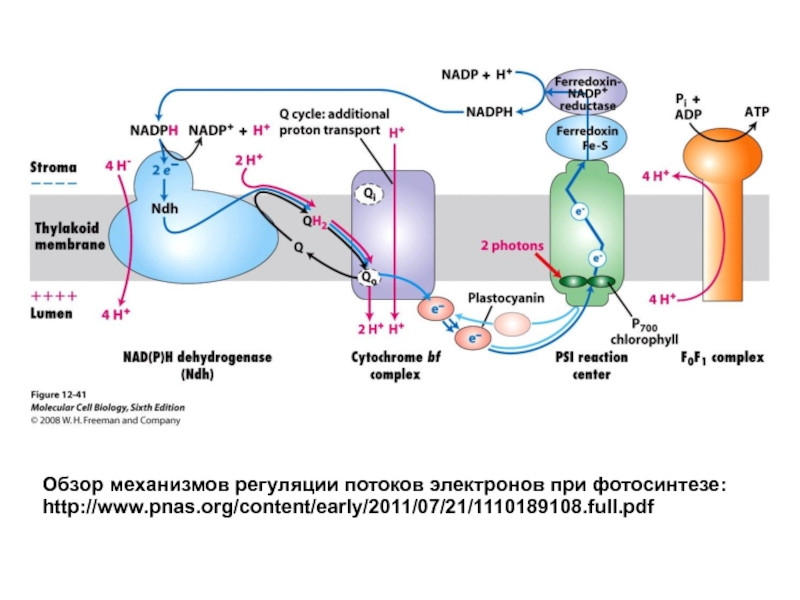
- 14. Обзор механизмов регуляции потоков электронов при фотосинтезе: http://www.pnas.org/content/early/2011/07/21/1110189108.full.pdf
Слайд 1Copyrights of Vadim Demidchik
Физиология растений
Демидчик Вадим Викторович
(д.б.н., зав. каф. физиологии
и
Слайд 2
ФС II и ФС I размещаются последовательно в цепи транспорта электронов
Для восстановления одной молекулы НАДФ+ в процессе фотосинтеза необходимо два электрона и два протона, при этом донором электронов является вода.
Фотоиндуцированное окисление воды происходит в ФС II, восстановление НАДФ+ – ФС I.
Таким образом, фотосистемы должны функционировать во взаимодействии для восстановления углерода до сахаров и выделения кислорода.
Современная «квантовая теория» передачи энергии в ранних стадиях фотосинтеза (теория Флемминга):
http://www.physorg.com/news95605211.html
Слайд 3
Поток электронов в фотосинтезе начинается с ФС II:
(компоненты расположены очень близко
1. Электрон от
первичного донора ФСII –
возбужденного Р680 (Р680* или Р680-)
(Р680 – один из специальных димеров хл. а - всего их два димера - приобретает более позитивное значение потенциала вследствие присоединения электронов от свето-собирающего комплекса фотосистемы 2 - ССКII)
переходит на
феофитин – первичный акцептор ФСII
это молекула хл., лишенная иона магния
после принятия электрона она возбуждается, приобретает отрицательный заряд и становится радикалом –
феофитин.-
Слайд 4
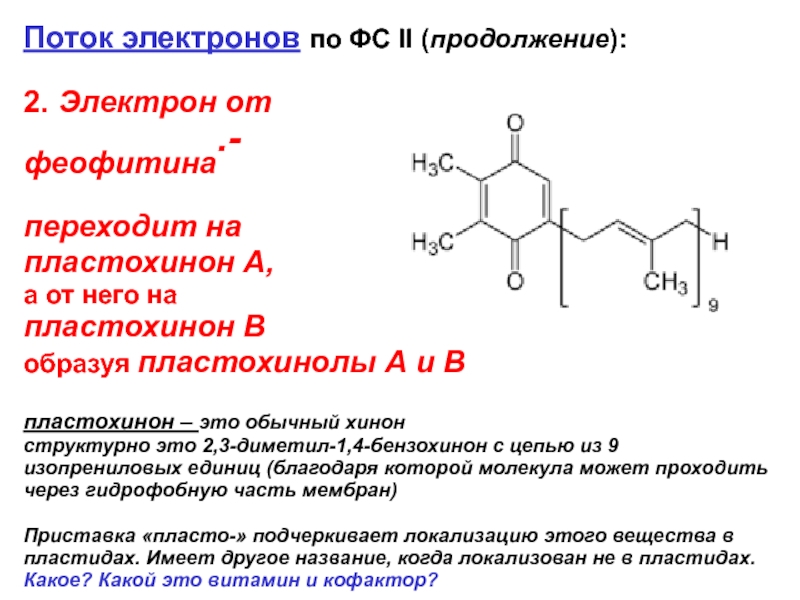
Поток электронов по ФС II (продолжение):
2. Электрон от
феофитина.-
переходит на
пластохинон
а от него на
пластохинон B
образуя пластохинолы А и B
пластохинон – это обычный хинон
структурно это 2,3-диметил-1,4-бензохинон с цепью из 9 изопрениловых единиц (благодаря которой молекула может проходить через гидрофобную часть мембран)
Приставка «пласто-» подчеркивает локализацию этого вещества в пластидах. Имеет другое название, когда локализован не в пластидах. Какое? Какой это витамин и кофактор?
Слайд 5
Поток электронов по ФС II (продолжение):
3. Восстановление Р680
электрон от воды
переходит
восстанавлиявая его обратно до Р680
это происходит в результате работы
The oxygen-evolving complex (OEC) – «кислород-выделяющий комплекс» также известного под другим названием - water-splitting complex – «водоразлогающий комплекс»
Это фермент, окисляющий воду . Процесс, катализируемый им, называют фотоокислением воды . Теория Кока (1970 г.) – фермент ОЕС может существовать в 5 состояниях S0, S1, S2, S3 и S4. При взаимодействии с окисленным Р680 фермент постепенно переходит в состояние S4, теряя 4 электрона, которые он забирает от 2 молекул воды . На Р680 электроны передаются через боковую ветвь тирозина D1-Y161.
OEC – сложно-устроенный металлопротеин , содержащий 4 атома марганца, 1 атом кальция и как минимум один атом хлора (возможно 2) + карбонат ионы - Mn4Ca1OxCl1–2(HCO3)y.
Предполагается, что ОЕС эволюционно возник, благодаря большой концентрации марганец-содержащих минералов ранцита и холандита в ранних океанах, из которых этот металл был утилизирован примитивными Cyanobacteria в качестве активного центра своих ферментов.
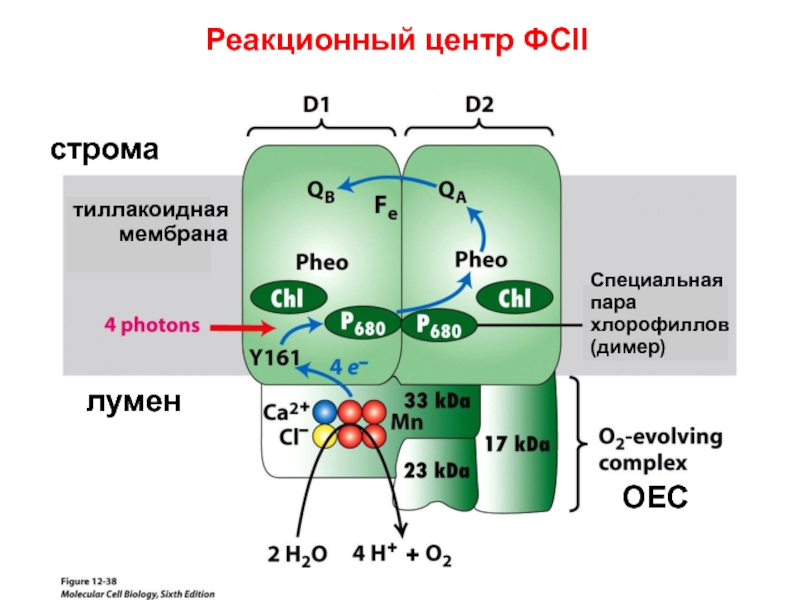
Слайд 6строма
лумен
тиллакоидная мембрана
Специальная пара хлорофиллов (димер)
Реакционный центр ФСII
ОЕС
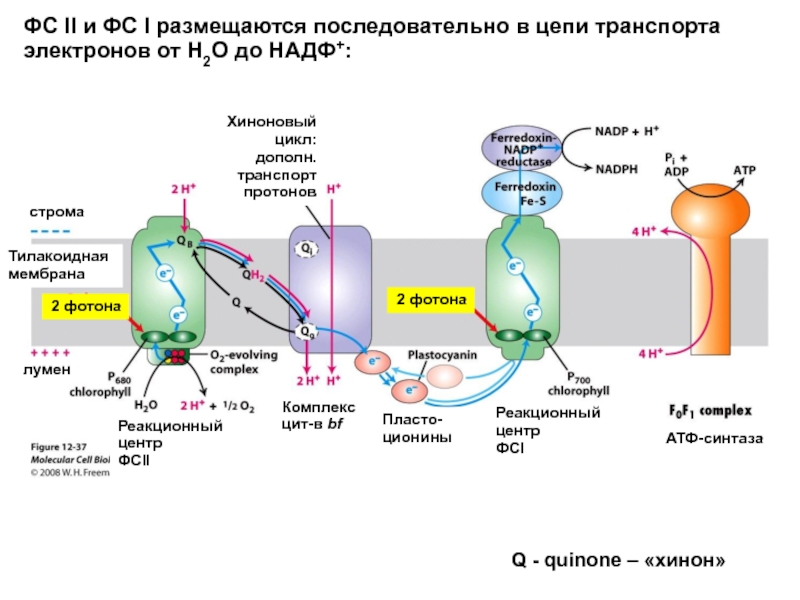
Слайд 8ФС II и ФС I размещаются последовательно в цепи транспорта электронов
Тилакоидная
мембрана
строма
лумен
Реакционный
центр
ФСII
Реакционный
центр
ФСI
Комплекс
цит-в bf
Хиноновый цикл:
дополн. транспорт
протонов
Q - quinone – «хинон»
Пласто-ционины
2 фотона
2 фотона
АТФ-синтаза
Слайд 9
Поток электронов (продолжение):
4. Работа комплекса цитохромов b6f
электрон от пластохинола (QH2)
переходит на
b6f - димер, каждый из мономеров которого состоит из 8 субъединиц:
4 большие субъединицы –
(1) цит. f (32 кДа),
(2) цит. b6 (25 кДа) с «высоко-» и «низко-энергетическими» гемовыми группами,
(3) комплекс Риске (19 кДа) – железосерный белок – содержит [2Fe-2S]-кластер,
(4) субъединица IV (17 кДа)
4 малые субъединицы – (все по 3-4 кДа) - PetG, PetL, PetM и PetN.
Общий молекулярный вес комплекса b6f – 217 кДа.
Слайд 10
Поток электронов (продолжение):
4. Работа комплекса цитохромов b6f -
«хиноновый цикл»
Первая часть
высокоэнергетический перенос:
- QH2 связывается с положительной стороной 'p‘ (лумен) комплекса b6f
- QH2 отдает электроны железосерному центру (Fe-S-центру) и превращается в семихинон (SQ) и также выделяет 2 протона (Н+) в тилакоидный лумен.
- восстановленный железо-серный центр переносит электроны через цитохром f до пластоцианина
В случае так-называемого низкоэнергетического переноса:
- семихинон транспортирует электроны на гем bp цитохрома b6
- гем bp переносит электроны на гем bn
- гем bn восстанавливает Q до SQ.
Слайд 11
Поток электронов (продолжение):
4. Работа комплекса цитохромов b6f -
«хиноновый цикл»
Вторая часть
- второй QH2 связывается с комплексом.
- в высокоэнергетическом переносе один электрон восстанавливает вторую молекулу пластоцианина
- в низкоэнергетическом переносе электрон от гема bn переносится на SQ, образуя Q2- - полностью восстановленную форму хинона, которая может принимать 2 протона из стромы и формировать QH2.
Регенерируемые окисленные Q и восстановленные QH2 могут передвигаться внутри мембраны в противоположные стороны.
Слайд 12
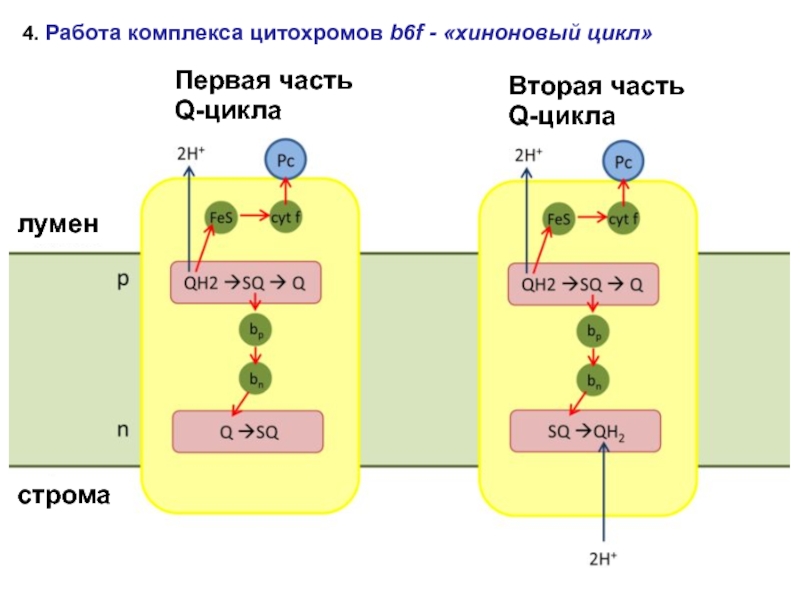
4. Работа комплекса цитохромов b6f - «хиноновый цикл»
Вторая часть Q-цикла
Первая часть
лумен
строма
Слайд 13
Поток электронов (продолжение):
5. Работа пластоцианинов (ПЦ)
Перенос электронов на ПЦ
Медь-содержащий (потому голубой)
Имеет мономерную структуру (10,5 кДа), всего 99 аминокислот.
ПЦ-Cu2+ может восстанавливаться цитохромом f до ПЦ-Cu+
ПЦ-Cu+ диффундирует внутри лумена и связывается с P700+.
P700+ окисляет ПЦ-Cu+ обратно до ПЦ-Cu2+.