- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводороды презентация
Содержание
- 1. Углеводороды
- 2. Урок 4. Предельные нециклические (ациклические) углеводороды. Алканы. Парафины.
- 3. План ответа: 1. Общая характеристика класса.
- 4. 1. Определение. Предельными углеводородами называются органические вещества,
- 5. 2. Строение: а) атом углерода
- 7. ё) атомы в молекуле могут относительно свободно
- 10. 3. Общая формула алканов: (CH4,
- 11. Задача: Относительная молекулярная масса предельного углеводорода 58
- 12. 4. Гомологический ряд: Органические вещества сходного строения
- 13. Название гомологов и их радикалов по
- 14. 5. Изомерия вещества, имеющие один и
- 15. Для алканов характерна самая простая изомерия
- 16. 6.Номенклатура ( МНК) Чтобы составить
- 17. Порядок действий : а. выделяют в структурной
- 18. б) в названии вещества цифрой указывают, при
- 19. г) когда разветвление начинается при атомах углерода,
- 20. д) название записывают, начиная с младшего радикал
- 21. 7. Получение алканов: а) из природного газа б) из нефти
- 22. 8. Физические свойства: СH4
- 23. 9.Химические свойства: 1. Все органические вещества
- 24. 2. Дегидрирование( отнятие водорода)
- 25. 3.Реакция замещения водорода на галоген. Механизм
- 26. 10.Отдельные представители: СН4- Метан Метан составляет
Слайд 1Углеводороды
Углеводородами называются органические вещества, состоящие только из атомов углерода и водорода.
Слайд 3План ответа:
1. Общая характеристика класса.
2. Строение.
3. Общая формула.
4. Гомологический ряд
5.
6. Изомерия.
7. Получение.
8. Физические свойства.
9. Химические свойства.
10.Отдельные представители
Слайд 41. Определение.
Предельными углеводородами называются органические вещества, в молекулах которых атомы углерода
Слайд 52. Строение:
а) атом углерода находится в возбуждённом состоянии, т.е. имеет
б) все связи в молекулах предельных углеводородов ковалентные неполярные(С-С) и полярные (С-Н)
Слайд 7ё) атомы в молекуле могут относительно свободно вращаться вокруг химических связей.
ж)Зигзагообразная
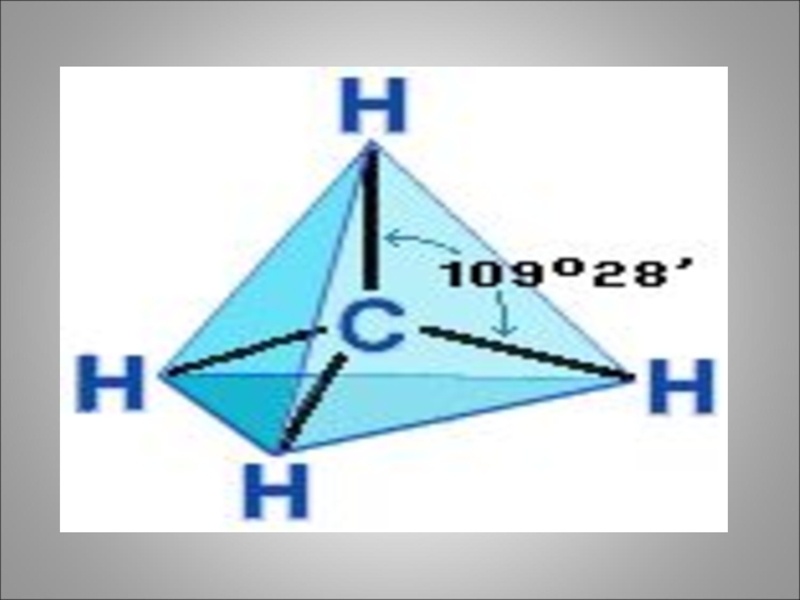
з)Четыре s-связи углерода направлены в пространстве под углом 109о28', что соответствует наименьшему отталкиванию электронов. Поэтому молекула простейшего представителя алканов – метана СН4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
Слайд 11Задача: Относительная молекулярная масса предельного углеводорода 58 определите его формулу.
Дано:
М(СnH2n+2)=58
решение:
М(СnH2n+2)=58
12n+1(2n+2)=14n+2=58
14n=56
n=4
Ответ:C4H10
Слайд 124. Гомологический ряд:
Органические вещества сходного строения (имеющие одну общую формулу) и
|
называются
гомологами.
| H - С-Н –
|
гомологическая разность
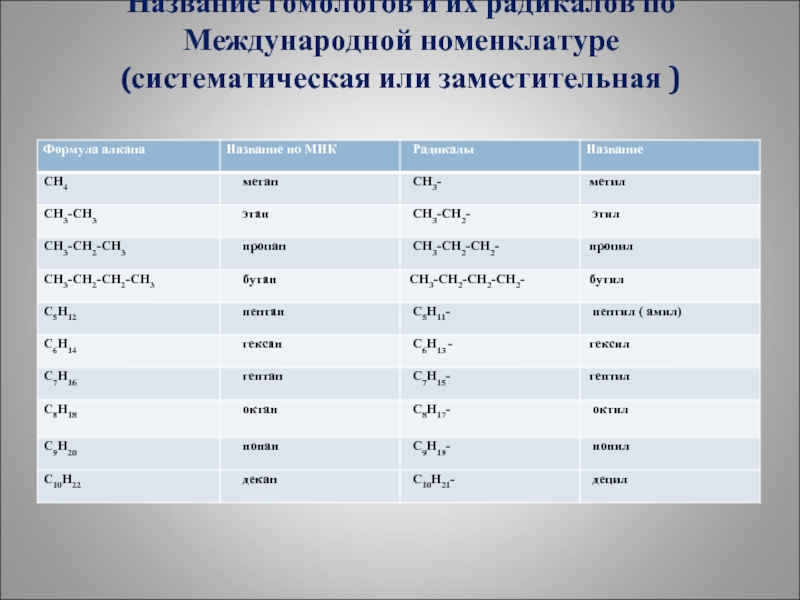
Слайд 13 Название гомологов и их радикалов по Международной номенклатуре
Слайд 145. Изомерия
вещества, имеющие один и тот же качественный и количественный
Слайд 15
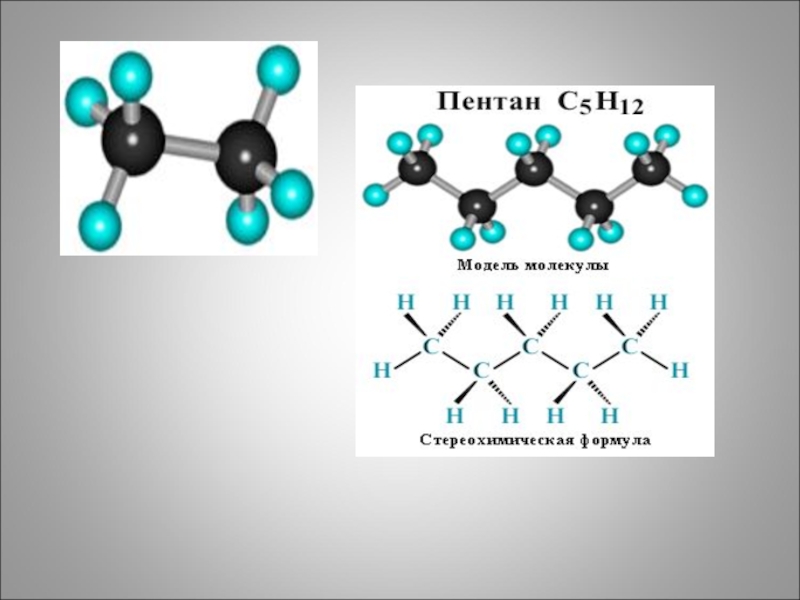
Для алканов характерна самая простая изомерия - структурная изомерия углеводородного скелета
Пример:
Алкан
СН3-СН2-СН2-СН2-СН3
н-пентан
и два изомера:
1) СН3-СН-СН2-СН3
|
СН3
2) CН3
| СН3 - С - СН3
|
CН3
Слайд 16
6.Номенклатура ( МНК)
Чтобы составить название углеводорода с разветвлённой цепью, его рассматривают
Слайд 17Порядок действий :
а.
выделяют в структурной формуле наиболее длинную углеродную цепь и
6 5 4 3 2 1 СН3 –СН2-СН2-СН-СН-СН3
| |
CH2 CH3
|
CH3
Слайд 18б) в названии вещества цифрой указывают, при каком атоме углерода находится
в) если замещающих групп несколько цифрами отмечают каждую из них;
6 5 4 3 2 1 СН3 –СН2-СН2-СН-СН-СН3
| |
CH2 CH3
|
CH3
Слайд 19г) когда разветвление начинается при атомах углерода, равноудалённых от концов главной
имеющий более простое строение.
6 5 4 3 2 1 СН3 –СН2-СН2-СН-СН-СН3
| |
CH2 CH3
|
CH3
Слайд 20д) название записывают, начиная с младшего радикал –заместителя; или по алфавиту
е) в конце пишут название выбранной цепи с окончанием -ан
6 5 4 3 2 1 СН3 –СН2-СН2-СН-СН-СН3
| |
CH2 CH3
|
CH3
2-метил-3этилгексан
Слайд 22
8. Физические свойства:
СH4
СН3-СН3
-СН3СН2 –СН3 газы
СН3-СН2-СН2-СН3
СН3-СН2-СН2-СН2-СН3
СН3-СН2-СН2-СН2-СH2 - СН3
C7H16
C8H18
C9H20
C10H22
С15Н32 жидкости
С16Н34
……… твёрдые вещества
с ростом количества атомов углерода возрастают Tкип и Тпл., а также плотность веществ.
В воде плохо растворимы, но растворяются в органических растворителях( спирт, бензол и т.д.)
Изомеры имеют Tкип и Тпл. ниже, чем соответствующие алканы нормального строения.
СН4 и С2Н6 – имеют специфический запаха, остальные обладают запахом бензина
Слайд 239.Химические свойства:
1. Все органические вещества горят с образованием углекислого газа и
СH4+ 2O2 => CO2 + 2 H2O + Q ( 880кДж)
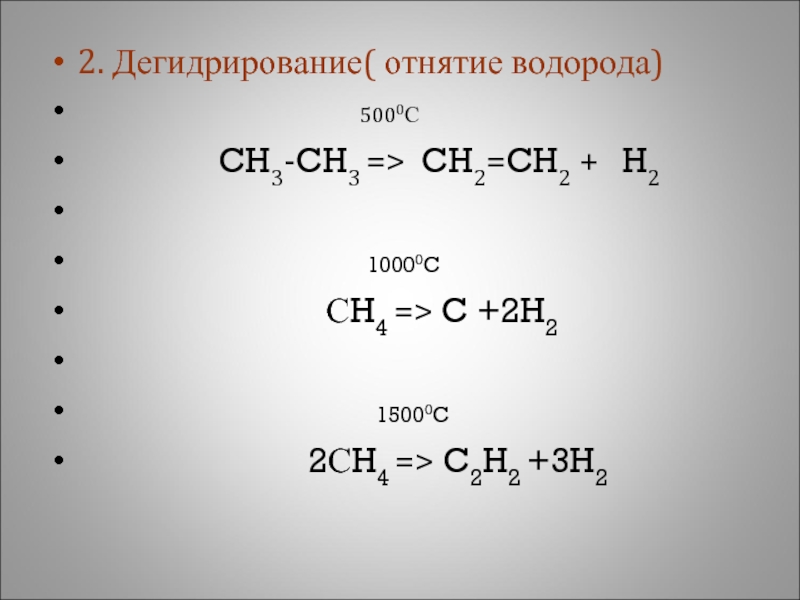
Слайд 242. Дегидрирование( отнятие водорода)
CH3-CH3 => CH2=CH2 + H2
10000C
СH4 => C +2H2
15000C
2СH4 => C2H2 +3H2
Слайд 253.Реакция замещения водорода на галоген.
Механизм реакции цепной свободно-радикальный ( пояснение на
Начинается с разрыва связей С-С С-Н
Сl-Cl
hy
Сl-Cl => Сl- +Cl-
Cl- + CH4 => CH3- + HCl
CH 3- + Cl-Cl => CH3 Cl + Cl-
Cl- + CH4 => CH3- + HCl и т.д.
пока Сl- + CH3- => CH3Cl и цепь прервётся
Если Сl2 в избытке, то образуется CH2Cl2 или CHCl3 и ССl4
+Cl2 +Cl2 +Cl2 +Cl2
СH4 => CH3Cl => CH2Cl2 => CHCl3 => CCl4
Слайд 2610.Отдельные представители:
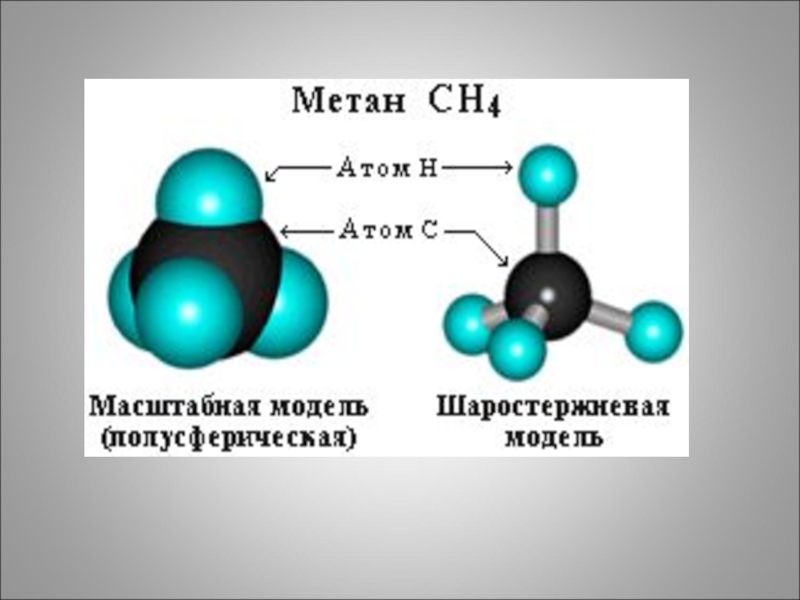
СН4- Метан
Метан составляет 87-90% болотного или шахтного газа
Применение:
1. В больших количествах используют как топливо.
2. Применяется для получения Н2, С2Н2-ацетилена, синтез газа
( СН4 + Н2О=> СО +3Н2 )
3.Исходное сырьё для получения формальдегида, метилового спирта и других органических веществ