- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Цветные реакции белков презентация
Содержание
- 1. Цветные реакции белков
- 2. Указатель реакций Биуретовая Уравнение реакции Проведение опыта
- 3. Функция качественных реакций Для аминокислот, постоянно встречающихся
- 4. Аминокислоты Основной структурной единицей белков служат a-аминокислоты.
- 5. Аминокислоты Вернуться
- 6. Биуретовая реакция Определяет наличие пептидной связи в растворе исследуемого соединения. пептидная связь
- 7. Биуретовая реакция Реакция обусловлена образованием биуретового комплекса
- 8. Биуретовая реакция Биуретовая реакция протекает так: +CuSO4 +NaOH Вернуться
- 9. Биуретовая реакция Вернуться
- 10. Нингидриновая реакция Качественная реакция на α -аминокислоты
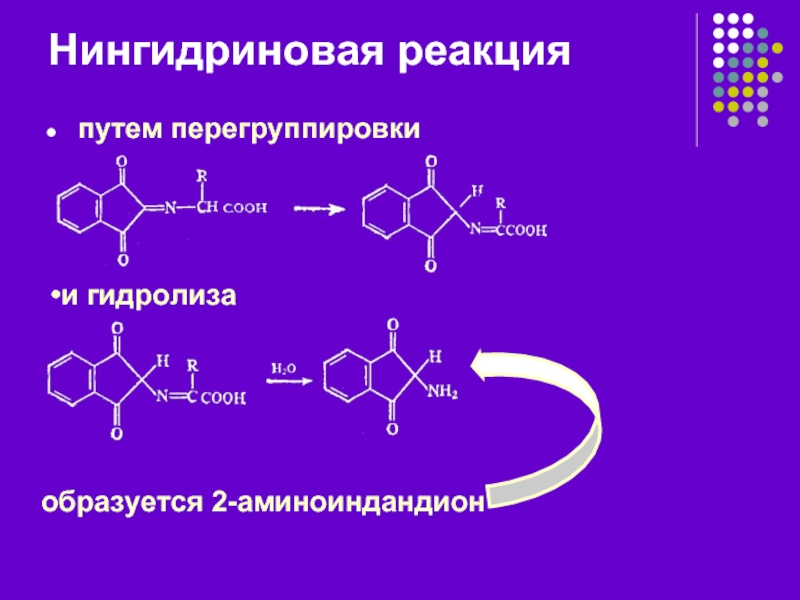
- 11. Нингидриновая реакция путем перегруппировки и гидролиза образуется 2-аминоиндандион
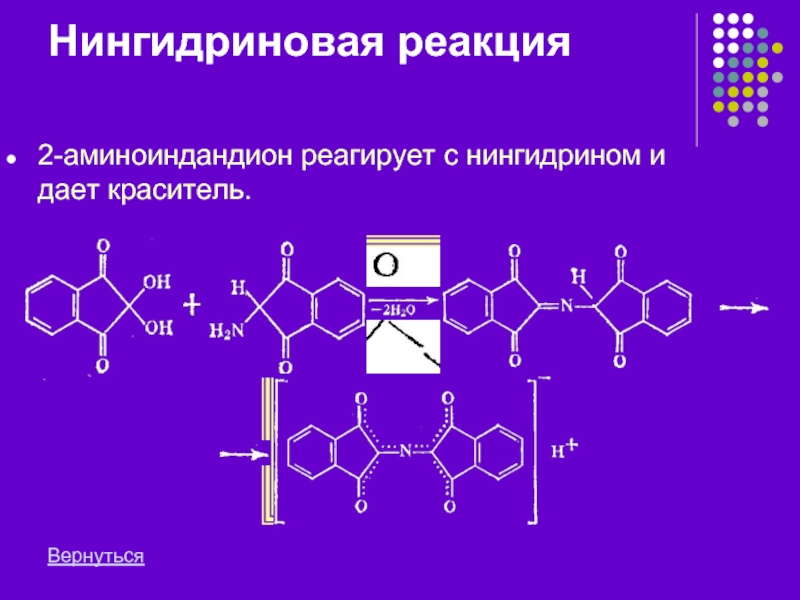
- 12. Нингидриновая реакция 2-аминоиндандион реагирует с нингидрином и дает краситель. Вернуться
- 13. Ксантопротеиновая реакция Определяет присутствие в белке ароматических
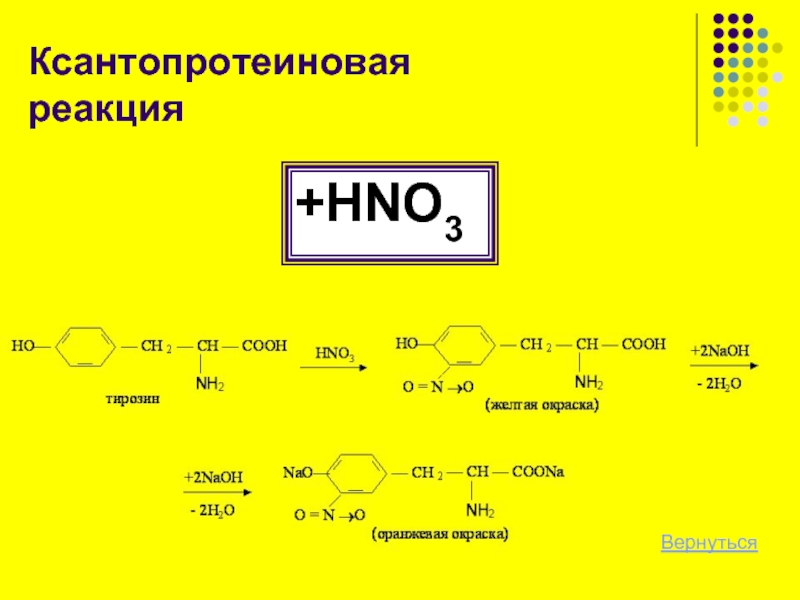
- 14. Ксантопротеиновая реакция +HNO3 Вернуться
- 15. Ксантопротеиновая реакция При действии концентрированной НNО3 на
- 16. Реакция Миллона Это реакция на аминокислоту тирозин
- 17. Реакция Миллона Реактив Миллона (раствор HgNO3 и
- 18. Рекомендации к проведению опыта К 2 мл
- 19. Реакция Гопкинса–Коле Эта реакция определяет аминокислоту триптофан.
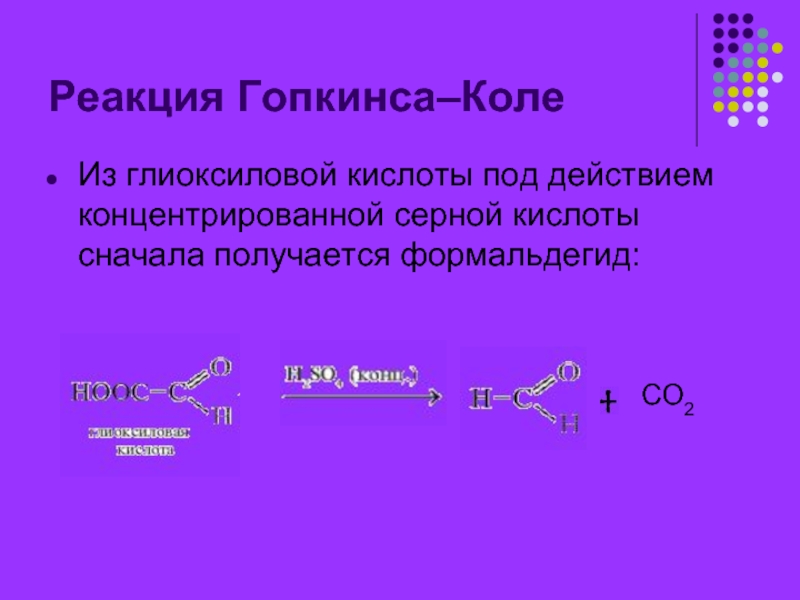
- 20. Реакция Гопкинса–Коле Из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается формальдегид: СО2
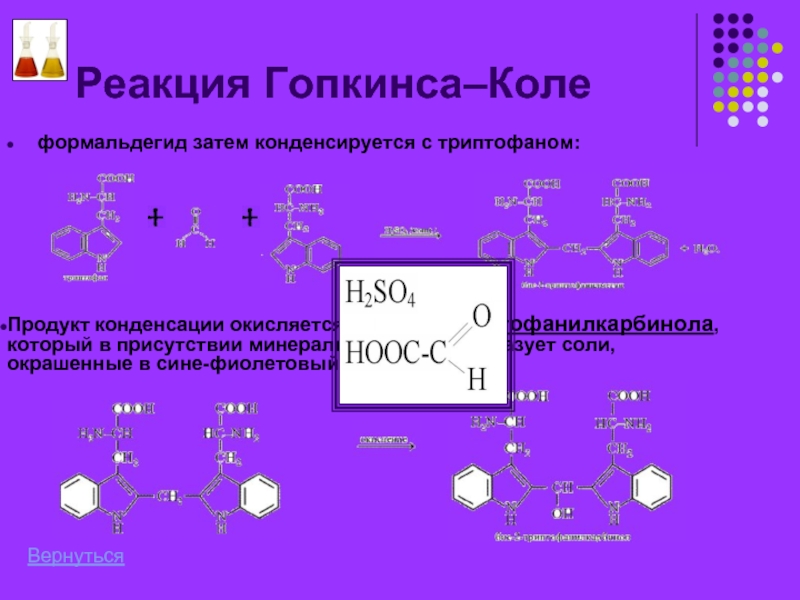
- 21. Реакция Гопкинса–Коле формальдегид затем конденсируется с триптофаном:
- 22. Рекомендации к проведению опыта Охладить до 0 °С
- 23. Реакция Паули (Диазореакция Паули) Эта реакция аминокислоту гистидин.
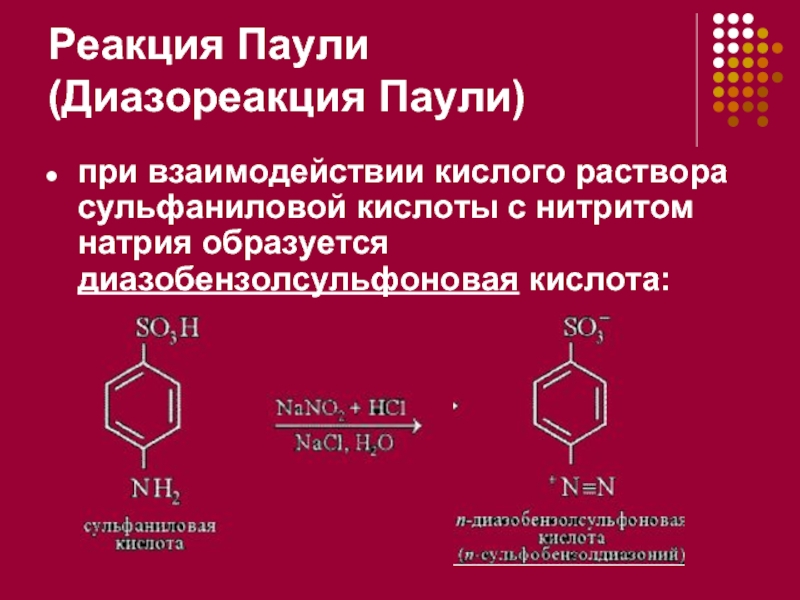
- 24. Реакция Паули (Диазореакция Паули) при взаимодействии кислого
- 25. Реакция Паули (Диазореакция Паули) Диазобензолсульфоновая кислота, взаимодействуя с гистидином, дает соединение вишнево-красного цвета: Вернуться
- 26. Рекомендации к проведению опыта В пробирку наливают
Слайд 2Указатель реакций
Биуретовая
Уравнение реакции
Проведение опыта
Нингидриновая
Ксантопротеиновая
Уравнение реакции
Проведение опыта
Миллона
Гопкинса-Коле
Диазореакция Паули
Слайд 3Функция качественных реакций
Для аминокислот, постоянно встречающихся в составе белков, разработано множество
Надо помнить, что все качественные реакции – это реакции не собственно на белки, а на определенные аминокислоты, входящие в их состав.
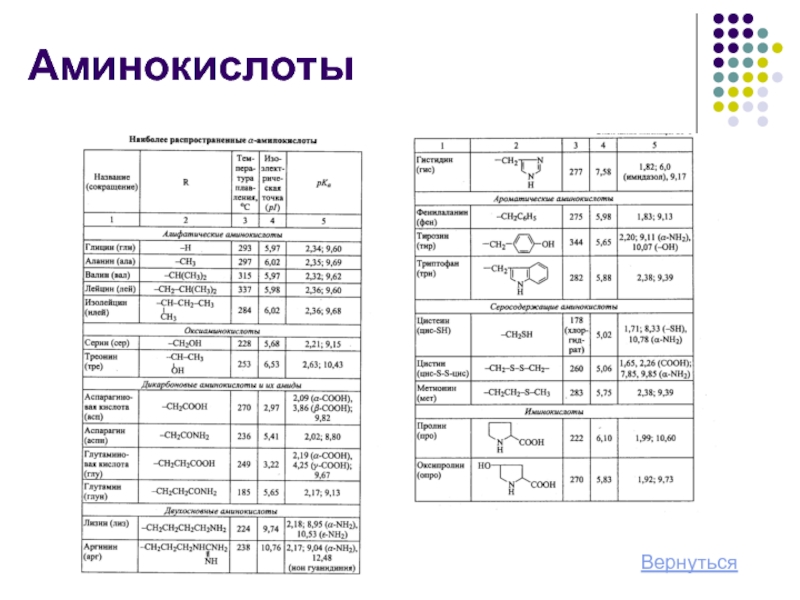
Слайд 4Аминокислоты
Основной структурной единицей белков служат a-аминокислоты. В состав большинства природных белков
Качественные реакции служат как для определения принадлежности вещества к классу белков, так и для идентификации входящих в его состав аминокислот
Наиболее распространенные аминокислоты см. таблицу
Слайд 6Биуретовая реакция
Определяет наличие пептидной связи в растворе исследуемого соединения.
пептидная связь
Слайд 7Биуретовая реакция
Реакция обусловлена образованием биуретового комплекса в результате соединения меди с
В пептидах и белках пептидная связь обычно находится в амидной форме (или кетоформе), но в щелочной среде она переходит в иминольную (енольную):
Слайд 10Нингидриновая реакция
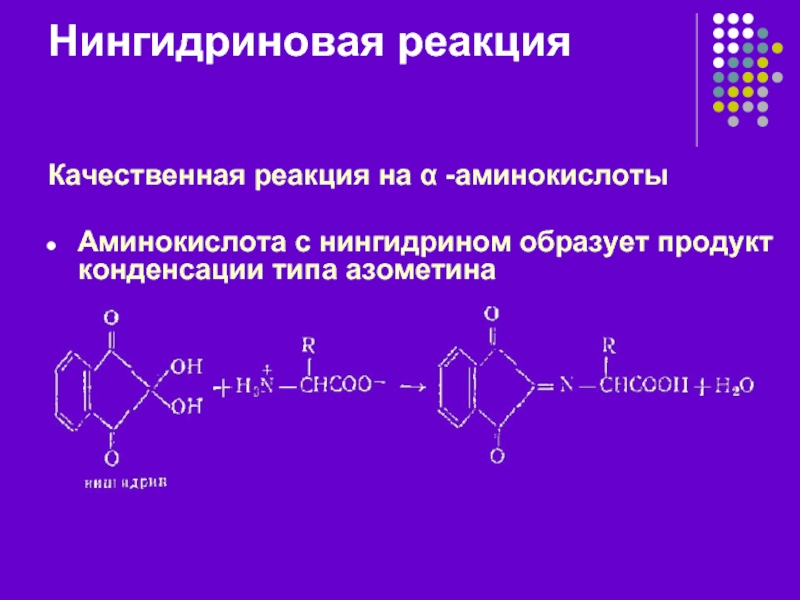
Качественная реакция на α -аминокислоты
Аминокислота с нингидрином образует продукт конденсации
Слайд 13Ксантопротеиновая реакция
Определяет присутствие в белке ароматических и гетероциклических α - аминокислот
триптофана,
фенилаланина,
тирозина,
гистидина.
Слайд 15Ксантопротеиновая реакция
При действии концентрированной НNО3 на раствор белка образуется нитросоединение, окрашенное
Вернуться
Слайд 17Реакция Миллона
Реактив Миллона (раствор HgNO3 и Hg(NO2)2 в разбавленной HNO3, содержащей
+HgNO3
+Hg(NO2)2
+HNO3
+HNO2
Вернуться
Слайд 18Рекомендации к проведению опыта
К 2 мл концентрированного раствора тирозина прибавляют ~1
встряхивают
осторожно нагревают пробирки на пламени спиртовки.
Образуется красное окрашивание.
Слайд 20Реакция Гопкинса–Коле
Из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается
СО2
Слайд 21Реакция Гопкинса–Коле
формальдегид затем конденсируется с триптофаном:
Продукт конденсации окисляется до бис-2-триптофанилкарбинола, который
Вернуться
Слайд 22Рекомендации к проведению опыта
Охладить до 0 °С насыщенного раствора щавелевой кислоты
К 2
Полученный осадок оксалата магния отфильтровать и декантировать небольшим количеством воды.
Фильтрат подкислить уксусной кислотой и довести до объема 200 мл (полученный раствор хранить в холодильнике!). Это и есть глиоксиловая кислота.
1 мл 0,005%-го раствора триптофана смешать с равным объемом глиоксиловой кислоты и к смеси прибавляют 10 капель раствора сульфата меди(II).
Небольшими порциями добавляют 2–3 мл концентрированной серной кислоты, охлаждая пробирку после приливания очередной порции кислоты током холодной воды (или в ванночке со льдом).
Полученную смесь оставляют на 10 мин при комнатной температуре, после чего ставят на 5 мин в кипящую водяную баню.
Наблюдается образование сине-фиолетового окрашивания
Слайд 24Реакция Паули (Диазореакция Паули)
при взаимодействии кислого раствора сульфаниловой кислоты с нитритом
Слайд 25Реакция Паули (Диазореакция Паули)
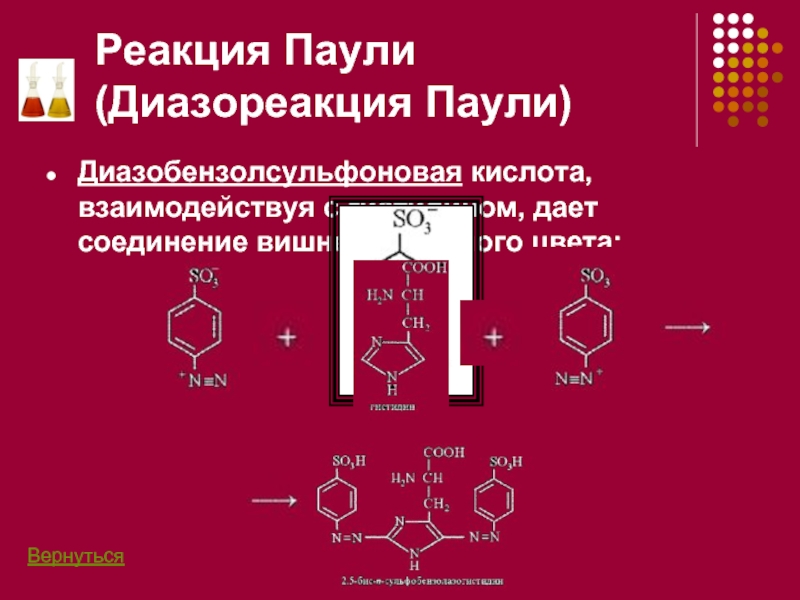
Диазобензолсульфоновая кислота, взаимодействуя с гистидином, дает соединение вишнево-красного
Вернуться
Слайд 26Рекомендации к проведению опыта
В пробирку наливают 1 мл 1%-го раствора сульфаниловой
Прибавляют 2 мл 0,5%-го раствора нитрита натрия
Сильно встряхивают
Немедленно приливают 2 мл 0,01%-го раствора гистидина
После перемешивания содержимого пробирки сразу приливают 6 мл 10%-го раствора соды.
Появляется интенсивная вишнево-красная окраска.