- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Роль системы управления рисками в профилактике осложнений фармакотерапии презентация
Содержание
- 1. Роль системы управления рисками в профилактике осложнений фармакотерапии
- 2. Современные лекарства подобны атомной энергии -
- 3. Рост численности серьезных, а также с летальными
- 4. Статистика Более 120 ЛС средств отозваны с
- 5. В базе данных ВОЗ о НПР
- 6. Динамика поступления сообщений о НПР ЛПУ
- 7. Биопрепараты и их аналоги Отмечается значительный рост
- 8. Особенности биопрепаратов Природные источники сырья Видоспецифичность
- 9. Различия между генериками и биоаналогами «Генерики» биологических
- 10. Лекарственные средства на основе нанотехнологий
- 11. Система управления рисками (СУР) Совокупность деятельности и
- 12. Задачи СУР Разработка и реализация мер по
- 13. Система управления рисками разрабатывается : Для
- 14. Согласно требованиям закона в странах ЕС и
- 15. План управления рисками Характеристика безопасности
- 16. Характеристика безопасности лекарств По данным доклинических испытаний
- 17. Основные задачи фармаконадзора в системе управления рисками
- 18. План фармаконадзора Оценка выявленных значимых
- 19. План фармаконадзора основан на: Характеристике безопасности ЛС
- 20. Меры по снижению рисков при применении
- 21. Меры, принимаемые для снижения рисков
- 22. Мизопростол Misoprostol – синтетический аналог простагландина Е1.
- 23. Серьезные НПР, возникающие при приеме Мизопростола Гиперстимуляция
- 24. ЕМЕА рекомендует приостановить действие лицензии на продажу
- 25. Административные решения в отношении биопрепаратов В постмаркетинговый
- 26. Перечень ЛС, в отношении которых разработана СУР
- 27. Перечень ЛС, в отношении которых разработана СУР
- 28. Меры, принимаемые для снижения рисков в России
- 29. Одновременное применение нескольких НПВС Пациентке 60 лет,
- 30. Одновременное применение нескольких НПВС Пациентку 32 лет
- 31. Письма – предупреждения в региональные центры мониторинга безопасности лекарственных средств, 2009 год
- 32. Письма – предупреждения в региональные центры мониторинга безопасности лекарственных средств, 2009 год
- 33. «Большинству людей кажется, что таблетки – это
- 34. Благодарю за внимание !
- 35. Правила управления рисками Характеристика безопасности План действия
- 36. Требования к регистрации биоаналогов Доказательство сопоставимости с
- 37. Регистрация биоаналогов: Безопасность - клинические и
- 38. Регистрация биоаналогов Проведение доклинических и клинических исследований
- 39. Административные решения в отношении биопрепаратов В инструкции
- 40. Меры, принимаемые для снижения рисков в России
- 41. Данные меры по снижению рисков при
- 42. Заключение В основе фармаконадзора лежат следующие 3
- 43. «Большинству людей кажется, что таблетки – это
Слайд 1Роль системы управления рисками
в профилактике
осложнений фармакотерапии
А.В. Астахова, В.К.Лепахин
Федеральный
Слайд 2Современные лекарства подобны атомной энергии - они могут принести как огромную
Сэр Деррик Данлоп
Первый председатель Комитета
по безопасности лекарств Великобритании
Слайд 3Рост численности серьезных, а также с летальными исходами НПР
Осложнения лекарственной терапии
За период с 1998 по 2005 гг. по данным FDA:
число сообщений о серьезных НПР при применении рецептурных ЛС увеличилось в США в 2,6 раза (с 34 966 в 1998 г. до 89 842 в 2005) г.
Число летальных исходов, вызванных рецептурными ЛС, увеличилось в 2,7 раза (с 5519 в 1998 г. до 15107 в 2005 г.)
В целом число серьезных НПР (серьезных и летальных) выросло в 4 раза больше, чем число выписанных рецептов
Lazarou J и соавт.1998г.
Moore TJ, et al. Arch Intern Med 2007;167(16):1752-1759.
Слайд 4Статистика
Более 120 ЛС средств отозваны с рынка ЕС за последние 10
33% из них отозваны в первые 2 года после регистрации
50% в первые пять лет
Слайд 5
В базе данных ВОЗ о НПР
более 5 000 000 сообщений
≈
из них связаны с нерациональным применением лекарственных средств, медицинскими ошибками и
недоучетом особенностей состояния организма больного
Слайд 6
Динамика поступления сообщений о НПР
ЛПУ
726
Ф.К.
348
2008 г.
2009 г.
Рег.центры и
ЛПУ
Фарм.компании
2 721
1 074
6 057
2007 г.
192
2010
1кв.
Ожидается поступление
10-12 тыс. сообщений
2 228
В 6 раз
Слайд 7Биопрепараты и их аналоги
Отмечается значительный рост числа биопрепаратов (БП)
(Увеличение
В настоящее время на международном рынке – более 200 БП
Около 300 БП - на стадии клинических исследований
БП составляют 22% и 24% от числа всех инновационных препаратов, одобренных соответственно в ЕС и FDA к 2006 году.
Слайд 8Особенности биопрепаратов
Природные источники сырья
Видоспецифичность
Сложная структура молекулы
Высокий молекулярный
Зависимость активности /безопасности от многих факторов
Разный механизм действия при разных заболеваниях
Сложный процесс производства – трудности воспроизведения партий одного и того же препарата
Сложности тестирования
Выраженная иммуногенность
Канцерогенность
Слайд 9Различия между генериками и биоаналогами
«Генерики» биологических продуктов не идентичны, они являются
Генерик- воспроизведенное лекарственное средство
Генерик идентичен оригиналу по химической структуре, качеству, биоэквивалентности, дозировке, показаниям, профилю безопасности
Слайд 10Лекарственные средства на основе нанотехнологий
К настоящему времени невозможно предсказать
Поэтому требуется тщательное изучение безопасности нанотехнологического ЛС в каждом конкретном случае его назначения
Слайд 11Система управления рисками (СУР)
Совокупность деятельности и мероприятий в области фармаконадзора, направленных
Слайд 12Задачи СУР
Разработка и реализация мер по снижению рисков
Оценка соотношения пользы и
Оценка эффективности мер
Коррекция мер в случае необходимости
Слайд 13Система управления рисками разрабатывается :
Для новых ЛС
Для новых ЛС при
Для ЛС, в отношении которых появились новые данные о безопасности
По требованию контрольно-разрешительных органов
JAMA 2008 Oct. 300 (16); 1887-96
Слайд 14Согласно требованиям закона в странах ЕС и США
Фармацевтические компании обязаны
план управления рисками для каждого нового препарата
JAMA 2008 Oct. 300 (16); 1887-96
Слайд 15План управления рисками
Характеристика безопасности
План фармаконадзора
Оценка необходимости в дополнительных мероприятиях для
Директива ЕС: ICHE2E
Слайд 16Характеристика безопасности лекарств
По данным доклинических испытаний
По данным КИ
Неблагоприятные побочные реакции на
Взаимодействия с ЛС и пищевыми продуктами и травами.
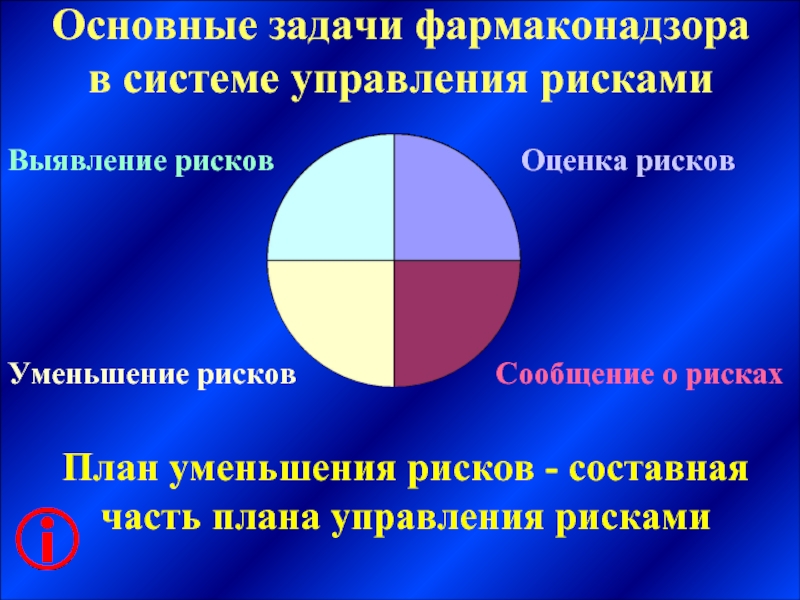
Слайд 17Основные задачи фармаконадзора в системе управления рисками
Оценка рисков
Выявление рисков
Уменьшение рисков
Сообщение о
План уменьшения рисков - составная часть плана управления рисками
Слайд 18 План фармаконадзора
Оценка выявленных значимых рисков
Оценка потенциальных значимых рисков
Определение значимой
недостающей информации
1
2
3
Слайд 19План фармаконадзора
основан на:
Характеристике безопасности ЛС
Описании методов фармаконадзора
Плана действий для оценки выявленных
Слайд 20Меры по снижению рисков при
применении ЛС
Мед.руководства для специалистов и пациентов,
Разъяснение
Ограничение числа назначаемых ЛС,
Информированное согласие,
Учет врачей, назначающих ЛС
Учет пациентов, получающих ЛС
Маркировка упаковки,
Административные решения (ограничение применения ЛС, изм. дозировок и др.)
Внесение предостережения в инструкцию,
Письма-предупреждения для врачей и пациентов,
Образовательные программы и коммуникационные связи.
Слайд 22Мизопростол
Misoprostol – синтетический аналог простагландина Е1.
Используется для профилактики и лечения
В России зарегистрирован под торговыми названиями:
Сайтотек, Миролют, Мизопростол, Мизопростол –ГПМЦ.
Слайд 23Серьезные НПР, возникающие при приеме Мизопростола
Гиперстимуляция матки с вероятностью ее разрыва.
Длительные и обильные кровотечения в постабортном периоде, требующие стационарного лечения.
Вероятность неполных абортов, требующих хирургического вмешательства.
По тератогенности мизопростол отнесен к категории «Х», что означает высокую вероятность рождения ребенка с аномалиями развития и уродствами.
http://www.accessdata.fda.gov/drugsatfda_docs/label/2002/19268slr037.pdf
Слайд 24ЕМЕА рекомендует приостановить действие лицензии на продажу Сибутрамина
Сибутрамин – средство для
В ходе исследования SCOUT* было выявлено повышение риска развития серьезных сердечно - сосудистых осложнений
Полученные данные имеют большое клиническое значение, т.к. у пациентов с избыточной массой тела и ожирением имеется изначально высокий риск развития сердечно - сосудистых осложнений.
Результаты других доступных исследований свидетельствуют о недостаточной эффективности препарата и об отсутствии стойкого эффекта после его отмены. [1]
http://www.ema.europa.eu/home.htm
*Sibutramine Cardiovascular OUTcomes
Слайд 25Административные решения в отношении биопрепаратов
В постмаркетинговый период были внесены изменения в
Меры по уменьшению рисков включали :
46 писем-предостережений, 19 предостережений, выделенных в черной рамке и 17 – непосредственных встреч с профессионалами
Слайд 26Перечень ЛС, в отношении которых разработана СУР (1)
Изотретиноин
Флутиказон
Золпидем
Напроксен
Бупропион
Варениклин
Диклофенак
Метформин
Интерферон бета-1б
Эксенатид
Целекоксиб
Микофенолат
Мелоксикам
Ибупрофен
Тамоксифен
Норфлоксацин
Амиодарон
Нортриптилин
Пароксетин
Пегинтерферон альфа-2а
Эпоэтин альфа
Ципрофлоксацин
Флуоксетин
Фентанил
Сулиндак
Колхицин
Метилфенидат
Рибавирин
Варфарин
Панкреатин
Дулоксетин
Флюразепам
Эфализумаб
Рибавирин
Метоклопрамид
Инфликсимаб
Метилфенидат
Сальматерол
Фенопрофен
Слайд 27Перечень ЛС, в отношении которых разработана СУР (2)
Арипипразол
Венлафаксин
Пимекролимус
Этанерцепт
Абакавир
Икодекстрин
Инсулин
Гемифлоксацин
Пироксикам
Офлоксацин
Формотерол
Адалимумаб
Индометацин
Тамоксифен
Ацитретин
Устекинумаб
Атомоксетин
Будесонид
Нилотиниб
Имипрамин
Тестостерон
Топирамид
Кеторолак
Бозентан
Телбивудин
Невирапин
Ритонавир
Леветирацетам
Телитромицин
Мефлохин
Лопинавир
Ламотриджин
Левофлоксацин
Флувоксамин
Прегабалин
Метоклопрамид
Мифепристон
Эпоэтин – бета
Омализумаб
Оланзапин
Слайд 28Меры, принимаемые для снижения рисков в России
Образовательные программы
Информационные письма, предоставляемые специалистам
Предложения по внесению изменений в инструкцию (для принятия административных решений)
Получение информированного согласия пациента
Подготовка рекомендаций по обеспечению безопасности применения ЛС (Варениклин, Сибутрамин, Золпидем)
Ограничение поставок (только в стационары и отдельные аптеки)
Слайд 29Одновременное применение нескольких НПВС
Пациентке 60 лет, получающей в стационарных условиях терапию
Примечание ФЦМБЛС:
Возможность повышения артериального давления описана в инструкциях по применению данных препаратов.
Причинно-следственная связь между применением ЛС и развитием гипертонического криза - вероятная.
Слайд 30Одновременное применение нескольких НПВС
Пациентку 32 лет с начала января 2010 года
Слайд 31Письма – предупреждения в региональные центры мониторинга безопасности лекарственных средств, 2009
Слайд 32Письма – предупреждения в региональные центры мониторинга безопасности лекарственных средств, 2009
Слайд 33«Большинству людей кажется, что таблетки – это снайперская пуля, без промаха
Е.М. Тареев
Слайд 35Правила управления рисками
Характеристика безопасности
План действия по оценке безопасности
Рекомендации по уменьшению рисков
Оценка
Слайд 36Требования к регистрации биоаналогов
Доказательство сопоставимости с оригиналом
Сопоставимость биоаналогичного продукта рассматривается для:
Лекарственного продукта
Активной субстанции
Недостаточность сравнения по фармакопейной статье либо другим опубликованным данным
Слайд 37Регистрация биоаналогов:
Безопасность - клинические и постмаркетинговые исследования
Безопасность должна быть подтверждена
Изучение иммуногенности
Необходимость предоставления планов управления рисками и фармаконадзора
Слайд 38Регистрация биоаналогов
Проведение доклинических и клинических исследований с целью определения разницы в
Необходимы клинические исследования для доказательства эффективности
Эффективность и безопасность оригинального продукта подтверждается для каждого из показаний к применению
Слайд 39Административные решения в отношении биопрепаратов
В инструкции на 41 биопрепарат из 175,
82 административных решения было принято в отношении этих препаратов (46 «писем – предостережений» специалистам, 17 - коммуникаций с профессионалами, 19 предостережений в черной рамке
JAMA. 2008;300(16):1887-1896.
Слайд 40Меры, принимаемые для снижения рисков в России
Образовательные программы
Информационные письма, предоставляемые специалистам
Предложения по внесению изменений в инструкцию (для принятия административных решений)
Получение информированного согласия пациента
Подготовка рекомендаций по обеспечению безопасности применения ЛС (Варениклин, Сибутрамин, Золпидем)
Ограничение поставок (только в стационары и отдельные аптеки)
Слайд 41Данные меры по снижению рисков при применении ЛС были применены в
Изотретиноин
Талидомид
Мизопростол
Сибутрамин
Рибавирин
Варениклин
Мифепристон
Клозапин
Слайд 42Заключение
В основе фармаконадзора лежат следующие 3 элемента:
Оценка выявленных значимых рисков
Оценка потенциальных
Определение значимой недостающей информации
Слайд 43«Большинству людей кажется, что таблетки – это снайперская пуля, без промаха
Е.М. Тареев