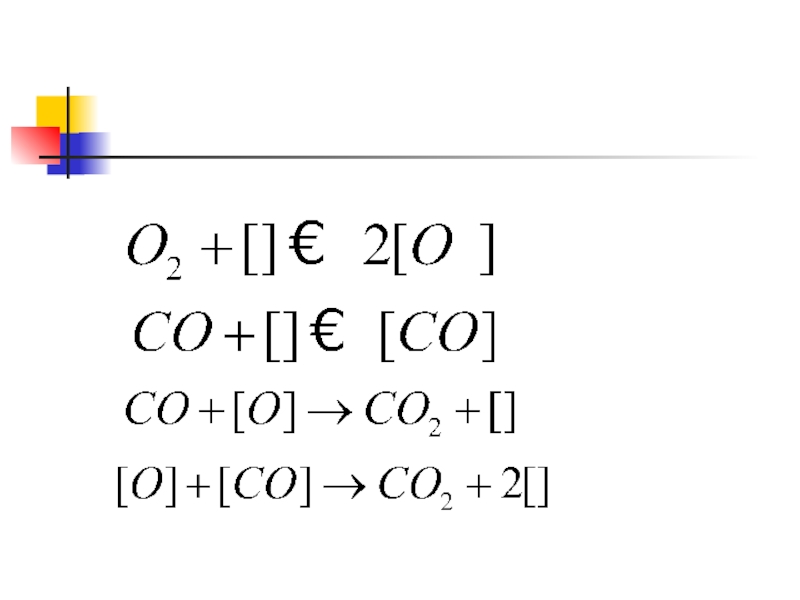- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Реакции окисления.Аспекты катализа презентация
Содержание
- 1. Реакции окисления.Аспекты катализа
- 2. Общие представления о механизме окисления на твердых
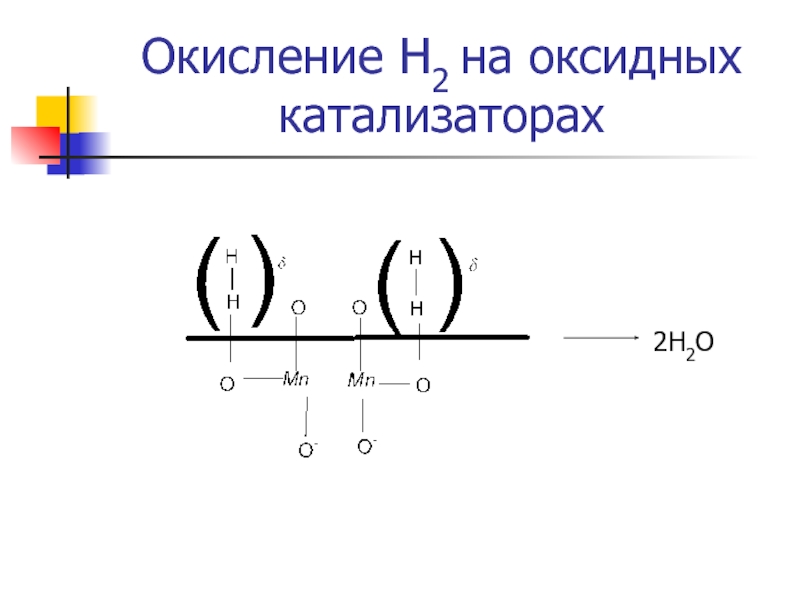
- 4. Окисление Н2 на оксидных катализаторах 2Н2О
- 5. Окисление Н2 на металлических катализаторах 1 вариант О2+2[ ] 2[O] H2+[O] H2O+[ ] Me=Pt, Pd H2O+
- 6. Окисление Н2 на металлических катализаторах 2 вариант
- 7. Каталитическое окисление СО Окисление СО на оксидных катализаторах СО+[O] СО2+[ ] 1/2 О2+[O] [O]
- 8. СО+[O2-]→ CO2+2e 2e+2[V5+]→2[V4+] [V4+] +O2→ [V5+O2-] [V5+O2-]+[V4+]→[V5+O-] [V5+O-]+[ V4+]→2[V5+]+[ O2-] [V5+O2-]+CO→CO2+ [V5+O-] [V5+O-]+ CO→CO2+[V4+]
- 9. Окисление СО на металлах Рогинский, Третьяков
- 11. Конверсия СО водяным паром СО + Н2О
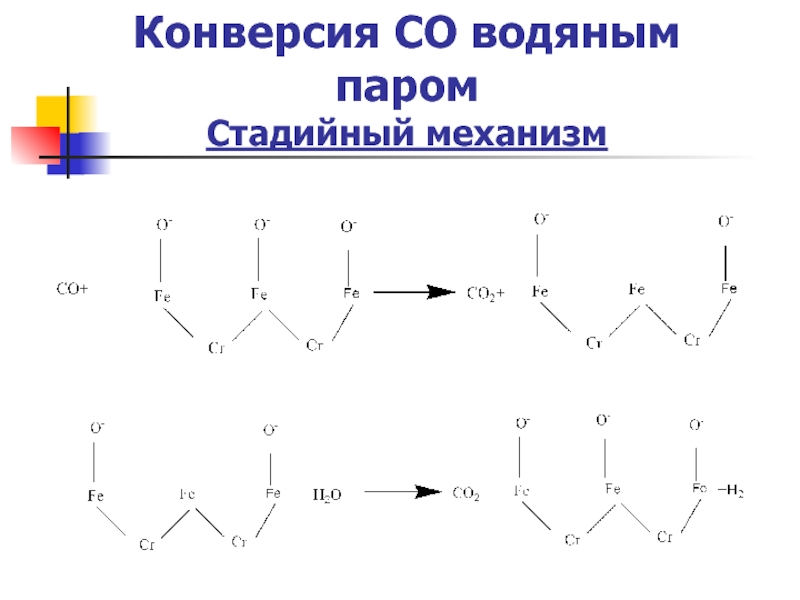
- 12. Конверсия СО водяным паром Стадийный механизм
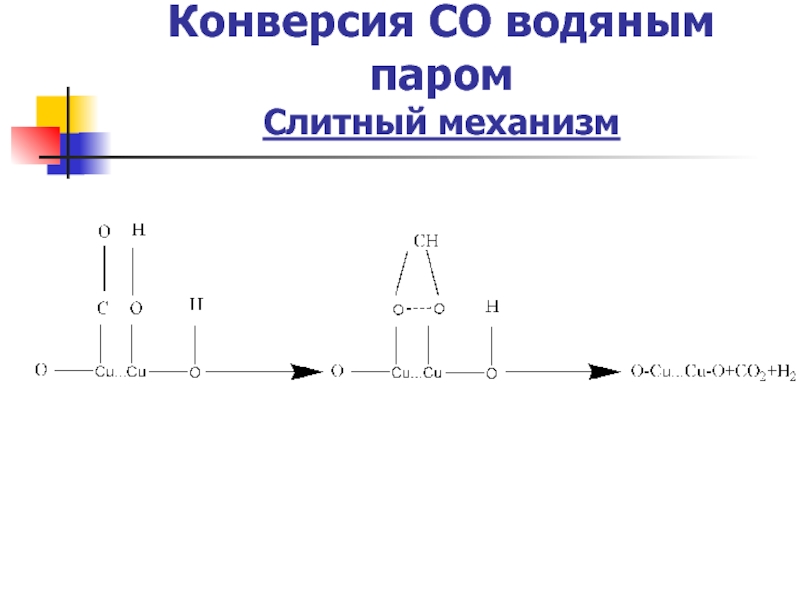
- 13. Конверсия СО водяным паром Слитный механизм
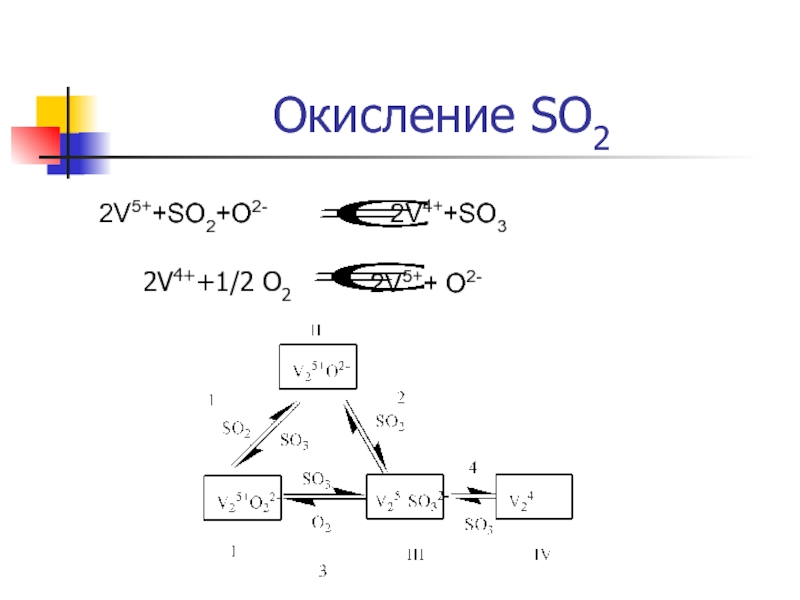
- 14. Окисление SO2 2V5++SO2+O2- 2V4++SO3 2V5++ O2- 2V4++1/2 O2
Слайд 2Общие представления о механизме окисления на твердых катализаторах
При окислении молекулярным кислородом
основным энергетическим препятствием является разрыв связи между атомами кислорода этот переход облегчается присоединением к кислороду электрона, и можно предполагать последовательное образование на поверхности катализатора следующих форм кислорода:
О2
О-2
О-
О2-


![Окисление Н2 на металлических катализаторах1 вариантО2+2[ ] 2[O]H2+[O] H2O+[ ]Me=Pt, PdH2O+](/img/tmb/3/293570/40926f7697b320e6902b0f774ee1ee1a-800x.jpg)
![Окисление Н2 на металлических катализаторах2 вариантH2+2[O] 2[OH]H2+2[OH] 2H2O+2[ ]Me=AgO2+2[O] 2[O]H2+2[ ] 2[ H][O]+2[H] H2O+3[ ]H2+[O] H2O+[ ]](/img/tmb/3/293570/35b2fd26674469ce4efbcda13cdf2043-800x.jpg)
![Каталитическое окисление СООкисление СО на оксидных катализаторах СО+[O] СО2+[ ] 1/2 О2+[O] [O]](/img/tmb/3/293570/b2cf817eadd01a96ec11834790bc3766-800x.jpg)
![СО+[O2-]→ CO2+2e2e+2[V5+]→2[V4+][V4+] +O2→ [V5+O2-][V5+O2-]+[V4+]→[V5+O-][V5+O-]+[ V4+]→2[V5+]+[ O2-][V5+O2-]+CO→CO2+ [V5+O-][V5+O-]+ CO→CO2+[V4+]](/img/tmb/3/293570/1cf004050a3f44297359442e2a0dd4a2-800x.jpg)