- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Процессы и аппараты обогащения. Флотация презентация
Содержание
- 1. Процессы и аппараты обогащения. Флотация
- 2. Флотация Единственный производительный процесс обогащения тонковкрапленных руд
- 3. Принцип флотации основан на свойстве поверхности проф. Игнаткина В.А.,2017
- 4. Флотация Положительные моменты Высокая степень концентрирования Высокая
- 5. Подготовка руды к флотации Измельчение до минус
- 6. Фазы при флотации Твердая (поверхность минерала, осадок
- 7. Виды флотации Масляная «Г-М-Т» Пленочная «Г-Ж-Т» Пенная «Г-Ж-Т» проф. Игнаткина В.А.,2017
- 8. проф. Игнаткина В.А.,2017 Вероятность образования флотокомплекса «пузырек-частица»
- 9. Мера смачиваемости Wa = σ ж
- 10. проф. Игнаткина В.А.,2017 Значения краевых углов смачивания (в градусах)
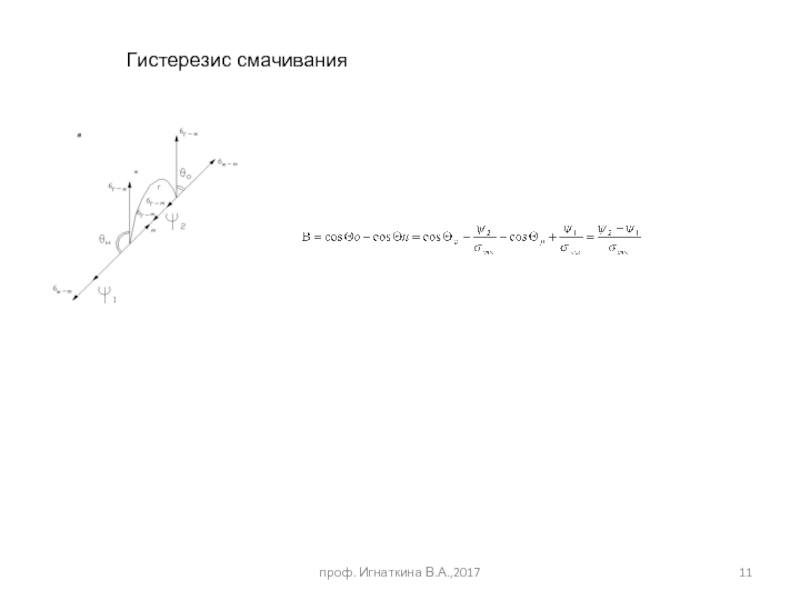
- 11. проф. Игнаткина В.А.,2017 Гистерезис смачивания
- 12. Термодинамика элементарного акта флотации Е1 = Sж-г
- 13. проф. Игнаткина В.А.,2017 h5 = hт
- 14. 1, 2 – переходные слои на поверхности
- 15. —
- 16. проф. Игнаткина В.А.,2017 – толщина плотной части
- 17. ХС – химические связи ВС –
- 18. π a σж-г Sin θ = ρgVпуз
- 19. Аполярные Полярные Минералы Сульфиды Несульфиды
- 20. Состояние поверхности минералов в воде Аполярные, тальк
- 21. Регуляторы среды Подавители Активаторы Собиратели пенообразователь Порядок подачи Флотореагенты проф. Игнаткина В.А.,2017
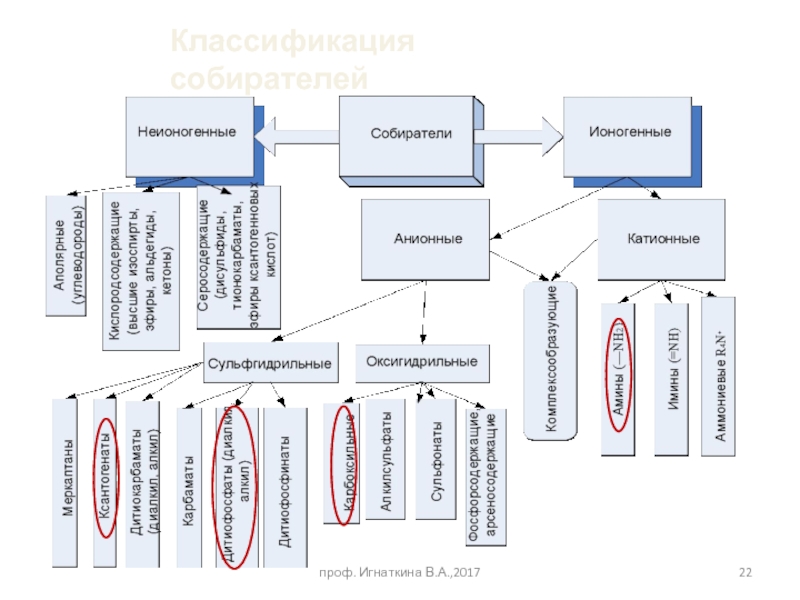
- 22. Классификация собирателей проф. Игнаткина В.А.,2017
- 23. Требования к собирателям Технологическая эффективность Низкая токсичность
- 24. Сульфидные минералы Сульфгидрильные собиратели Несульфидные минералы Оксигидрильные
- 25. Традиционные широко используемые собиратели При флотации сульфидов
- 26. Ксантогенаты
- 27. ROH + KOH + CS2
- 28. Регуляторы среды рН проф. Игнаткина В.А.,2017
- 29. Сводная информация по регуляторам среды проф. Игнаткина В.А.,2017 рК1=6,37 рК2=10,33
- 30. Подавители Механизмы действия Вытеснение собирателя (ПР) -
- 31. Активаторы Соли меди для повышения вероятности закрепления
- 32. Сводная информация по активаторам флотации проф. Игнаткина В.А.,2017
- 33. Модификаторы сульфидных руд Сернистый натрий - Na2S
- 34. Модификаторы несульфидных руд Жидкое стекло Na2SiO3 Крахмал КМЦ Полифосфаты проф. Игнаткина В.А.,2017
- 35. Активные центры на поверхности Активными центрами являются
- 36. I – объем сульфида; II –закрепление
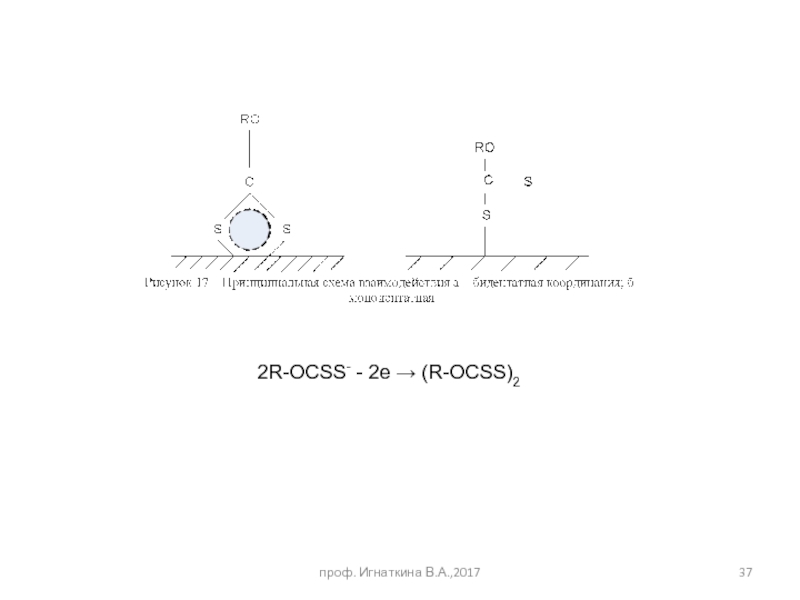
- 37. проф. Игнаткина В.А.,2017 2R-OCSS- - 2e → (R-OCSS)2
- 38. Успех элементарного акта флотации зависит от Присутствия
- 39. проф. Игнаткина В.А.,2017
- 40. Собиратели для несульфидных минералов и руд Олеиновая
- 41. проф. Игнаткина В.А.,2017 ИМ 50 R =
- 42. проф. Игнаткина В.А.,2017 R-NH2 +H+ → [RNH3]+
- 43. Пенообразователь Повышает дисперсность газовой фазы Препятствует коалесценции
- 44. 2-х фазная пена Ж-Г
- 45. в–пленочная пена (по В.И. Классену)[7] б-агрегатная пена
- 46. ОПСБ С4Н9-[CH2-CH-O]n-OH CH3 МИБК CH3-CH2-CH2-CH-CH3 CH3 OH
- 47. В упрощенном виде скорость флотации может быть
- 48. Способы насыщения воздухом Специальными устройствами (механические,
- 49. Классификация флотационных машин механические,
- 50. механическая (а), пневмомеханическая (б) и пневматическая флотомашина
- 51. проф. Игнаткина В.А.,2017 Операции флотации Основная Контрольная
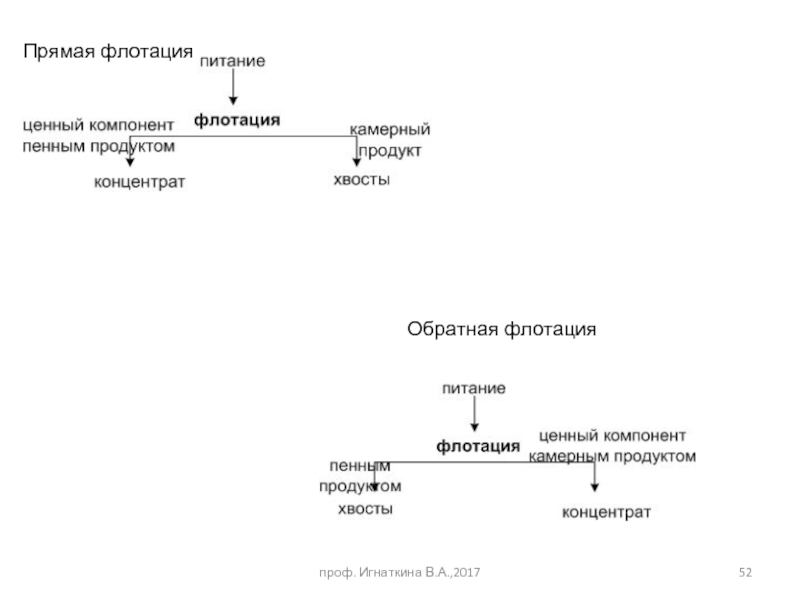
- 52. проф. Игнаткина В.А.,2017 Прямая флотация Обратная флотация
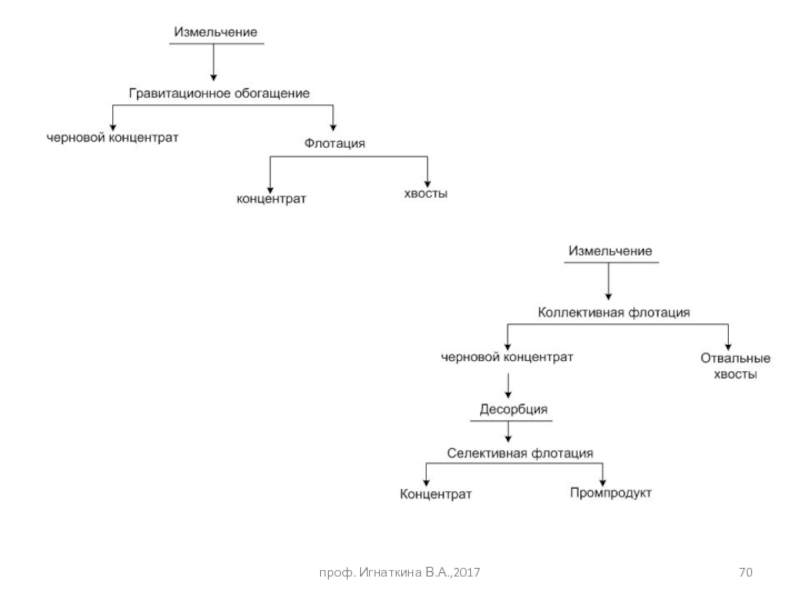
- 53. Прямая селективная флотация проф. Игнаткина В.А.,2017
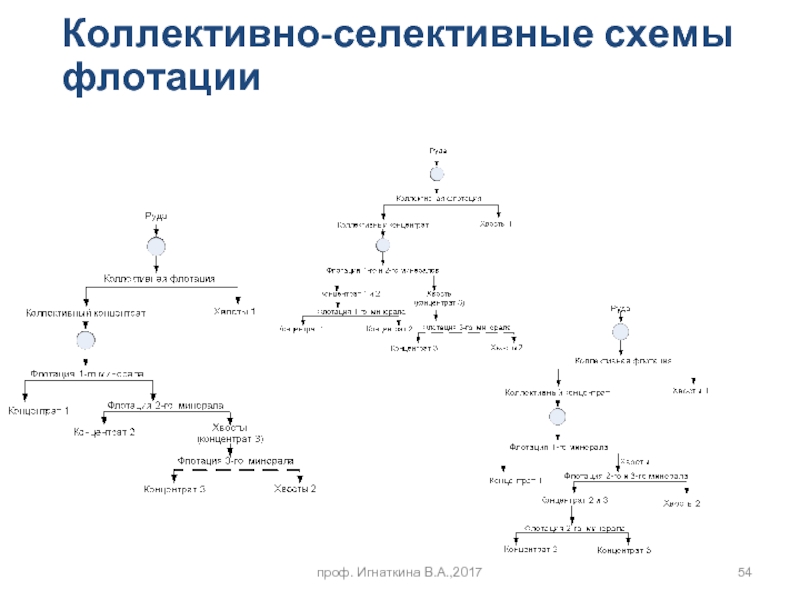
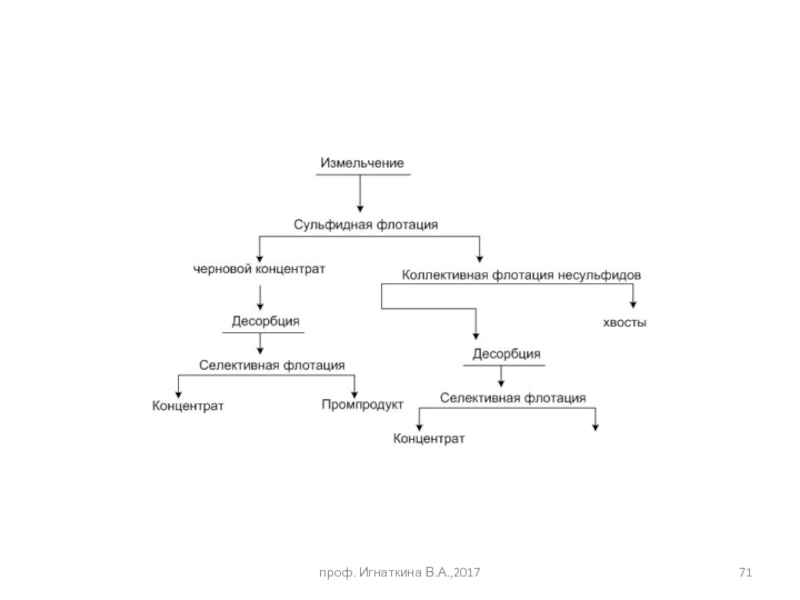
- 54. проф. Игнаткина В.А.,2017 Коллективно-селективные схемы флотации
- 55. Межцикловая флотация Неравномерная вкрапленность, наличие легко шламуемых и окисляемых (вторичные сульфиды меди) проф. Игнаткина В.А.,2017
- 56. Типизация руд, минералов
- 57. Сульфидные руды Сульфидные минералы - основной источник
- 58. Основные медные минералы проф. Игнаткина В.А.,2017
- 59. проф. Игнаткина В.А.,2017 Требования к медным концентратам
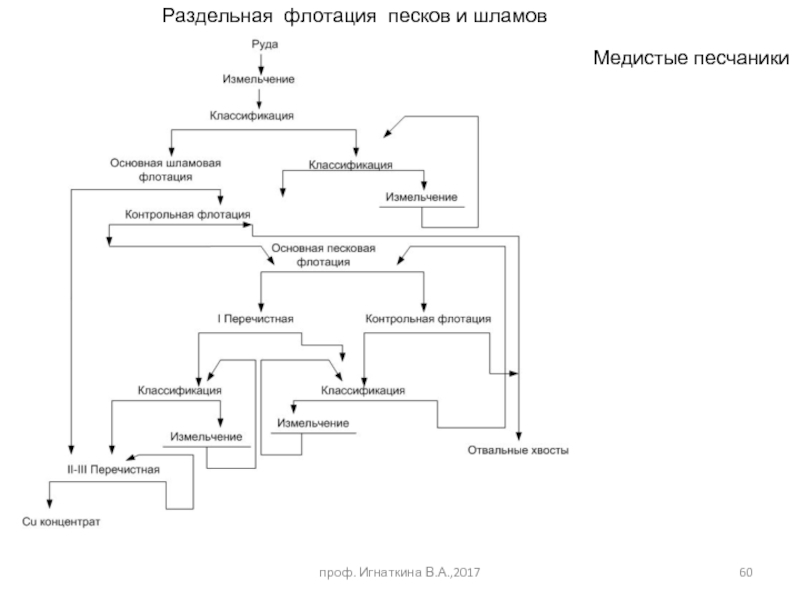
- 60. Раздельная флотация песков и шламов Медистые песчаники проф. Игнаткина В.А.,2017
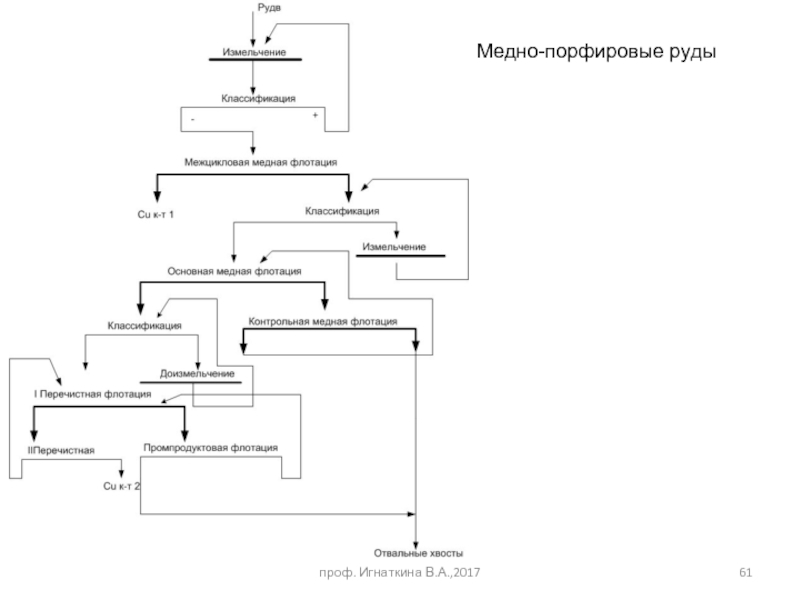
- 61. проф. Игнаткина В.А.,2017 Медно-порфировые руды
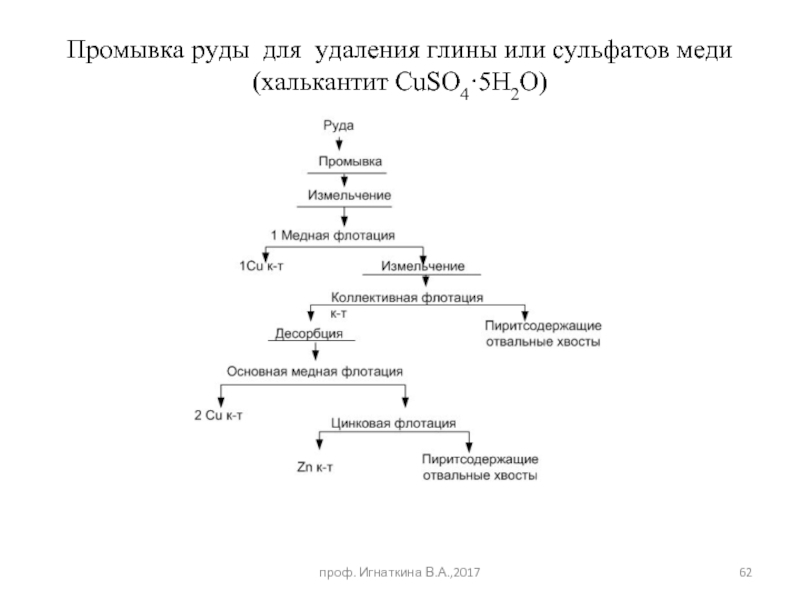
- 62. Промывка руды для удаления глины или сульфатов
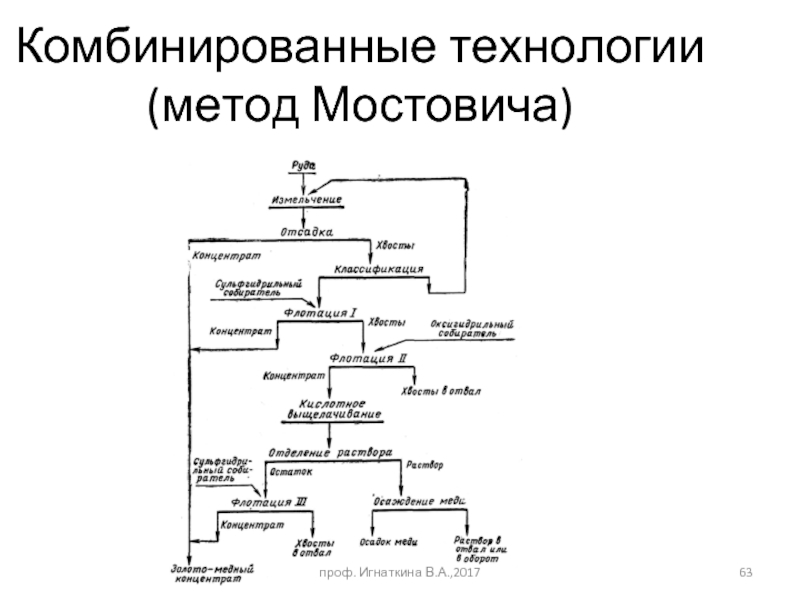
- 63. Комбинированные технологии (метод Мостовича) проф. Игнаткина В.А.,2017
- 64. Полярные несульфиды Оксиды (Fe2O3, FeTiO3, MnO2, лопарит
- 65. Реагентные режимы несульфидных руд Регуляторы среды (кислоты
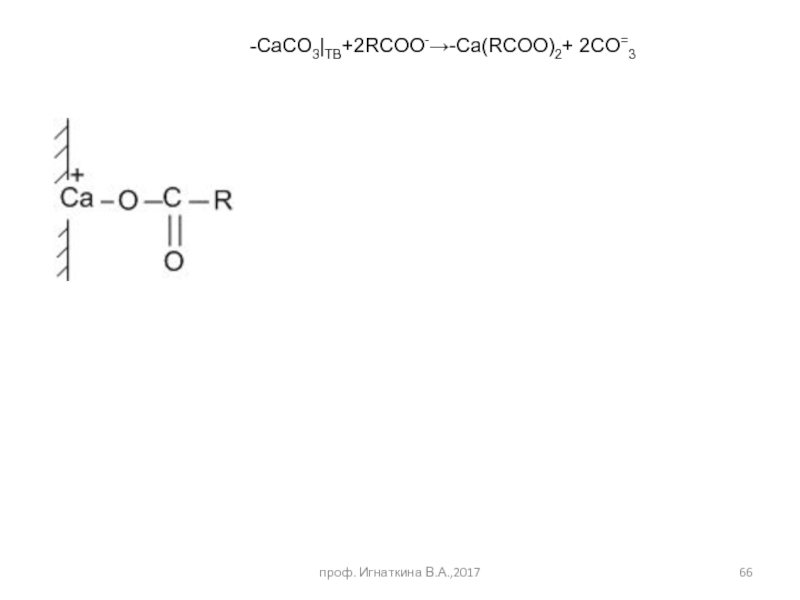
- 66. -CaCO3|ТВ+2RCOO-→-Ca(RCOO)2+ 2CO=3 проф. Игнаткина В.А.,2017
- 67. Особенности использования производных карбоновых кислот Мицелообразование –
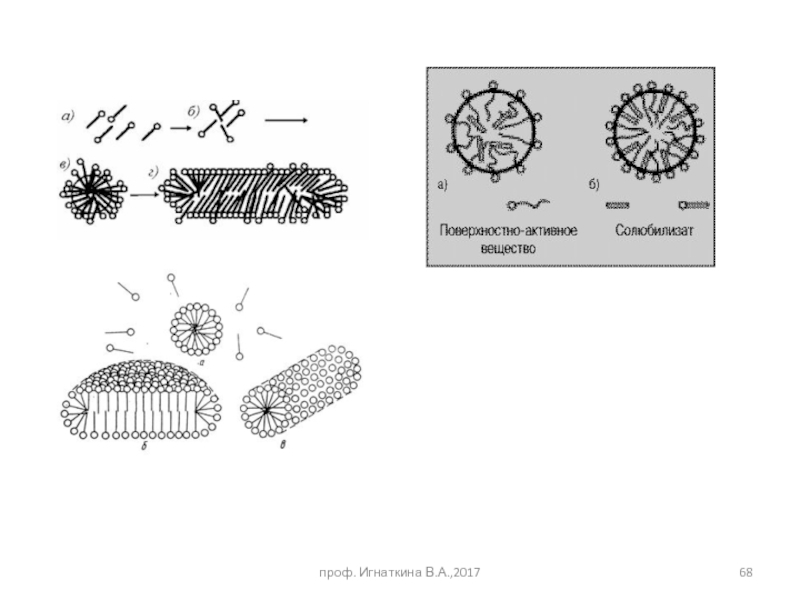
- 68. проф. Игнаткина В.А.,2017
- 69. Плавиковая кислота HF активирует полевые шпаты Берилл
- 70. проф. Игнаткина В.А.,2017
- 71. проф. Игнаткина В.А.,2017
- 72. Высокотемпературные воздействия Обжиг для разрушения кальцита,
- 73. Десорбция с применением пропарки сульфиды Высокотемпературная в
- 74. проф. Игнаткина В.А.,2017 Характеристика минералов (фазовый), содержание компонента, вкрапленность Прямая селективная или коллективно-селективная ?
- 75. проф. Игнаткина В.А.,2017 Неравномерная вкрапленность минералов, хрупкость минералов Стадиальное измельчение
- 76. проф. Игнаткина В.А.,2017 Неравномерное гранулометрическое распределение минералов
- 77. Флотация Железные руды Получение суперконцентратов угли Флотация шламов (селективная флокуляция) проф. Игнаткина В.А.,2017
Слайд 2Флотация
Единственный производительный процесс обогащения тонковкрапленных руд
Флотация позволяет выделить из полезных ископаемых
Процесс извлечения твердых минеральных частиц (реже жидких) из тонкодисперсных трехфазных систем, основан на различиях разделяемых частиц по смачиванию водой. Плохо смачиваемые водой (гидрофобные) частицы при столкновении с воздушными пузырьками концентрируются на поверхности раздела фаз Ж- Г и выводятся из пульпы в пену.
проф. Игнаткина В.А.,2017
Слайд 4Флотация
Положительные моменты
Высокая степень концентрирования
Высокая производительность
Высокая селективность разделения
Отрицательные моменты
Высокие удельные расходы воды
Организация складирования отходов флотационного обогащения (выход хвостов от 60 до 98 %)
Потери ценных компонентов со сростками (>100 мкм) и шламами (< 20 (10) мкм)
проф. Игнаткина В.А.,2017
Слайд 5Подготовка руды к флотации
Измельчение до минус 0,1 мм
Разбавление водой до содержания
проф. Игнаткина В.А.,2017
Слайд 6Фазы при флотации
Твердая (поверхность минерала, осадок и т.д.)
Жидкая (вода, реже «масло-вода»,
Газовая (воздух, кислород, азот, углекислый газ и др.)
проф. Игнаткина В.А.,2017
Слайд 8проф. Игнаткина В.А.,2017
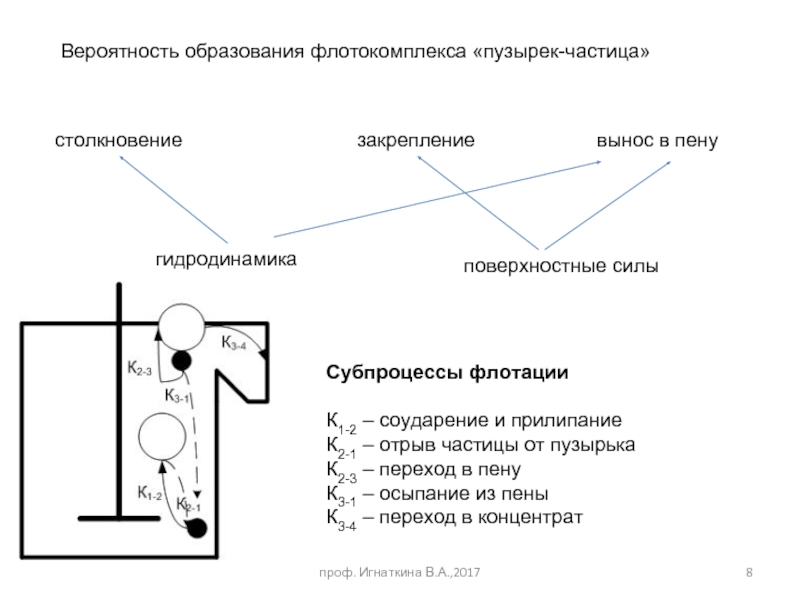
Вероятность образования флотокомплекса «пузырек-частица»
столкновение
закрепление
вынос в пену
гидродинамика
поверхностные силы
Субпроцессы флотации
К1-2 –
К2-1 – отрыв частицы от пузырька
К2-3 – переход в пену
К3-1 – осыпание из пены
К3-4 – переход в концентрат
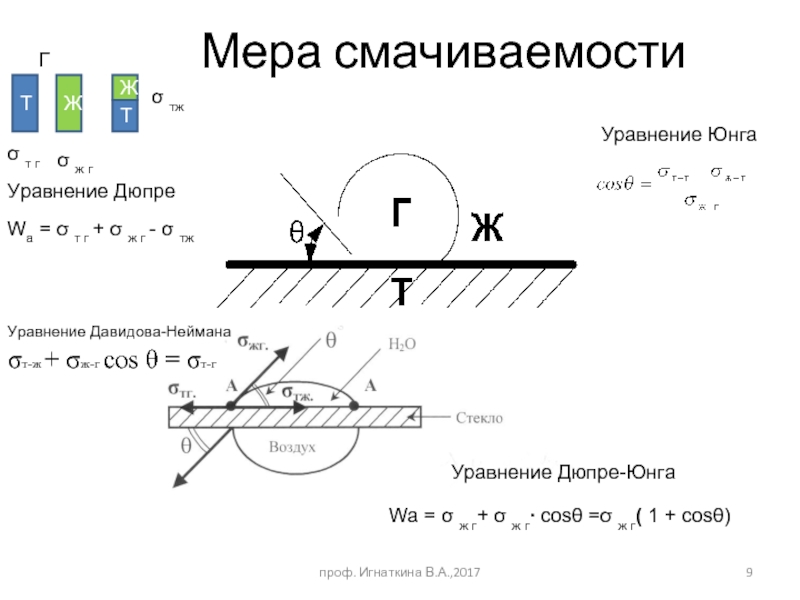
Слайд 9Мера смачиваемости
Wa = σ ж г+ σ ж г∙ cosθ =σ
Wa = σ т г + σ ж г - σ тж
проф. Игнаткина В.А.,2017
σт-ж + σж-г сos θ = σт-г
Уравнение Давидова-Неймана
Уравнение Юнга
Уравнение Дюпре-Юнга
Уравнение Дюпре
Т
Ж
Г
Т
Ж
σ т г
σ ж г
σ тж
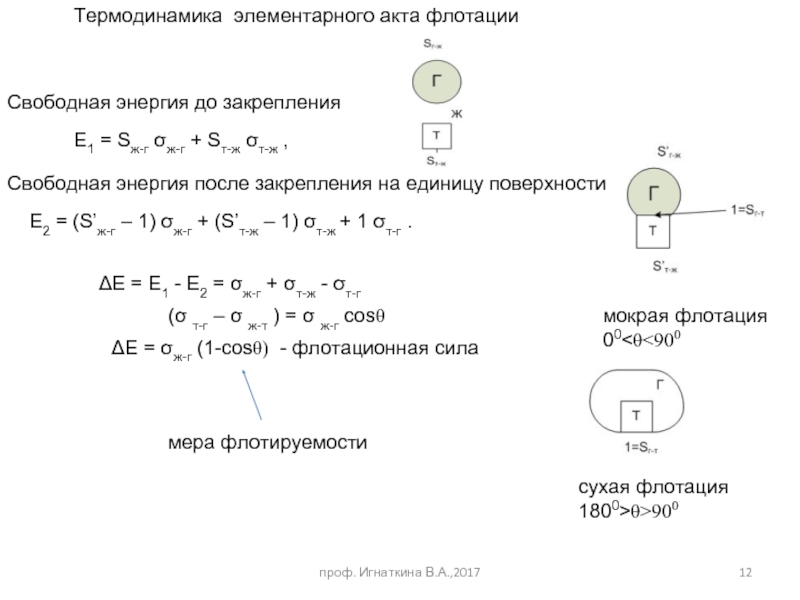
Слайд 12Термодинамика элементарного акта флотации
Е1 = Sж-г σж-г + Sт-ж σт-ж ,
Свободная энергия до закрепления
Е2 = (S’ж-г – 1) σж-г + (S’т-ж – 1) σт-ж + 1 σт-г .
Свободная энергия после закрепления на единицу поверхности
ΔЕ = Е1 - Е2 = σж-г + σт-ж - σт-г
(σ т-г – σ ж-т ) = σ ж-г cosθ
ΔЕ = σж-г (1-cosθ) - флотационная сила
мера флотируемости
мокрая флотация
00<θ<900
сухая флотация
1800>θ>900
проф. Игнаткина В.А.,2017
Слайд 13проф. Игнаткина В.А.,2017
h5 = hт + hп
[h5 - h4]
Кинетическая
mv2/r
Гидродинамика потока
[h4 - h3]
Самопроизвольное уменьшение энергии
[h3 – h2]
толщина прослоя скачком утончается и разрывается
h1
остаточный слой
имеет молекулярные размеры и является термодинамически устойчивым, соответствуя минимуму свободной энергии.
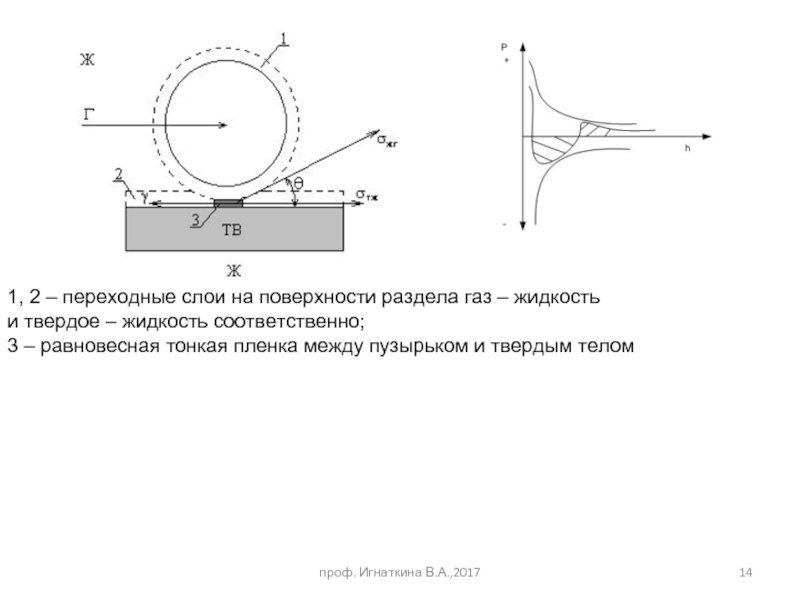
Слайд 141, 2 – переходные слои на поверхности раздела газ – жидкость
и твердое – жидкость соответственно;
3 – равновесная тонкая пленка между пузырьком и твердым телом
проф. Игнаткина В.А.,2017
Слайд 15
— молекулярная составляющая, обусловленная вандерваальсовыми силами ;
—
— электростатическая составляющая, возникающая при перекрытии (или деформации);
толщина диффузионного слоя; мкм
1000 А0
10-100 нм
проф. Игнаткина В.А.,2017
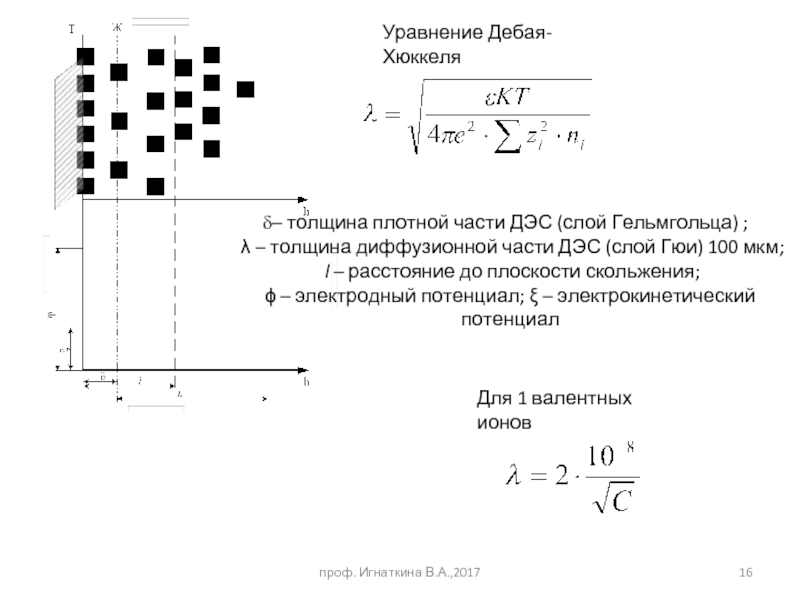
Слайд 16проф. Игнаткина В.А.,2017
– толщина плотной части ДЭС (слой Гельмгольца) ;
λ
l – расстояние до плоскости скольжения;
ϕ – электродный потенциал; ξ – электрокинетический потенциал
Уравнение Дебая-Хюккеля
Для 1 валентных ионов
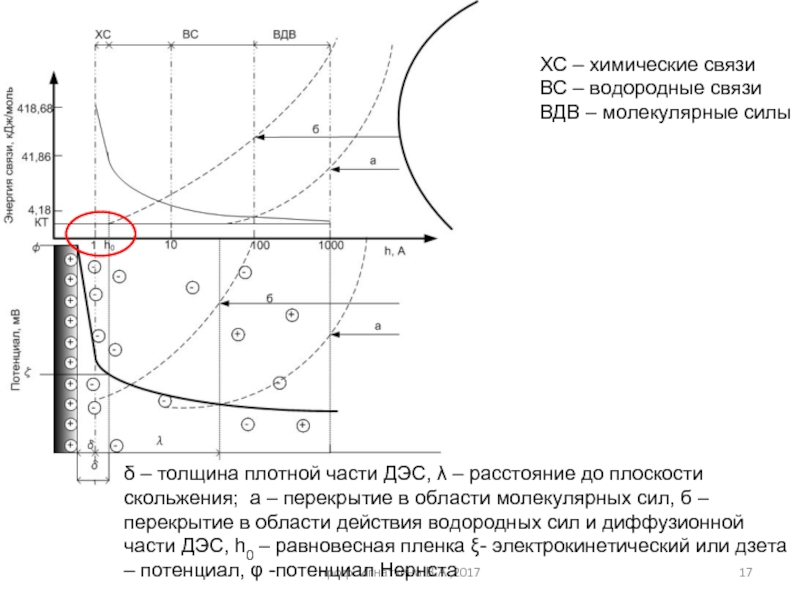
Слайд 17
ХС – химические связи
ВС – водородные связи
ВДВ – молекулярные силы
проф. Игнаткина
ИИλλ
δ – толщина плотной части ДЭС, λ – расстояние до плоскости скольжения; а – перекрытие в области молекулярных сил, б – перекрытие в области действия водородных сил и диффузионной части ДЭС, h0 – равновесная пленка ξ- электрокинетический или дзета – потенциал, φ -потенциал Нернста
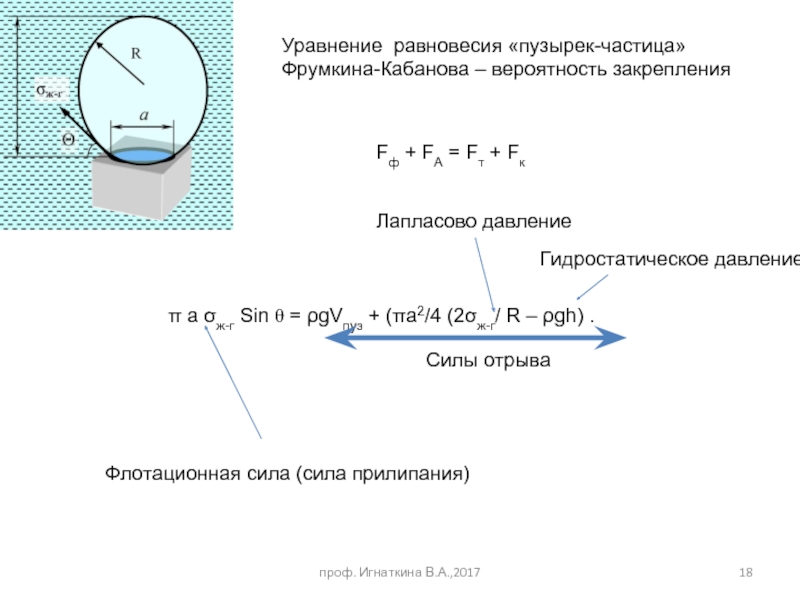
Слайд 18π a σж-г Sin θ = ρgVпуз + (πa2/4 (2σж-г/ R
Уравнение равновесия «пузырек-частица»
Фрумкина-Кабанова – вероятность закрепления
Флотационная сила (сила прилипания)
Силы отрыва
Fф + FА = Fт + Fк
проф. Игнаткина В.А.,2017
Лапласово давление
Гидростатическое давление
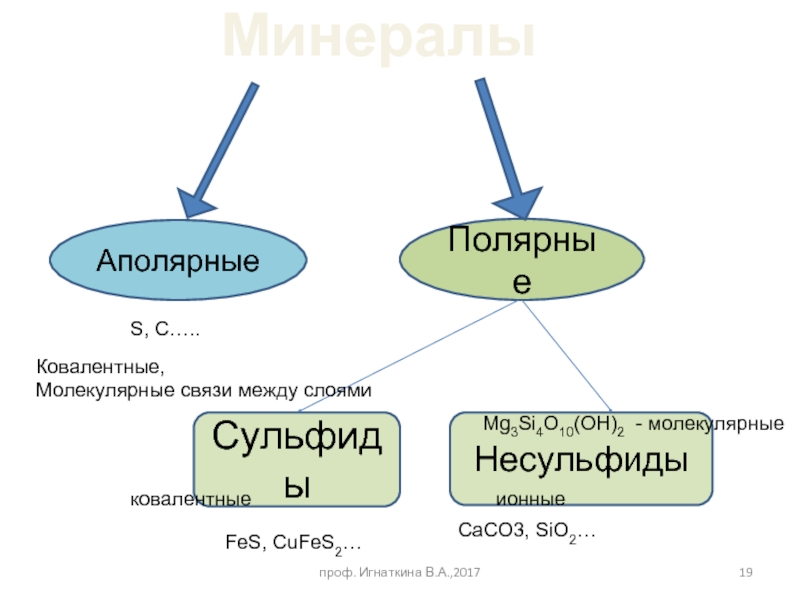
Слайд 19Аполярные
Полярные
Минералы
Сульфиды
Несульфиды
проф. Игнаткина В.А.,2017
S, C…..
FeS, CuFeS2…
CaCO3, SiO2…
Ковалентные,
Молекулярные связи между слоями
ковалентные
ионные
Mg3Si4O10(OH)2 - молекулярные
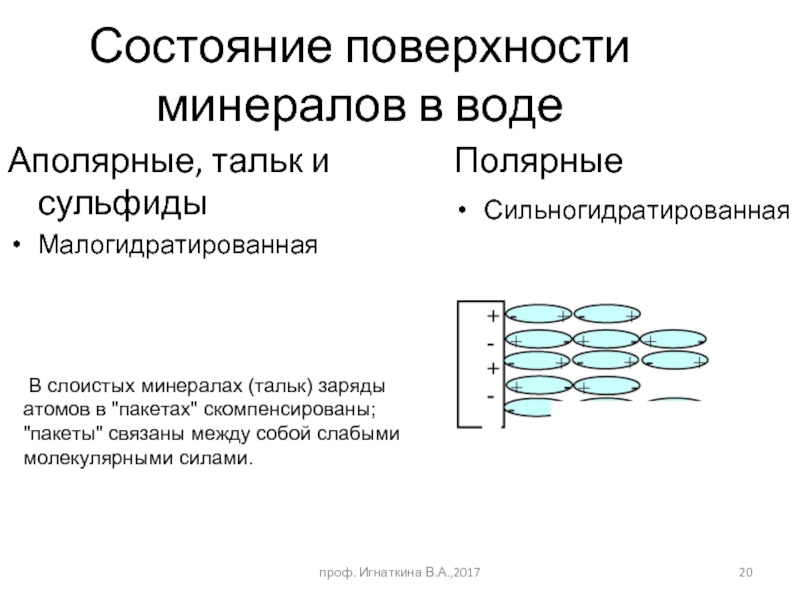
Слайд 20Состояние поверхности минералов в воде
Аполярные, тальк и сульфиды
Малогидратированная
Полярные
Сильногидратированная
проф. Игнаткина В.А.,2017
В
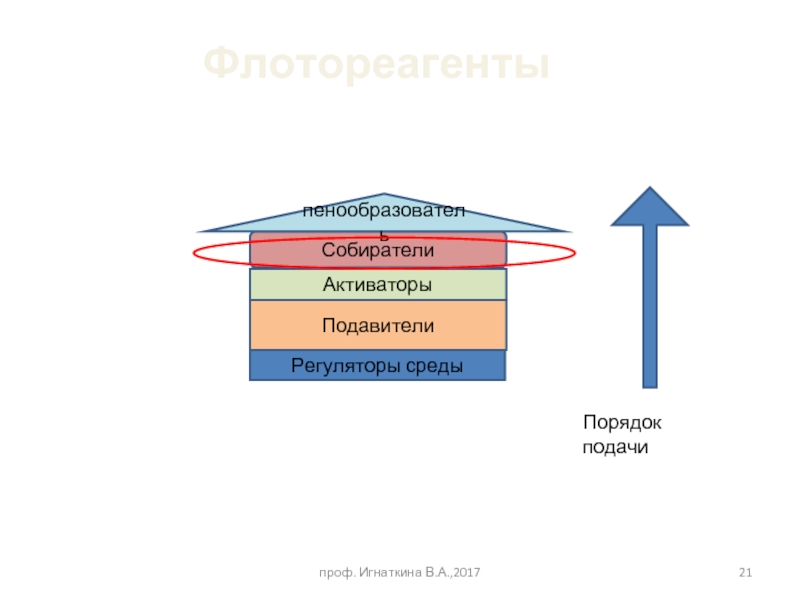
Слайд 21Регуляторы среды
Подавители
Активаторы
Собиратели
пенообразователь
Порядок подачи
Флотореагенты
проф. Игнаткина В.А.,2017
Слайд 23Требования к собирателям
Технологическая эффективность
Низкая токсичность (3,4 класс)
Промышленное производство
Доступная стоимость
проф. Игнаткина В.А.,2017
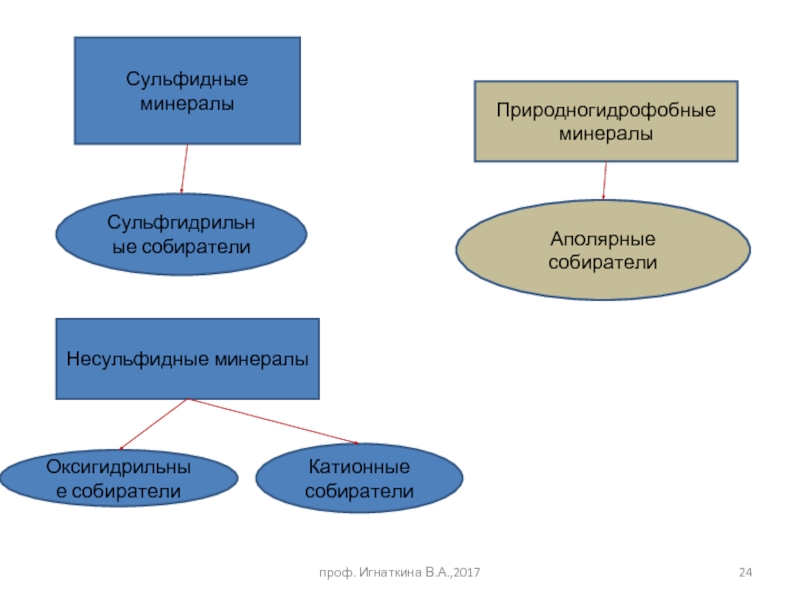
Слайд 24Сульфидные минералы
Сульфгидрильные собиратели
Несульфидные минералы
Оксигидрильные собиратели
Катионные собиратели
Аполярные собиратели
Природногидрофобные минералы
проф. Игнаткина В.А.,2017
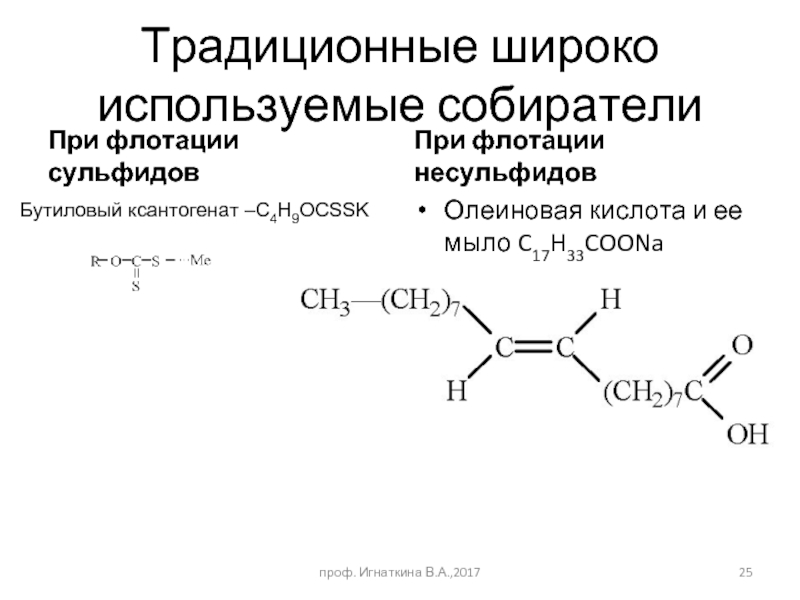
Слайд 25Традиционные широко используемые собиратели
При флотации сульфидов
При флотации несульфидов
Олеиновая кислота и ее
проф. Игнаткина В.А.,2017
Бутиловый ксантогенат –С4H9OCSSK
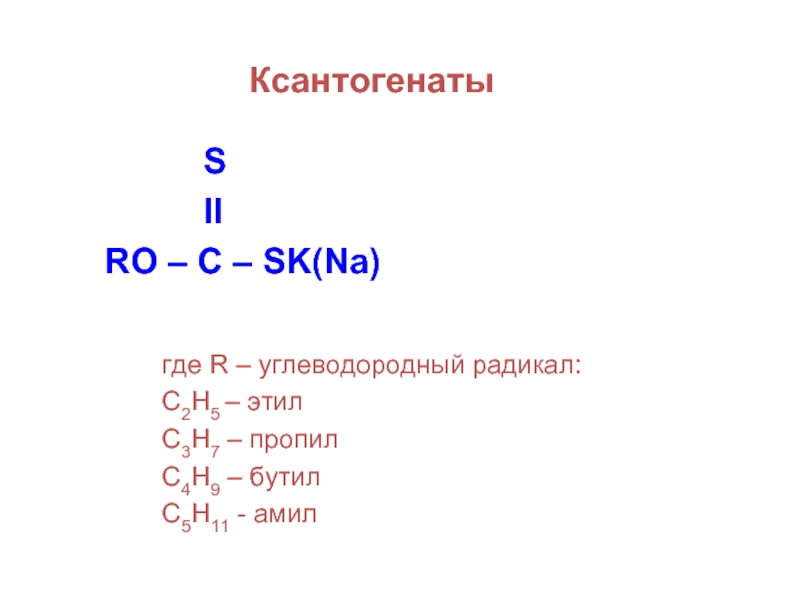
Слайд 26Ксантогенаты
S
RO – C – SK(Na)
где R – углеводородный радикал:
С2Н5 – этил
С3Н7 – пропил
С4Н9 – бутил
С5Н11 - амил
Слайд 27
ROH + KOH + CS2 = ROCSSK
Диссоциация
ROCSSK
Окисление
2ROCSSK - 2e (ROCSS)-2 + 2K+
Синтез
Слайд 30Подавители
Механизмы действия
Вытеснение собирателя (ПР) - Na2S
Окисление или восстановление поверхности минералов (кислород
Растворение (цианид NaCN)
Гидрофилизация без вытеснения собирателя (КМЦ, крахмал, Na2SiO3)
проф. Игнаткина В.А.,2017
Слайд 31Активаторы
Соли меди для повышения вероятности закрепления ионогенных собирателей (CuSO4)
Кислоты (H2SO4, HF)
Кремнефтористый
проф. Игнаткина В.А.,2017
Слайд 33Модификаторы сульфидных руд
Сернистый натрий - Na2S
Гидросульфид натрия NaHS
Бисульфит натрия NaHSO3
Натрий персульфат,
Тиосульфат натрия Na2S2O3
Метабисульфит натрия Na2S2O5
Сернистый газ SO2
МФТК – низкомолекулярный депрессор сульфидов меди и пирита на основе тиокарбаминовой кислоты
Модифицированный КМЦ
проф. Игнаткина В.А.,2017
Слайд 34Модификаторы несульфидных руд
Жидкое стекло Na2SiO3
Крахмал
КМЦ
Полифосфаты
проф. Игнаткина В.А.,2017
Слайд 35Активные центры на поверхности
Активными центрами являются анионы, катионы, атомы с ненасыщенными
Активными центрами поверхности являются также макро- и микродефекты кристаллической структуры твердых тел. Макродефекты - микротрещины и микропоры, а также межкристаллические границы зерен; микродефекты - это нарушение стехиометрического состава кристаллов, а также нарушение в периодичности расположения атомов в кристаллической решетке (линейные и винтовые дислокации).
Поверхностные соединения образуются в результате конкуренции молекул воды с ионами и молекулами флотореагентов за активные центры
проф. Игнаткина В.А.,2017
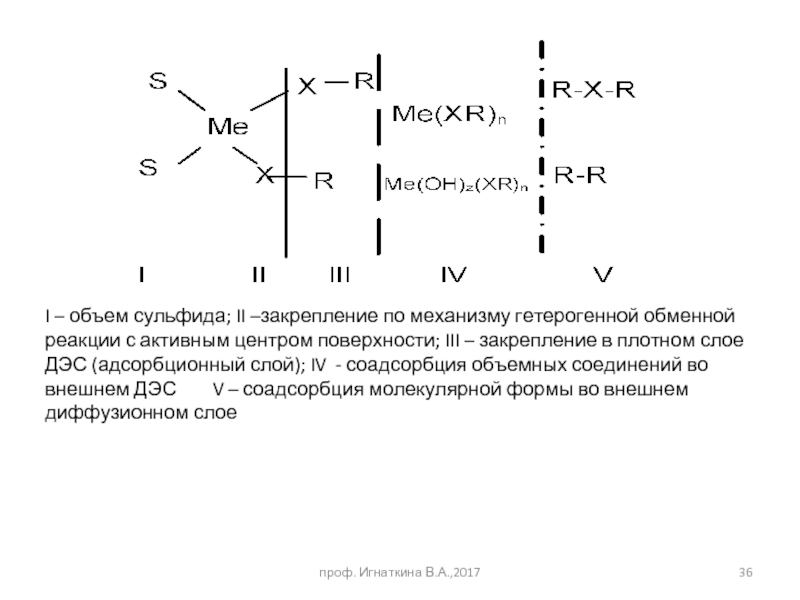
Слайд 36
I – объем сульфида; II –закрепление по механизму гетерогенной обменной реакции
проф. Игнаткина В.А.,2017
Слайд 38Успех элементарного акта флотации зависит от
Присутствия на минерале 2-х форм сорбции
Создание условий достижения точки нулевого заряда поверхности (ТНЗ), когда электрокинетический потенциал поверхности (ЭКП) равен нулю, а величина свободной поверхностной энергии максимальна.
проф. Игнаткина В.А.,2017
Слайд 40Собиратели для несульфидных минералов и руд
Олеиновая кислота или олеат натрия –
Заменители олеиновой кислоты – таловые масла, синтетические жирные кислоты С12-С18 ненасыщенные карбоновые кислоты и их мыла
Алкилсульфаты, алкилсульфонаты – ROSO3; RSO3
Производные фосфорных кислот
Катионные собиратели
проф. Игнаткина В.А.,2017
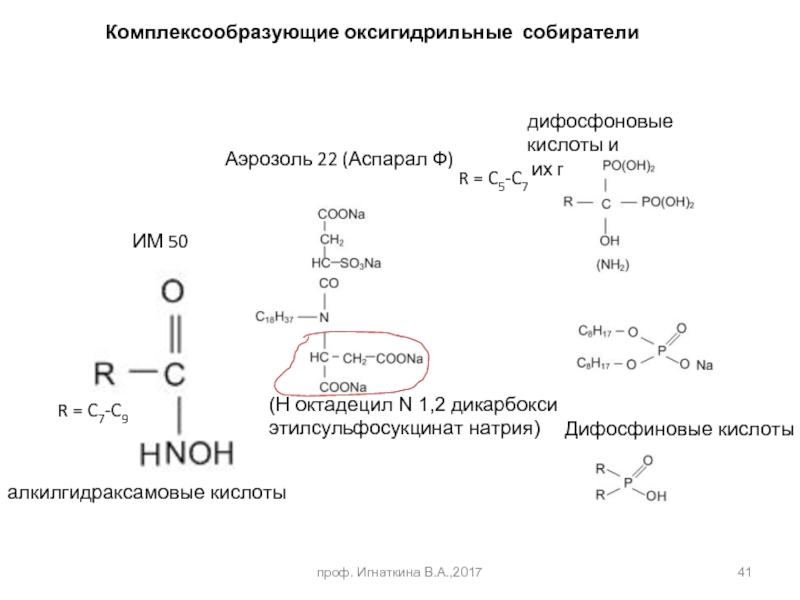
Слайд 41проф. Игнаткина В.А.,2017
ИМ 50
R = C7-C9
Аэрозоль 22 (Аспарал Ф)
дифосфоновые кислоты и
R = C5-C7
Комплексообразующие оксигидрильные собиратели
(Н октадецил N 1,2 дикарбокси этилсульфосукцинат натрия)
алкилгидраксамовые кислоты
Дифосфиновые кислоты
Слайд 42проф. Игнаткина В.А.,2017
R-NH2 +H+ → [RNH3]+
Kd =4,3·10-4
Катионные собиратели закрепляются в ДЭС,
HCOOH
HCl
Слайд 43Пенообразователь
Повышает дисперсность газовой фазы
Препятствует коалесценции пузырьков
Снижает скорость подъема пузырька – увеличивает
Увеличивает прочность пузырька и устойчивость пены при подъеме
Собирательное действие пенообразователей
проф. Игнаткина В.А.,2017
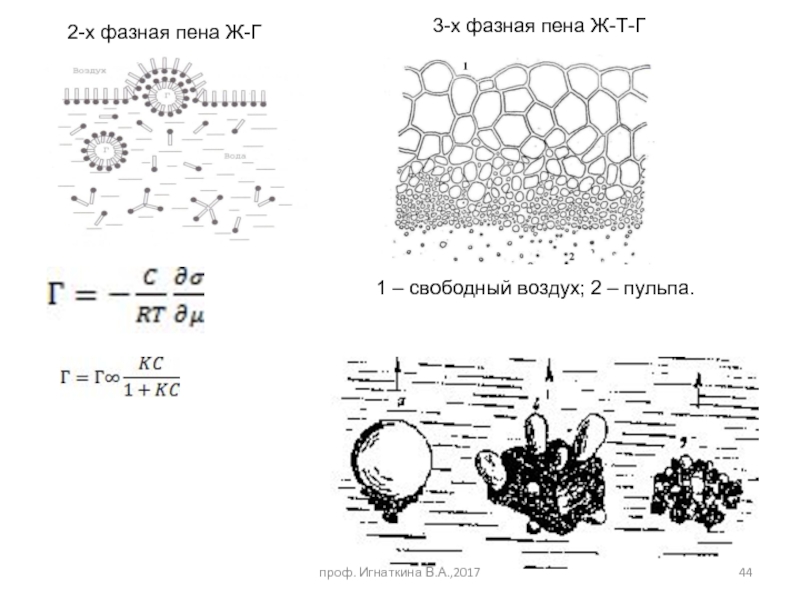
Слайд 442-х фазная пена Ж-Г
1 – свободный воздух; 2 – пульпа.
3-х фазная
проф. Игнаткина В.А.,2017
Слайд 45в–пленочная пена (по В.И. Классену)[7]
б-агрегатная пена
а–пленочно-структурная пена
Строение пенного слоя
проф. Игнаткина В.А.,2017
Слайд 46ОПСБ
С4Н9-[CH2-CH-O]n-OH
CH3
МИБК
CH3-CH2-CH2-CH-CH3
CH3
OH
терпинеол
С10H17OH
T-80
диоксановые
и
пирановые
Фенольные – нейтральная среда
Спиртовые – щелочная
Алкилсульфаты - слабокислая
OH, C=O, COO,
проф. Игнаткина В.А.,2017
Слайд 47В упрощенном виде скорость флотации может быть определена как (уравнение Белоглазова):
ln
проф. Игнаткина В.А.,2017
1 – постоянная скорость
2 – уменьшение скорости флотации к концу флотации
3 –увеличении скорости к концу флотации
4 – экстремальная, может быть следствием изменения
концентрации реагентов в пульпе
Величина ln 1/(1–ε) называется коэффициентом удельной скорости флотации.
Слайд 48Способы насыщения воздухом
Специальными устройствами (механические, пневмомеханические, пневматические флотомашины)
Перепад давлений (напорная)
Разрежение
Электролиз (электрофлотация)
проф. Игнаткина В.А.,2017
Слайд 49
Классификация флотационных машин
механические,
пневмомеханические
пневматические
напорные флотаторы
электрофлотаторы
проф. Игнаткина В.А.,2017
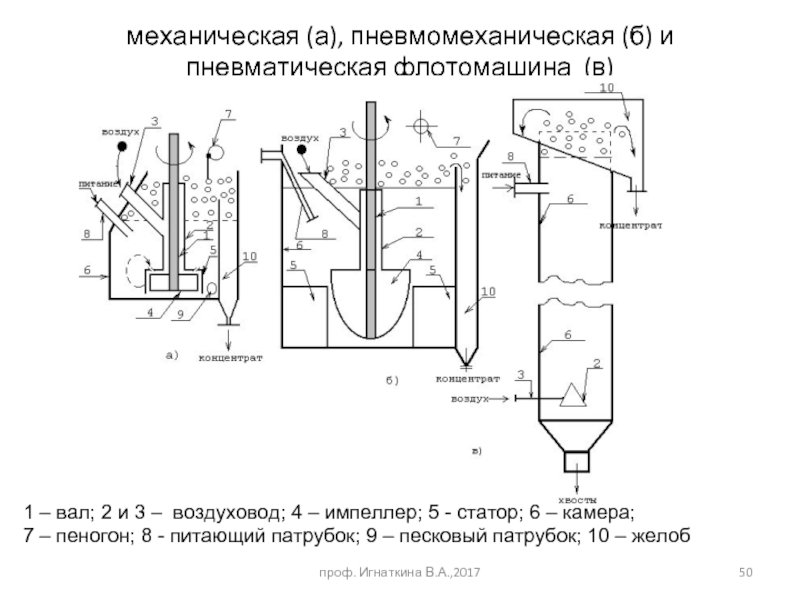
Слайд 50механическая (а), пневмомеханическая (б) и пневматическая флотомашина (в)
1 – вал; 2
7 – пеногон; 8 - питающий патрубок; 9 – песковый патрубок; 10 – желоб
проф. Игнаткина В.А.,2017
Слайд 51проф. Игнаткина В.А.,2017
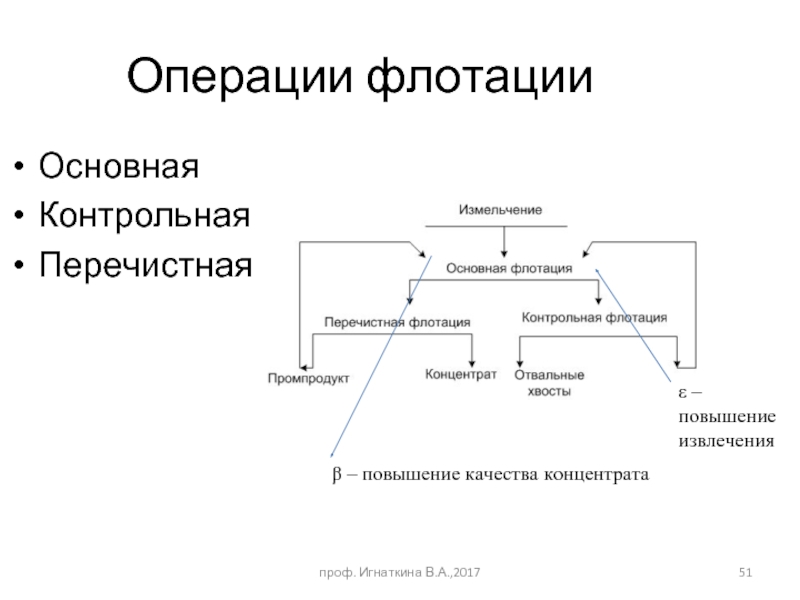
Операции флотации
Основная
Контрольная
Перечистная
ε – повышение извлечения
β – повышение качества концентрата
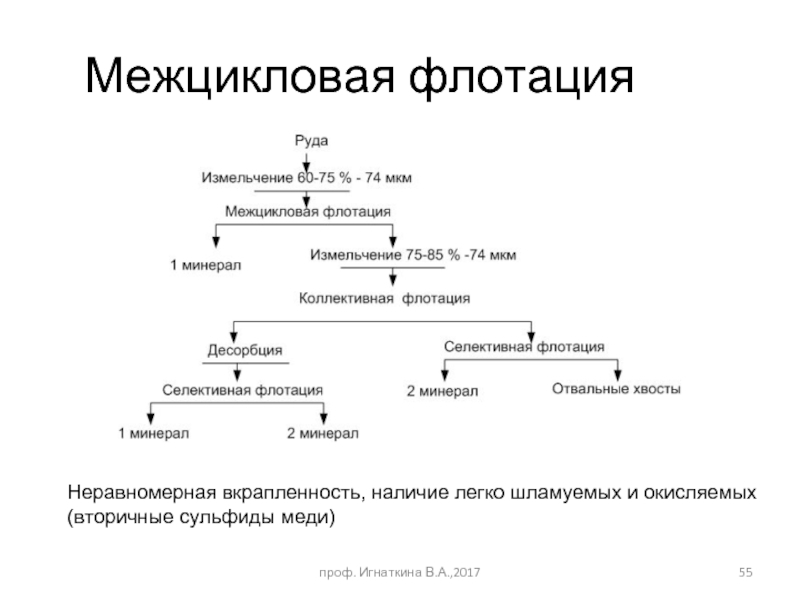
Слайд 55Межцикловая флотация
Неравномерная вкрапленность, наличие легко шламуемых и окисляемых
(вторичные сульфиды меди)
проф. Игнаткина
Слайд 56Типизация руд, минералов М.А.
Природногидрофобные – графит, угли, самородная сера, тальк (Mg3Si4O10(OH)2)
Руды сульфидных минералов тяжелых цветных металлов и самородные металлы – галенит PbS, сульфиды меди Cu2S, CuS, сфалерит ZnS, золото, серебро, платиноиды, самородная медь и др.
Смешанные и окисленные руды тяжелых цветных металлов – азурит Cu3(СО3)2(ОН)2, малахит Cu2CO3(OH)2, церуссит PbCO3 и др.
Несульфидные руды с полярными солеобразными минералами с щелочноземельными катионами (Ca, Ba, Sr) – кальцит CaCO3, шеелит CaWO4, повелит CaMoO4 , апатит Са5[PO4]3(F, Cl, ОН), флюорит CaF2, барит BaSO4и др.
Руды, содержащие оксидные минералы черных металлов (железо, марганец, хром) и цветных редких металлов (касситерит SnO2, ильменит FeTiO3, рутил TiO2и др.)
Руды, содержащие силикаты и алюмосиликаты (берилл Al2[Be3(Si6O18)], сподумен LiAl(Si2O6), породные минералы)
Руды, содержащие растворимые соли (галит NaCl, сильвин KCl)
проф. Игнаткина В.А.,2017
Слайд 57Сульфидные руды
Сульфидные минералы - основной источник меди и других тяжелых цветных
Сопутствующие – благородные металлы (Аu, Ag, МПГ), редкие металлы и редкоземельные элементы
проф. Игнаткина В.А.,2017
Слайд 59проф. Игнаткина В.А.,2017
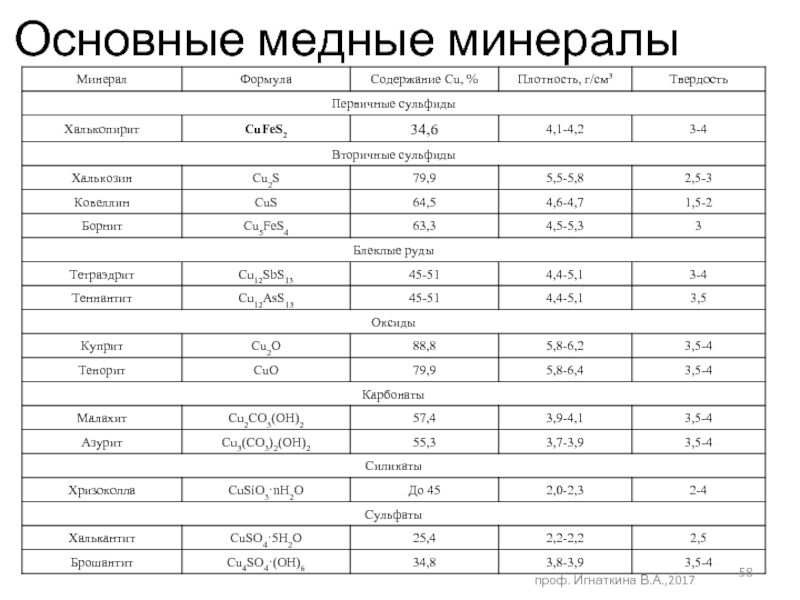
Требования к медным концентратам
ГОСТ Р 52998-2008 - Концентрат медный.
Дата введения 2010-01-01
As≤0,6 (1,2 %); Mo≤0,12 (0,18 %); влажность≤7 %
Слайд 62Промывка руды для удаления глины или сульфатов меди (халькантит CuSO4·5H2O)
проф.
Слайд 64Полярные несульфиды
Оксиды (Fe2O3, FeTiO3, MnO2, лопарит (Na,Ce,Ca,Sr,Th)(Ti,Nb,Fe)O3
Солеобразующие (CaF2, CaCO3, Ca5(PO4)3F …)
Силикаты
проф. Игнаткина В.А.,2017
Слайд 65Реагентные режимы несульфидных руд
Регуляторы среды (кислоты (серная H2SO4, плавиковая HF), щелочи
Модификаторы (кислоты, кремнефтористый натрий Na2SiF6, щавелевая кислота H2C2O4, КМЦ, крахмал, сернистый Na2S натрий…)
Оксигидрильные собиратели (карбоновые кислоты R-COOH и их мыла R-COONa (олеат, таловые масла, СЖК), алкилсульфаты R-OSO3, алкилфосфаты, Аспарал Ф R –( COO, NH, OSO3)
проф. Игнаткина В.А.,2017
C18
Слайд 67Особенности использования производных карбоновых кислот
Мицелообразование – растворимость олеиновой кислоты 20 мг/л
Олеат натрия 309 мг/л (1,1·10-3 моль/л) при 50 0С
Температура флотации не менее 16 0С
Повышенное пенообразование
проф. Игнаткина В.А.,2017
Слайд 69Плавиковая кислота HF
активирует
полевые шпаты
Берилл Al2Be3(Si6O18)
депрессирует
Кварц SiO2
Сподумен LiAl(Si2O6)
проф. Игнаткина В.А.,2017
Слайд 72Высокотемпературные воздействия
Обжиг для разрушения кальцита,
Восстановительная сульфидизация,
Декрипитация – растрескивание минералов при их нагревании
проф. Игнаткина В.А.,2017
Слайд 73Десорбция с применением пропарки
сульфиды
Высокотемпературная в щелочной среде (разделение Cu-Mo коллективного концентрата)
Высокотемпературная в среде сернистого натрия (разделение Cu-Mo коллективного концентрата) – восстановительные условия
кальциевые
Метод Петрова – с жидким стеклом Na2SiO3 (2,5-4 %) при температуре 70-85 0С)
проф. Игнаткина В.А.,2017
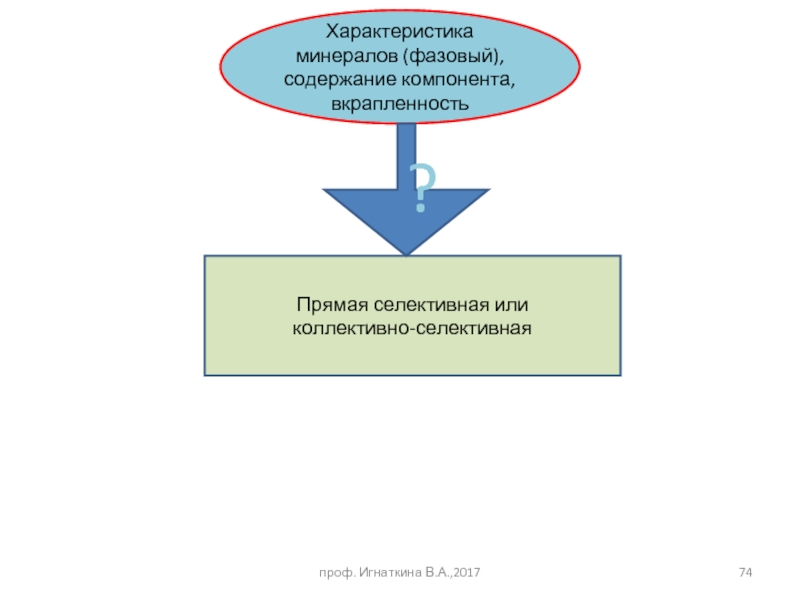
Слайд 74проф. Игнаткина В.А.,2017
Характеристика минералов (фазовый), содержание компонента, вкрапленность
Прямая селективная или
коллективно-селективная
?
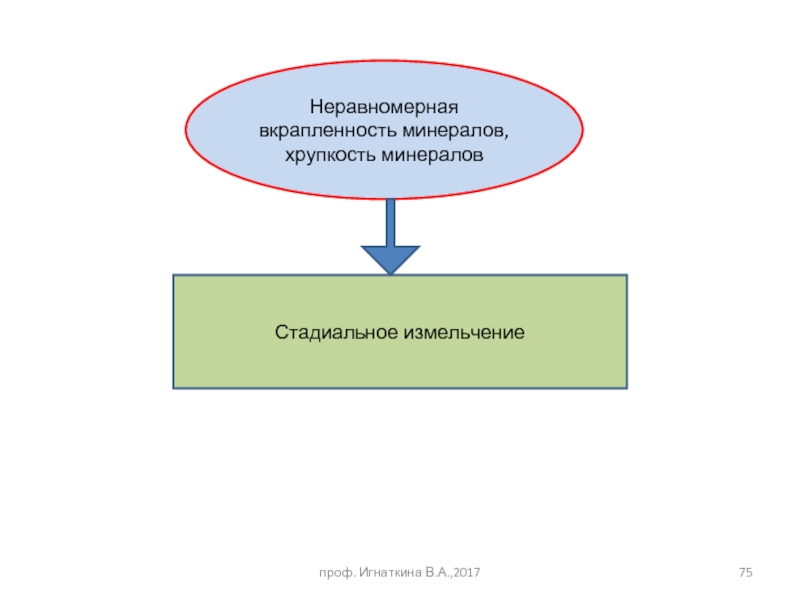
Слайд 75проф. Игнаткина В.А.,2017
Неравномерная вкрапленность минералов, хрупкость минералов
Стадиальное измельчение
Слайд 76проф. Игнаткина В.А.,2017
Неравномерное гранулометрическое распределение минералов
Комбинирование с другими обогатительными процессами







![проф. Игнаткина В.А.,2017h5 = hт + hп [h5 - h4] Кинетическая энергияmv2/rГидродинамика потока[h4 - h3]](/img/tmb/1/89139/535b1f7c28b001d4a5d9affa7fa1893c-800x.jpg)














![проф. Игнаткина В.А.,2017R-NH2 +H+ → [RNH3]+Kd =4,3·10-4Катионные собиратели закрепляются в ДЭС, химическая адсорбция маловероянаHCOOHHCl](/img/tmb/1/89139/e780f3268e8862dfff278af1126bbcfb-800x.jpg)

![в–пленочная пена (по В.И. Классену)[7]б-агрегатная пенаа–пленочно-структурная пенаСтроение пенного слояпроф. Игнаткина В.А.,2017](/img/tmb/1/89139/3791740c1b9939c468d01f5572d106b1-800x.jpg)
![ОПСБС4Н9-[CH2-CH-O]n-OHCH3МИБКCH3-CH2-CH2-CH-CH3CH3OHтерпинеолС10H17OHT-80диоксановыеипирановыеФенольные – нейтральная средаСпиртовые – щелочная Алкилсульфаты - слабокислаяOH, C=O, COO, SO3, OSO3, N, NH2.проф.](/img/tmb/1/89139/387554d46b250481d6d967b7b7a581d5-800x.jpg)