- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Oxidarea biologicaLantul respiratorFosforilarea oxidativa презентация
Содержание
- 1. Oxidarea biologicaLantul respiratorFosforilarea oxidativa
- 2. OBIECTIVELE Oxidarea biologică. Dehidrogenarea substratelor - sursa
- 3. Oxidarea biologică. Dehidrogenarea substratelor. Enzimele dehidrogenării. Oxidarea
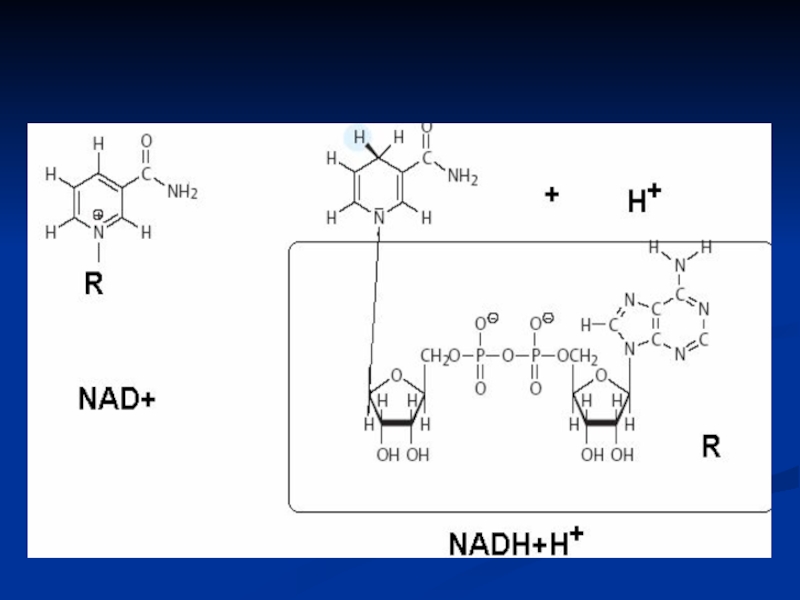
- 4. SUBSTRATELE NAD 1. Izocitrat +NAD→ alfa-cetoglutarat +NADH+H
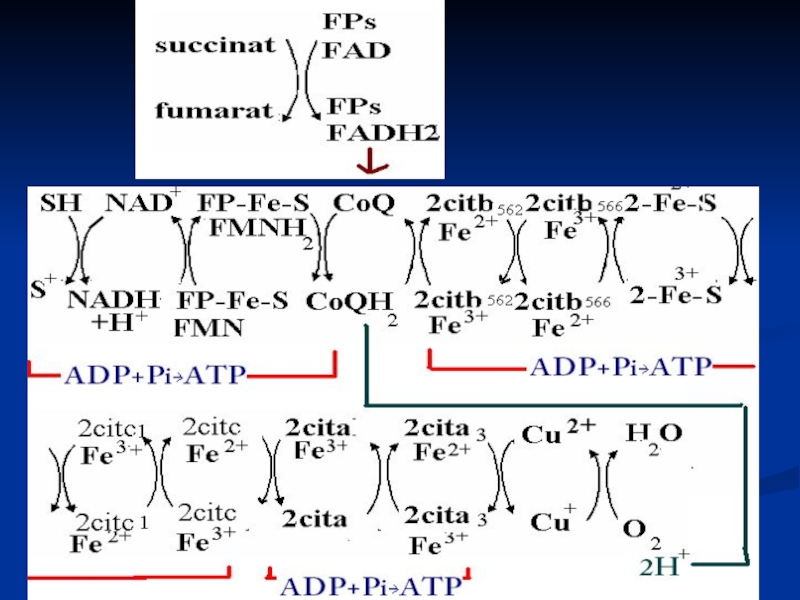
- 5. SUBSTRATELE FAD dependente Succinat +FAD →Fumarat +FADH2
- 6. Lanţul respirator (LR). Rolul. Structura. LR
- 7. Componentele LR 1. NADH+H sau FADH2 2.
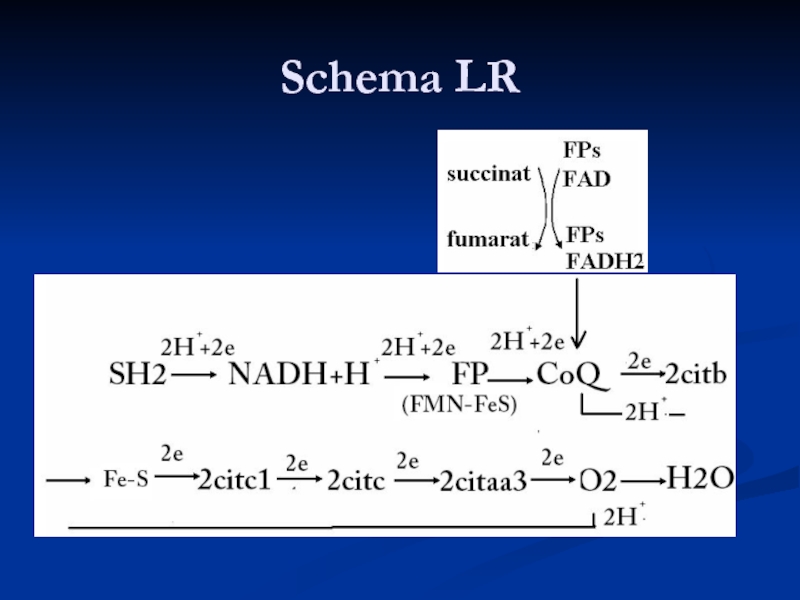
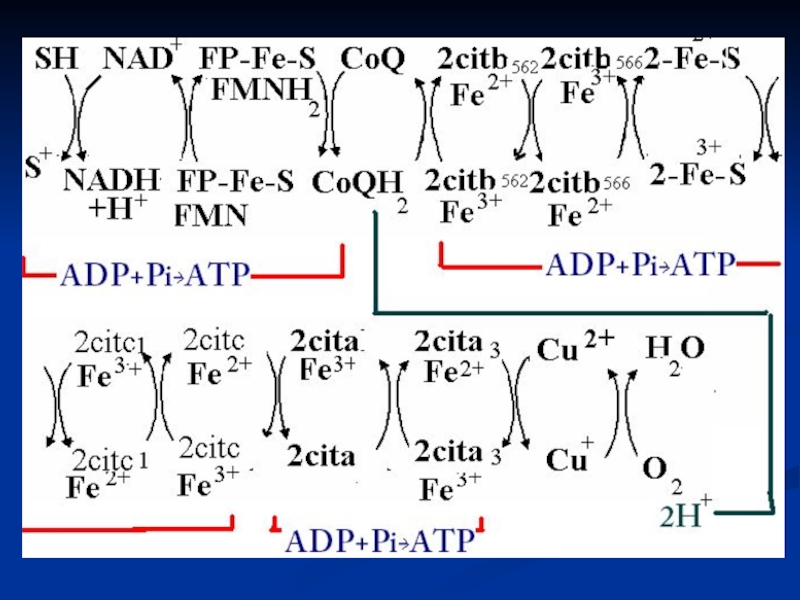
- 8. Schema LR
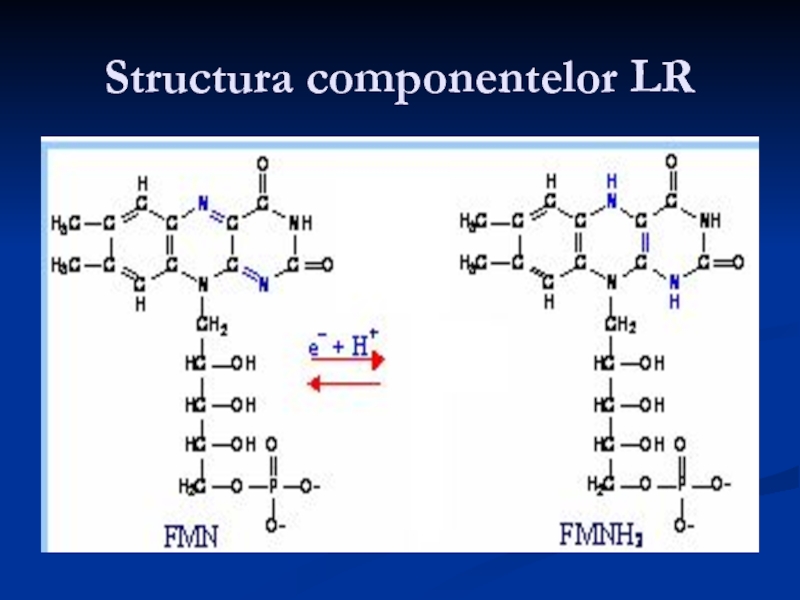
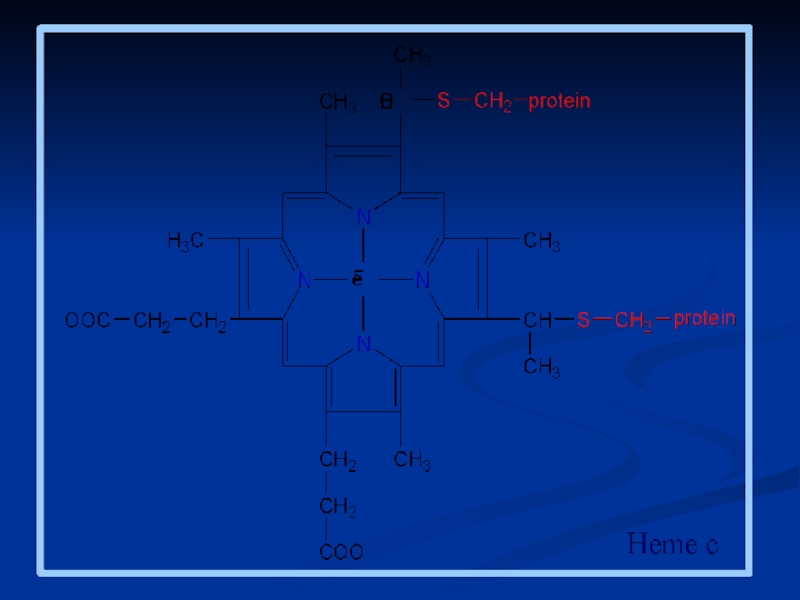
- 10. Structura componentelor LR
- 13. Potenţialul de O/R Transferul p şi
- 14. Cu cît potenţialul redox este mai
- 15. transferul în trepte permite eliberarea energiei
- 16. FOSFORILAREA OXIDATIVĂ reprezintă sinteza ATP din ADP
- 17. Composition of Respiratory Chain Complexes
- 18. Complexul I- NADH → CoQ – reductază
- 19. Complexul II- succinat - CoQ-reductaza Variaţia de
- 20. Complexul III- CoQ- citocrom c reductaza Variaţia
- 21. Complexul IV- citocromoxidază Catalizează adiţia a 4ē
- 22. Complexul V – ATP-sintetază alcătuită din:
- 23. Mitochondrial ATP
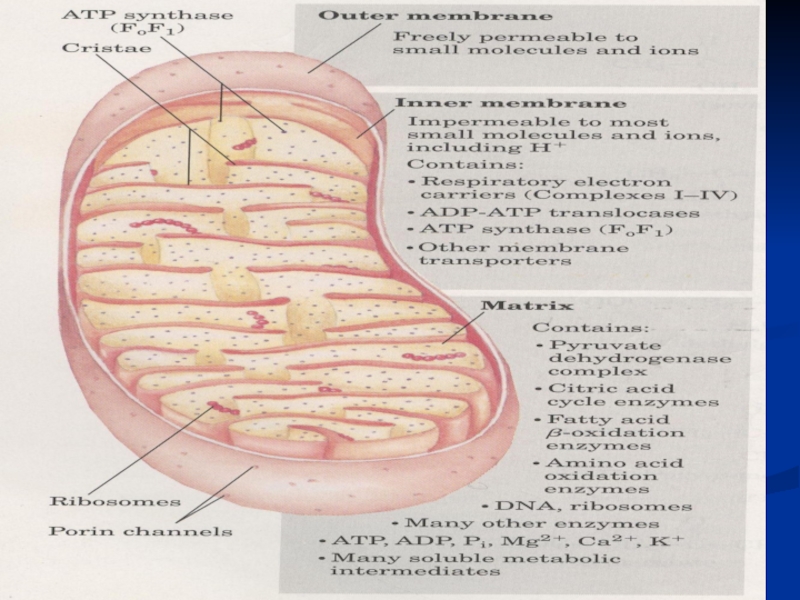
- 24. Toate componentele LR sunt dispuse în membrana
- 27. Locusurile unde are loc sinteza ATP
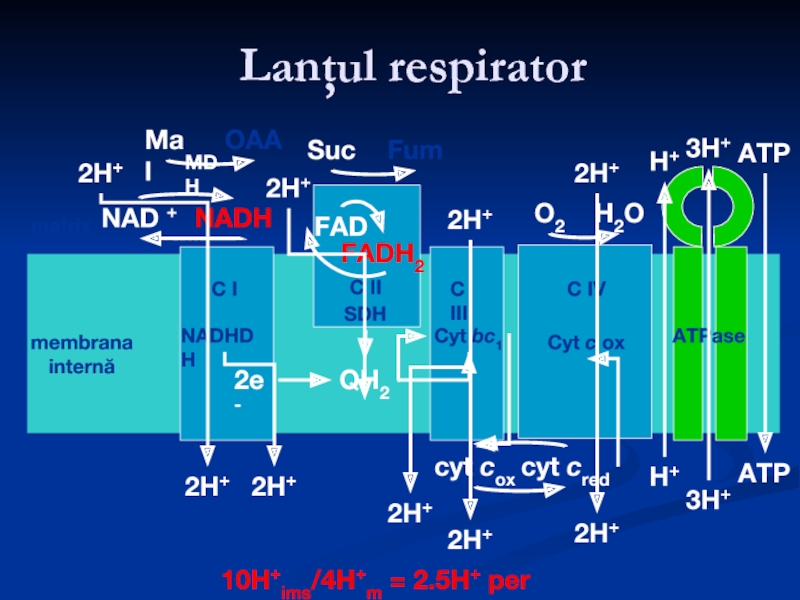
- 29. Lanţul respirator matrix membrana internă spaţiul intermembranar 10H+ims/4H+m = 2.5H+ per ATP
- 30. Bilanţul general în procesele LR-FO. NADH
- 32. Ipoteze principale cu privire la procesele de
- 33. Ipoteza lui Mitchell Ce postulează că
- 34. Gradientul protonilor are 2 componente :
- 36. Datele experimentale ce confirmă: S-a confirmat generarea
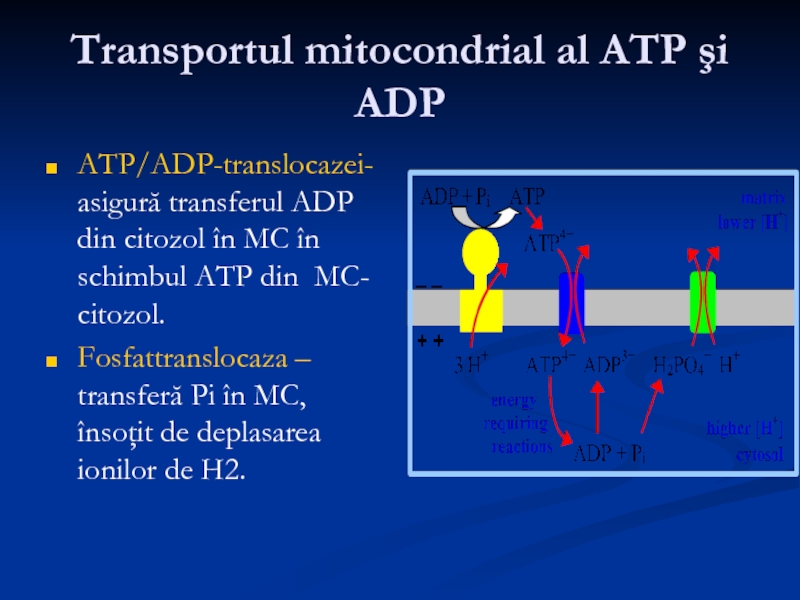
- 37. Transportul mitocondrial al ATP şi ADP ATP/ADP-translocazei-
- 38. Controlul respirator Organismele vii sintetizează ATP
- 39. Controlul respirator Controlul respiraţiei se înfăptuieşte prin
- 40. Decuplarea produselor de oxidare şi fosforilare, principalii
- 41. Protonoforii → măresc permeabilitatea membranei
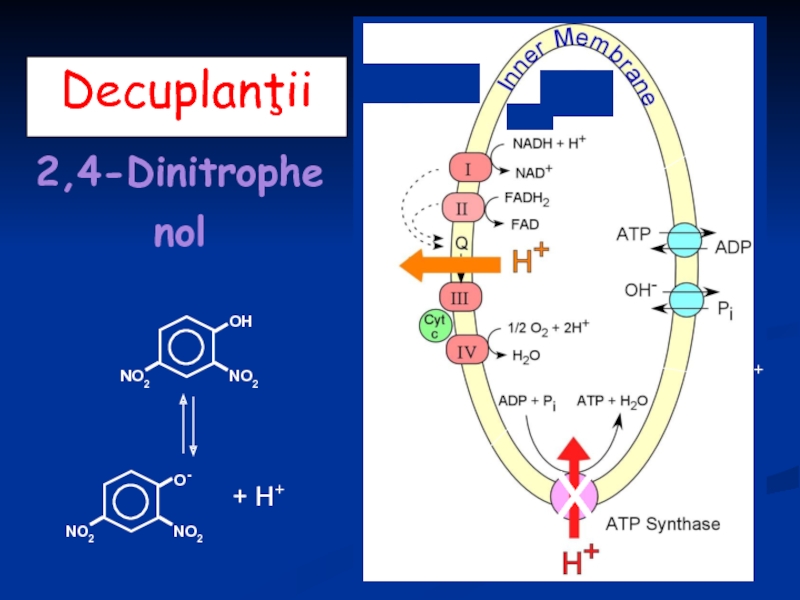
- 42. Decuplanţii 2,4-Dinitrophenol X
- 43. Inhibitorii ai fosforilării acţionează asupra ATP-sintetazei.
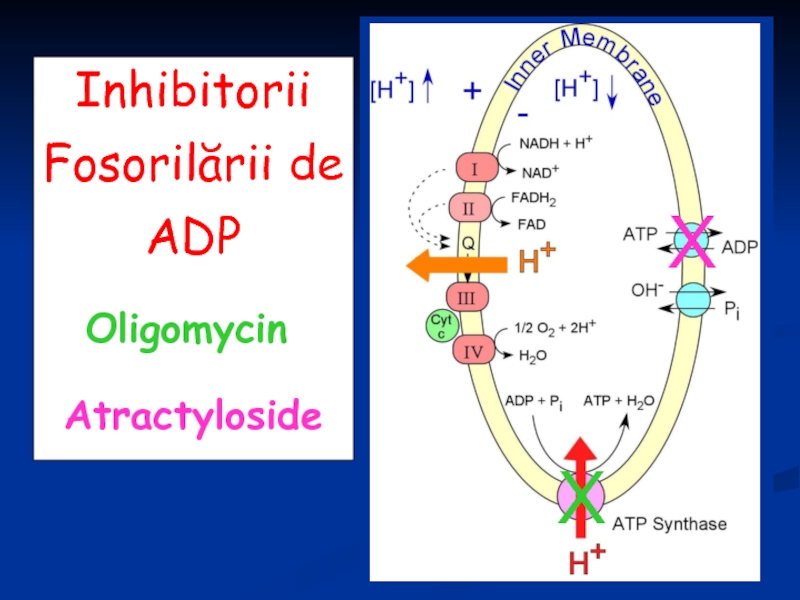
- 44. Inhibitorii Fosorilării de ADP
- 45. Fosforilarea oxidativă este influenţată de o
- 46. Respiraţia liberă – are loc decuplarea FO
- 47. Oxidarea microsomală Un alt tip
- 48. Rolul OM Rolul: plastic şi dezintoxicare. În
- 49. Noţiune de radicali liberi. Oxidarea peroxidică a
- 50. Aceşti produşi iniţiază OPL, ce se
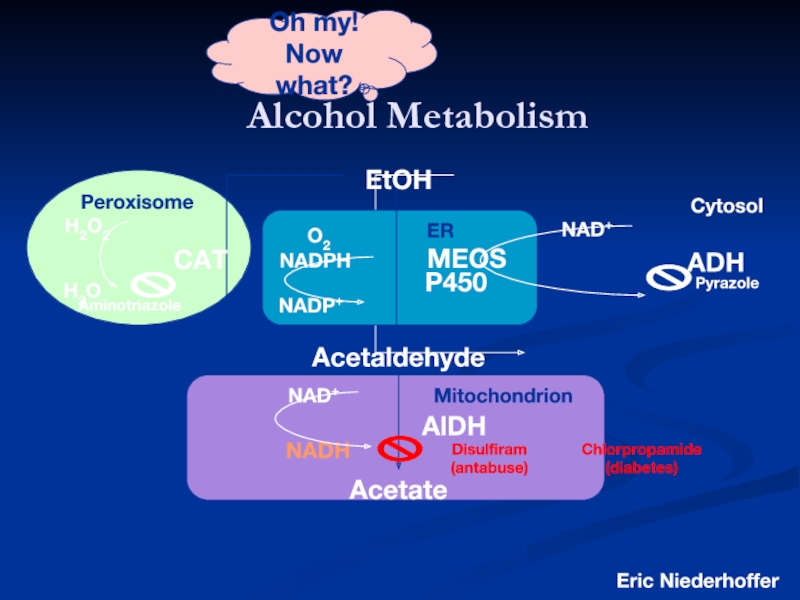
- 51. Alcohol Metabolism Eric Niederhoffer SIU-SOM EtOH Acetaldehyde Acetate Oh my! Now what?
Слайд 2OBIECTIVELE
Oxidarea biologică. Dehidrogenarea substratelor - sursa energetică pentru sinteza ATP -
Lanţul respirator (schema). Complexele enzimatice. Acceptorii principali de electroni şi protoni, structura lor chimică.
Potenţialul de oxido-reducere a componentelor lanţului respirator. Fosforilarea oxidativă. Locurile de fosforilare. Produsele finale ale oxidării.
Reglarea intensităţii funcţionării lanţului respirator. Coeficientul P/O, controlul respirator.
Decuplarea produselor de oxidare şi fosforilare, principalii agenţi decuplanţi. Rolul biologic al produsului de decuplare, respiraţia liberă.
Mitocondriile, structura şi permeabilitatea selectivă a membranelor pentru diferiţi cumpuşi.. Sistemele-navetă de transport al echivalenţilor de reducere.
Ipotezele principale, care explică procesele fosforilării oxidative. Ipoteza lui Mitchell.
Oxidarea microzomală, rolul citocromului P450 în reacţiile de oxido-reducere.
Vitaminele şi rolul lor în procesele de oxidare biologică.
Noţiune de radicali liberi. Oxidarea peroxidică a acizilor graşi nesaturaţi din membrane. Sistemele de protecţie a celulei de acumilarea radicalilor liberi.
Слайд 3Oxidarea biologică. Dehidrogenarea substratelor. Enzimele dehidrogenării.
Oxidarea biologică (OB) reprezintă totalitatea reacţiilor
Rolul: asigură organismul cu energie accesibilă în formă de ATP.
OB are loc prin reacţii de dehidrogenare → donarea atomilor de H2 sub formă de protoni şi electroni: H2→2H +2 ē.
Are loc sub acţiunea enzimelor → dehidrogenaze, ale căror Co sunt NAD+ şi FAD
Слайд 4SUBSTRATELE NAD
1. Izocitrat +NAD→ alfa-cetoglutarat +NADH+H
E- izocitratDH
2. Alfa-cetoglutarat +NAD → succinil
E-alfacetoglutaratDH
3.Malat +NAD →OA+NADH+H
E-malatDH
4.Lactat +NAD →Piruvat +NADH+H
E-lactatDH
5. Gliceraldehidfosfat +NAD +H3PO4→1,3 difosfoglicerat +NADH+H
E- GAP DH
6. Hidroxiacil CoA +NAD →cetoacil Co-A +NADH+H
E-hidroxiacil -CoA DH
Слайд 5SUBSTRATELE FAD dependente
Succinat +FAD →Fumarat +FADH2
E- succinat DH
Acil CoA + FAD
E- acil CoA DH
NADH+H+ şi FADH2 rezultaţi în reacţiile de oxidare a acestor substrate transferă p şi ē în lanţul respirator.
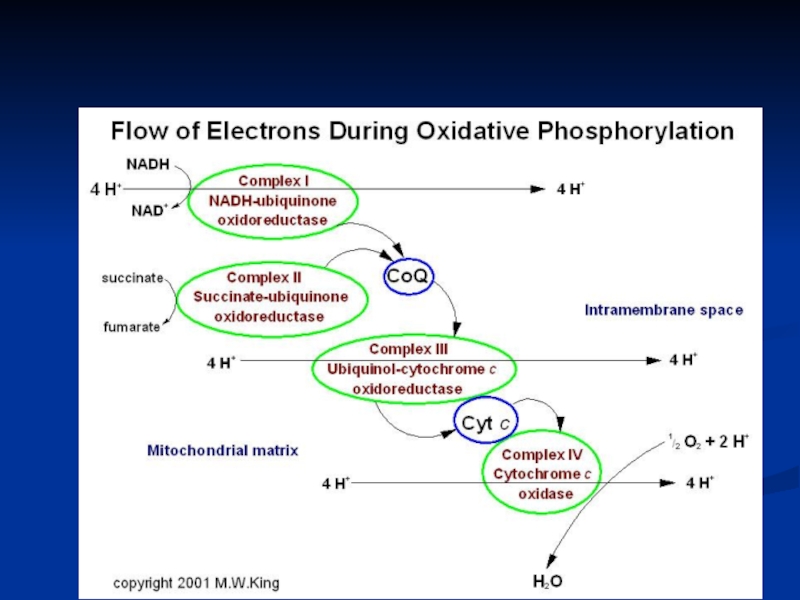
Слайд 6Lanţul respirator (LR). Rolul. Structura.
LR - un ansamblu (complex) de
Este ultima etapă a degradării aerobe.
Este localizat în membrana internă a MC Funcţia LR:
Prin transferul protonilor şi electronilor → Co se reoxidează, putînd asigura dehidrogenări în continuare.
Cînd Co se reoxidează, se eliberează energie ce serveşte la sinteza ATP.
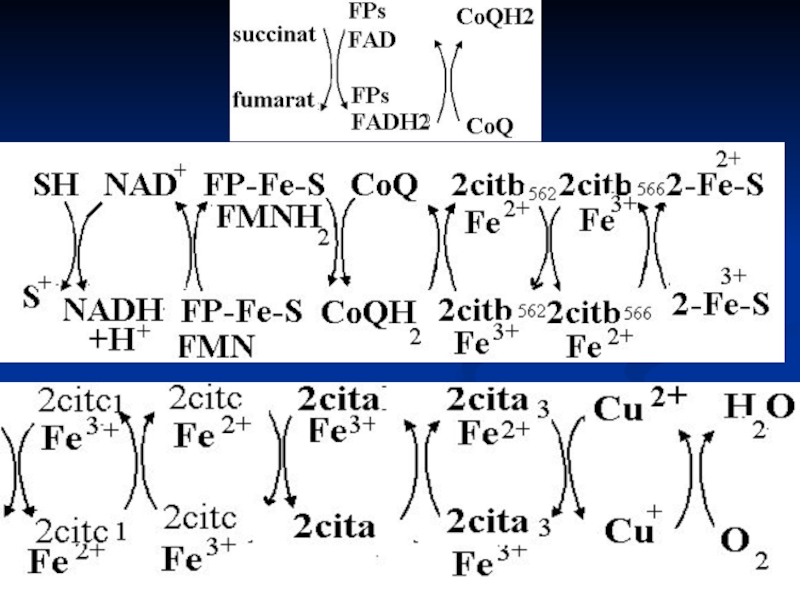
Слайд 7Componentele LR
1. NADH+H sau FADH2
2. Flavoproteinele FP: preiau p şi e-
FPN (NADH DH) - ca Co FMN - preia H2 de la NADH+H
FPs (succinatDH)- ca Co FAD- preia H2 de la FADH2
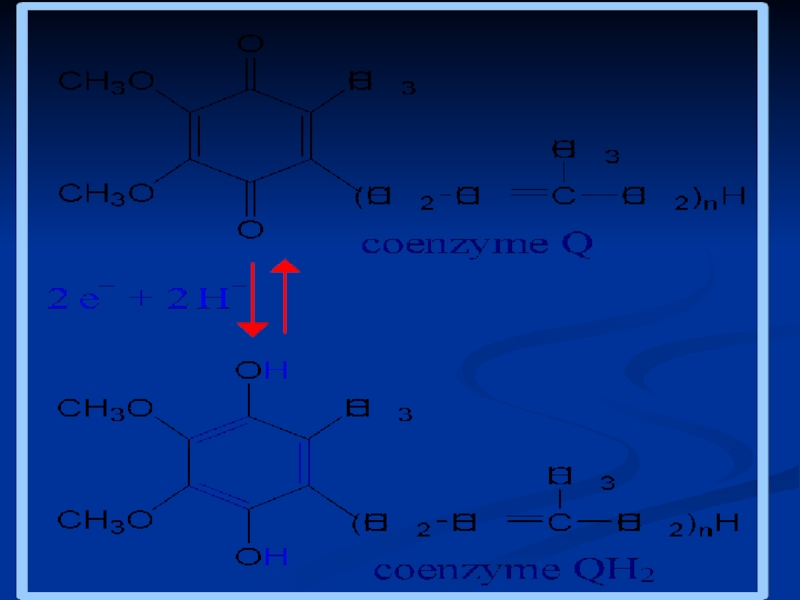
3. CoQ-ubichinona – până la CoQ sunt transportaţi atât p cât şi e-
4. Sistemul de citocromi: b, c1, c, a şi a3
Sunt compuşi heteroproteici,a căror grupare prostetică este hemul
Transportă doar e – Fe+++ + e- ←→ Fe++
1 citocrom transportă doar 1e- - 2 e- sunt transportaţi de 2 citocromi
5. Fe-S proteinele –sunt localizate :
a. între FP şi CoQ
b. între cit b şi citc1
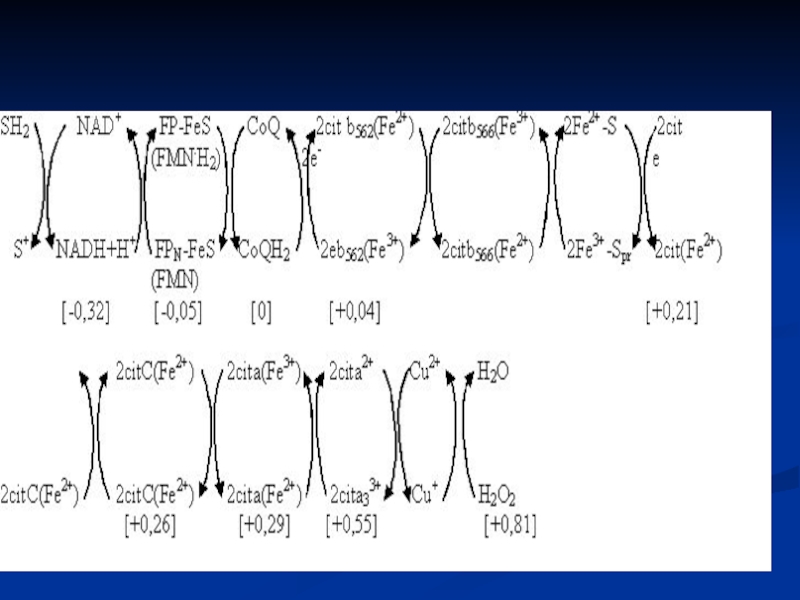
Слайд 13 Potenţialul de O/R
Transferul p şi ē de la NADH sau
Fiecare sistem redox (O/R) este alcătuit dintr-un donor şi acceptor de echivalenţi reducători.
Fiecare sistem redox din LR posedă un potenţial de oxido-reducere (potenţial redox), care se măsoară în volţi.
Potenţialul redox standard –E0 – mărime egală cu forţa electromotoare exprimată în volţi, ce apare în semiconductor, în care donorul de e- şi acceptorul acţionează în concentraţie de 1,0 mol, la t =25 *c, şi pH 7,0 formând un echilibru cu elecrodul ce adiţionează e- de la donor şi-i transferă la acceptor.
Слайд 14
Cu cît potenţialul redox este mai electronegativ cu atât este mai
Sistemele redox sunt aranjate în ordinea creşterii potenţialului de oxido-reducere.
Слайд 15
transferul în trepte permite eliberarea energiei în “pachete” a cărei valoare
Torentul de ē e orientat în direcţia micşorării energiei libere a sistemului
Cu cît e mai mare diferenţa potenţialului dintre 2 redox perechi → cu atît mai mare e diminuarea energiei libere la transferul ē.
Ştiind potenţialul redox al fiecărei perechi se pot calcula modificarea energiei libere standard.
ΔG = -nFΔE
n-numărul de ē
F-constanta lui Faraday (23062 cal/V∙mol)
ΔE0-diferenţa de potenţial
ΔG = -2∙23062[+0,82-(-0,32)] = -52,6 kcal
7,3 x 3 = 21,9 cal
Randamentul utilizării energiei libere – 42%
Слайд 16FOSFORILAREA OXIDATIVĂ
reprezintă sinteza ATP din ADP şi Pi (cuplată cu LR),
Deoarece transferul de ē are loc treptat, energia se eliberează „în pachete” – în trepte . Pentru a se forma ATP diferenţa de potenţial trebuie să fie nu mai mică de 0,22V.
Funcţionarea cuplată a LR şi FO este asigurată de 5 complexe
Слайд 18Complexul I- NADH → CoQ – reductază
Căderea de potenţail 0,42V →
ΔG0 = -19,4 kcal/mol - 1mol ATP, restul se degajă sub formă de căldură
Inhibat: rotenonă(otravă pentru peşti), Na amital (barbiturat); pericidină (antibiotic)
Слайд 19Complexul II- succinat - CoQ-reductaza
Variaţia de potenţial este de 0,07V;
ΔG0
Inhibat – malonat (inhibiţie competitivă)
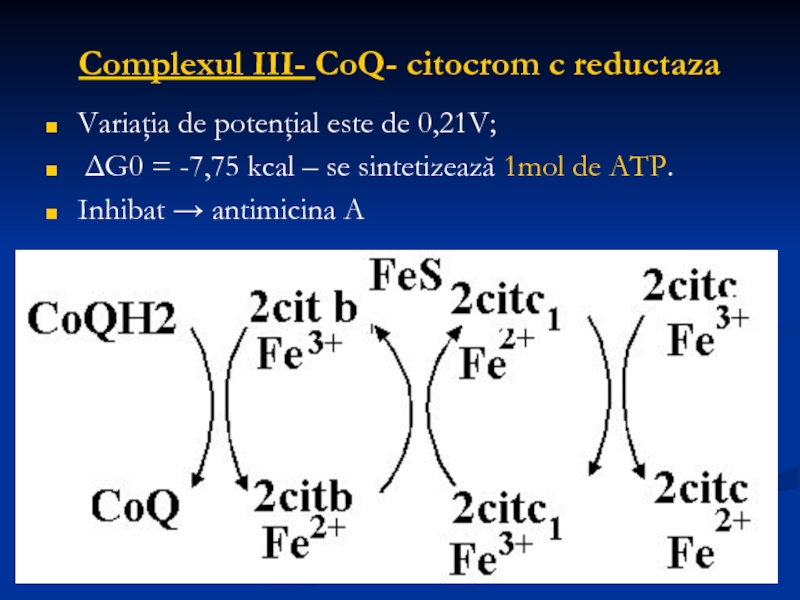
Слайд 20Complexul III- CoQ- citocrom c reductaza
Variaţia de potenţial este de 0,21V;
Inhibat → antimicina A
Слайд 21Complexul IV- citocromoxidază
Catalizează adiţia a 4ē la O2 molecular (a 2ē
O2 + 4ē + 4H+ → 2H2O
Căderea de potenţial de 0,54V.
ΔG = -24,8 kcal → se sintetizează 1mol de ATP
Inhibat: CO, ozide, cianide.
Слайд 22Complexul V – ATP-sintetază
alcătuită din:
F0 → străbate membrana internă a
F1- partea catalitică - factor de cuplare 1:
se află în intregime în matrixul mitocondrial (formă de sferă).
e alcătuită din cinci tipuri de proteine ααα (α3), βββ (β3), γ, δ, ε.
la acest nivel are loc reacţia de condensare a ADP + Pi →ATP+H2O
Inhibată: oligomicină, atractilatul (glicozidă)
Слайд 23
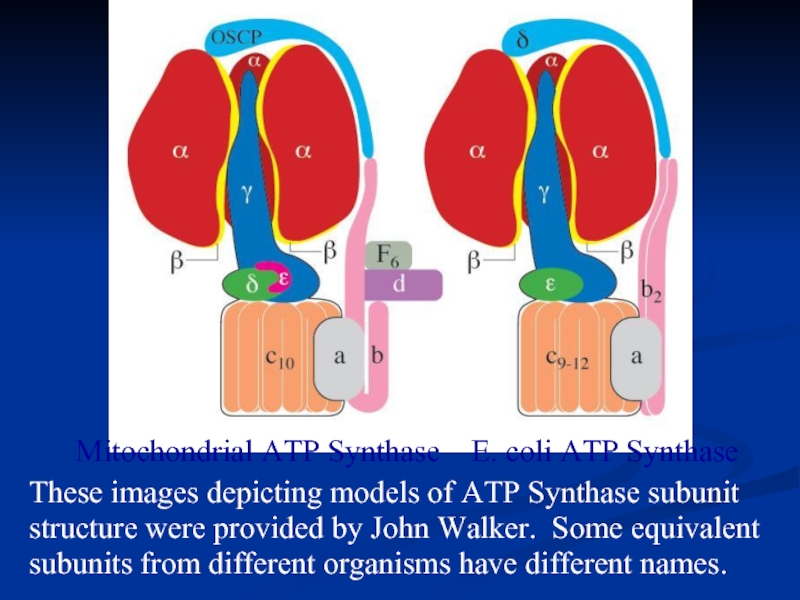
Mitochondrial ATP Synthase E. coli ATP Synthase
These
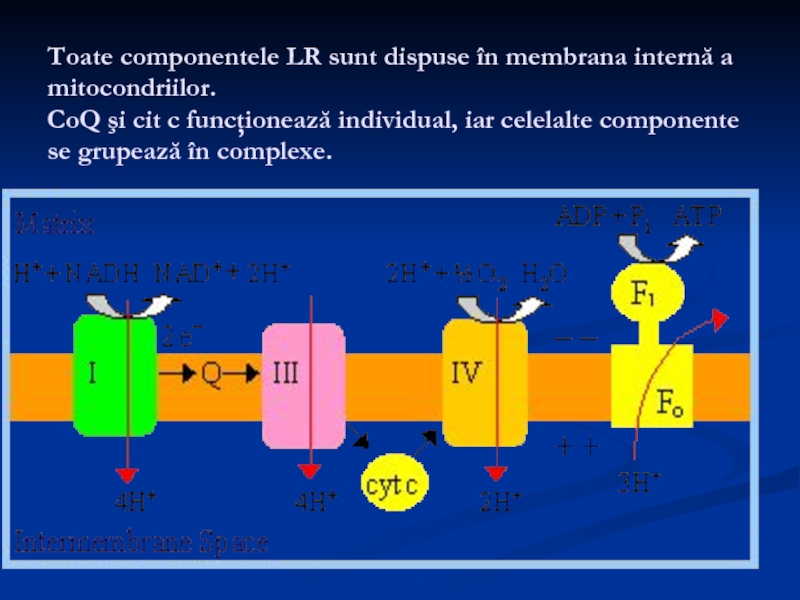
Слайд 24Toate componentele LR sunt dispuse în membrana internă a mitocondriilor. CoQ
Слайд 27
Locusurile unde are loc sinteza ATP se numesc puncte de fosforilare.
NADH+H----CoQ
Cit b----citc
cita--cita3
Слайд 30Bilanţul general în procesele LR-FO.
NADH + H+ + ½O2 + 3ADP
FADH + H+ + ½O2 + 2ADP + 2Pi → FAD + 2ATP + 3H2O
Raportul între numărul de moli de ATP produşi şi O2 consumat este numit „cît de fosforilare” P/O.
De la NADH+H pînă la O2 - P/O = 3/1 – ramura lungă,
De la FADH2 pînă la O2 - P/O = 2/1 – ramura medie.
P/O reflectă cuplarea transportului H+ şi ē (respiraţia) şi fosforilarea (sinteza ATP). Coeficient indică ce cantitate de P anorganic (H3PO4) se transformă în P organic (ATP) la transportul unei perechi de H+ şi ē în LR.
Слайд 32Ipoteze principale cu privire la procesele de FO. Ipoteza lui Mitchell
Prin ce mecanism energia eliberată în LR este cuplată cu formarea ATP?
Teoria chimică, numită şi a intermediatorilor comuni (produşi intermediatori macroergici, precursori de ATP).
Teoria conformaţională (energia este preluată de o proteină într-o conformaţie activă, ce stimulează ATP).
Teoria chemiosmotică (Mitchell, 1961).
Слайд 33Ipoteza lui Mitchell
Ce postulează că starea intermediară energetică care determină
⇒ la transferul unei perechi de ē (energia eliberată) pompează 3 perechi de H2+ din interiorul MC spre exterior(spaţiu intermembranar).
Astfel partea externă a membranei interne a MC→ pozitiv, dar cea internă – negativ –
apare gradient de c%/ potenţialul transmembranar
Слайд 34
Gradientul protonilor are 2 componente :
1. Electrică (potenţial de membrană -
2 de pH (∆ pH)gradientul H+
Protonii revin din spaţiu intermembranar în mitocondrii prin partea F0 (deoarece restul membranei este impermiabilă).
Acest flux de protoni este forţa morice care determină la nivelul subunităţii F1 sinteza de ATP din ADP+Pi
Unul din postulatele teoriei chemiosmotice prevede că apa rezultată în reacţia de formare a ATP din ADP şi Pi se ionizează spontan, ionii H+fiind dirijati spre interiorul mitocondriei (ei urmînd să creeze gradientul protonic) în timp ce ionii OH- sînt dirijati spre spapul intermembranar
Слайд 36Datele experimentale ce confirmă:
S-a confirmat generarea gradientului de protoni în cele
S-a demonstrat ca pH matrixului mitocondrial creşte, iar cel al mediului extern al membranei MC – scade (acid).
S-a argumentat că transferul H+ din MC în timpul transportului de ē şi revenirii lor prin ATP-sintetaza sunt comparabile cu viteza lor din cadrul FO în MC intacte.
Слайд 37Transportul mitocondrial al ATP şi ADP
ATP/ADP-translocazei- asigură transferul ADP din citozol
Fosfattranslocaza – transferă Pi în MC, însoţit de deplasarea ionilor de H2.
Слайд 38Controlul respirator
Organismele vii sintetizează ATP în raport cu necesititatea lui –
Deoarece LR şi FO – etapa finală a degradării G, L, P controlul respirator se poate efectua atât prin compuşi direct implicaţi în LR şi FO, cât şi prin intermediatorii degradării celor 3 clase.
Rolul primordial îi revine ADP.
F1 din ATP - sintetază rămâne blocat în lipsă de ADP.
Intensitatea transferului de protoni prin F0 deasemenea e determinată de nivelul ADP.
ADP – reglator alosteric (+) pentru mai multe E ce sunt implicate în degradarea G, L şi P.
Слайд 39Controlul respirator
Controlul respiraţiei se înfăptuieşte prin intermediul acceptorului - ADP.
Lipsa
Слайд 40Decuplarea produselor de oxidare şi fosforilare, principalii agenţi decuplanţi.
La FO
Integritatea membranei interne a MC → orice leziune duce la perderea capacităţii de FO (în timp ce transferul de ē poate continua).
Impermeabilitatea membranei interne pentru ionii H+ OH- K+ Cl-.
FO poate fi decuplată cu ajutorul unor substanţe chimice, ce inhibă sinteza ATP dar neafectînd decuplanţi – agenţi decuplanţi. La acţiunea lor respiraţia creşte, iar FO este inhibată.
protonofori
AD
ionoforele
Слайд 41
Protonoforii → măresc permeabilitatea membranei pentru protoni(H+), lichidând potenţialul transmembranar.
a.g.
2,4 dinitrofenol
salicilaţii (antiinflamatoare)
dicumarol (anticoagulant)
T3 şi T4 (h.gl.tiroide)
Ionoforele – ei leagă şi transferă ionii prin membrană:
- valinomicina (↑ K+) , nigericina (↑ K+), gramicidina A → Na+, K+; H+.
Слайд 43
Inhibitorii ai fosforilării acţionează asupra ATP-sintetazei. Oligomicina blochează pătrunderea H+ prin
Слайд 45
Fosforilarea oxidativă este influenţată de o serie de agenţi clasaţi în
- agenti de decuplare- permit transportul electronilordar blochează fosforilarea. Ex.2,4 dinitrofenolul facilitează trecerea prin membrană a H+
- inhibitorii fosforilării oxidative Ex Oligomicina -împedică şi transportul şi fosforilarea oxidativă.
- Ionoforii - formează complexe liposolubile cu cationi specifici trecîndui prin membrană.
Слайд 46Respiraţia liberă
– are loc decuplarea FO de LR şi toată energia
Astfel MC devin o sobă, ce produc căldură. E necesar în situaţii, când necesitatea căldurii este mai mare decât ATP.
În ţesutul adipos brun – MC sunt specializate la producerea căldurii (nou-născuţi, animale în hibernare) – termogenina.
Слайд 47Oxidarea microsomală
Un alt tip de reacţii de OB este cel
Lanţurile monooxigenazice de oxidare sunt lanţuri scurte de transport al H+ şi ē a căror sursă sunt NADPH+H
SH + O2 +NADPH + H+ → S-OH + H2O + NADP+ ⇒ reducerea O2 şi incorporarea lui în anumiţi compuşi chimici (include un atom de O, celălalt este redus la H2O).
un asemenea lanţ este microsomial - localizat în RE al celulelor hepatice şi suprarenale. Rol esenţial îl are cit P450 (activatorul O2). El cuprinde o FP (FAD) la nivelul căreia H2 este disproporţionat în H+ şi ē.
Слайд 48Rolul OM
Rolul: plastic şi dezintoxicare.
În ficat – hidroxilarea medicamentelor, neutralizarea toxinelor,
În medulosuprarenale – sinteza noradrenalinei şi adrenalinei.
În corticosuprarenale – sinteza colesterolului, hormonilor gluco- şi mineralocorticoizi.
Слайд 49Noţiune de radicali liberi. Oxidarea peroxidică a AG nesaturaţi. Sistemul de
La reducerea incompletă a O2 se formează forme reactogene şi agresive ale substanţei cum ar fi: superoxidanionul, peroxid; hidroxil sau peroxidul de hidrogen.
Слайд 50
Aceşti produşi iniţiază OPL, ce se petrece în lanţ cu generarea
În condiţii fiziologice ORL şi OPL sunt implicate în reînnoirea membranelor biologice, degradarea substanţelor fagocitare; biosinteza icosanoizilor.
Amplificarea lor poate condiţiona moartea celulei (lezarea membranelor).
SAO → sistem de protecţie → AO (enzimatic, neenzimatic)
SOD → transformarea O2- • în H2O2
2 O2- +2H+ → O2- + H2O2
Catalaza 2H2O2 → 2H2O + O2
Glutation reductaza
glutationperoxidaza