- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Массовая доля химического элемента в веществе. Закон постоянства состава вещества. презентация
Содержание
- 1. Массовая доля химического элемента в веществе. Закон постоянства состава вещества.
- 2. m(пирога)=500г
- 3. Решите задачу Магний массой 4,8 г вступает
- 7. Массовая доля элемента в веществе –
- 8. Решите задачу: Рассчитайте массу магния, которая вступит
- 9. Решите задачу: Какие массы исходных веществ необходимо
- 10. Закон постоянства состава вещества Вещества имеют постоянный
Слайд 2
m(пирога)=500г m(куска)=100г
Какова
массовая доля куска от всего пирога?
100г/500г=1/5 или 20%
100г/500г=1/5 или 20%
ω (»омега») – массовая доля
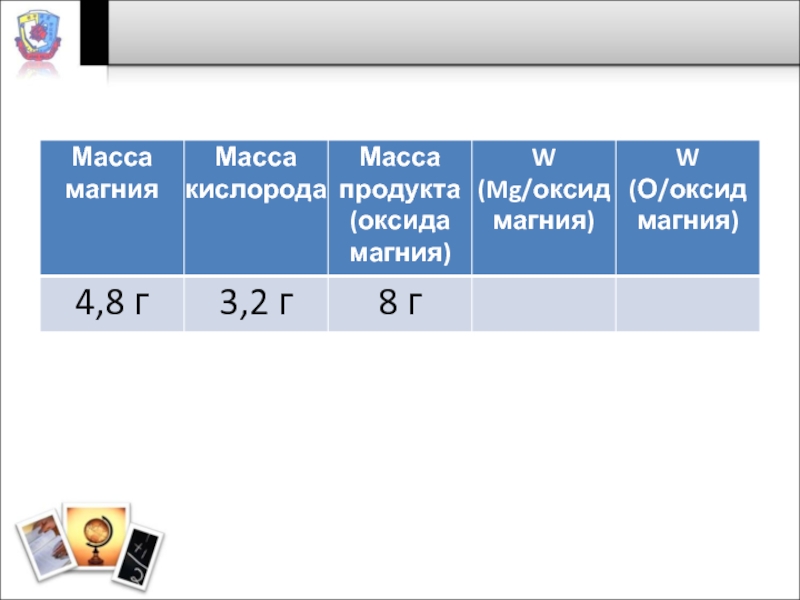
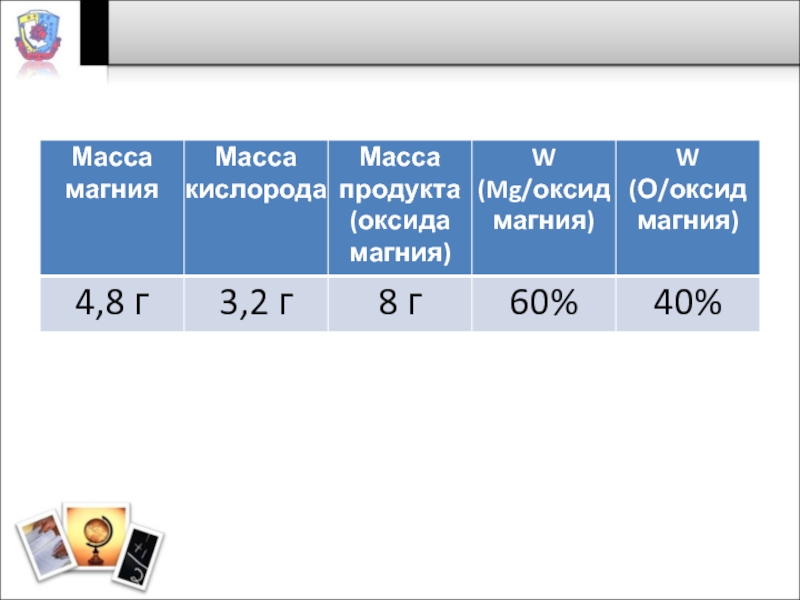
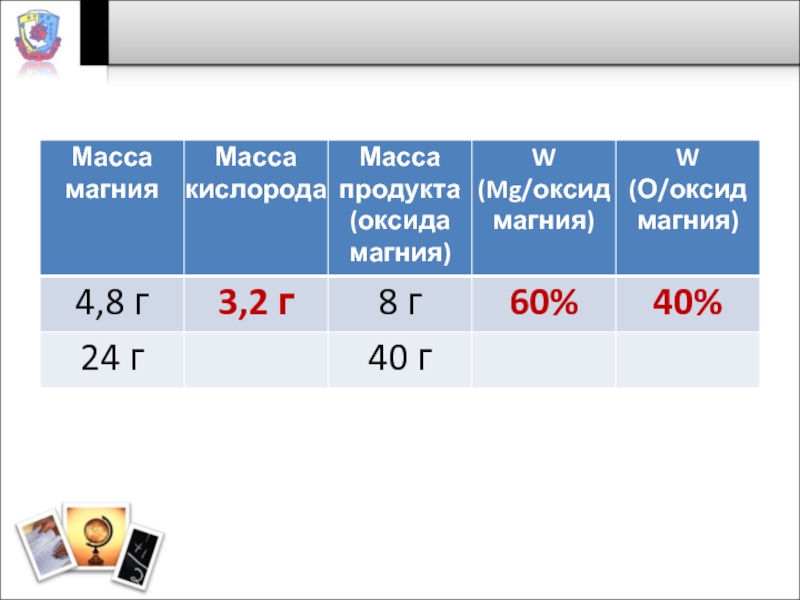
Слайд 3Решите задачу
Магний массой 4,8 г вступает в реакцию соединения с кислородом.
При этом образуется 8 г оксида магния.
1) Чему равна масса вступившего в реакцию магния?
2) Каковы массовые доли магния и кислорода в продукте реакции – оксиде магния?
1) Чему равна масса вступившего в реакцию магния?
2) Каковы массовые доли магния и кислорода в продукте реакции – оксиде магния?
Слайд 7
Массовая доля элемента в веществе – отношение массы атомов данного элемента,
входящих в состав вещества, к массе всего вещества.
ω (%)
ω (%)
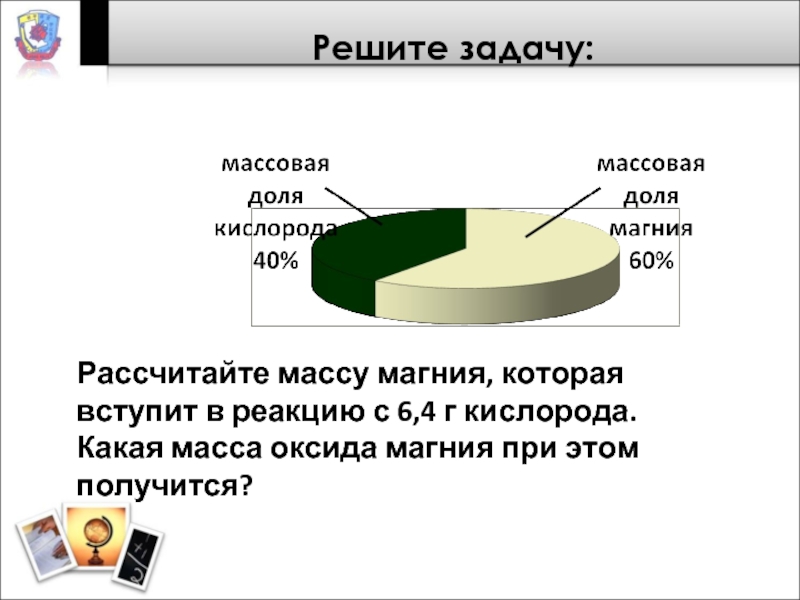
Слайд 8Решите задачу:
Рассчитайте массу магния, которая вступит в реакцию с 6,4 г
кислорода. Какая масса оксида магния при этом получится?
Слайд 9Решите задачу:
Какие массы исходных веществ необходимо взять для получения 32 г
сернистого газа, если массовые доли серы и кислорода в нем составляют по 50%?
Слайд 10Закон постоянства состава вещества
Вещества имеют постоянный состав независимо от места и
способа их получения. (Жозеф Луи Пруст)