- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кристаллические решетки презентация
Содержание
- 1. Кристаллические решетки
- 2. ТВЕРДЫЕ ВЕЩЕСТВА
- 3. КРИСТАЛЛИЧЕСКОЕ ВЕЩЕСТВО ОБРАЗУЕТ КРИСТАЛЛЫ СОВЕРШЕННО ОПРЕДЕЛЕННОЙ ФОРМЫ.
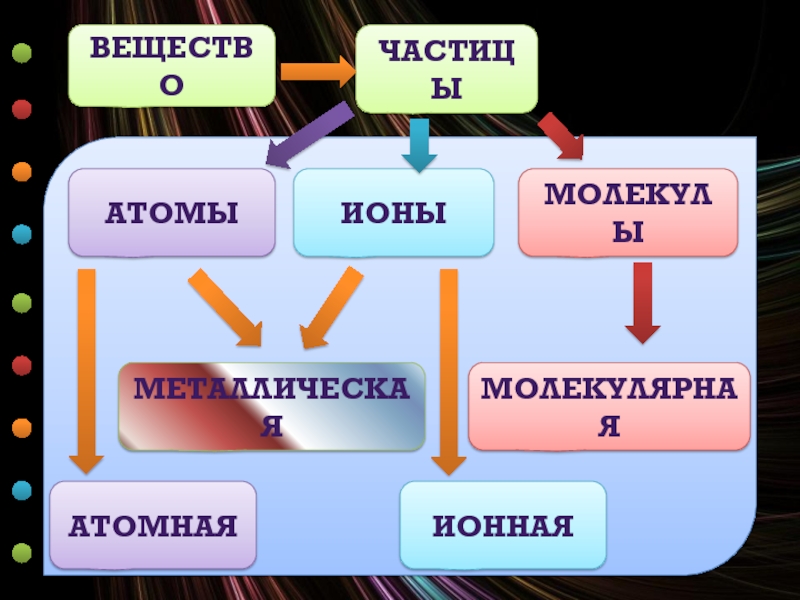
- 4. ВЕЩЕСТВО ЧАСТИЦЫ АТОМЫ ИОНЫ
- 5. ИОННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА В узлах
- 6. Однако, если ионы расплавлены или растворены,
- 7. Если пытаться деформировать ионную решетку, один из
- 8. МОЛЕКУЛЯРНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
- 9. НЕМЕТАЛЛЫ, НЕОРГАНИЧЕСКИЕ И ОРГАНИЧЕСКИЕ ВЕЩЕСТВА Хлорид фосфора (V) Бром Фенол
- 10. В узлах находятся атомы, связанные между
- 11. Алмаз Бор мелкокристаллический особочистый Германий Кремний
- 12. МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА В узлах находятся
- 14. – ЭЛЕКТРОПРОВОДНОСТЬ
- 15. ПЛАСТИЧНОСТЬ, КОВКОСТЬ
- 16. МЕТАЛЛЫ И СПЛАВЫ Бериллий Чугун (коррозия) Латунь
Слайд 2
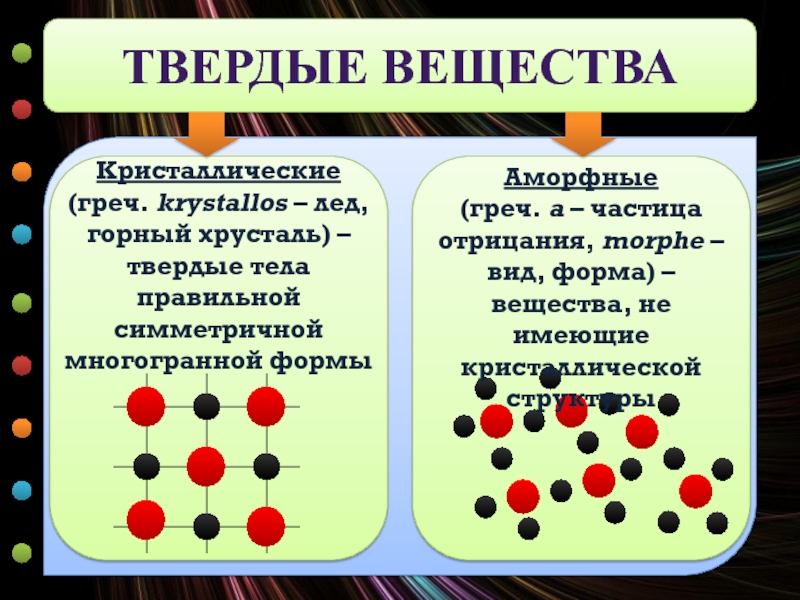
ТВЕРДЫЕ ВЕЩЕСТВА
Кристаллические
(греч. krуstallos – лед, горный хрусталь) – твердые тела
Аморфные
(греч. а – частица отрицания, morphе – вид, форма) – вещества, не имеющие кристаллической структуры
Слайд 3КРИСТАЛЛИЧЕСКОЕ ВЕЩЕСТВО ОБРАЗУЕТ КРИСТАЛЛЫ СОВЕРШЕННО ОПРЕДЕЛЕННОЙ ФОРМЫ.
Кристаллическая решетка –пространственный каркас, который
Узлы кристаллической решетки – точки, в которых размещены частицы.
Слайд 5
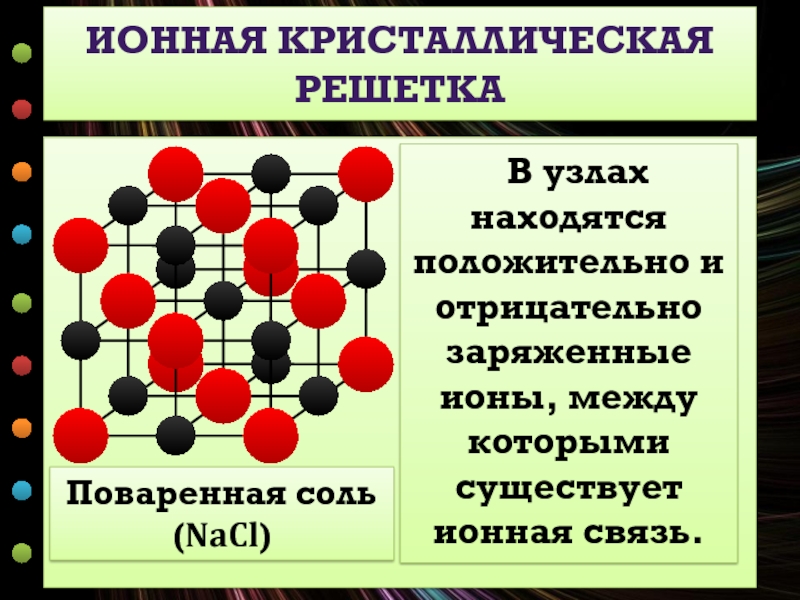
ИОННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
В узлах находятся положительно и отрицательно заряженные ионы,
Поваренная соль (NaCl)
Слайд 6
Однако, если ионы расплавлены или растворены, они могут двигаться и переносить
ЭЛЕКТРОПРОВОДНОСТЬ
В твердом состоянии ионы прочно связаны в решетке и не могут двигаться и переносить заряд, т.е. проводить электрический ток; таким образом, в твердом состоянии ионные соединения являются изоляторами.
+
–
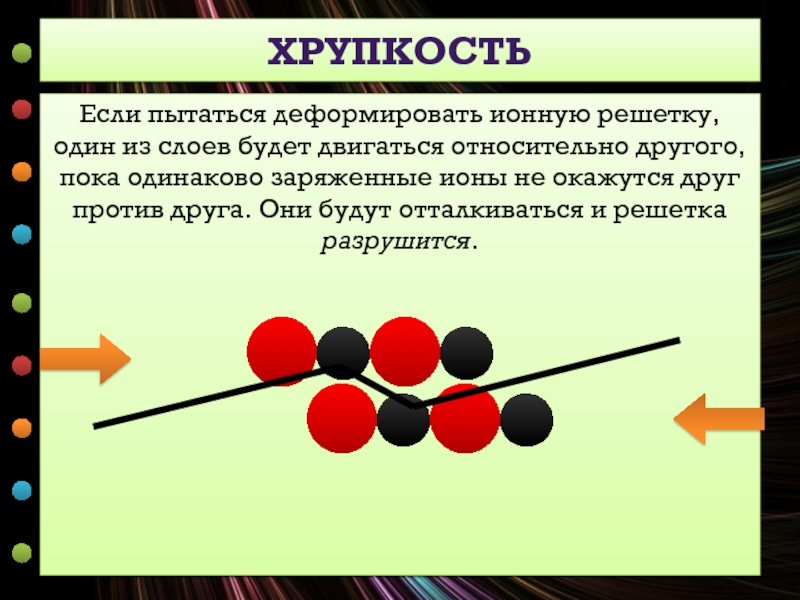
Слайд 7Если пытаться деформировать ионную решетку, один из слоев будет двигаться относительно
ХРУПКОСТЬ
Слайд 8
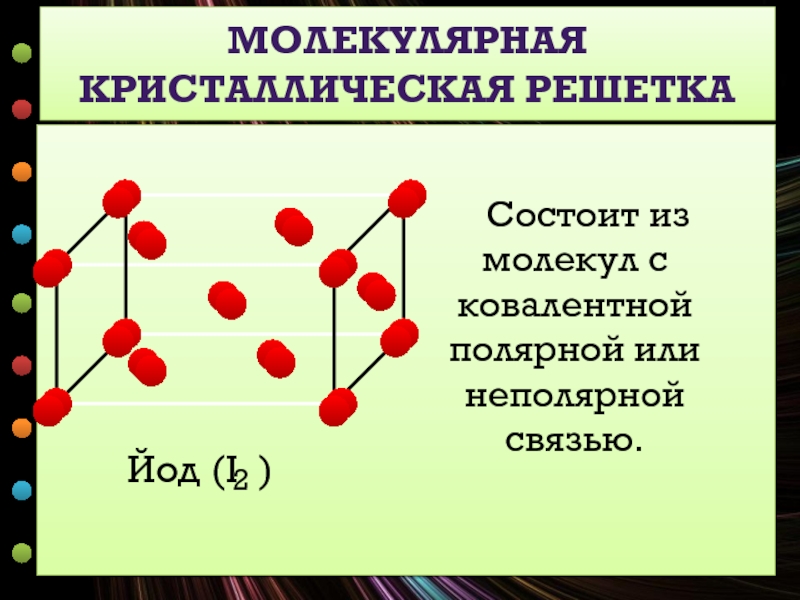
МОЛЕКУЛЯРНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
Состоит из молекул с ковалентной полярной
Слайд 10
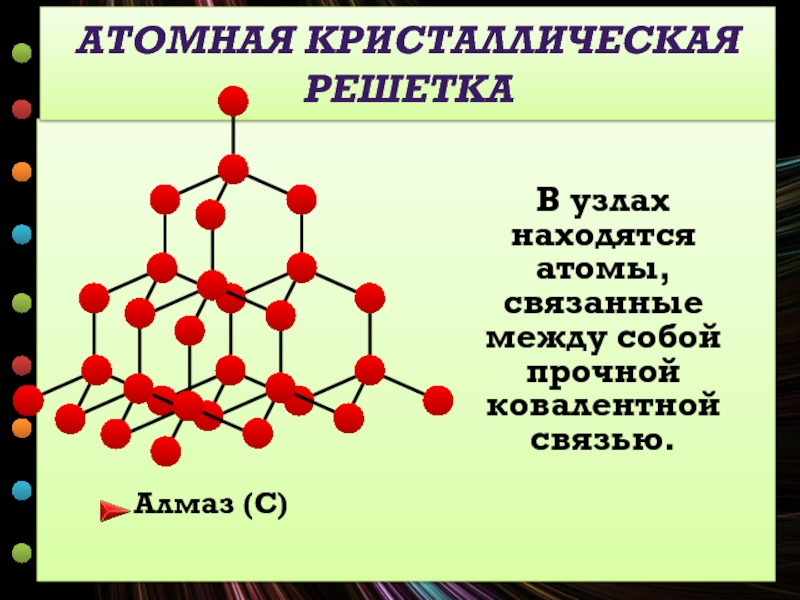
В узлах находятся атомы, связанные между собой прочной ковалентной связью.
АТОМНАЯ КРИСТАЛЛИЧЕСКАЯ
Слайд 12
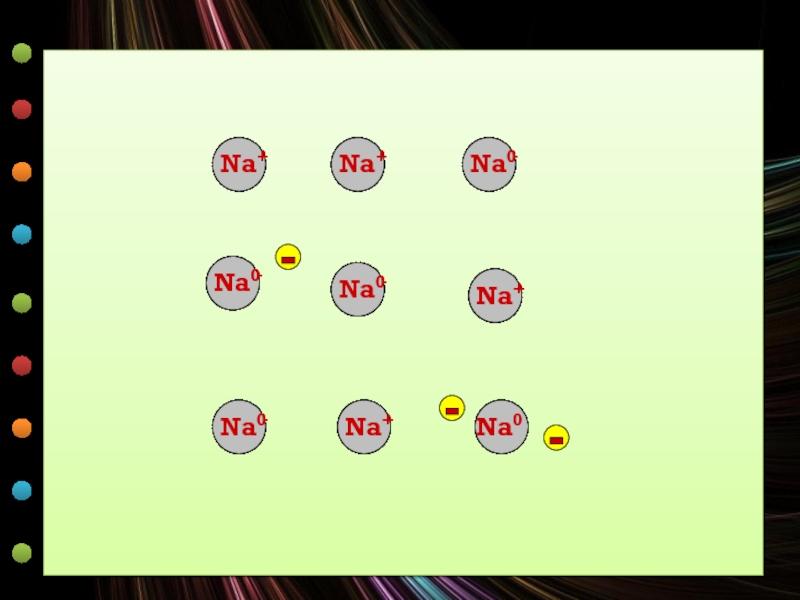
МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
В узлах находятся отдельные атомы и положительные ионы, между
Слайд 14
–
ЭЛЕКТРОПРОВОДНОСТЬ
+
В металлической решетке присутствует большое число делокализованных внешних электронов. Если
Слайд 15
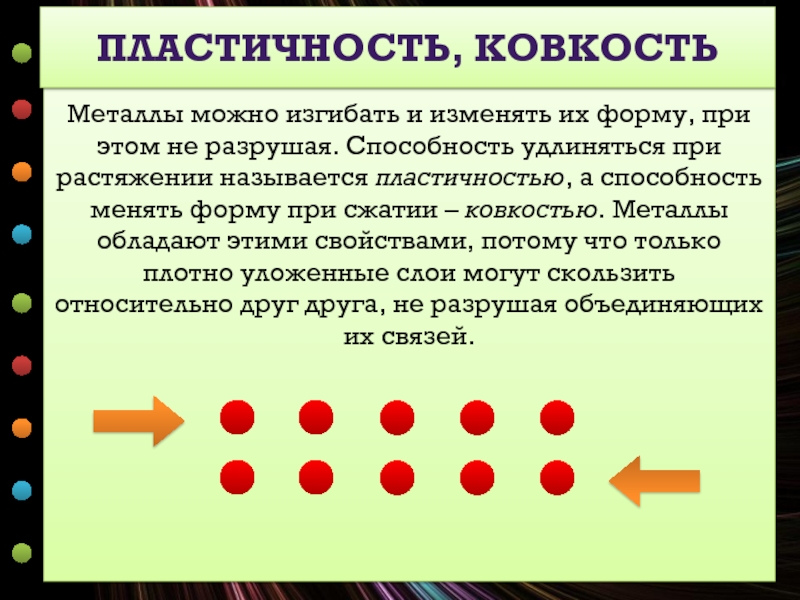
ПЛАСТИЧНОСТЬ, КОВКОСТЬ
Металлы можно изгибать и изменять их форму, при этом не