- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коррозия презентация
Содержание
- 1. Коррозия
- 2. 08/09/2019 О чем узнаем Коррозия металла
- 3. 08/09/2019 Коррозия – это разрушение металлов
- 4. 08/09/2019 Химическая коррозия Химическая коррозия металлов вызывается
- 5. 08/09/2019 Электрохимическая коррозия Электрохимическая коррозия металлов
- 6. 08/09/2019 Упрощенно процесс коррозии можно выразить уравнением
- 7. 08/09/2019 Опыты В первый стакан наливаем воду
- 8. 08/09/2019 Результаты опытов После трёх дней:
- 9. 08/09/2019 Выводы: Чем дальше в ряду напряжений
- 10. 08/09/2019 Вред коррозии Ежегодно из-за коррозии теряется
- 11. 08/09/2019 Коррозия вызывает серьёзные экологические последствия
- 12. 08/09/2019 Способы защиты от коррозии применение химически
- 13. 08/09/2019 Домашнее задание: § 10, упр. 4-6, стр. 51
Слайд 208/09/2019
О чем узнаем
Коррозия металла
Химическая и электрохимическая коррозия
Способы
Опыты
Слайд 308/09/2019
Коррозия – это разрушение металлов и сплавов под воздействием окружающей
Коррозия (от лат. corrodere – разъедать)
Слайд 408/09/2019
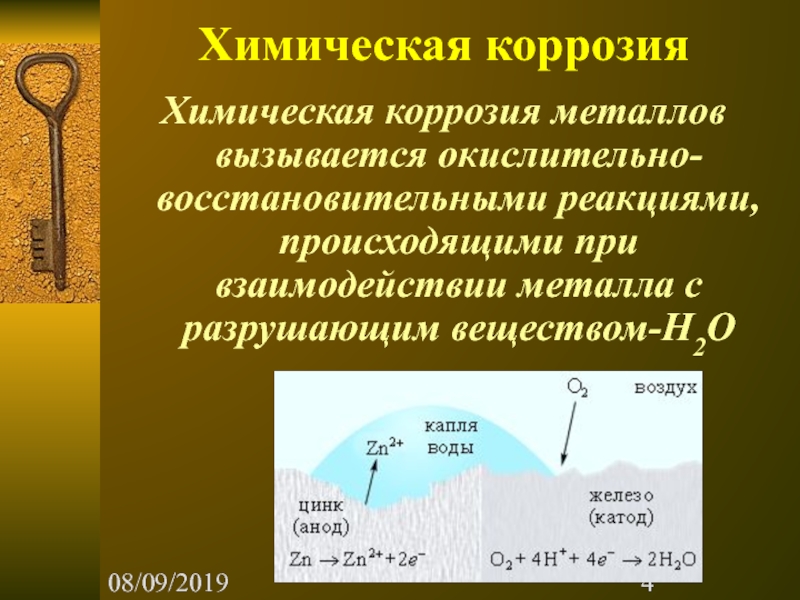
Химическая коррозия
Химическая коррозия металлов вызывается окислительно-восстановительными реакциями, происходящими при взаимодействии металла
Слайд 508/09/2019
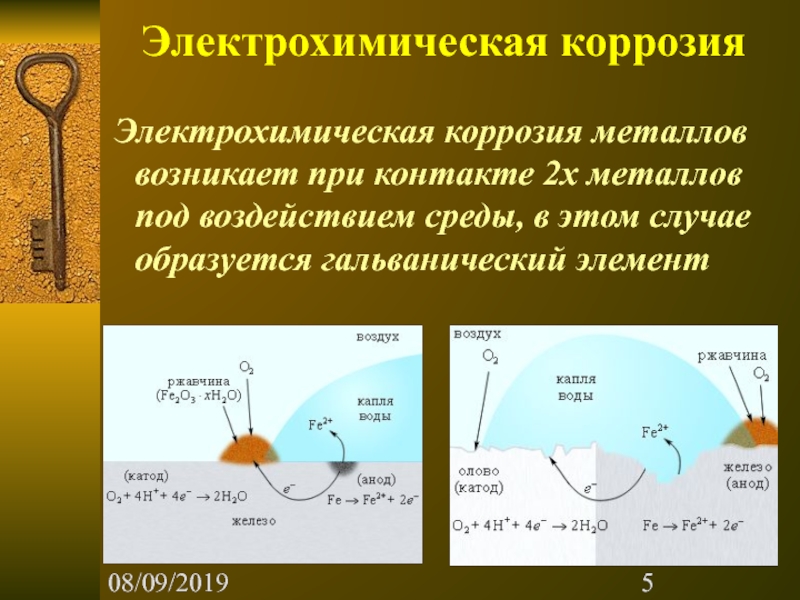
Электрохимическая коррозия
Электрохимическая коррозия металлов возникает при контакте 2х металлов под
Слайд 608/09/2019
Упрощенно процесс коррозии можно выразить уравнением химической реакции
4Fe + 3O2+ 6H2O
У поэта В.Шефнера есть очень образные строчки:
Коррозия – рыжая крыса,
Грызёт металлический лом.
Слайд 708/09/2019
Опыты
В первый стакан наливаем воду и кладем гвоздь
Во второй стакан
в третий - солёную воду и кладём туда алюминиевую проволоку и гвоздь
в четвертый - солёную воду и кладём медный провод и гвоздь
И оставляем их на три дня…
Вода
Соленая вода.
Соленая вода
Солёная вода
Берётся четыре стакана
Слайд 808/09/2019
Результаты опытов
После трёх дней:
В 1 –ом стакане гвоздь немного заржавел
Во 2 –ом стакане гвоздь больше всего заржавел и тоже выпал осадок (так как соль это самый лучший окислитель)
В 3 –ем стакане алюминиевый провод заржавел лучше, чем гвоздь и тоже выпал осадок
В четвёртом стакане с медной проводом ничего не случилось, а вот гвоздь заржавел и в именно этом стакане выпал самый большой осадок
Слайд 908/09/2019
Выводы:
Чем дальше в ряду напряжений стоят друг от друга металлы, тем
Коррозию металлов вызывают такие компоненты окружающей среды как вода, кислород, оксиды углерода и серы, появившиеся в воздухе, водные растворы солей (морская вода, грунтовые воды). Эти вещества непосредственно окисляют металлы – происходит химическая коррозия.
Слайд 1008/09/2019
Вред коррозии
Ежегодно из-за коррозии теряется около четверти всего произведённого в мире
Однако не только потеря металлов . Но и порча изготовленных из них изделий обходиться очень дорого.
Затраты на ремонт или на замену деталей судов , автомобилей , аппаратуры химических производств, приборов и коммуникаций во много раз превышают стоимость металла, из которого они изготовлены.
Слайд 1108/09/2019
Коррозия вызывает серьёзные экологические последствия
Утечка газа, нефти и других опасных
Понятно почему на защиту металлов от коррозии тратятся большие средства
Вред коррозии
Слайд 1208/09/2019
Способы защиты от коррозии
применение химически стойких сплавов (нержавеющие стали , содержащие
защита поверхности металла покрытиями: а) металлами образующими на своей поверхности прочные плёнки б)неметаллами – лаками, красками, эмалями, смолами, создающие защитные плёнки
Подавление влияния
коррозионной среды
ингибиторами
Электрохимическими
методами - применение
протекторов