- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Консультация экспертов ЕГЭ по химии2012 год презентация
Содержание
- 1. Консультация экспертов ЕГЭ по химии2012 год
- 2. С1 Cr2(SO4)3 + Br2 +
- 3. C2-2012
- 4. Демо-2012 Соль, полученную при растворении железа в
- 5. Решение 2Fe + 6H2SO4 = Fe2(SO4)3 +
- 6. 1 Продукт взаимодействия лития с азотом обработали
- 7. 1 - Решение 6Li + N2 =
- 8. 2 Навеску алюминия растворили в разбавленной азотной
- 9. 2 - Решение 10Al + 36HNO3 =
- 10. 3 Сульфид цинка обработали раствором соляной кислоты.
- 11. 3 - Решение ZnS + 2HCl =
- 12. Задание на дом. 1 Фосфат кальция сплавили
- 13. Задание на дом. 2 На сухой хлорид
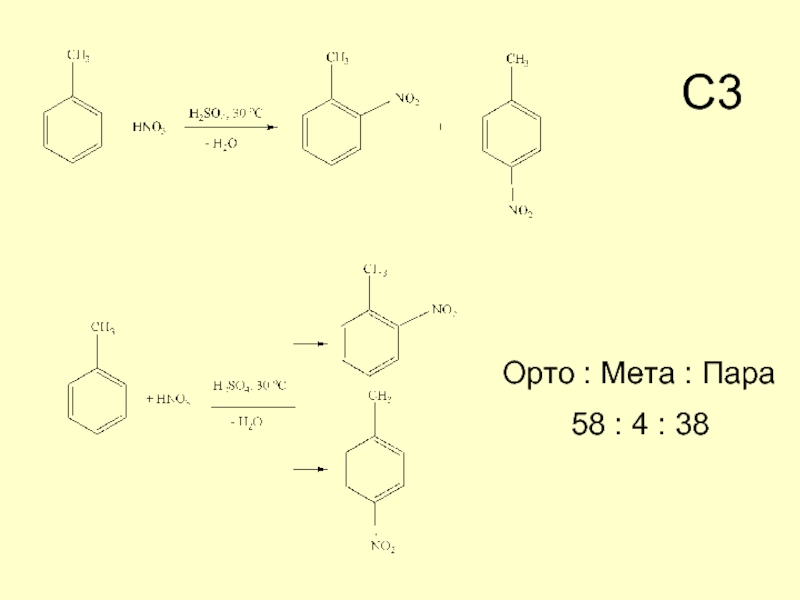
- 14. С3 Орто : Мета : Пара 58 : 4 : 38
Слайд 2С1
Cr2(SO4)3 + Br2 + NaOH =
=
Na2CrO4 + NaBr + Na2SO4+ H2O
2 Cr+3 – 3e- → Cr+6 ок-е
3 Br2 + 2e- → 2Br -1 в-е
2
3
6
16
3
8
Слайд 4Демо-2012
Соль, полученную при растворении железа в горячей концентрированной серной кислоте, обработали
избытком гидроксида натрия.
Выпавший бурый осадок отфильтровали и прокалили.
Полученное вещество сплавили с железом.
Напишите уравнения описанных реакций
Выпавший бурый осадок отфильтровали и прокалили.
Полученное вещество сплавили с железом.
Напишите уравнения описанных реакций
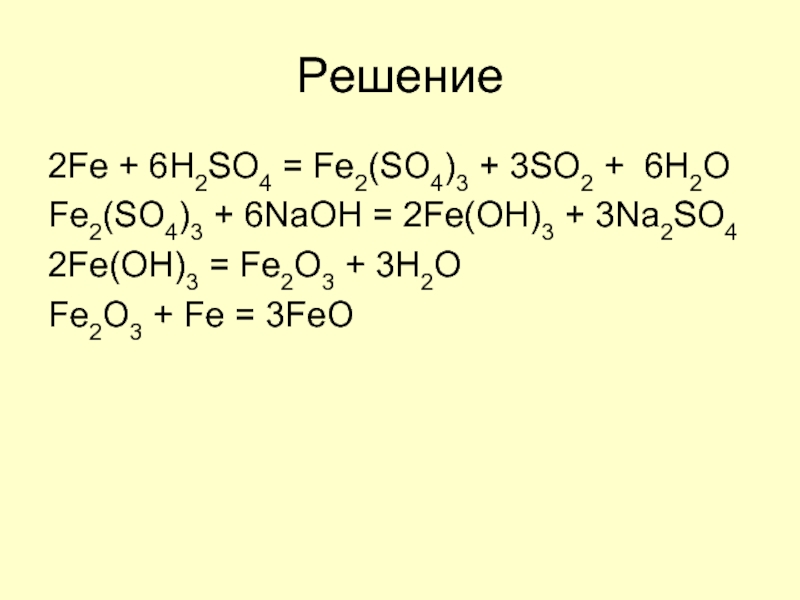
Слайд 5Решение
2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 6NaOH
= 2Fe(OH)3 + 3Na2SO4
2Fe(OH)3 = Fe2O3 + 3H2O
Fe2O3 + Fe = 3FeO
2Fe(OH)3 = Fe2O3 + 3H2O
Fe2O3 + Fe = 3FeO
Слайд 61
Продукт взаимодействия лития с азотом обработали водой.
Полученный газ пропустили через
раствор серной кислоты до прекращения химических реакций.
Полученный раствор обработали хлоридом бария.
Раствор профильтровали, а фильтрат смешали с раствором нитрита натрия и нагрели.
Полученный раствор обработали хлоридом бария.
Раствор профильтровали, а фильтрат смешали с раствором нитрита натрия и нагрели.
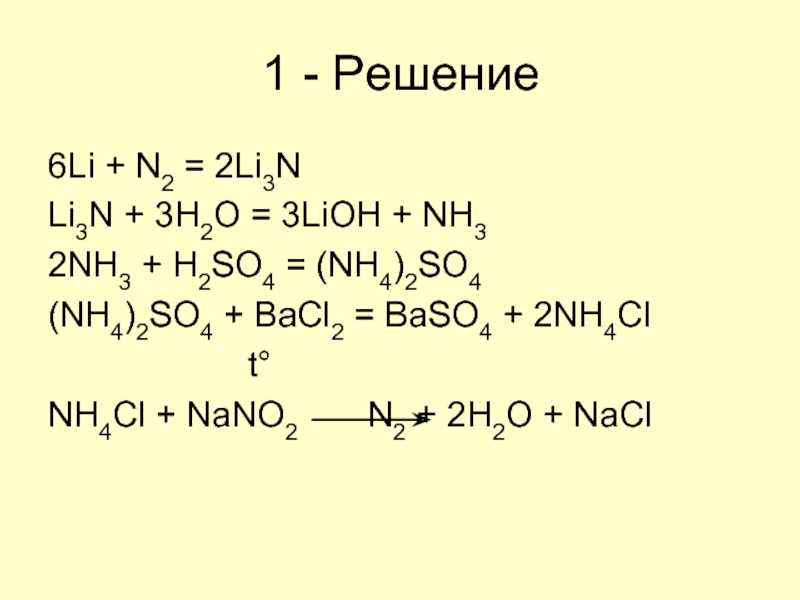
Слайд 71 - Решение
6Li + N2 = 2Li3N
Li3N + 3H2O = 3LiOH
+ NH3
2NH3 + H2SO4 = (NH4)2SO4
(NH4)2SO4 + BaCl2 = BaSO4 + 2NH4Cl
t°
NH4Cl + NaNO2 N2 + 2H2O + NaCl
2NH3 + H2SO4 = (NH4)2SO4
(NH4)2SO4 + BaCl2 = BaSO4 + 2NH4Cl
t°
NH4Cl + NaNO2 N2 + 2H2O + NaCl
Слайд 82
Навеску алюминия растворили в разбавленной азотной кислоте, при этом выделялось газообразное
простое вещество.
К полученному раствору добавили карбонат натрия до полного прекращения выделения газа.
Выпавший осадок отфильтровали и прокалили, фильтрат упарили, полученный твёрдый остаток сплавили с хлоридом аммония.
Выделившийся газ смешали с аммиаком и нагрели полученную смесь.
К полученному раствору добавили карбонат натрия до полного прекращения выделения газа.
Выпавший осадок отфильтровали и прокалили, фильтрат упарили, полученный твёрдый остаток сплавили с хлоридом аммония.
Выделившийся газ смешали с аммиаком и нагрели полученную смесь.
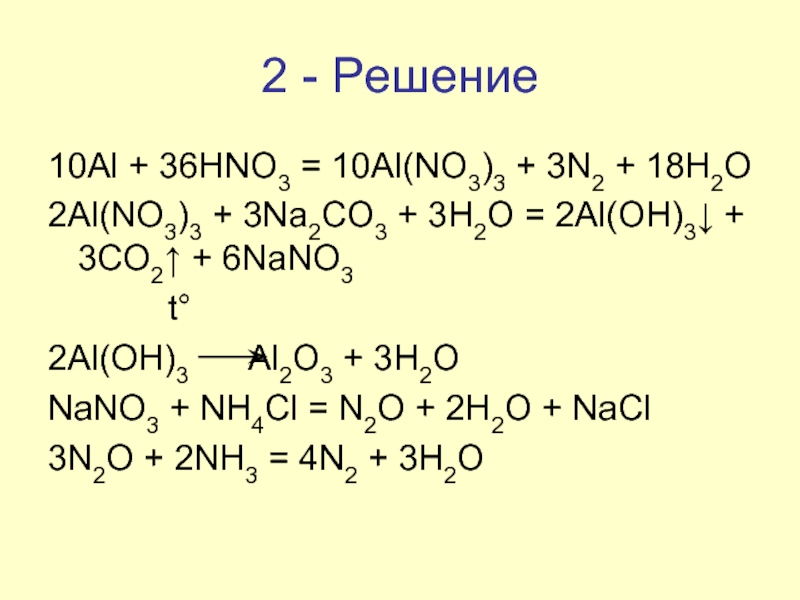
Слайд 92 - Решение
10Al + 36HNO3 = 10Al(NO3)3 + 3N2 + 18H2O
2Al(NO3)3
+ 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 6NaNO3
t°
2Al(OH)3 Al2O3 + 3H2O
NaNO3 + NH4Cl = N2O + 2H2O + NaCl
3N2O + 2NH3 = 4N2 + 3H2O
t°
2Al(OH)3 Al2O3 + 3H2O
NaNO3 + NH4Cl = N2O + 2H2O + NaCl
3N2O + 2NH3 = 4N2 + 3H2O
Слайд 103
Сульфид цинка обработали раствором соляной кислоты.
Полученный газ пропустили через избыток
раствора гидроксида натрия, затем добавили раствор хлорида железа(II).
Полученный осадок подвергли обжигу.
Полученный газ смешали с кислородом и пропустили над катализатором
Полученный осадок подвергли обжигу.
Полученный газ смешали с кислородом и пропустили над катализатором
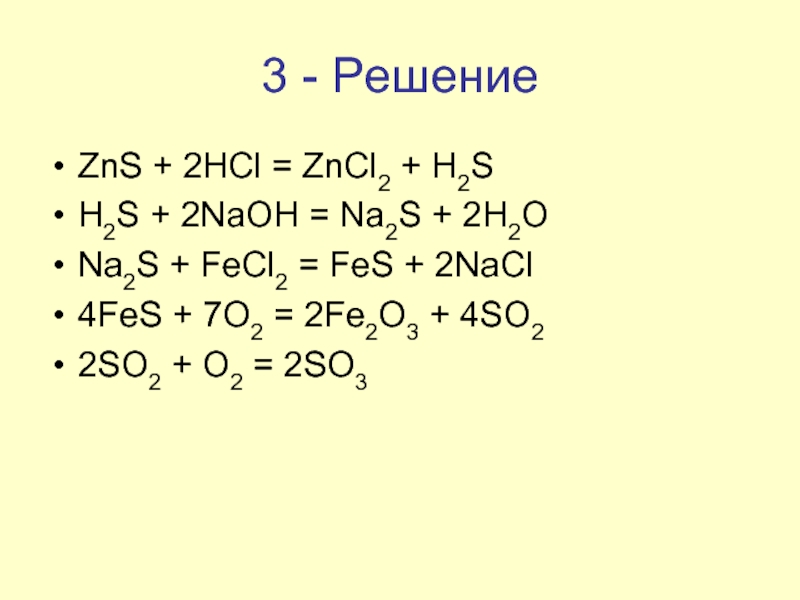
Слайд 113 - Решение
ZnS + 2HCl = ZnCl2 + H2S
H2S + 2NaOH
= Na2S + 2H2O
Na2S + FeCl2 = FeS + 2NaCl
4FeS + 7O2 = 2Fe2O3 + 4SO2
2SO2 + O2 = 2SO3
Na2S + FeCl2 = FeS + 2NaCl
4FeS + 7O2 = 2Fe2O3 + 4SO2
2SO2 + O2 = 2SO3
Слайд 12Задание на дом. 1
Фосфат кальция сплавили с углём и песком, затем
полученное простое вещество сожгли в избытке кислорода, продукт сжигания растворили в избытке едкого натра. К полученному раствору прилили раствор хлорида бария. Полученный осадок обработали избытком фосфорной кислоты.
Слайд 13Задание на дом. 2
На сухой хлорид натрия подействовали концентрированной серной кислотой
при слабом нагревании, образующийся газ пропустили в раствор гидроксида бария. К полученному раствору прилили раствор сульфата калия. Полученный осадок сплавили с углем. Полученное вещество обработали соляной кислотой.