- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
"Химические свойства одноосновных (предельных) карбоновых кислот" презентация
Содержание
- 1. "Химические свойства одноосновных (предельных) карбоновых кислот"
- 2. На уроке мы должны: изучить химические
- 3. Давайте подумаем: 1. Какие вещества называют к/кислотами?
- 4. К\кислоты в природе
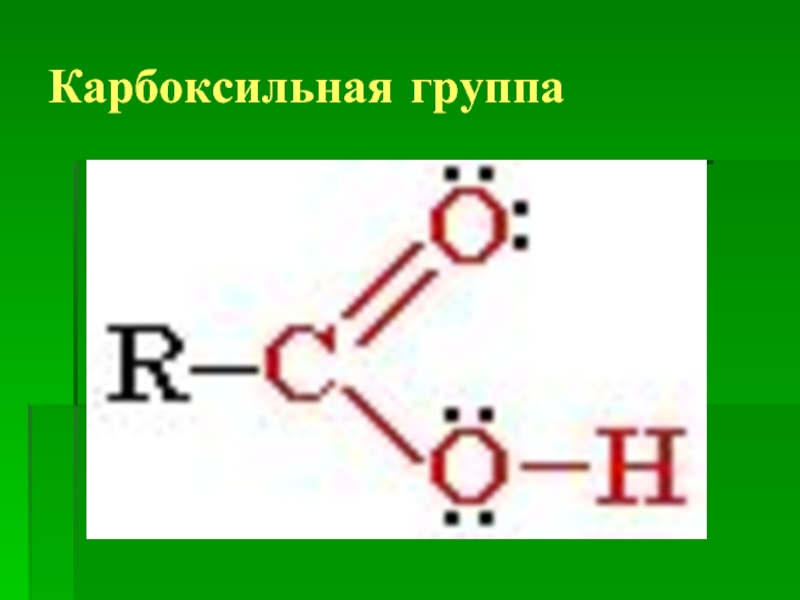
- 5. Карбоксильная группа
- 6. Классификация карбоновых кислот По числу
- 7. Общая формула одноосновных кислот предельного ряда?
- 8. Представители предельных карбоновых кислот? Метановая или муравьиная
- 9. Простейшие карбоновые кислоты
- 10. Муравьиная кислота. Муравьиная кислота. Муравьиная
- 11. Что такое «ледяная» уксусная кислота? Безводная Почему так названа?
- 12. Внимание, видеоопыт.
- 13. Тест «5» за 5 минут 1.Двухосновной кислотой
- 14. Ответы 1.Двухосновной кислотой является А) лимонная
- 15. 1 Общие кислотные свойства
- 16. А) Диссоциация карбоновых кислот: СН3–COOH ↔ СН3–COO-
- 17. Внимание, видеоопыт!
- 18. Б) Взаимодействие с металлами Запишите уравнение реакции
- 19. От чего зависит скорость взаимодействия металлов с
- 20. Посмотрим видеоопыт
- 21. В) Взаимодействие с основаниями
- 22. Атом водорода в гидроксиле карбоксильной группы
- 23. Запишите уравнение реакции СН3–COOH + NaOH →
- 24. Г) Взаимодействие с оксидами металлов
- 25. Запишите уравнение реакции в общем виде R–COOH + MeО → R–COOMe + H2О
- 26. С какими солями реагировали неорганические кислоты? Кислоты
- 27. Внимание, видеоопыт!
- 28. Запишите уравнение реакции СН3–COOH + Na2СО3 →
- 29. 2.Специфические свойства к\кислот Все данные свойства являются
- 30. А)Галогенирование (замещение идет в альфа-положении). Замещение
- 31. Б) Замещение –ОН группы. Реакция этерификации -
- 32. Реакция этерификации – образование сложных эфиров при взаимодействии карбоновых кислот со спиртами
- 33. 3. Специфические свойства метановой кислоты Чем метановая
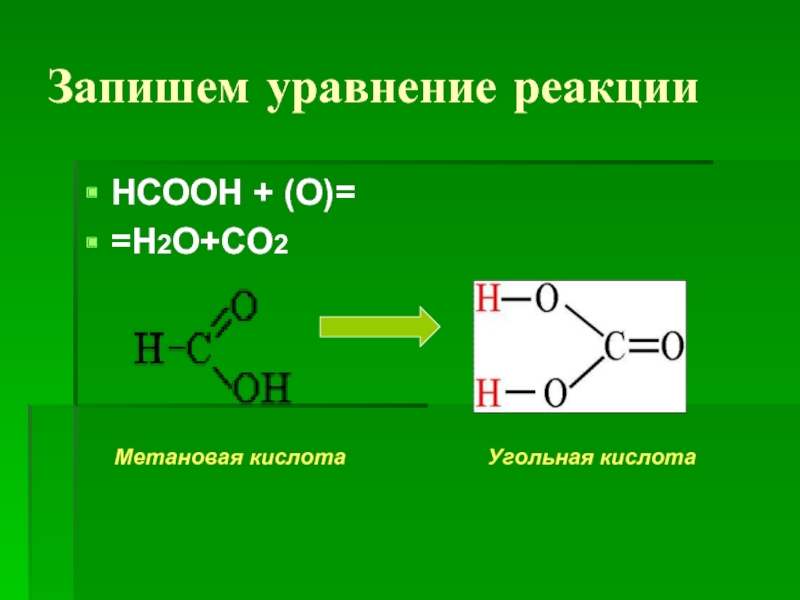
- 34. В) Окисление метановой кислоты
- 35. Запишем уравнение реакции НСООН + (О)= =Н2О+СО2
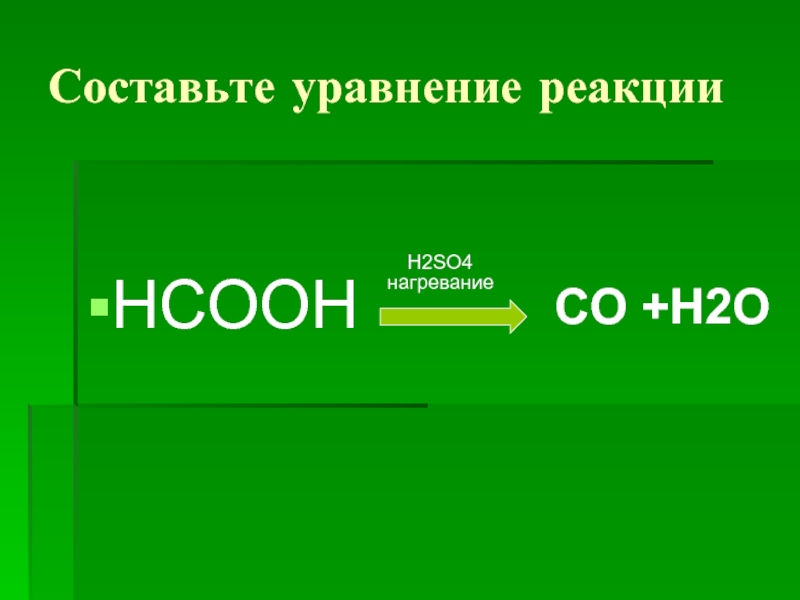
- 36. Г) Разложение метановой кислоты
- 37. Составьте уравнение реакции НСООН нагревание СО +Н2О H2SO4
- 38. Выводы . Общие свойства, характерные для
- 39. Домашнее задание Устно: Изучить параграф 20 (стр 180-181 )
- 40. Самостоятельная работа 1. Какой объем газа (при
Слайд 2На уроке мы должны:
изучить химические свойства одноосновных карбоновых кислот на примере
уксусной кислоты; специфические свойства карбоновых кислот;
вспомнить взаимное влияние атомов в молекулах карбоновых кислот;
развивать логическое мышление, умение обобщать и делать выводы.
вспомнить взаимное влияние атомов в молекулах карбоновых кислот;
развивать логическое мышление, умение обобщать и делать выводы.
Слайд 3Давайте подумаем:
1. Какие вещества называют к/кислотами?
Органические соединения, в молекулах которых
углеводородный радикал связан с карбоксильной группой
Где они встречаются?
Где они встречаются?
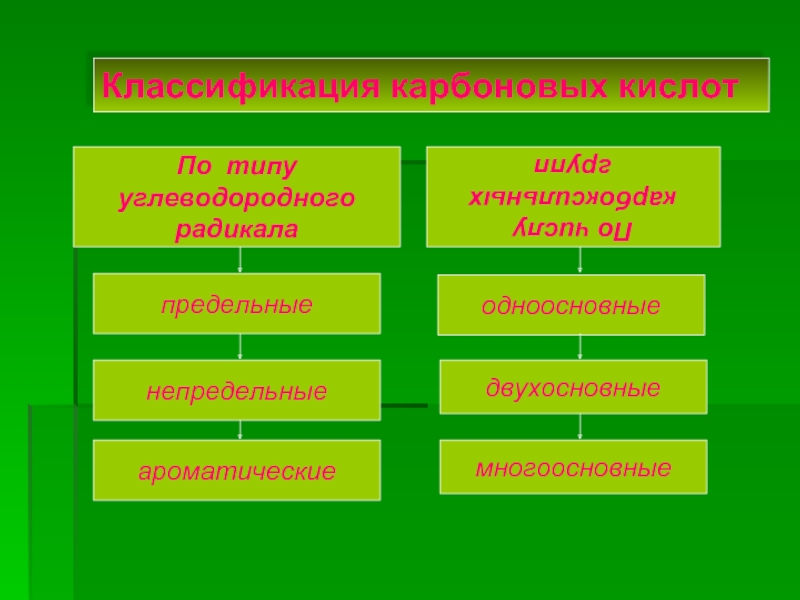
Слайд 6Классификация карбоновых кислот
По числу карбоксильных
групп
непредельные
ароматические
одноосновные
двухосновные
многоосновные
предельные
По типу углеводородного
радикала
Слайд 8Представители предельных карбоновых кислот?
Метановая или муравьиная
Этановая или уксусная
Пропановая или пропионовая
Бутановая и
т.д.
Слайд 10Муравьиная кислота.
Муравьиная кислота.
Муравьиная кислота –
НСООН. Жидкость с резким
запахом. Содержится
в
хвое, крапиве, едких выделе-
ниях муравьев и пчел.
Применяется для получения
лекарственных средств,
пестицидов и растворителей.
хвое, крапиве, едких выделе-
ниях муравьев и пчел.
Применяется для получения
лекарственных средств,
пестицидов и растворителей.
Слайд 13Тест «5» за 5 минут
1.Двухосновной кислотой является
А) лимонная Б) яблочная В)щавелевая
Г) акриловая
2.К ароматическим кислотам относится
А) щавелевая Б)масляная В) фталевая Г)молочная
3.Малоновая и метандикарбоновая кислота являются
А) изомерами Б)гомологами В)одним и тем же веществом Г)ядовитыми веществами
4.Из за взаимного влияния атомов в карбоксильной группе
А) связь О-Н ослабляется Б) атом С притягивает к себе неподеленную электронную пару атома кислорода в группе ОН
В) атом Н более подвижен Г) все перечисленное
5.Консервант под кодом Е-260 это кислота
А) метановая Б)этановая В) щавелевая Г) молочная
2.К ароматическим кислотам относится
А) щавелевая Б)масляная В) фталевая Г)молочная
3.Малоновая и метандикарбоновая кислота являются
А) изомерами Б)гомологами В)одним и тем же веществом Г)ядовитыми веществами
4.Из за взаимного влияния атомов в карбоксильной группе
А) связь О-Н ослабляется Б) атом С притягивает к себе неподеленную электронную пару атома кислорода в группе ОН
В) атом Н более подвижен Г) все перечисленное
5.Консервант под кодом Е-260 это кислота
А) метановая Б)этановая В) щавелевая Г) молочная
Слайд 14Ответы
1.Двухосновной кислотой является
А) лимонная Б) яблочная В)щавелевая Г) акриловая
2.К ароматическим
кислотам относится
А) щавелевая Б)масляная В) фталевая Г)молочная
3.Малоновая и метандикарбоновая кислота являются
А) изомерами Б)гомологами В)одним и тем же веществом Г)ядовитыми веществами
4.Из за взаимного влияния атомов в карбоксильной группе
А) связь О-Н ослабляется Б) атом С притягивает к себе неподеленную электронную пару атома кислорода в группе ОН
В) атом Н более подвижен Г) все перечисленное
5.Консервант под кодом Е-260 это кислота
А) метановая Б)этановая В) щавелевая Г) молочная
А) щавелевая Б)масляная В) фталевая Г)молочная
3.Малоновая и метандикарбоновая кислота являются
А) изомерами Б)гомологами В)одним и тем же веществом Г)ядовитыми веществами
4.Из за взаимного влияния атомов в карбоксильной группе
А) связь О-Н ослабляется Б) атом С притягивает к себе неподеленную электронную пару атома кислорода в группе ОН
В) атом Н более подвижен Г) все перечисленное
5.Консервант под кодом Е-260 это кислота
А) метановая Б)этановая В) щавелевая Г) молочная
Слайд 16А) Диссоциация карбоновых кислот:
СН3–COOH ↔ СН3–COO- + H+
образующийся ион водорода
придает раствору кислую среду.
С какими простыми веществами реагируют кислоты?
С активными металлами
С какими простыми веществами реагируют кислоты?
С активными металлами
Слайд 18Б) Взаимодействие с металлами
Запишите уравнение реакции уксусной кислоты с магнием
СН3–COOH +Mg
→
(CH3–COO)2Mg + H2↑
Уравните
2СН3–COOH +Mg →(CH3–COO)2Mg + H2↑
ацетат магния
(CH3–COO)2Mg + H2↑
Уравните
2СН3–COOH +Mg →(CH3–COO)2Mg + H2↑
ацетат магния
Слайд 19От чего зависит скорость взаимодействия металлов с уксусной кислотой?
От активности металла
и концентрации кислоты
Концентрированная или разбавленная кислота будет реагировать с магнием быстрее?
Концентрированная или разбавленная кислота будет реагировать с магнием быстрее?
Слайд 22
Атом водорода в гидроксиле карбоксильной группы обладает большой подвижностью, легко отщепляясь
в виде положительно заряженного иона водорода и обуславливая кислотные свойства карбоновых кислот
Слайд 26С какими солями реагировали неорганические кислоты?
Кислоты реагируют с солями более слабых
кислот. Из неорганических кислот какая кислота слабая? (применяем в качестве напитка)
Угольная (газвода)
Угольная (газвода)
Слайд 28Запишите уравнение реакции
СН3–COOH + Na2СО3 →
CH3–COONa + СО2↑ + H2О
Уравните
2СН3–COOH + Na2СО3 →
2CH3–COONa + СО2↑ + H2О
Слайд 292.Специфические свойства к\кислот
Все данные свойства являются общими химическими свойствами для всех
кислот, как органических, так и неорганических. Но карбоновые кислоты, как представители органических соединений, обладают и особыми свойствами, так называемыми – специфическими.
Слайд 30А)Галогенирование (замещение идет в альфа-положении).
Замещение Н может протекать не только
в функциональной группе, но и в радикале
СН3–COOH + Cl–Cl → СН2Cl–COOH + HCl
2-хлоруксусная кислота
СН3–COOH + Cl–Cl → СН2Cl–COOH + HCl
2-хлоруксусная кислота
Слайд 31Б) Замещение –ОН группы.
Реакция этерификации - образование сложных эфиров (при нагревании
в присутствии серной кислоты).
С3Н7–COOH + СН3–CH2OH ↔
С3Н7–COOСН2 СН3 + H2О
Этилбутанат (фруктовый запах)
С3Н7–COOH + СН3–CH2OH ↔
С3Н7–COOСН2 СН3 + H2О
Этилбутанат (фруктовый запах)
Слайд 32Реакция этерификации – образование сложных эфиров при взаимодействии карбоновых кислот со
спиртами
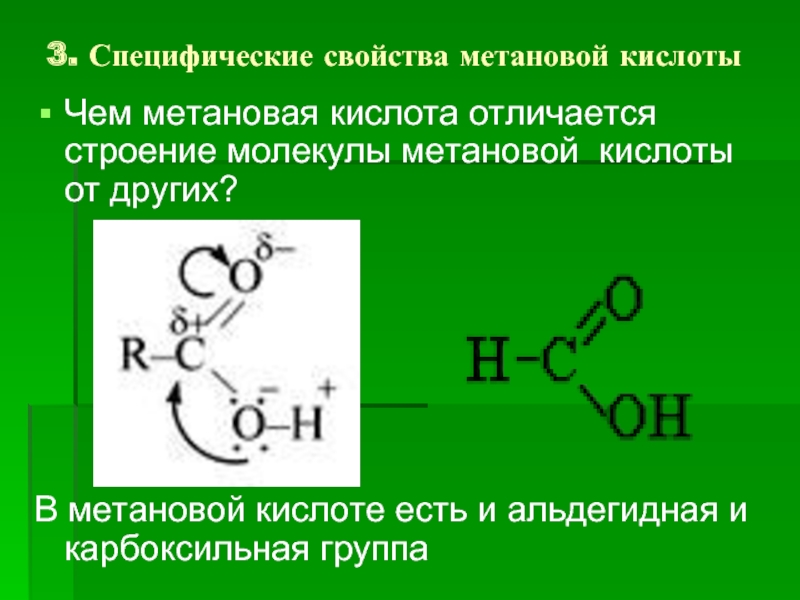
Слайд 333. Специфические свойства метановой кислоты
Чем метановая кислота отличается строение молекулы метановой
кислоты от других?
В метановой кислоте есть и альдегидная и карбоксильная группа
В метановой кислоте есть и альдегидная и карбоксильная группа
Слайд 38Выводы
. Общие свойства, характерные для класса карбоновых кислот, обусловлены наличием в
молекулах гидроксильной группы, которая содержит резко полярную связь между атомами водорода и кислорода.
Для карбоновых кислот характерны свойства как общие с неорганическими кислотами, так и специфические, присущие только органическим кислотам
Для карбоновых кислот характерны свойства как общие с неорганическими кислотами, так и специфические, присущие только органическим кислотам
Слайд 40Самостоятельная работа
1. Какой объем газа (при н.у.) выделится при взаимодействии раствора
уксусной кислоты массой 100 г (массовая доля вещества 55%), с металлическим натрием, массой 10 г?
2. Составьте уравнения химических реакции согласно цепочке превращении:
Углерод → Этан → Этилен → Этанол → Этановая кислота → Ацетат магния
3. Закончите уравнения химических реакции, напишите их в молекулярном и ионном виде:
а) HCOOH + Mg = б) CH3COOH + KOH = в) C2H5COOH + CaO =
2. Составьте уравнения химических реакции согласно цепочке превращении:
Углерод → Этан → Этилен → Этанол → Этановая кислота → Ацетат магния
3. Закончите уравнения химических реакции, напишите их в молекулярном и ионном виде:
а) HCOOH + Mg = б) CH3COOH + KOH = в) C2H5COOH + CaO =