- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические свойства кислотных оксидов презентация
Содержание
- 1. Химические свойства кислотных оксидов
- 2. Вспомним, что такое кислотные оксиды? Кислотные
- 3. Кислотные оксиды реагируют: 1. Со щелочами. В
- 4. Запишите уравнения самостоятельно, назовите продукты реакции SO2
- 5. Проверь себя: SO2 + 2KOH → K2SO3
- 6. Кислотные оксиды реагируют: 2. С водой. При
- 7. Чтобы не ошибиться в составлении формулы соли
- 8. Кислотные оксиды реагируют: 3. С основными оксидами.
- 9. Запишите уравнения самостоятельно, назовите продукты реакции CaO
- 10. Проверь себя: CaO + CO2 → CaCO3
- 11. Кислотные оксиды реагируют: 4. Менее летучие кислотные
- 12. Кислотные оксиды реагируют: 5. Кислотный оксид, содержащий
- 13. Выполни тест для закрепления темы 1.
- 14. Выполни тест для закрепления темы 3.
- 15. Выполни тест для закрепления темы 5.
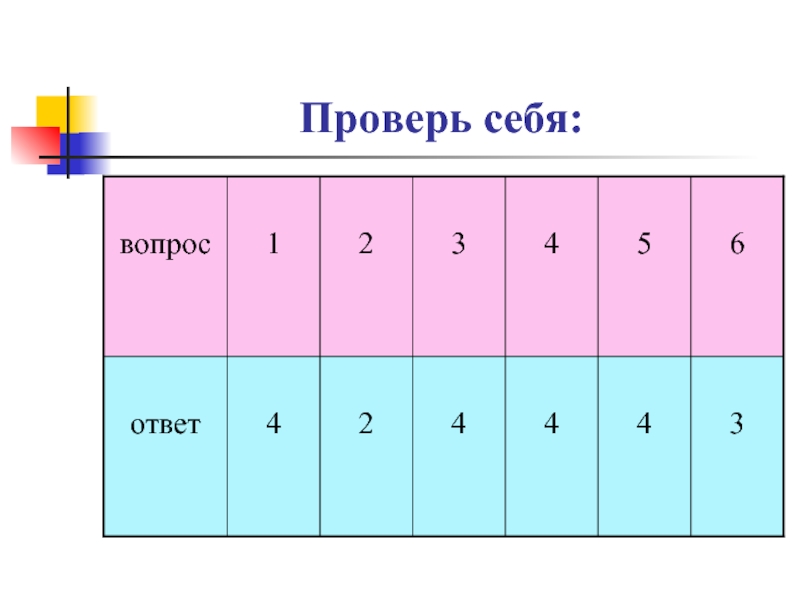
- 16. Проверь себя:
Слайд 2Вспомним,
что такое кислотные оксиды?
Кислотные оксиды – это солеобразующие оксиды неметаллов,
например:
+4
SO2 – оксид серы (IV)
+6
SO3 – оксид серы (VI)
+5
P2O5 – оксид фосфора (V)
+4
SO2 – оксид серы (IV)
+6
SO3 – оксид серы (VI)
+5
P2O5 – оксид фосфора (V)
Слайд 3Кислотные оксиды реагируют:
1. Со щелочами. В результате реакции образуются соль и
вода. Эта реакция служит доказательством кислотного характера оксида.
SO3 + 2NaOH → Na2SO4 + H2O
сульфат натрия вода
CO2 + Ca(OH)2 → CaCO3↓ + H2O
карбонат кальция вода
SO3 + 2NaOH → Na2SO4 + H2O
сульфат натрия вода
CO2 + Ca(OH)2 → CaCO3↓ + H2O
карбонат кальция вода
Слайд 4Запишите уравнения самостоятельно, назовите продукты реакции
SO2 + KOH →
P2O5 + LiOH
→
SO3 + Ba(OH)2 →
CO2 + NaOH →
SO3 + Ba(OH)2 →
CO2 + NaOH →
Слайд 5Проверь себя:
SO2 + 2KOH → K2SO3 + H2O
сульфит калия вода
P2O5 + 6LiOH → 2Li3PO4 + 3H2O
фосфат лития вода
SO3 + Ba(OH)2 → BaSO4↓+ H2O
сульфат бария
CO2 + 2NaOH → Nа2CO3 + H2O
карбонат натрия
P2O5 + 6LiOH → 2Li3PO4 + 3H2O
фосфат лития вода
SO3 + Ba(OH)2 → BaSO4↓+ H2O
сульфат бария
CO2 + 2NaOH → Nа2CO3 + H2O
карбонат натрия
Слайд 6Кислотные оксиды реагируют:
2. С водой. При этом образуется кислота. Исключением является
SiO2.Он с водой не реагирует, а кремниевую кислоту получают косвенным путем.
SO3 + H2O → H2SO4
серная кислота
P2O5 + 3H2O → 2H3PO4
фосфорная кислота
SO3 + H2O → H2SO4
серная кислота
P2O5 + 3H2O → 2H3PO4
фосфорная кислота
Слайд 7Чтобы не ошибиться в составлении формулы соли вспомните, что …
кислотному оксиду
SO2 соответствует H2SO3
кислотному оксиду SO3 соответствует H2SO4
кислотному оксиду CO2 соответствует H2CO3
кислотному оксиду P2O5 соответствует H3PO4
кислотному оксиду SiO2 соответствует H2SiO3
кислотному оксиду N2O5 соответствует HNO3
кислотному оксиду SO3 соответствует H2SO4
кислотному оксиду CO2 соответствует H2CO3
кислотному оксиду P2O5 соответствует H3PO4
кислотному оксиду SiO2 соответствует H2SiO3
кислотному оксиду N2O5 соответствует HNO3
Слайд 8Кислотные оксиды реагируют:
3. С основными оксидами. При этом образуется соль.
CO2 +
CaO → CaCO3
карбонат кальция
SO3 + K2O → K2SO4
сульфат калия
карбонат кальция
SO3 + K2O → K2SO4
сульфат калия
Слайд 9Запишите уравнения самостоятельно, назовите продукты реакции
CaO + CO2 →
Li2O + CO2
→
BaO + SO2 →
Na2O + SO3 →
K2O + P2O5 →
BaO + SO2 →
Na2O + SO3 →
K2O + P2O5 →
Слайд 10Проверь себя:
CaO + CO2 → CaCO3 - карбонат кальция
Li2O + CO2
→ Li2CO3 - карбонат лития
BaO + SO2 → BaSO3- сульфит бария
Na2O + SO3 → Na2SO4 – сульфат натрия
3K2O + P2O5 →2K3PO4 – фосфат калия
BaO + SO2 → BaSO3- сульфит бария
Na2O + SO3 → Na2SO4 – сульфат натрия
3K2O + P2O5 →2K3PO4 – фосфат калия
Слайд 11Кислотные оксиды реагируют:
4. Менее летучие кислотные оксиды вытесняют более летучие кислотные
оксиды из их солей.
сплавление
Na2CO3 + SiO2 → Na2SiO3 + CO2↑
сплавление
Na2CO3 + SiO2 → Na2SiO3 + CO2↑
Слайд 12Кислотные оксиды реагируют:
5. Кислотный оксид, содержащий элемент, способный повысить степень окисления,
может реагировать с кислородом.
+4 +6
2SO2 + O2 → 2SO3
+4 +6
2SO2 + O2 → 2SO3
Слайд 13Выполни тест
для закрепления темы
1. Большинство кислотных оксидов реагирует:
1. только с
водой
2. только с кислотами
3. со щелочами и кислотами
4. с водой и щелочами
2. Укажите номер кислотного оксида:
1.K2O 3. H2SO3
2. P2O5 4. BaO
2. только с кислотами
3. со щелочами и кислотами
4. с водой и щелочами
2. Укажите номер кислотного оксида:
1.K2O 3. H2SO3
2. P2O5 4. BaO
Слайд 14Выполни тест
для закрепления темы
3. С оксидом углерода (IV) взаимодействует:
1. P2O5
3. HCl
2. Na2SO4 4. CaO
4. Оксид серы (VI) не реагирует с:
1. NaOH 3. CaO
2. H2O 4. CO2
2. Na2SO4 4. CaO
4. Оксид серы (VI) не реагирует с:
1. NaOH 3. CaO
2. H2O 4. CO2
Слайд 15Выполни тест
для закрепления темы
5. Оксид фосфора (V) не реагирует с:
1.
H2O 3. NaOH
2. CaO 4. SO3
6. Укажите оксиды, взаимодействующие между собой:
1.Li2O и CaO 3. SO3 и Na2O
2. CO2 и SiO2 4. BaO и MgO
2. CaO 4. SO3
6. Укажите оксиды, взаимодействующие между собой:
1.Li2O и CaO 3. SO3 и Na2O
2. CO2 и SiO2 4. BaO и MgO