- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические свойства бензола презентация
Содержание
- 1. Химические свойства бензола
- 2. Химические свойства бензола определяются строением его молекулы.
- 3. Нитрование. При действии на бензол смеси концентрированных
- 4. Галогенирование (хлорирование, бромирование, иодирование) осуществляется в присутствии
- 5. Сульфирование. При взаимодействии с серной кислотой бензол образует бензолсульфоновую кислоту.
- 6. Алкилирование – замещение атома водорода в бензольном
- 7. Реакции присоединения протекают с большим трудом. На
- 8. К действию окислителей бензол довольно устойчив. Он
- 9. На воздухе бензол горит коптящим пламенем 2С6Н6 + 15О2 = 12СО2+ 6Н2О
- 10. Реакции замещения после введения в бензольное ядро
- 11. Заместители первого рода (-CH3, -CH2R, -CHR2, CR3,
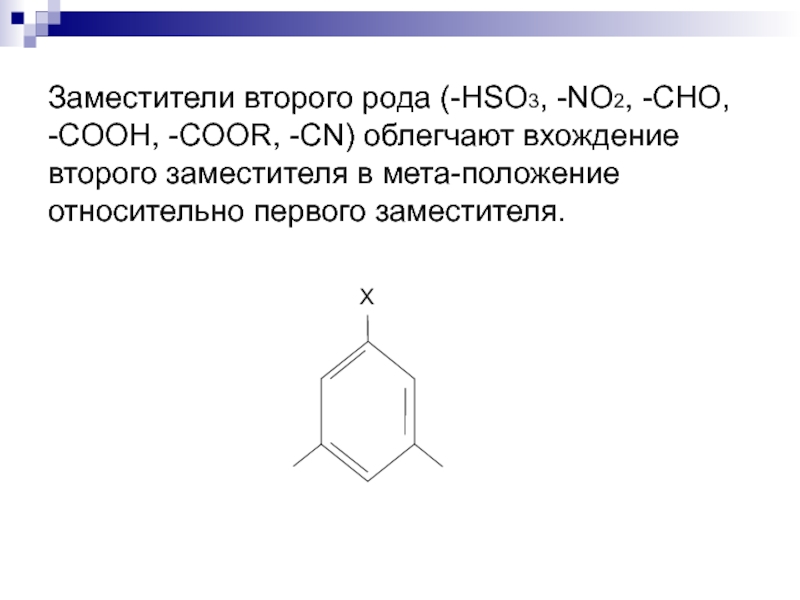
- 12. Заместители второго рода (-HSO3, -NO2, -CHO, -COOH,
- 13. Сила заместителей первого рода –OH > –NH2
- 14. ЗАКРЕПЛЕНИЕ ПРОЙДЕННОГО МАТЕРИАЛА: 1. Запишите реакции нитрования
- 15. РЕШЕНИЕ РАСЧЕТНЫХ ЗАДАЧ: Для сжигания ароматического углеводорода
- 16. ДОМАШНЕЕ ЗАДАНИЕ: § 26(1-3). Из задачника
Слайд 2Химические свойства бензола определяются строением его молекулы. Образование сопряженной π-электронной системы
сопровождается выделением 150кДж энергии. Это так называемая энергия стабилизации, благодаря которой ароматические системы обладают повышенной устойчивостью.
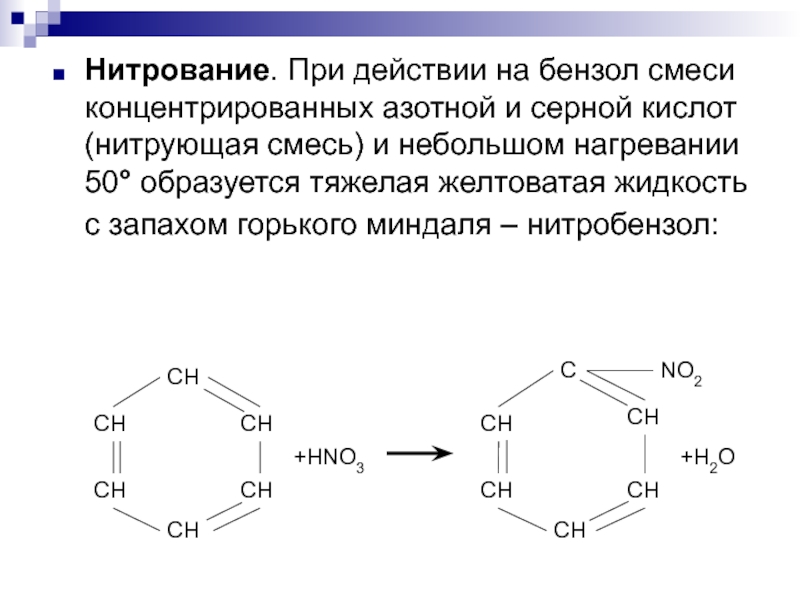
Слайд 3Нитрование. При действии на бензол смеси концентрированных азотной и серной кислот
(нитрующая смесь) и небольшом нагревании 50° образуется тяжелая желтоватая жидкость с запахом горького миндаля – нитробензол:
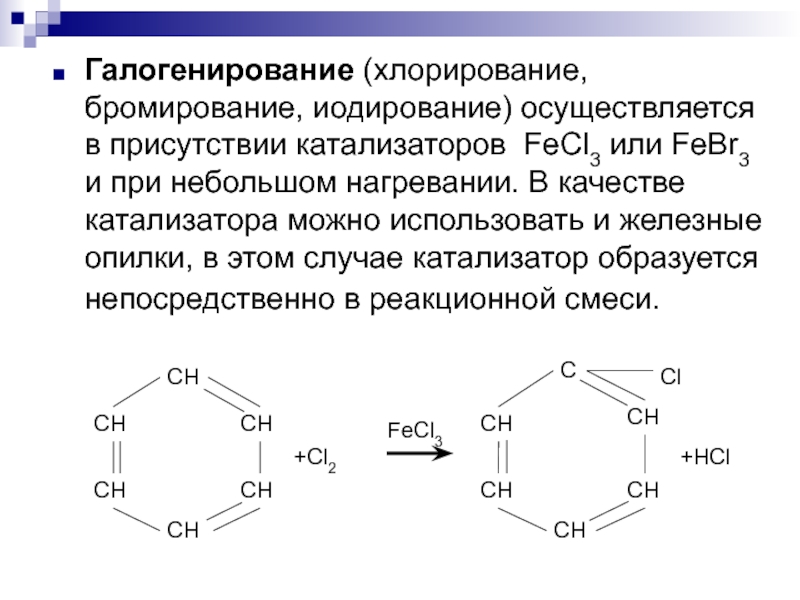
Слайд 4Галогенирование (хлорирование, бромирование, иодирование) осуществляется в присутствии катализаторов FeCl3 или FeBr3
и при небольшом нагревании. В качестве катализатора можно использовать и железные опилки, в этом случае катализатор образуется непосредственно в реакционной смеси.
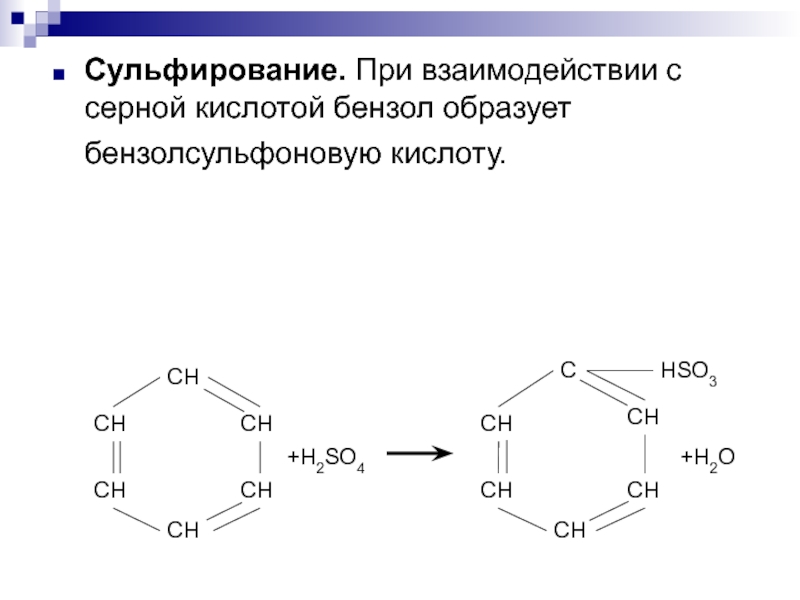
Слайд 5Сульфирование. При взаимодействии с серной кислотой бензол образует бензолсульфоновую кислоту.
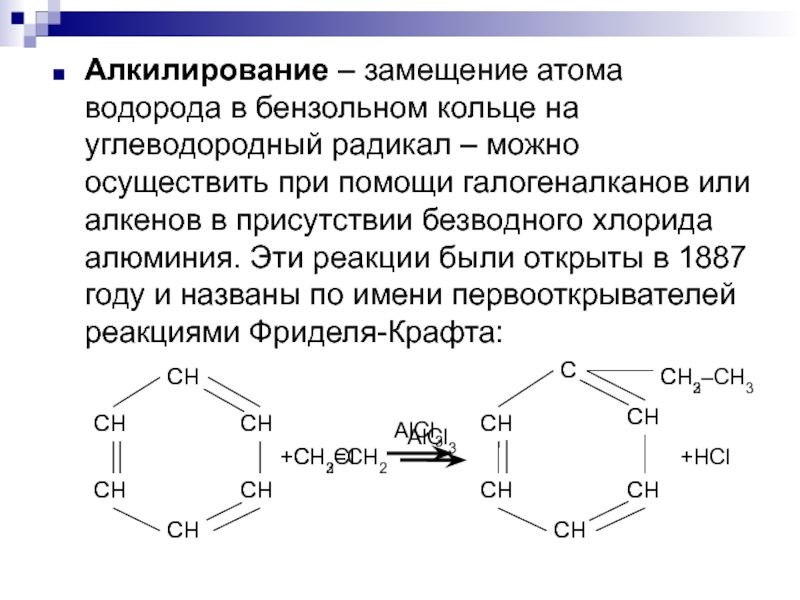
Слайд 6Алкилирование – замещение атома водорода в бензольном кольце на углеводородный радикал
– можно осуществить при помощи галогеналканов или алкенов в присутствии безводного хлорида алюминия. Эти реакции были открыты в 1887 году и названы по имени первооткрывателей реакциями Фриделя-Крафта:
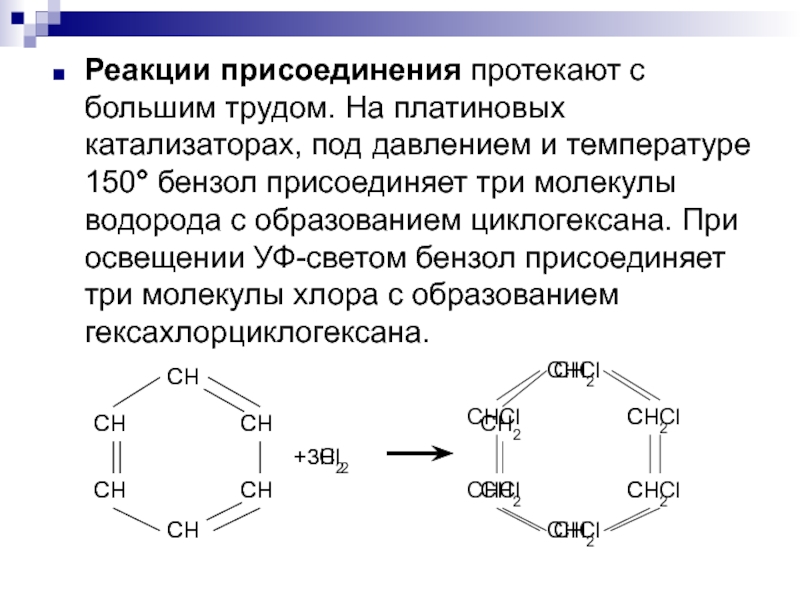
Слайд 7Реакции присоединения протекают с большим трудом. На платиновых катализаторах, под давлением
и температуре 150° бензол присоединяет три молекулы водорода с образованием циклогексана. При освещении УФ-светом бензол присоединяет три молекулы хлора с образованием гексахлорциклогексана.
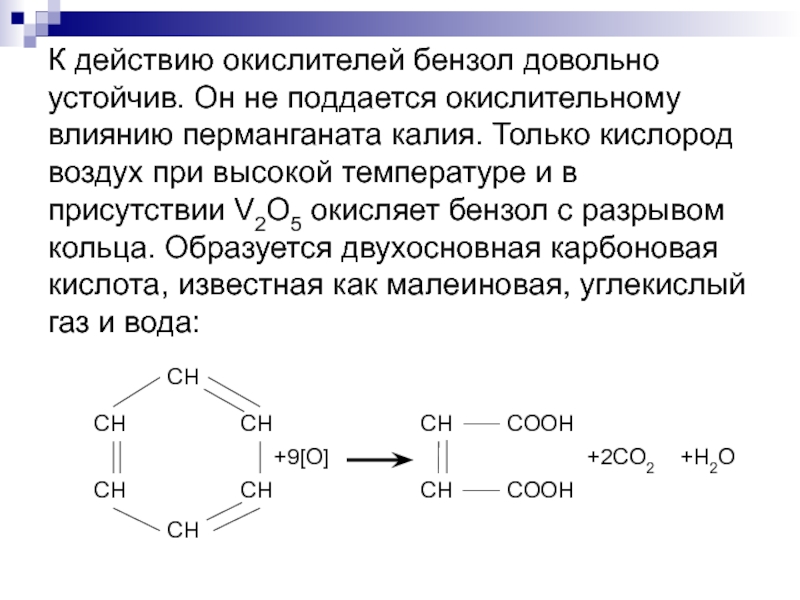
Слайд 8К действию окислителей бензол довольно устойчив. Он не поддается окислительному влиянию
перманганата калия. Только кислород воздух при высокой температуре и в присутствии V2O5 окисляет бензол с разрывом кольца. Образуется двухосновная карбоновая кислота, известная как малеиновая, углекислый газ и вода:
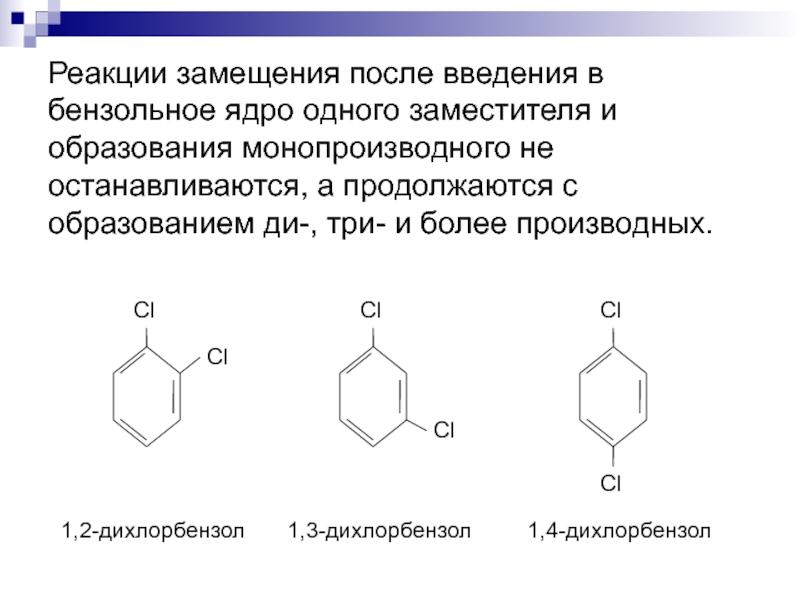
Слайд 10Реакции замещения после введения в бензольное ядро одного заместителя и образования
монопроизводного не останавливаются, а продолжаются с образованием ди-, три- и более производных.
1,2-дихлорбензол
1,3-дихлорбензол
1,4-дихлорбензол
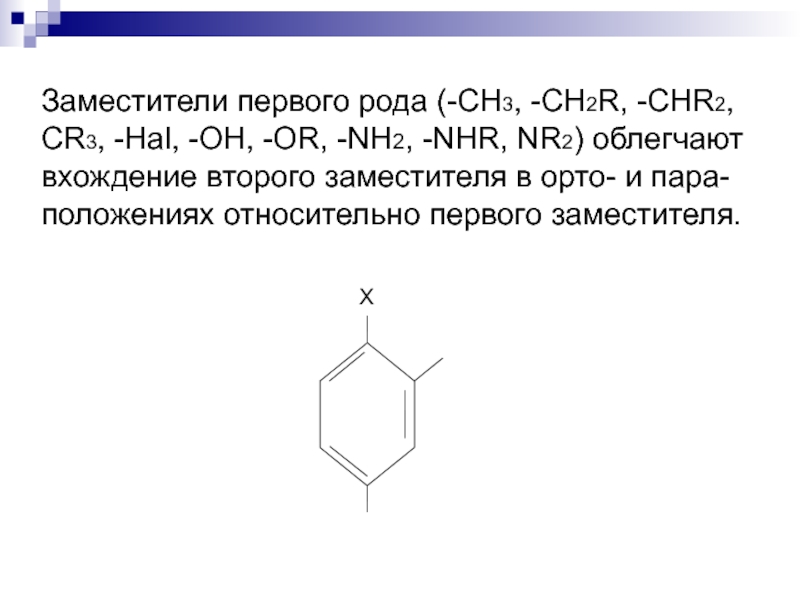
Слайд 11Заместители первого рода (-CH3, -CH2R, -CHR2, CR3, -Hal, -OH, -OR, -NH2,
-NHR, NR2) облегчают вхождение второго заместителя в орто- и пара-положениях относительно первого заместителя.
Слайд 12Заместители второго рода (-HSO3, -NO2, -CHO, -COOH, -COOR, -CN) облегчают вхождение
второго заместителя в мета-положение относительно первого заместителя.
Слайд 13Сила заместителей первого рода –OH > –NH2 > –NHR > –NR2 > >
–OR > –CR3 > –CHR2 > –CH2R >
> –CH3 > –Hal
Сила заместителей второго рода –CN > –COOH > –COOR > –CHO > –NO2 >–HSO3
Слайд 14ЗАКРЕПЛЕНИЕ ПРОЙДЕННОГО МАТЕРИАЛА:
1. Запишите реакции нитрования и сульфирования бензола по первой
и второй стадии. Продукты реакции назовите.
2. Запишите реакции хлорирования и алкилирования бензола по первой и второй стадии. Продукты реакции назовите.
3. Запишите реакции хлорирования 1,3-диметилбензола, 1,2-диметилбензола, 1-метил-2-нитробензола, 1-метил-3-нитробензола, 1-метил-2-аминобензол Труднее или легче будут протекать эти реакции по сравнению с реакциями хлорирования?
2. Запишите реакции хлорирования и алкилирования бензола по первой и второй стадии. Продукты реакции назовите.
3. Запишите реакции хлорирования 1,3-диметилбензола, 1,2-диметилбензола, 1-метил-2-нитробензола, 1-метил-3-нитробензола, 1-метил-2-аминобензол Труднее или легче будут протекать эти реакции по сравнению с реакциями хлорирования?
Слайд 15РЕШЕНИЕ РАСЧЕТНЫХ ЗАДАЧ:
Для сжигания ароматического углеводорода массой 21,2г потребовалось 47,14л кислорода.
Определите его молекулярную формулу, запишите и назовите возможные изомеры, укажите тип гибридизации каждого атома углерода.
Вычислите, какую массу бензола подвергли хлорированию на свету, если при этом было получено 11,35г продукта, что составляет 65% от теоретически возможного.
Смесь бензола с гексеном-1 массой 20г обесцвечивает 381г 4,2% раствора брома. Определить массовые доли компонентов в исходной смеси.
Вычислите, какую массу бензола подвергли хлорированию на свету, если при этом было получено 11,35г продукта, что составляет 65% от теоретически возможного.
Смесь бензола с гексеном-1 массой 20г обесцвечивает 381г 4,2% раствора брома. Определить массовые доли компонентов в исходной смеси.
Слайд 16ДОМАШНЕЕ ЗАДАНИЕ:
§ 26(1-3).
Из задачника «Органическая химия. Сборник самостоятельных работ 11
класс» Работа II, варианты 4(3), 6(3сл), 7(3), 8(3), 11(3), 13(3сл).