- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристика щелочных металлов презентация
Содержание
- 1. Характеристика щелочных металлов
- 2. Металлы Сu, Au, Ag не взаимодействуют с
- 3. Как изменяются металлические свойства в группе?
- 4. Радиусы атомов элементов 1А группы
- 5. Сравнение свойств Что общего в атомном строении
- 6. ИСТОРИЯ ОТКРЫТИЯ Натрий и калий – 1807г.
- 7. Происхождение названий Li (1817) лат. " литос"
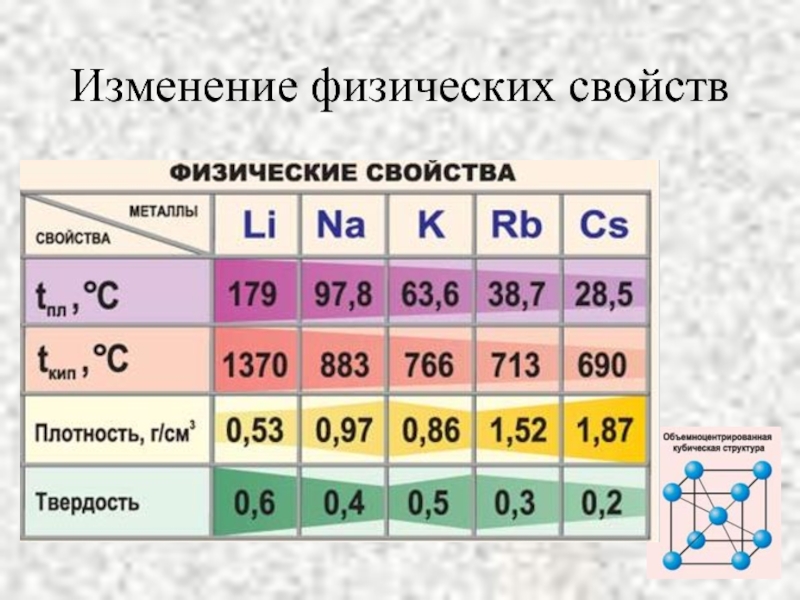
- 8. Изменение физических свойств
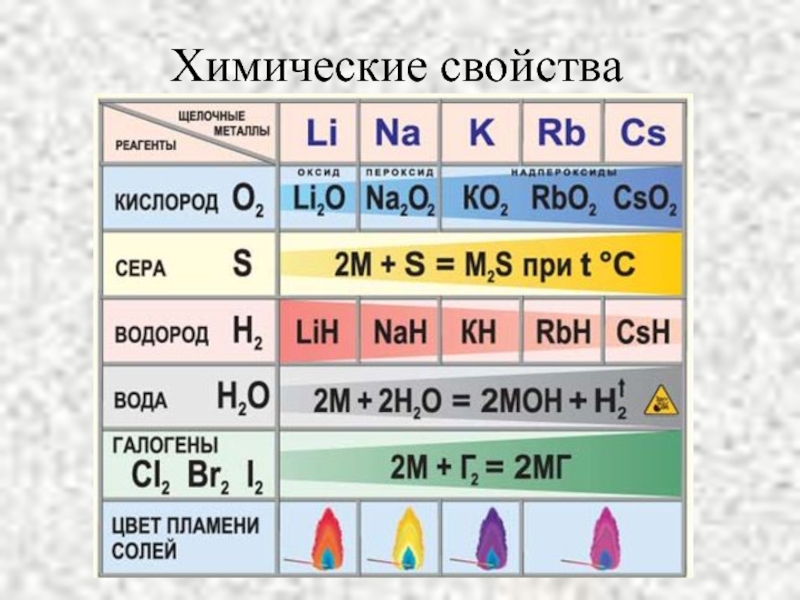
- 9. Химические свойства
- 10. Оксид лития Оксид натрия Оксиды щелочных металлов Составьте общую формулу оксидов.
- 11. KOH – гидроксид калия NaOH – гидроксид
- 12. Нахождение в природе Встречаются ли щелочные металлы в природе в свободном состоянии?
- 14. Немного истории Древнегреческий поэт Гомер,
- 15. Поваренная соль и география Поваренная соль
- 16. Поваренная соль в организме человека
- 17. Применение поваренной соли Производство химических веществ
- 18. Сколько нужно времени для того, чтобы съесть
- 19. Карбонат калия - поташ Калийная селитра соли щелочных металлов
- 20. Задание На странице 130 учебника найдите
- 21. Проверьте Na2CO3 – кальцинированная сода Na2CO3*10Н2О
- 22. Тест-проверка Вариант 1.
- 23. Домашнее задание 1 уровень: Прочитать параграф 24,
- 24. О каком элементе идет речь?
- 25. Соблюдайте правила техники безопасности!
Слайд 2Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании.
Металлы
Для металлов характерна металлическая кристаллическая решетка.
У атомов металлов на внешнем уровне 1-3 электрона.
У атомов металлов на внешнем уровне 1-3 электрона.
Металлы являются восстановителями и окислителями.
Для металлов характерна металлическая кристаллическая решетка.
Металлы обладают электропроводностью и теплопроводностью.
При взаимодействии с кислородом металлы принимают электроны.
Все металлы активно взаимодействуют с кислотами.
Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании.
Мg, Be относятся к щелочноземельным металлам.
Уберите лишнее
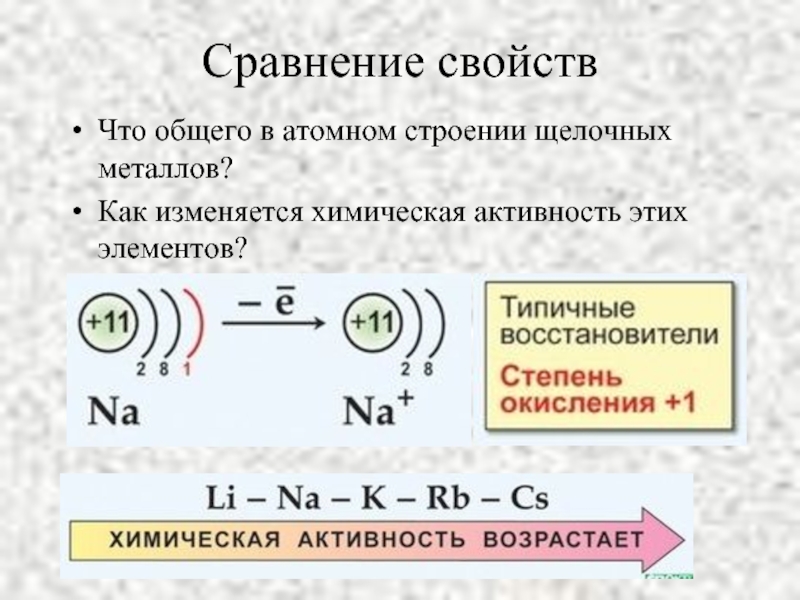
Слайд 5Сравнение свойств
Что общего в атомном строении щелочных металлов?
Как изменяется химическая активность
Слайд 6ИСТОРИЯ ОТКРЫТИЯ
Натрий и калий – 1807г. Английский химик и физик Г.Дэви
Литий открыт в 1817г. шведским химиком И. Арфведсон. Этот минерал выглядит как самый обыкновенный камень, и поэтому металл назвали литием, от греческого «литос» - камень.
Слайд 7Происхождение названий
Li (1817) лат. " литос" - камень
Na (1807) араб. "натрум"
К (1807) араб. "алкали" - щелочь
Rb (1861) лат. "рубидус" - темно-красный
Cs (1860) лат. "цезиус" - небесно-голубой
Fr (1939) от названия страны Франция – его на Земле всего 25 мг.
Слайд 11KOH – гидроксид калия
NaOH – гидроксид натрия
LiOH – гидроксид лития
Гидроксиды щелочных
Какова общая формула
гидроксидов?
Слайд 14Немного истории
Древнегреческий поэт Гомер, назвал поваренную соль «божественной». В
Слайд 15Поваренная соль и география
Поваренная соль известна человеку с незапамятных времен,
Слайд 16Поваренная соль в организме человека
Соль – обязательная составная часть
Слайд 17Применение поваренной соли
Производство химических веществ
--- соляной кислоты
---
--- хлора
--- соды
Для консервирования
Приправа к пище
Производство мыла
Слайд 18Сколько нужно времени для того, чтобы съесть пуд соли?
Есть
Оказывается это можно сделать всего за год с небольшим. Ведь потребность соли для нормального питания человека составляет не менее 7 килограммов в год.
Слайд 20Задание
На странице 130 учебника найдите ответ на вопрос: чем похожи
Слайд 21Проверьте
Na2CO3 – кальцинированная сода
Na2CO3*10Н2О – кристаллическая или стиральная сода
Na2НCO3 –
Слайд 23Домашнее задание
1 уровень: Прочитать параграф 24, Выяснить: Какая связь между подводной
2 уровень: + №3 решить задачу.
3 уровень + №4 вспомнить качественные реакции на ион хлора и карбонат-ион