- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Фенолы презентация
Содержание
- 1. Фенолы
- 2. План урока Фенолы Классификация фенолов Строение молекулы
- 3. Фенолы – органические вещества, молекулы которых содержат
- 4. Фенолы классифицируют по атомности, т.е. по количеству
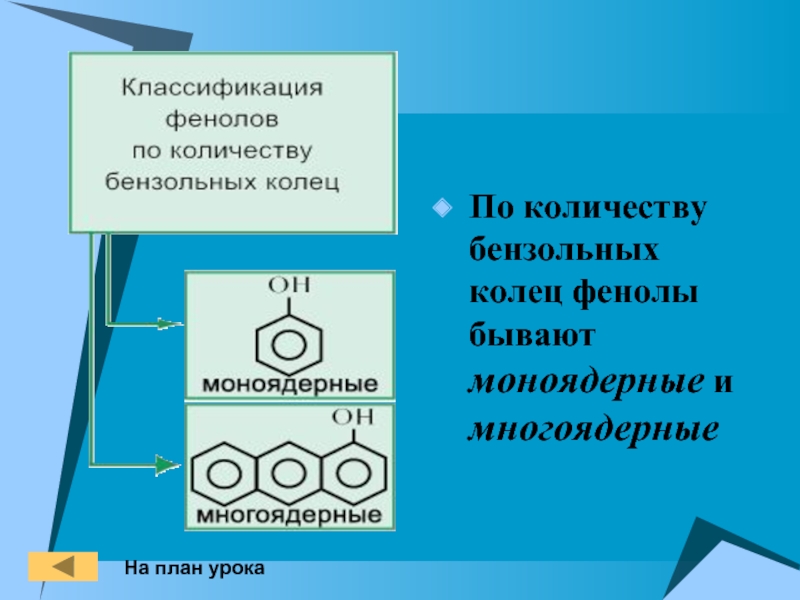
- 5. По количеству бензольных колец фенолы бывают моноядерные и многоядерные На план урока
- 6. Номенклатура При составлении названия фенолов нумерация атомов
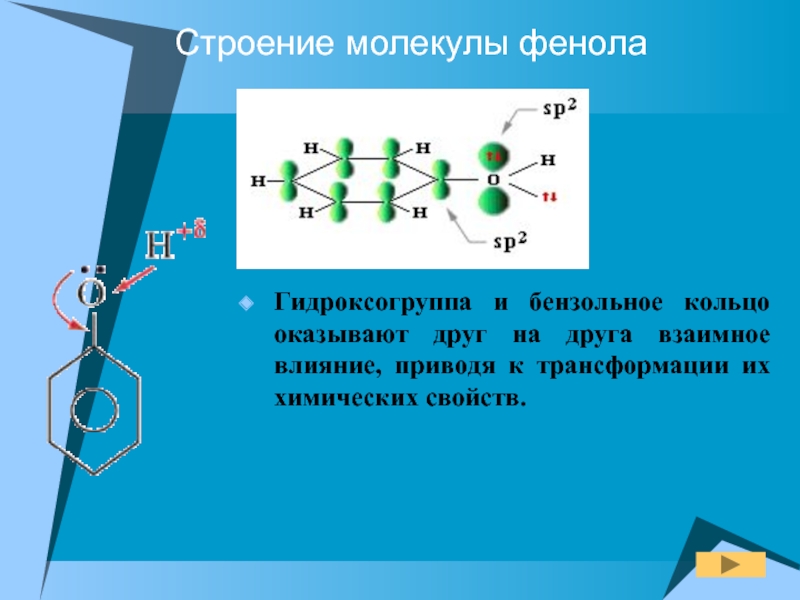
- 7. Строение молекулы фенола Гидроксогруппа и бензольное кольцо
- 8. Физические свойства фенола Фенол - твёрдое бесцветное
- 9. на план урока
- 10. Химические свойства фенола Химические свойства фенола обусловлены
- 11. Химические свойства, обусловленные наличием гидроксильной группы 1.
- 12. 2.Взаимодействие с натрием Фенол, как и спирты,
- 13. 3. Взаимодействие со щелочами
- 15. Карболовая кислота
- 16. Химические свойства, обусловленные наличием бензольного ядра
- 17. 2. Реакции замещения. А. Галогенирование
- 19. Б. Нитрование фенола Нитрование
- 20. В результате полного нитрования фенола
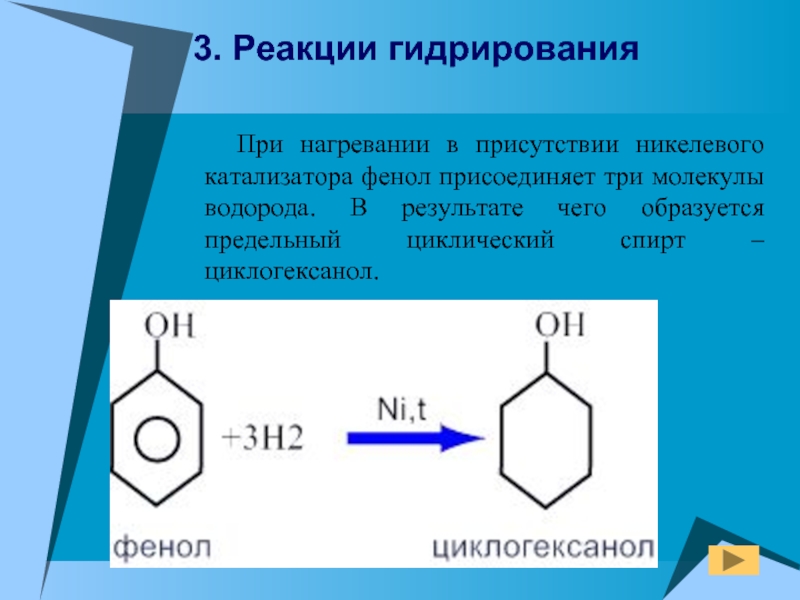
- 21. При нагревании в присутствии никелевого
- 22. 4.Реакции поликонденсации с альдегидами На план урока
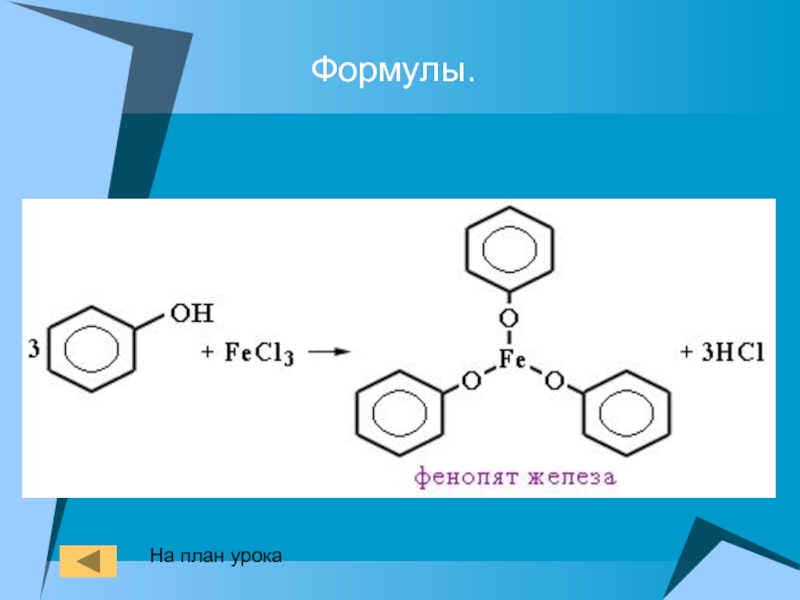
- 23. 5. Качественная реакция на фенол
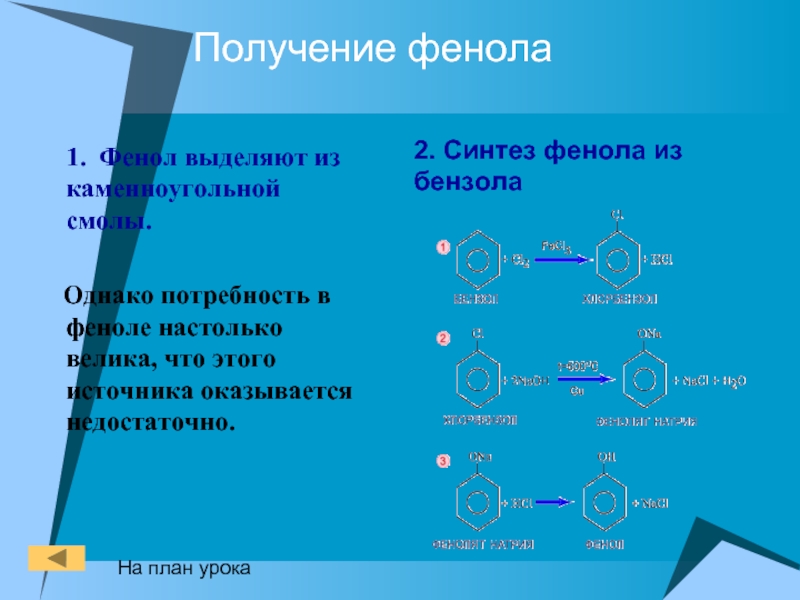
- 25. Получение фенола 1. Фенол выделяют из каменноугольной
- 26. Применение фенола. Фенол применяют для производства фенолформальдегидных
- 28. Сфера применения фенолов
Слайд 2План урока
Фенолы
Классификация фенолов
Строение молекулы
Физические свойства фенола
Химические свойства фенола
Получение
Применение
Чем опасен фенол
Симптомы отравления
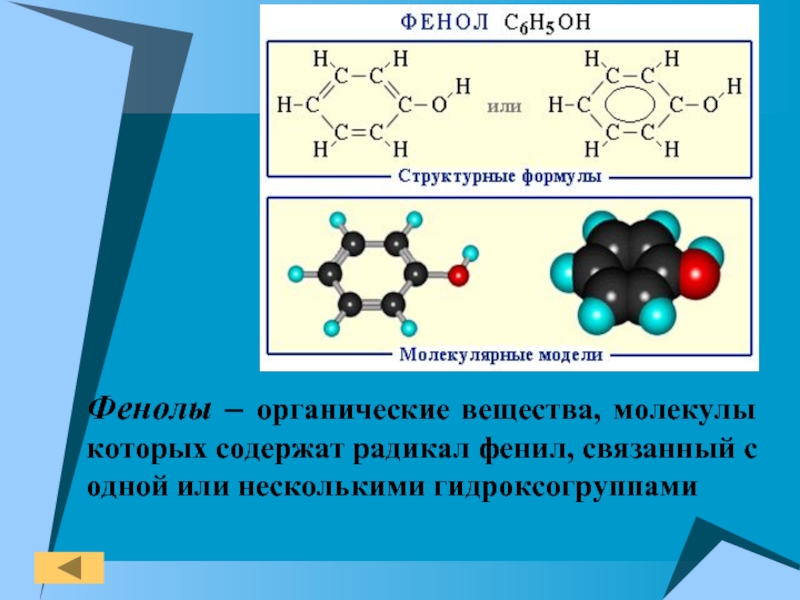
Слайд 3Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с
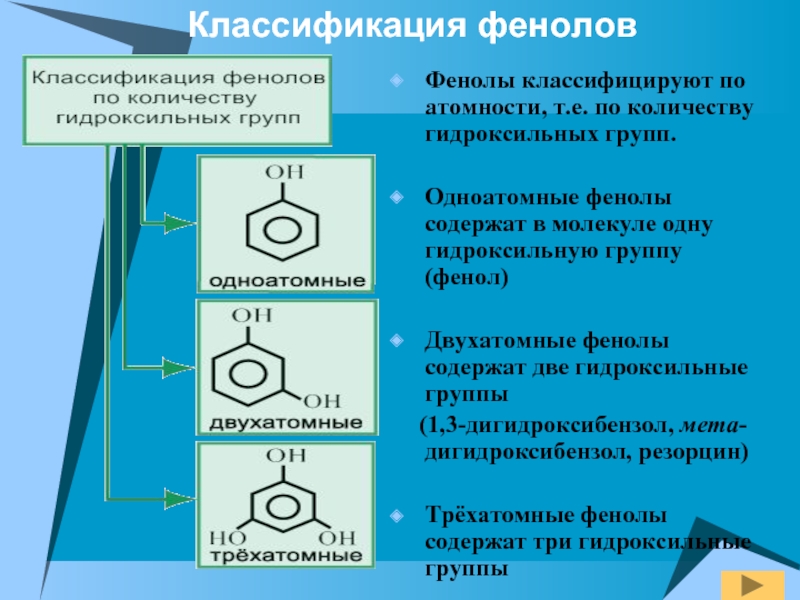
Слайд 4Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп.
Одноатомные фенолы
Двухатомные фенолы содержат две гидроксильные группы
(1,3-дигидроксибензол, мета-дигидроксибензол, резорцин)
Трёхатомные фенолы содержат три гидроксильные группы
Классификация фенолов
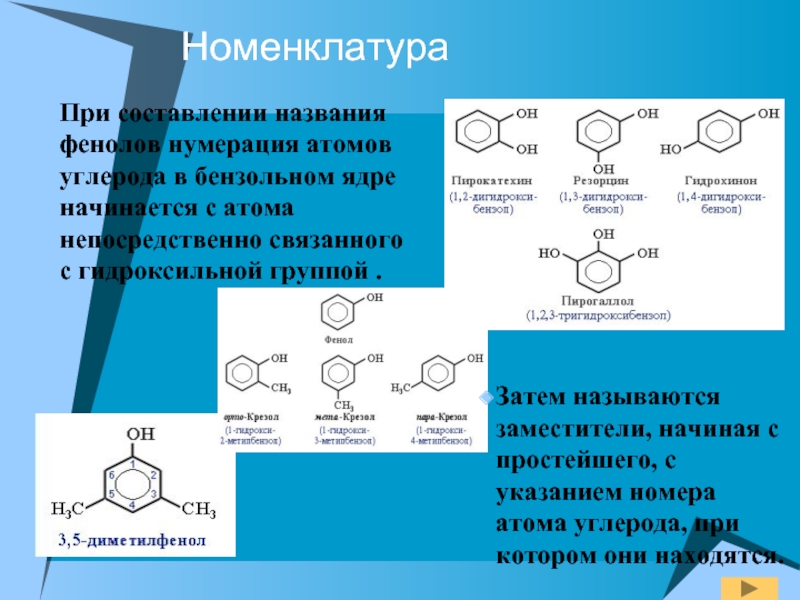
Слайд 6Номенклатура
При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается
Затем называются заместители, начиная с простейшего, с указанием номера атома углерода, при котором они находятся.
Слайд 7Строение молекулы фенола
Гидроксогруппа и бензольное кольцо оказывают друг на друга взаимное
Слайд 8Физические свойства фенола
Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного окисления
Фенол ядовит! При попадании на кожу вызывает ожоги поэтому с фенолом необходимо обращаться осторожно!
Слайд 10Химические свойства фенола
Химические свойства фенола обусловлены наличием в его молекуле
гидроксильной группы
бензольного
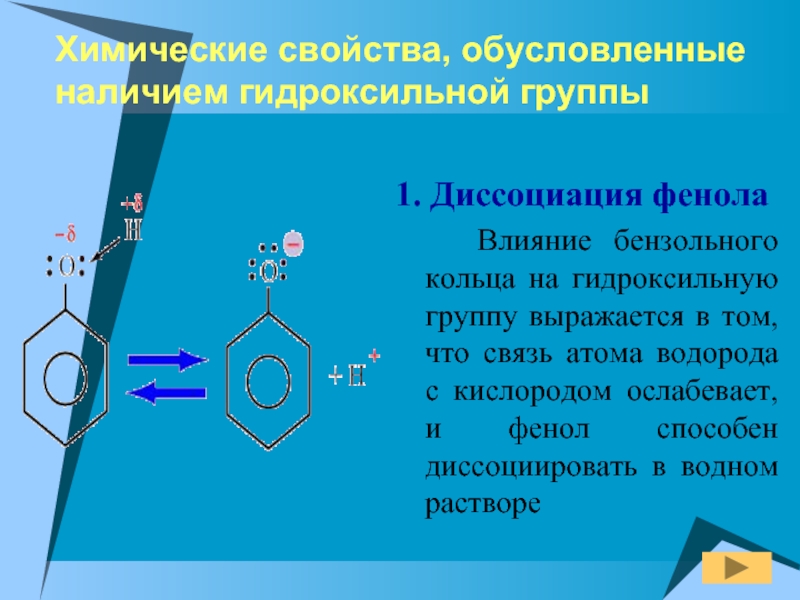
Слайд 11Химические свойства, обусловленные наличием гидроксильной группы
1. Диссоциация фенола
Влияние бензольного
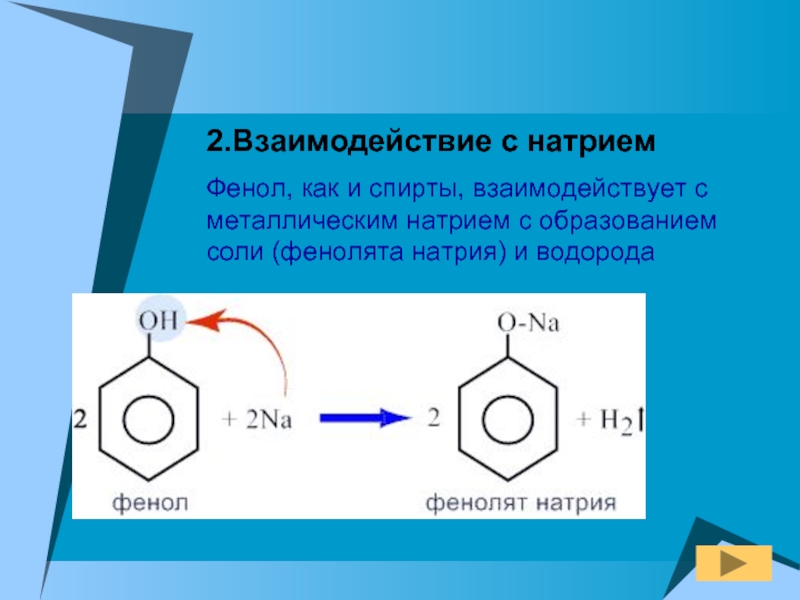
Слайд 122.Взаимодействие с натрием
Фенол, как и спирты, взаимодействует с металлическим натрием с
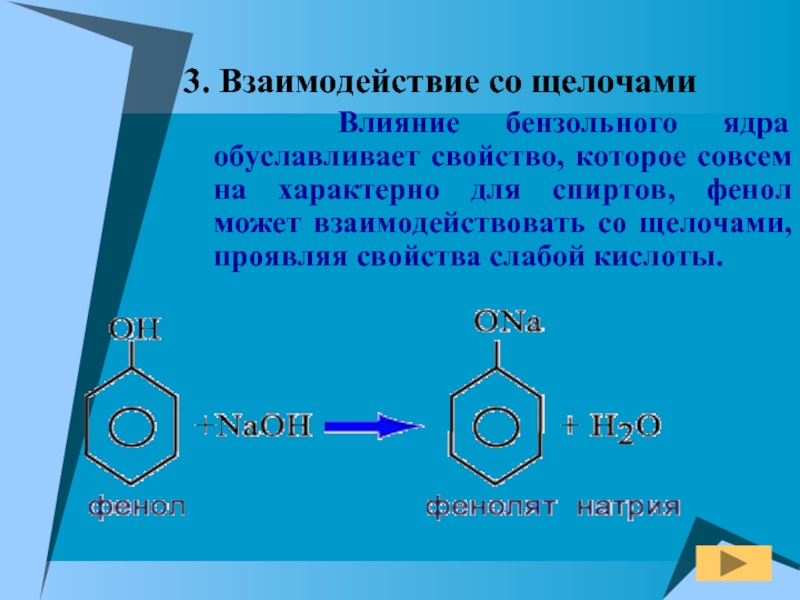
Слайд 133. Взаимодействие со щелочами
Влияние бензольного ядра обуславливает свойство,
Слайд 15
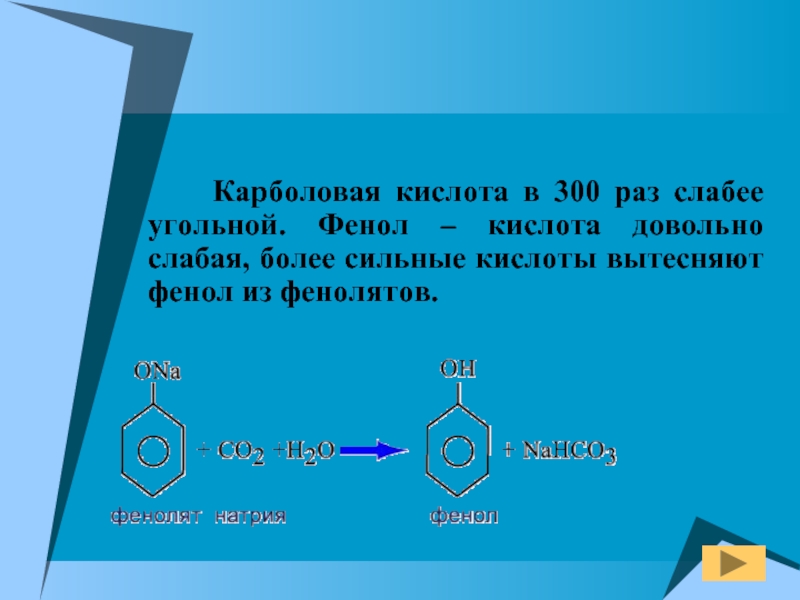
Карболовая кислота в 300 раз слабее угольной.
Слайд 16Химические свойства, обусловленные наличием бензольного ядра
Отличия от ароматических
1. Реакции окисления
Фенол окисляется кислородом воздуха, приобретая фиолетовую окраску.
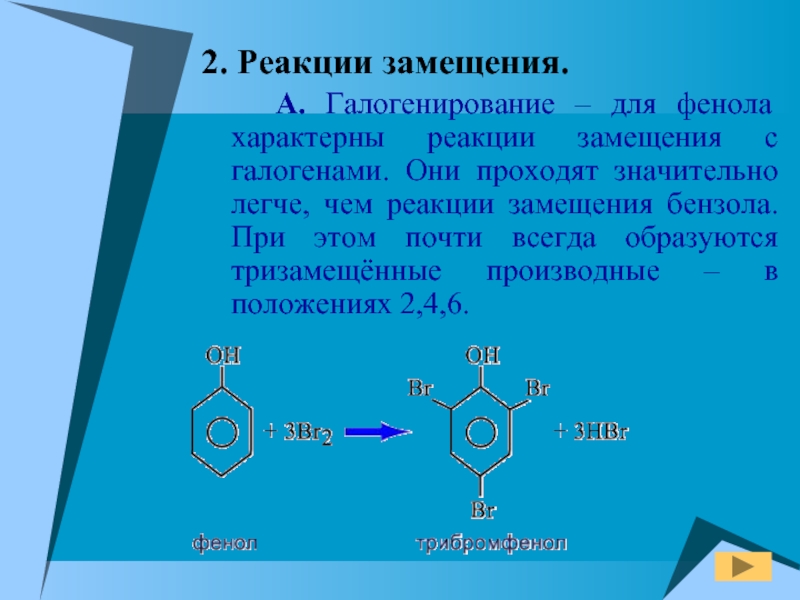
Слайд 172. Реакции замещения.
А. Галогенирование – для фенола характерны реакции
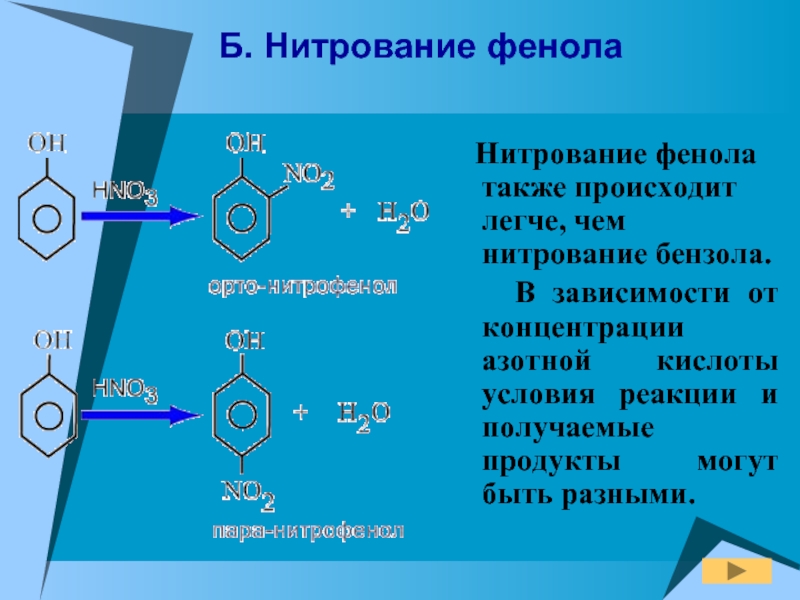
Слайд 19Б. Нитрование фенола
Нитрование фенола также происходит легче, чем нитрование
В зависимости от концентрации азотной кислоты условия реакции и получаемые продукты могут быть разными.
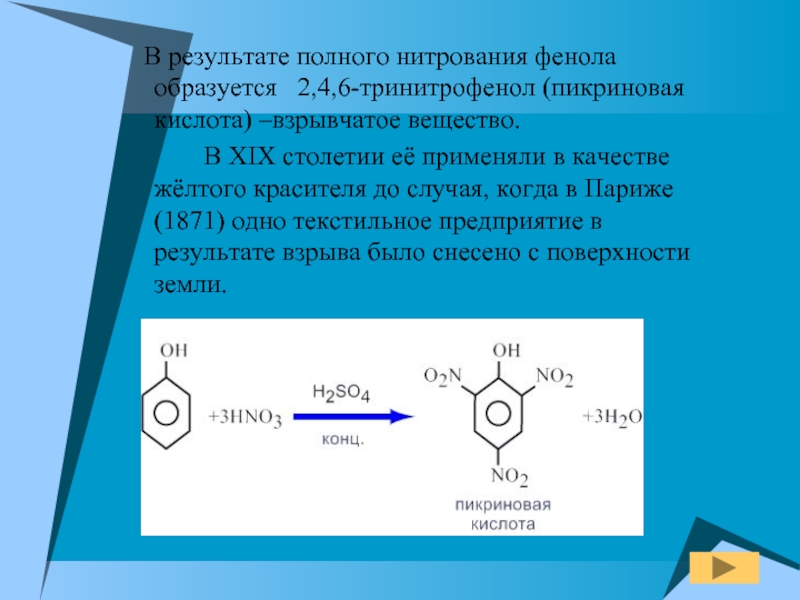
Слайд 20 В результате полного нитрования фенола образуется 2,4,6-тринитрофенол (пикриновая
В XIX столетии её применяли в качестве жёлтого красителя до случая, когда в Париже (1871) одно текстильное предприятие в результате взрыва было снесено с поверхности земли.
Слайд 21 При нагревании в присутствии никелевого катализатора фенол присоединяет три
3. Реакции гидрирования
Слайд 25Получение фенола
1. Фенол выделяют из каменноугольной смолы.
Однако потребность
2. Синтез фенола из бензола
На план урока
Слайд 26Применение фенола.
Фенол применяют для производства фенолформальдегидных пластмасс, синтетического волокна капролактам, красителей,
На план урока
Слайд 27
Практически сразу после получения фенола ученые установили, что это химическое вещество обладает не только полезными свойствами, что позволяет его использовать в различных сферах науки и производства, но и является сильнодействующим ядом. Так, вдыхание паров фенола в течение непродолжительного времени может привести к раздражению носоглотки, ожогам дыхательных путей и последующему отеку легких с летальным исходом. При соприкосновении раствора фенола с кожей образуются химические ожоги, которые впоследствии трансформируются в язвы.
Слайд 28 Сфера применения фенолов достаточно широка, но
Дело в том, что фенол и его производные без труда проникают в организм человека через кожу и желудочно-кишечный тракт, а пары фенола – через легкие. В организме фенол легко образует соединения с другими веществами, присутствующими в организме. Чем выше концентрация фенола в крови, тем сильнее его неблагоприятное влияние на здоровье человека.