- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Этапы разработкилекарственных препаратов презентация
Содержание
- 1. Этапы разработкилекарственных препаратов
- 2. Фаза 3 Пере-
- 3. Процесс разработки лекарственного препарата Аналитические методы Лекарственная форма Производство Химический синтез
- 4. Зачем нужны клинические испытания Ряд заболеваний иначе
- 5. Популяция Большая группа людей, проживающая в определенном
- 6. Выборка Часть популяции, полученная путем отбора
- 7. Плацебо Лекарственная форма, неотличимая от исследуемого препарата
- 8. Плацебо-эффект Изменение состояния пациента (отмечаемое сами пациентом
- 9. Вклад различных причин в суммарный лечебный эффект
- 10. Рандомизация Распределение пациентов по группам случайным путём,
- 11. Открытые и «слепые» исследования Слепой/маскированный метод -
- 12. «Слепой» метод «Простой слепой метод» - у
- 13. Типы исследований во времени
- 14. Дизайн клинических испытаний Несравнительные исследования Сравнительные исследования
- 15. Параллельный дизайн
- 16. Перекрёстный дизайн Популяция Рандомизация
- 17. Типы клинических испытаний в зависимости от цели
- 18. I фаза - фармакологические исследования Переносимость
- 19. Исследования I фазы позволяют Установить переносимость Оценить/описать
- 20. II фаза - установление терапевтической эффективности Оценка
- 21. Исследования II фазы позволяют Оценить применения для
- 22. III фаза - подтверждение терапевтической эффективности Контролируемые
- 23. Исследования III фазы позволяют Продемонстрировать/подтвердить эффективность Установить
- 24. IV фаза - терапевтическое применение Сравнительные исследования
- 25. Исследования IV фазы позволяют Окончательно установить соотношение
- 26. Постмаркетинговые наблюдательные исследования Анкеты, наблюдательные исследования, в
- 27. Протокол испытания Документ, который описывает задачи, методологию,
- 28. Основные элементы протокола (I) Элемент Цель
- 29. Основные элементы протокола (II) Элемент Исследуемое
- 30. Структура протокола Титульный лист Клинический раздел Организационно-административный
- 31. Многоцентровое клиническое испытание Клиническое испытание, проводимое
- 32. Good Clinical Practice (GCP) «Качественная клиническая практика»
- 33. Мета-анализ Количественный анализ объединённых результатов нескольких клинических
- 34. Мета-анализ (II) Отдельные исследования должны быть сходны
- 35. Ошибки в интерпретации результатов исследований Экстраполяция данных
- 36. Ошибки в интерпретации результатов исследований (II) В
- 37. БЕЗОПАСНОСТЬ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
- 38. Лекарственные препараты Терапевтические эффекты Побочные эффекты
- 40. Данные о побочных эффектах Безопасность больного
- 41. Выявление побочных эффектов . D.Laurence, P.Bennet, Clinical Pharmacology
- 42. Частота сообщений число сообщений о ПЭ число пациентов, принимающих препарат =
- 43. Термины Нежелательные явления Побочные эффекты лекарств Серьезные нежелательные явления Непредвиденные побочные эфекты
- 44. Нежелательные явления Любые выявленные у пациента, получающего
- 45. Побочные эффекты лекарств Любая неблагоприятная реакция, связанная
- 46. Серьезные нежелательные явления Любые неблагоприятные клинические
- 47. Непредвиденный побочный эффект лекарства Нежелательная реакция, характер
Слайд 2
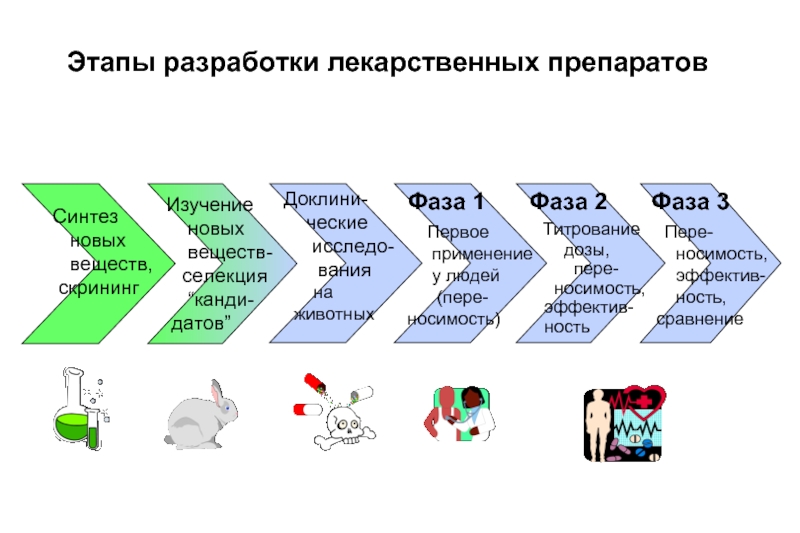
Фаза 3
Пере-
носимость,
эффектив-
сравнение
Фаза 1
Первое
применение
у людей
(пере-носимость)
Фаза 2
Титрование
дозы,
пере-
носимость,
эффектив-
ность
Доклини-
ческие
исследо-
вания
на
животных
Изучение
новых
веществ-
селекция
“канди-
датов”
Синтез
новых
веществ,
скрининг
Этапы разработки лекарственных препаратов
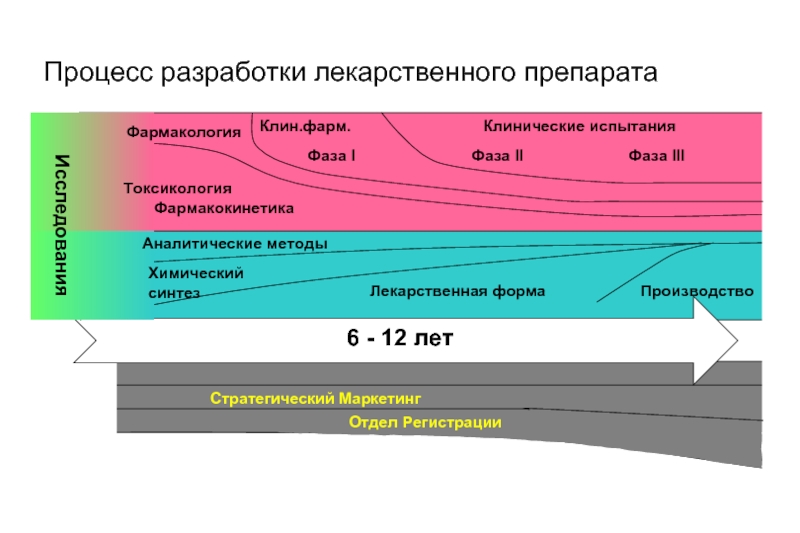
Слайд 3Процесс разработки лекарственного препарата
Аналитические методы
Лекарственная форма
Производство
Химический синтез
Слайд 4Зачем нужны клинические испытания
Ряд заболеваний иначе протекает у животных
В эксперименте невозможно
Данные экспериментов на животных не могут быть экстраполированы на человека
Отдельное наблюдение мало информативно
Слайд 5Популяция
Большая группа людей, проживающая в определенном географическом регионе
например, популяция жителей
или обладающих некоторым общим признаком
например, женщины старше 60 лет; пациенты, госпитализированные в определенную клинику;пациенты с определенным заболеванием).
Слайд 6Выборка
Часть популяции, полученная путем отбора
Выборка должна быть репрезентативна, т.е. отражать
Данные, полученные на выборке, экстраполируются на популяцию
Слайд 7Плацебо
Лекарственная форма, неотличимая от исследуемого препарата по внешнему виду, цвету, вкусу
Слайд 8Плацебо-эффект
Изменение состояния пациента (отмечаемое сами пациентом или лечащим врачом), связанное с
Выражен у седативных, снотворных, противозудных, болеутоляющих препаратов.
Минимален у антимикробных препаратов, антиметаболитов, контрацептивов
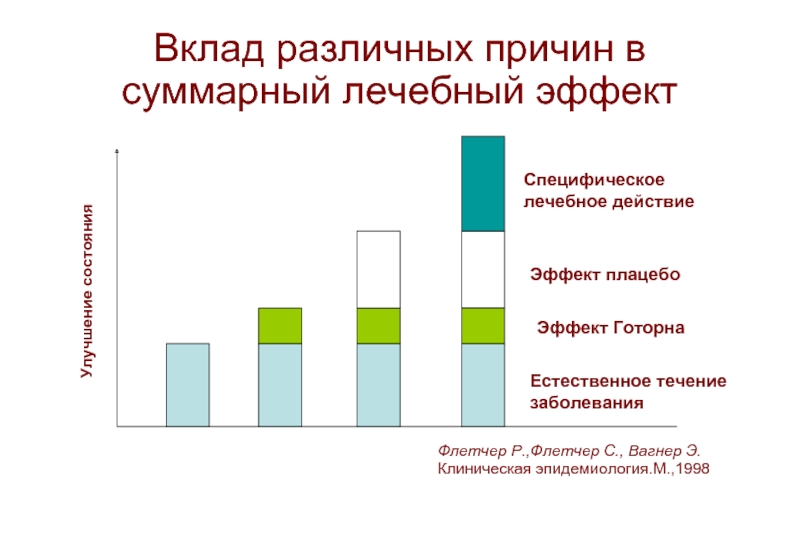
Слайд 9Вклад различных причин в суммарный лечебный эффект
Естественное течение заболевания
Эффект Готорна
Эффект плацебо
Специфическое
Флетчер Р.,Флетчер С., Вагнер Э. Клиническая эпидемиология.М.,1998
Улучшение состояния
Слайд 10Рандомизация
Распределение пациентов по группам случайным путём, благодаря чему достигается отсутствие различий
Слайд 11Открытые и «слепые» исследования
Слепой/маскированный метод - метод, при котором одной
Правила проведения качественных клинических испытаний в РФ
Слайд 12«Слепой» метод
«Простой слепой метод» - у пациента отсутствует информация о том,
«Двойной слепой метод» - информация отсутствует у пациента и исследователя
«Двойной слепой метод» позволяет избегать субъективности при распределении пациентов по группам и при оценке результатов лечения
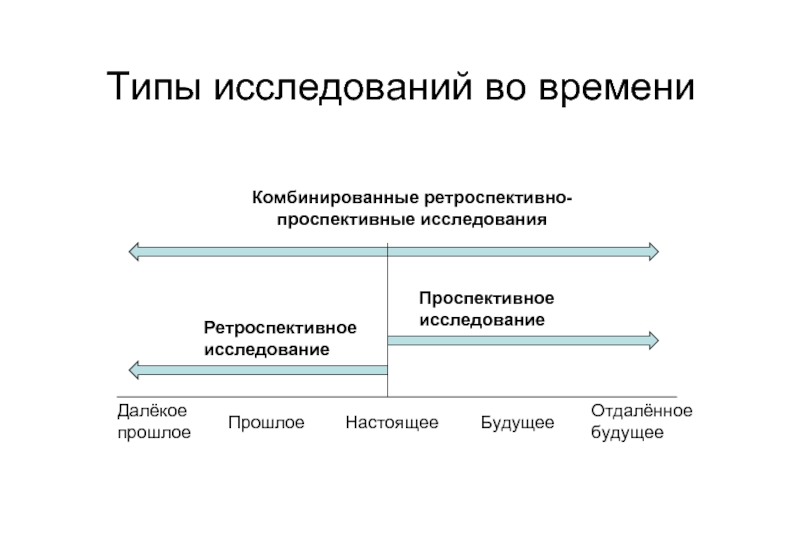
Слайд 13Типы исследований во времени
Проспективное исследование
Ретроспективное исследование
Комбинированные ретроспективно-проспективные исследования
Далёкое прошлое
Настоящее
Прошлое
Будущее
Отдалённое будущее
Слайд 14Дизайн клинических испытаний
Несравнительные исследования
Сравнительные исследования
параллельный (дизайн параллельных
перекрёстный дизайн
последовательный
соответствующих пар
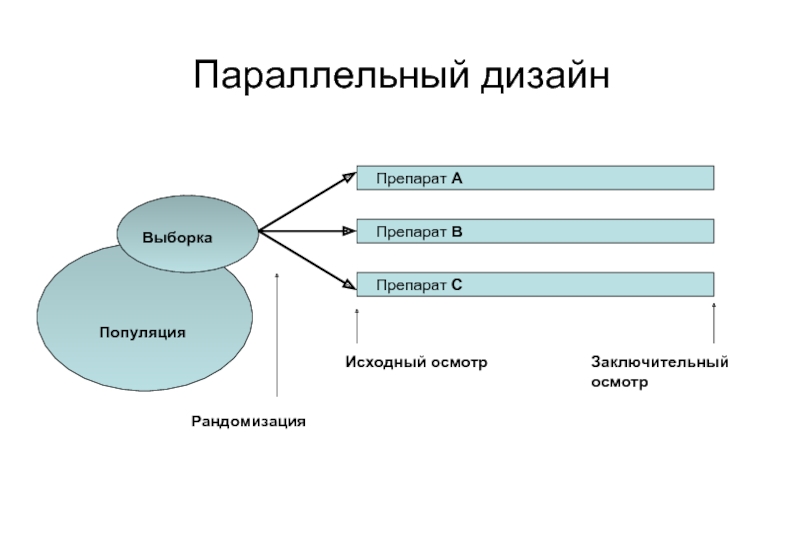
Слайд 15Параллельный дизайн
Популяция
Рандомизация
Выборка
Исходный осмотр
Заключительный осмотр
Препарат А
Препарат В
Препарат С
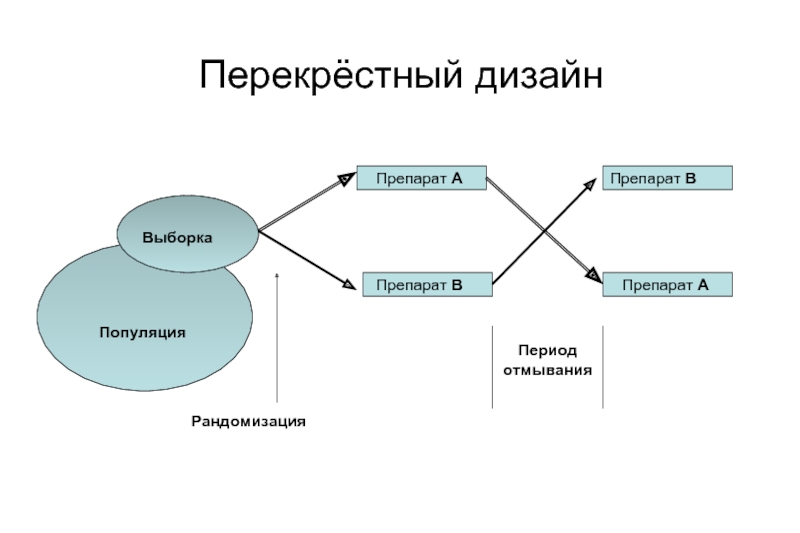
Слайд 16Перекрёстный дизайн
Популяция
Рандомизация
Выборка
Препарат А
Препарат В
Препарат В
Препарат А
Период отмывания
Слайд 17Типы клинических испытаний в зависимости от цели
Фармакологические исследования у человека
Установление терапевтической
Подтверждение терапевтической эффективности
Терапевтическое применение
Слайд 18I фаза - фармакологические исследования
Переносимость повышающихся доз
Фармакокинетика и фармакодинамика
при однократном
при многократном введении
Лекарственные взаимодействия
Обычно исследования I фазы проводятся на взрослых здоровых добровольцах, реже - на больных
Слайд 19Исследования I фазы позволяют
Установить переносимость
Оценить/описать фармакокинетику и фармакодинамику
Исследовать лекарственные взаимодействия
Оценить активность
Слайд 20II фаза - установление терапевтической эффективности
Оценка эффективности, используя суррогатные, фармакологические маркёры
Исследования взаимосвязи доза - эффект
Исследования II фазы проводятся на маленькой выборке хорошо отобранной узкой популяции больных в относительно короткие сроки
Как правило - открытые несравнительные исследования
Слайд 21Исследования II фазы позволяют
Оценить применения для целевой популяции (больных)
Оценить дозы для
Обеспечить основу для подтверждающих исследований (дизайн, размер выборки)
Слайд 22III фаза - подтверждение терапевтической эффективности
Контролируемые исследования эффективности и безопасности
Рандомизированные параллельные исследования взаимосвязи доза-эффект
Исследования III фазы проводятся на больших выборках
Как правило - рандомизированные сравнительные исследования
Слайд 23Исследования III фазы позволяют
Продемонстрировать/подтвердить эффективность
Установить профиль безопасности
Адекватно оценить соотношение польза/риск
Установить взаимосвязь
Обеспечивают основу для регистрации препарата по определённым показаниям
Слайд 24IV фаза - терапевтическое применение
Сравнительные исследования эффективности, безопасности
Исследования с истинными итоговыми
Исследования с дополнительными итоговыми маркёрами
Фармакоэкономические исследования
Часто проводятся на большой выборке
Проводятся после регистрации в соответствии с утверждёнными показаниями/противопоказаниями
Слайд 25Исследования IV фазы позволяют
Окончательно установить соотношение польза/риск для всей или специальной
Выявить редкие побочные эффекты
Окончательно определить дозировки препарата, в т.ч. для специальных популяций
Оценить качество жизни на фоне применения препарата
Слайд 26Постмаркетинговые наблюдательные исследования
Анкеты, наблюдательные исследования, в отличие от контролируемых испытаний IV
Тем не менее они позволяют
выявлять редкие побочные эффекты,
определять предпочтения врачей и больных,
ознакомить широкий круг врачей с новым препаратом
Слайд 27Протокол испытания
Документ, который описывает задачи, методологию, процедуры, статистические аспекты и организацию
Правила проведения качественных клинических испытаний в РФ
Слайд 28Основные элементы протокола (I)
Элемент
Цель исследования
Значимость (исходные данные)
План исследования
Дизайн исследования
Сроки
Субъекты исследования
Критерии включения
Критерии
План отбора пациентов
Цель
На какие вопросы должно ответить исследование?
Почему эти вопросы являются важными?
Как будет проводиться исследование? Когда?
Кто будет являться субъектами исследования?
Слайд 29Основные элементы протокола (II)
Элемент
Исследуемое лечение
Исследуемый препарат
Препарат(ы) сравнения
Переменные интереса
Статистические вопросы
Гипотеза
Размер выборки
Аналитический
Цель
Какой препарат будет применяться? Доза? Путь введения?
Какие измерения будут сделаны?
Сколько пациентов необходимо включить? Как будет анализироваться исследование?
Слайд 30Структура протокола
Титульный лист
Клинический раздел
Организационно-административный раздел
Этические и правовые вопросы
Мониторинг исследования
Регистрация данных
Статистический анализ
Конфиденциальность
Публикация
Приложения
Слайд 31Многоцентровое клиническое испытание
Клиническое испытание, проводимое по единому протоколу более чем
Правила проведения качественных клинических испытаний в РФ
Слайд 32Good Clinical Practice (GCP)
«Качественная клиническая практика»
Стандарты, в соответствии с которыми планируются,
European GCP Guidelines, 1991
Слайд 33Мета-анализ
Количественный анализ объединённых результатов нескольких клинических испытаний одного и того же
Используется для обобщенного представления результатов многих испытаний и для увеличения доказательности результатов испытаний
Флетчер Р.,Флетчер С., Вагнер Э. Клиническая эпидемиология.М.,1998
Слайд 34Мета-анализ (II)
Отдельные исследования должны быть сходны между собой по характеристикам пациентов,
Мета-анализ исследований с недостаточным размером выборки может суммировать их случайные ошибки!
Слайд 35Ошибки в интерпретации результатов исследований
Экстраполяция данных in vitro на человека
Экстраполяция данных
Статистические ошибки (например, недостаточный размер выборки)
Применение суррогатных маркёров в качестве переменных интереса (например, лабораторный показатель в отрыве от клинической картины)
Слайд 36Ошибки в интерпретации результатов исследований (II)
В малых исследованиях могут быть получены
«Выпячивание» статистически достоверных, но клинически мало значимых различий
Слайд 40Данные о побочных эффектах
Безопасность больного
Предупреждения для врача
Информация для пациента
Информация для органов
Требование законодательства РФ
Слайд 43Термины
Нежелательные явления
Побочные эффекты лекарств
Серьезные нежелательные явления
Непредвиденные побочные эфекты
Слайд 44Нежелательные явления
Любые выявленные у пациента, получающего лекарственное средство, или субъекта клинического
Слайд 45Побочные эффекты лекарств
Любая неблагоприятная реакция, связанная с применением лекарственного средства в
Применительно к клиническим исследованиям этот термин означает все негативные реакции, связанные с использованием любой дозы исследуемого лекарственного средства.
Слайд 46Серьезные нежелательные явления
Любые неблагоприятные клинические проявления, которые вне зависимости от
- приводят к смерти
- представляют угрозу жизни
- требуют госпитализации или ее продления
- приводят к стойкой или выраженной нетрудоспособности / инвалидности
- являются врожденной аномалией / пороком развития