- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЕГЭ по химии презентация
Содержание
- 1. ЕГЭ по химии
- 2. Количество участников и итоги 2011 г. В
- 3. www.fipi.ru
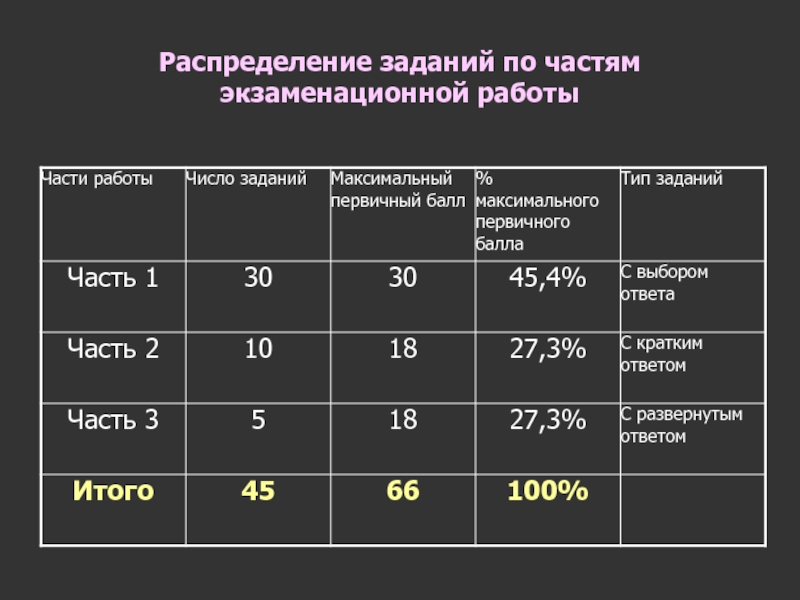
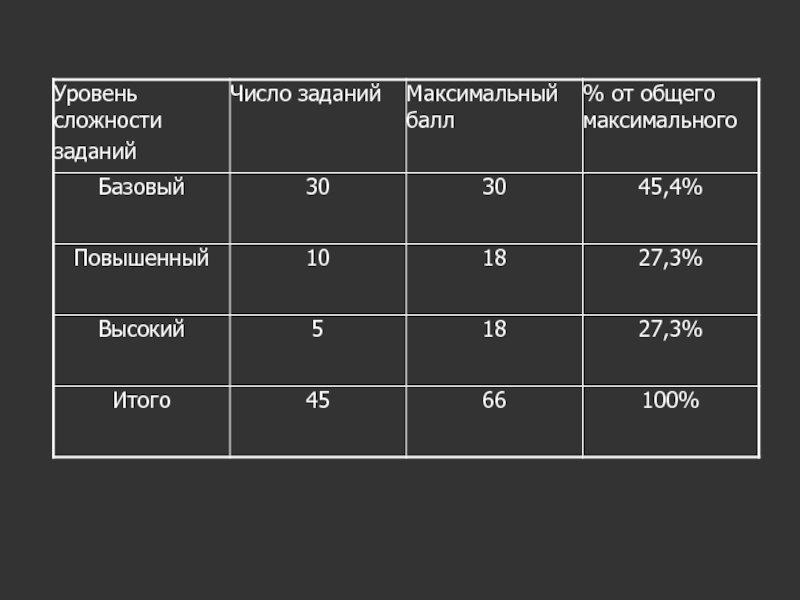
- 6. Распределение заданий по частям экзаменационной работы
- 8. Структура КИМ ЕГЭ 2011 A1 Строение атома A2 Периодический
- 9. A8 Классификация и
- 10. A14 Изомеры и гомологи. σ- и π-Связи.
- 11. A21 Классификация реакций А22 Скорость реакций A23
- 12. A28 Вещества в нашей жизни. Применение веществ.
- 13. Изменения в ЕГЭ 2011 г.
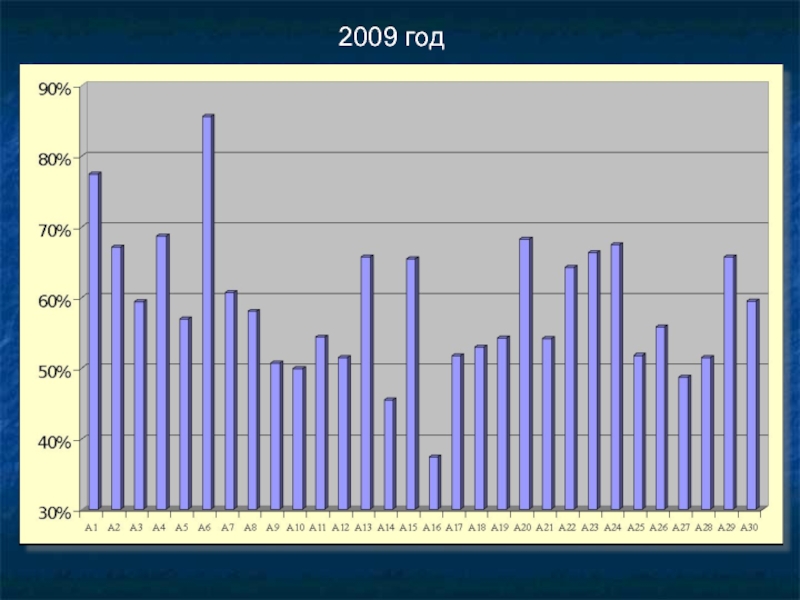
- 14. 2009 год
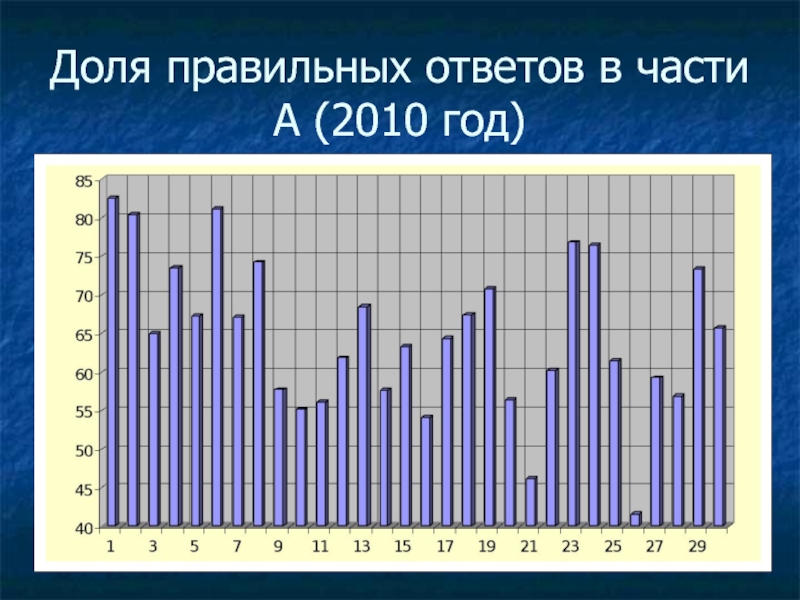
- 15. Доля правильных ответов в части А (2010 год)
- 16. Часть B B1 Классификация и номенклатура
- 17. Часть B B5 Химические свойства
- 18. B1 Установите соответствие между названием органического вещества
- 19. B2 Установите соответствие между уравнением реакции и
- 20. B3 Установите соответствие между формулой соли и
- 21. B4 Установите соответствие между химической формулой соли
- 22. B5 Установите соответствие между названием оксида и
- 23. B6 Радикальный механизм хлорирования метана состоит из
- 24. B7 В отличие от этилового спирта фенол:
- 25. B8 Для характеристики диметиламина справедливы утверждения: 1)
- 26. B9 Какую массу оксида бария необходимо взять
- 27. B10 При растворении оксида железа(III) в избытке
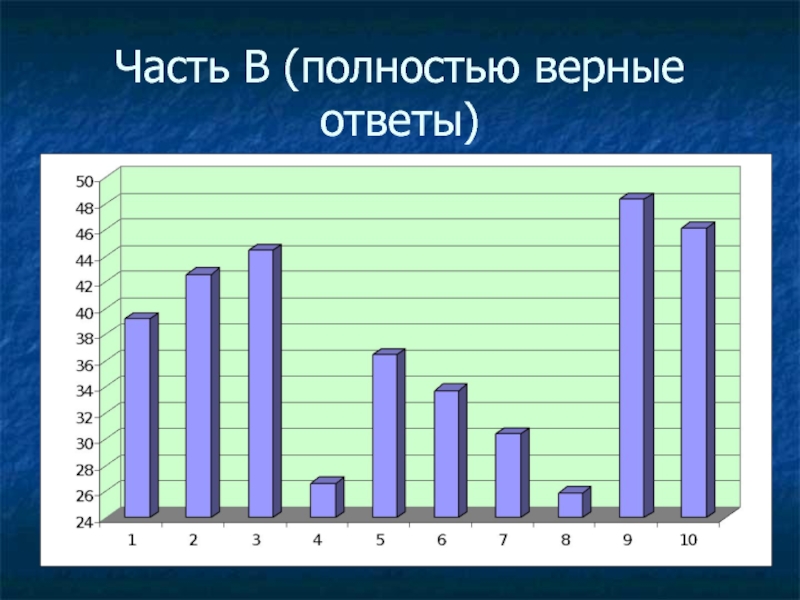
- 28. Часть В (полностью верные ответы)
- 29. Доля верных ответов в части B (2009 год)
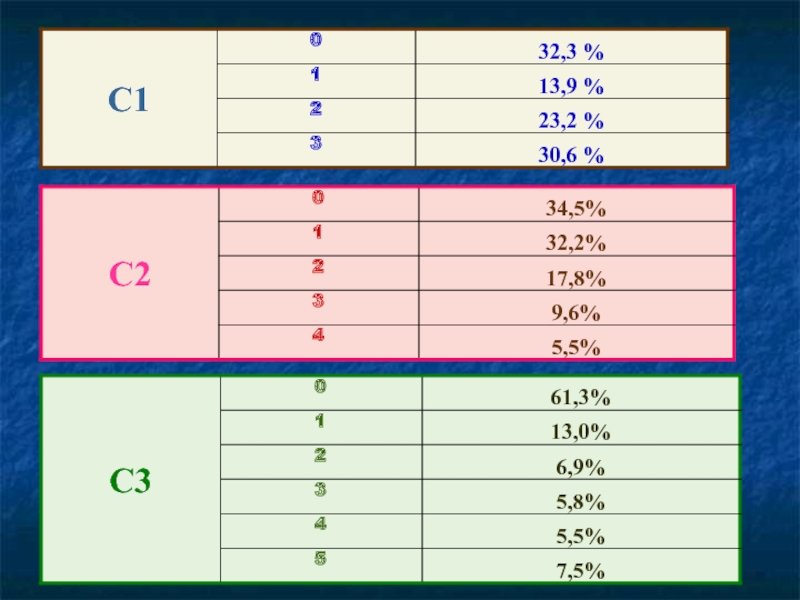
- 30. Часть С
- 31. С1 Используя метод электронного баланса, составьте уравнение
- 32. C2 Даны вещества: сера сероводород азотная кислота
- 33. С3 Напишите уравнения реакций, с помощью которых
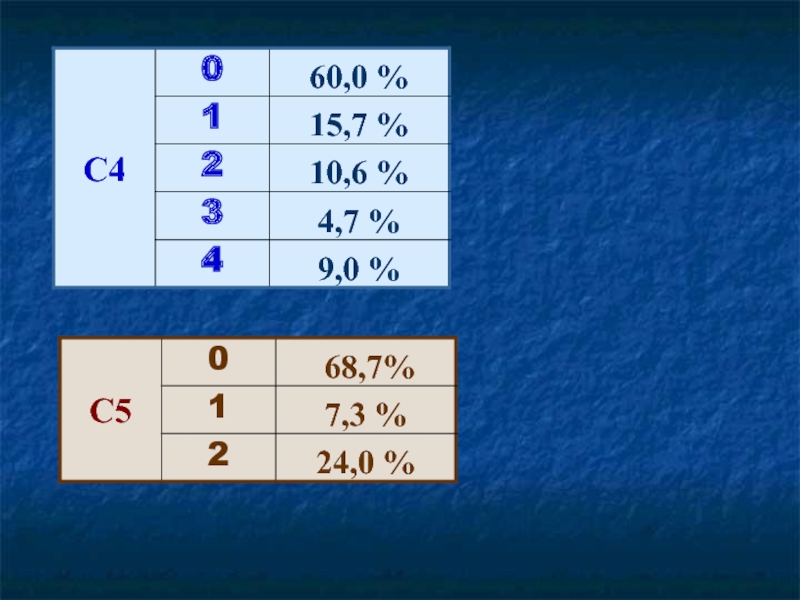
- 34. C4 Какой объем хлора (н.у.) выделится, если
- 35. С5 При взаимодействии одного и того же
- 38. Работа конфликтной комиссии Всего подано заявлений 57 (2,13%) Удовлетворено – 3 (5,3% от поданных)
- 39. Спасибо за внимание!
Слайд 2Количество участников и итоги 2011 г.
В СПб
Зарегистрировано - 3703
Явились - 2671
Неудовлетворительно – 156 чел. (5,84%)
Средний балл – 54,43
Получили 100 баллов – 8 чел.
(3,1% по РФ)
По РФ
Неуд – 6,75%, ср. балл 56,04
В 2009 году
10,94% - «2»
Ср.балл – 51,65
Слайд 8Структура КИМ ЕГЭ 2011
A1 Строение атома
A2 Периодический закон и ПСХЭ
A3 Общая характеристика металлов
A4
A5 Химическая связь
A6 Электроотрицательность. Степени окисления и валентность
A7 Кристаллические решетки
Слайд 9A8 Классификация и
номенклатура веществ
A9
А10 Оксиды
A11 Основания и кислоты
A12 Химические свойства солей
A13 Генетическая связь между классами неорганических веществ
Слайд 10A14 Изомеры и гомологи. σ- и π-Связи. Типы гибридизации
A15 Углеводороды
A16 Спирты и
A17 Альдегиды, КК, сл.эфиры, жиры, белки и углеводы
A18 Получение углеводородов
A19 Получение кислородсодержащих орг.
A20 Взаимосвязь органических веществ
Слайд 11A21 Классификация реакций
А22 Скорость реакций
A23 Хим.равновесие. Принцип Ле Шателье
A24 Электролитическая диссоциация
A25
A26 Гидролиз солей
A27 ОВР
Слайд 12A28 Вещества в нашей жизни. Применение веществ. Распознавание веществ
A29 Химия
A30 Термохимический расчет
Слайд 16Часть B
B1 Классификация и номенклатура веществ
B2 Степени окисления. ОВР
B3
B4 Гидролиз
Слайд 17Часть B
B5 Химические свойства классов неорганических веществ
B6 Углеводороды
B7
B8 Азотсодержащие орг.вещества
B9 Задача
B10 Задача
Слайд 18B1
Установите соответствие между названием органического вещества и его химической формулой
Название вещества
А)
Б) диметиламин
В) нитробензол
Г) этиламин
Химическая формула
1) CH3NH2
2) (CH3)2NH
3) C2H5NH2
4) C3H7NH2
5) C6H5NH2
6) C6H5NO2
B1
5
2
6
3
Слайд 19B2
Установите соответствие между уравнением реакции и изменением степени окисления восстановителя в
Название вещества
А) H2S + 2Na = Na2S + H2
Б) S + 2HI = I2 + H2S
В) SO2 + NO2 = SO3 + NO
Г) 4NO2 + O2 + 2H2O = 4HNO3
Изменение
степени окисления
восстановителя
1) +6 → +4
2) -1 → 0
3) +4 → +6
4) 0 → +1
5) +4 → +5
6) 0 → -2
B2
4
2
3
5
Слайд 20B3
Установите соответствие между формулой соли и уравнением процесса, протекающего на катоде
Формула соли
А) KCl
Б) AlBr3
В) CuSO4
Г) AgNO3
Уравнение катодного процесса
1) К+ + 1e- = K0
2) 2H2O + 2e- = H2 + 2OH-
3) 2H2O – 4e- = O2 + 4H+
4) Cu2+ + 1e- = Cu+
5) Ag+ + 1e- = Ag0
6) Cu2+ + 2e- = Cu0
B3
2
2
6
5
Слайд 21B4
Установите соответствие между химической формулой соли и реакцией среды её водного
Формула соли
А) Na2S
Б) K2SO3
В) Cs2SO4
Г) Al2(SO4)3
Реакция среды
1) кислая
2) нейтральная
3) щелочная
B4
3
3
2
1
Слайд 22B5
Установите соответствие между названием оксида и формулами веществ, с которыми он
Название оксида
А) оксид кремния(IV)
Б) оксид азота(IV)
В) оксид бария
Г) оксид железа(III)
Формулы веществ
1) H2SO3, CO, H2
2) Fe2O3, H2O, NH3
3) C, КОН, CaCO3
4) NaOH, H2O, N2
5) H2O, SO3, H3PO4
6) H2O, HNO3, Pt
Слайд 23B6
Радикальный механизм хлорирования метана состоит из стадий:
1) разложение метана на атомы
2)
3) разложение метана на радикалы
4) развитие цепи
5) обрыв цепи
6) разветвление цепи
B6
2
4
5
Слайд 24B7
В отличие от этилового спирта фенол:
1) взаимодействует с гидроксидом кальция
2) легко
3) взаимодействует со щелочными металлами
4) вступает в реакции с галогеноводородами
5) образует простые эфиры
6) при действии карбоновых кислот не образует сложных эфиров
B7
1
2
6
Слайд 25B8
Для характеристики диметиламина справедливы утверждения:
1) это вещество кристаллическое при обычных условиях
2)
3) не растворяется в воде
4) реагирует с гидроксидами щелочноземельных металлов
5) образует соль с хлороводородом
6) проявляет заметные основные свойства
B8
2
5
6
Слайд 26B9
Какую массу оксида бария необходимо взять для приготовления 342 г раствора
(Запишите число с точностью до десятых).
m(Ba(OH)2) = 342•0,05 = 17,1 г
BaO + H2O = Ba(OH)2
17,1 г
171 г/моль
0,1 моль
0,1 моль
153 г/моль
15,3 г
15,3
B9
1
5
,
3
Слайд 27B10
При растворении оксида железа(III) в избытке азотной кислоты образовалась соль массой
Fe2O3 + 6HNO3 = 2Fe(NO3)3 + 3H2O
121 г
242 г/моль
0,5 моль
0,25 моль
160 г/моль
40 г
40
B10
4
0
Слайд 31С1
Используя метод электронного баланса, составьте уравнение реакции:
Si + HNO3 + HF
= H2SiF6 + NO + …
Определите окислитель и восстановитель.
Слайд 32C2
Даны вещества:
сера
сероводород
азотная кислота (конц.)
серная кислота (конц.)
Приведите уравнения четырех возможных реакций
Слайд 33С3
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
H2O, KOH,
пропилацетат
X1
X2
кат.
1200 °
изб. Br2
X3
CH4
винилацетилен
Слайд 34C4
Какой объем хлора (н.у.) выделится, если к 200 мл 35%-ной соляной
Какая масса гидроксида натрия в холодном растворе прореагирует с таким количеством хлора?
Слайд 35С5
При взаимодействии одного и того же количества алкена с различными галогеноводородами
Определите молекулярную формулу алкена.