- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки презентация
Содержание
- 1. Белки
- 2. Белки (полипептиды) − биополимеры, построенные из остатков
- 3. Схема образования полипептида
- 4. Макромолекулы белков имеют строго упорядоченное
- 5. Первичная структура – определенный набор и последовательность α-аминокислотных остатков в полипептидной цепи .
- 6. Вторичная структура – конформация полипептидной
- 7. Третичная структура – форма закрученной
- 8. Четвертичная структура – агрегаты нескольких
- 12. Гидролиз При гидролизе белков образуются аминокислоты.
- 14. Презентацию разработали: Сточанский Иван, 11 класс Тимощук Анастасия, 11 класс Учитель: Корягина С.В.
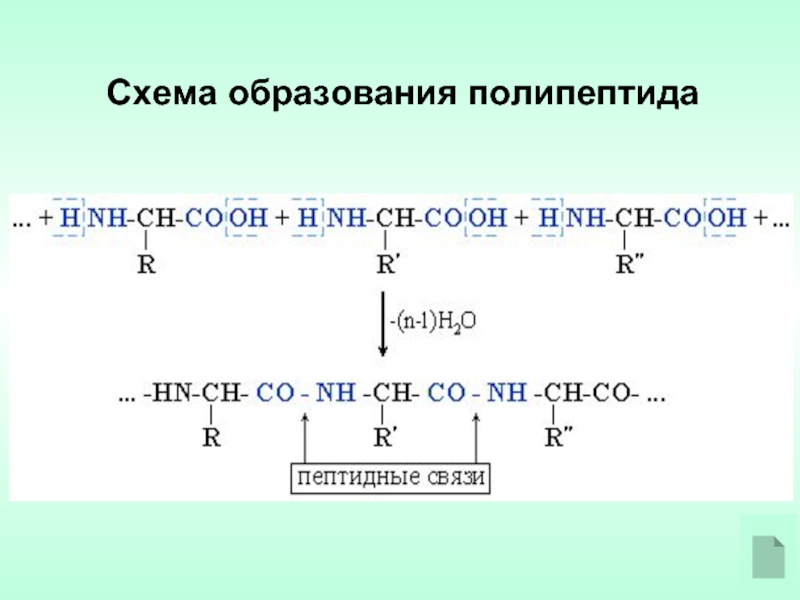
Слайд 2Белки (полипептиды) − биополимеры, построенные из остатков
α-аминокислот, соединенных пептидными связями.
Пептидной
связью называют амидную связь –CO–NH–, образованную при взаимодействии α-аминокислот за счет реакции между аминогруппой NH2 одной молекулы и карбоксильной группы COOH – другой.
Слайд 4 Макромолекулы белков имеют строго упорядоченное химическое и
пространственное строение, исключительно
важное для проявления ими определенных биологических свойств.
Выделяют 4 уровня структурной организации белков:
Первичная структура
Вторичная структура
Третичная структура
Четвертичная структура
Выделяют 4 уровня структурной организации белков:
Первичная структура
Вторичная структура
Третичная структура
Четвертичная структура
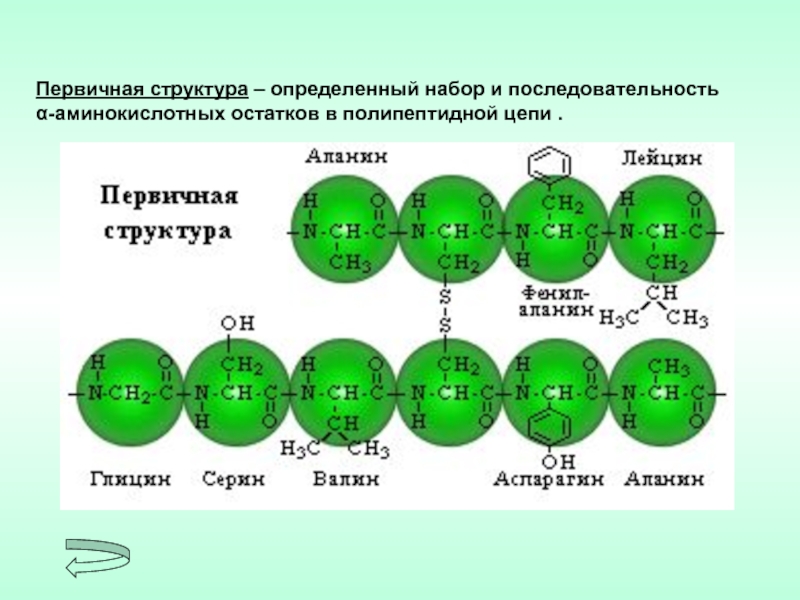
Слайд 5Первичная структура – определенный набор и последовательность
α-аминокислотных остатков в полипептидной цепи
.
Слайд 6Вторичная структура –
конформация полипептидной цепи, закрепленная множеством водородных связей между
группами N–H и С=О.
Одна из моделей вторичной структуры – α-спираль .
Одна из моделей вторичной структуры – α-спираль .
Слайд 7Третичная структура
– форма закрученной спирали в пространстве,
образованная главным образом
за счет дисульфидных мостиков -S-S-,
водородных связей, гидрофобных и ионных взаимодействий.
водородных связей, гидрофобных и ионных взаимодействий.
Слайд 8Четвертичная структура
– агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за
счет взаимодействия разных полипептидных цепей.
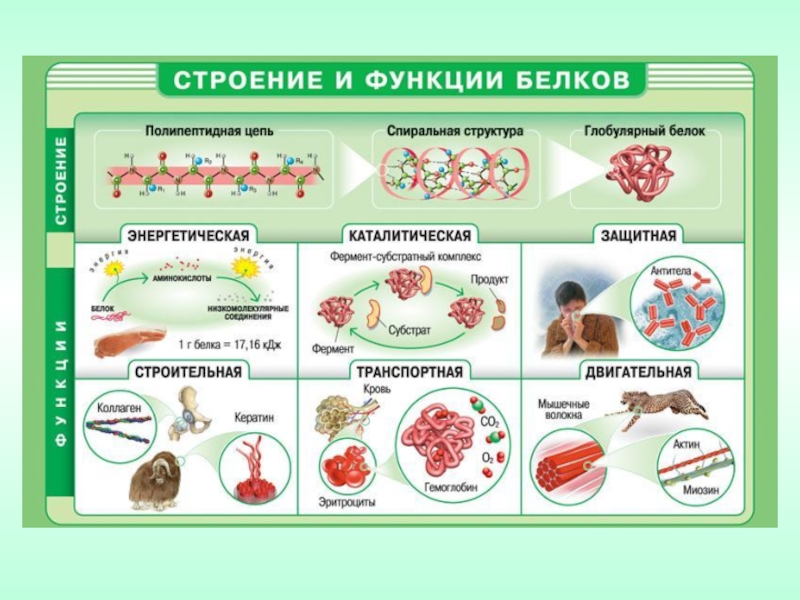
Слайд 10 Функции белков в природе:
каталитические
(ферменты);
регуляторные (гормоны);
структурные (кератин шерсти, фиброин шелка, коллаген);
двигательные (актин, миозин);
транспортные (гемоглобин);
запасные (казеин, яичный альбумин);
защитные (иммуноглобулины) и т.д.
регуляторные (гормоны);
структурные (кератин шерсти, фиброин шелка, коллаген);
двигательные (актин, миозин);
транспортные (гемоглобин);
запасные (казеин, яичный альбумин);
защитные (иммуноглобулины) и т.д.
Слайд 12Гидролиз
При гидролизе белков образуются аминокислоты.
Денатурация.
При нагревании белков происходит разрушение
сначала четвертичной, потом третичной структуры белка и так далее. При прекращении нагревания молекулы белка снова объединяются в сложные структуры. Следовательно, полностью разрушить белок можно только при очень высоком нагревании, при котором разрушается первичная структура – полипептидная цепь.
Цветные реакции:
Для белков характерно сворачивание и образование жёлтого осадка при действии азотной кислоты (ксантопротеиновая реакция) и образование фиолетового окрашивания при взаимодействии белка с гидроксидом меди (II) (биуретовая реакция)
Цветные реакции:
Для белков характерно сворачивание и образование жёлтого осадка при действии азотной кислоты (ксантопротеиновая реакция) и образование фиолетового окрашивания при взаимодействии белка с гидроксидом меди (II) (биуретовая реакция)
Свойства белков