- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Азотная кислота презентация
Содержание
- 1. Азотная кислота
- 2. Основные вопросы Строение молекулы азотной кислоты. Физические
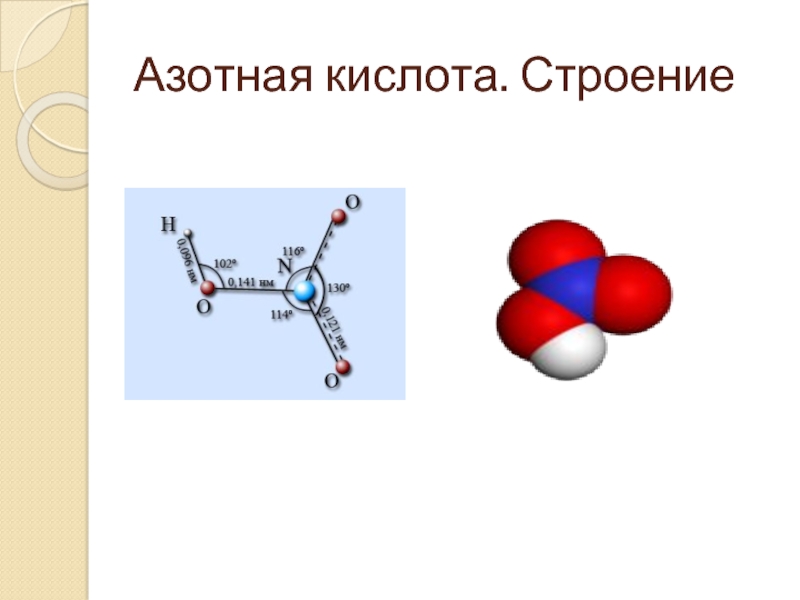
- 3. Азотная кислота. Строение
- 4. Физические свойства Дымящаяся жидкость, ρ=1,52 г/мл, безцветная,
- 5. Получение HNO3 В лаборатории
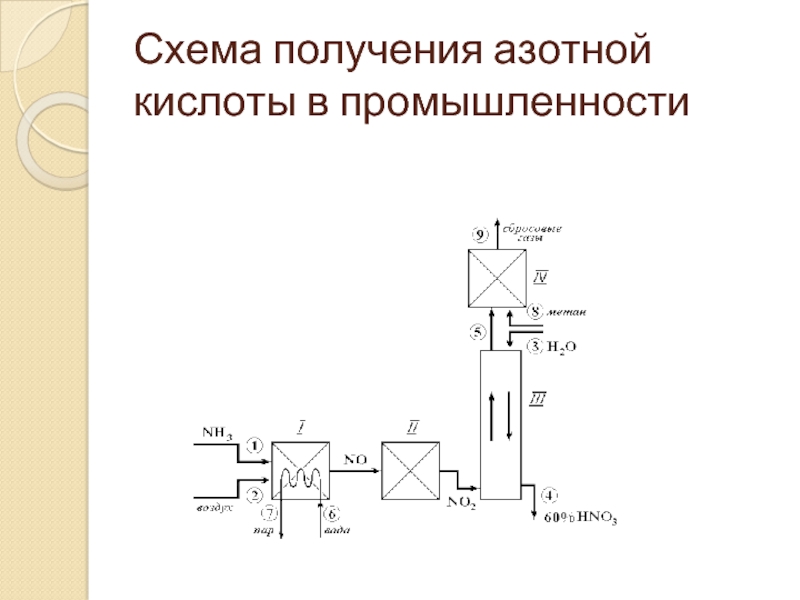
- 6. Схема получения азотной кислоты в промышленности
- 7. Химические свойства Азотная кислота является сильным
- 8. Свойства общие с другими кислотами Составьте уравнения
- 9. Проверьте уравнения 2HNO3 + Mg(OH)2 = Mg(NO3)2
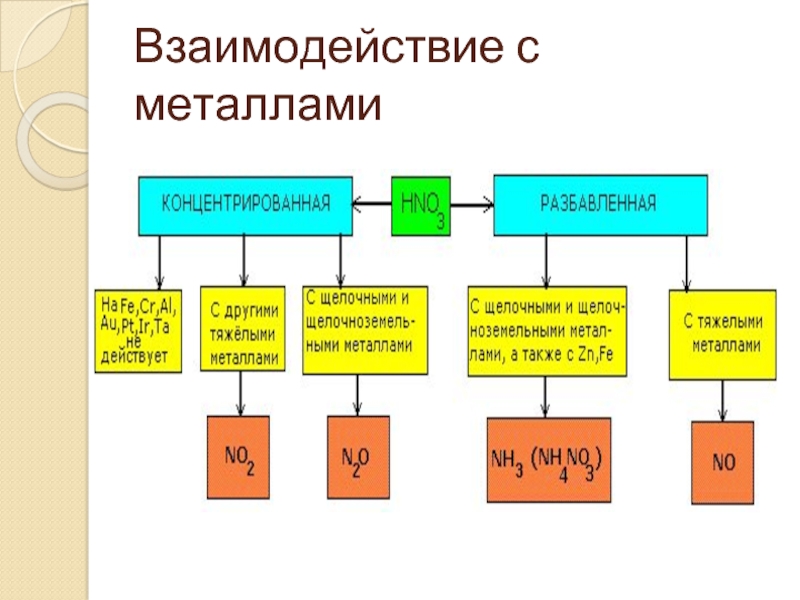
- 10. Взаимодействие с металлами
- 11. Лабораторный эксперимент № 1 В пробирку
- 12. Проверьте себя Cu + HNO3 (КОНЦ.) = Сu(NO3)2 + NO2 + H2O
- 13. Лабораторный эксперимент № 2 В пробирку
- 14. Проверьте себя Cu + HNO3(разб.) = Cu(NO3)2
- 15. Подведение итогов Каковы физические свойства азотной
- 16. Применение азотной кислоты и нитратов Азотная кислота
Слайд 2Основные вопросы
Строение молекулы азотной кислоты.
Физические свойства.
Получение азотной кислоты.
Химические свойства.
Свойства нитратов.
Применение азотной
кислоты и нитратов.
Слайд 4Физические свойства
Дымящаяся жидкость, ρ=1,52 г/мл, безцветная, едкий запах, Ткип=82,6ºС
Т=-42ºС - прозрачные кристаллы, очень гигроскопична
Сильный окислитель. Разрушает животные и растительные ткани
Сильный окислитель. Разрушает животные и растительные ткани
Слайд 5Получение HNO3
В лаборатории
NaNO3(ТВ.)+H2SO4(КОНЦ)=NaHSO4 + HNO3↑
В промышлености 4NH3 + 5O2 = 4NO + 6H2O + Q 2NO + O2 = 2NO2(при охлаждении) 4NO2 + O2 + 2H2O ↔ 4HNO3 + Q
В промышлености 4NH3 + 5O2 = 4NO + 6H2O + Q 2NO + O2 = 2NO2(при охлаждении) 4NO2 + O2 + 2H2O ↔ 4HNO3 + Q
Слайд 7Химические свойства
Азотная кислота является сильным окислителем, концентрированная азотная кислота окисляет серу
до серной, а фосфор - до фосфорной кислот, некоторые органические соединения (например амины и гидразины, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Слайд 8Свойства общие с другими кислотами
Составьте уравнения реакций
HNO3 + Mg(OH)2 =
HNO3
+ Al2O3 =
HNO3 + (NH4)2CO3 =
HNO3 + (NH4)2CO3 =
Слайд 9Проверьте уравнения
2HNO3 + Mg(OH)2 = Mg(NO3)2 + 2H2O (реакция нейтрализации)
6HNO3 +
Al2O3 = 2Al(NO3)3 + 3H2O (реакция обмена)
2HNO3 + (NH4)2CO3 = 2NH4NO3 + CO2î + H2O (реакция обмена)
2HNO3 + (NH4)2CO3 = 2NH4NO3 + CO2î + H2O (реакция обмена)
Слайд 11Лабораторный эксперимент № 1
В пробирку с концентрированной азотной кислотой осторожно
добавляйте несколько тонких кусочков медной проволоки. Реакция идёт без нагревания, учащиеся наблюдают изменение цвета раствора и выделение красно-бурого газа NO2
Составьте уравнение происходящей реакции
Составьте уравнение происходящей реакции
Слайд 13Лабораторный эксперимент № 2
В пробирку с разбавленной азотной кислотой осторожно
добавляйте несколько тонких кусочков медной проволоки. Реакция идёт при нагревании. Наблюдайте изменение цвета раствора и выделение бесцветного газа NO
Составьте уравнение происходящей реакции
Составьте уравнение происходящей реакции
Слайд 14Проверьте себя
Cu + HNO3(разб.) = Cu(NO3)2 + NO + H2O
0 +1
Cu – 2e = Cu 3 восстановитель окисляется
+5 +2
N + 3e = N 2окислитель восстанавливается 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
Cu – 2e = Cu 3 восстановитель окисляется
+5 +2
N + 3e = N 2окислитель восстанавливается 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
Слайд 15Подведение итогов
Каковы физические свойства азотной кислоты?
Почему азотную кислоту хранят в склянках
из тёмного стекла?
Почему азотную кислоту используют для получения взрывчатых веществ?
Перечислите особенности взаимодействия азотной кислоты с металлами.
С какими металлами не реагирует азотная кислота?
Почему азотную кислоту используют для получения взрывчатых веществ?
Перечислите особенности взаимодействия азотной кислоты с металлами.
С какими металлами не реагирует азотная кислота?
Слайд 16Применение азотной кислоты и нитратов
Азотная кислота широко используется для получения нитросоединений.
В
смеси с соляной кислотой образует «царскую водку», которая растворяет большинство металлов, в том числе и золото.
Соли азотной кислоты — нитраты — широко используются как удобрения. При этом практически все нитраты хорошо растворимы в воде. Поэтому в виде минералов их природе чрезвычайно мало; исключение составляют чилийская (натриевая) селитра и индийская селитра (нитрат калия). Большинство нитратов получают искусственно.
Соли азотной кислоты — нитраты — широко используются как удобрения. При этом практически все нитраты хорошо растворимы в воде. Поэтому в виде минералов их природе чрезвычайно мало; исключение составляют чилийская (натриевая) селитра и индийская селитра (нитрат калия). Большинство нитратов получают искусственно.