- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Антибиотики презентация
Содержание
- 1. Антибиотики
- 2. Александр Флеминг открытие пенициллина 1928
- 3. Ермольева Зинаида Виссарионовна Первый отечественный пенициллин (крустозин) был получен из P. crustosum в 1942 г.
- 4. Критерии эффективности Терапевтический индекс — частное от
- 5. Спектр активности антимикробных средств. Антимикробные агенты действуют
- 6. Препараты узкого спектра активны в отношении небольших
- 7. Антибактериальные, противогрибковые и антипротозойные препараты тормозят рост
- 8. К антибактериальным химиотерапевтическим средствам относят антибиотики,
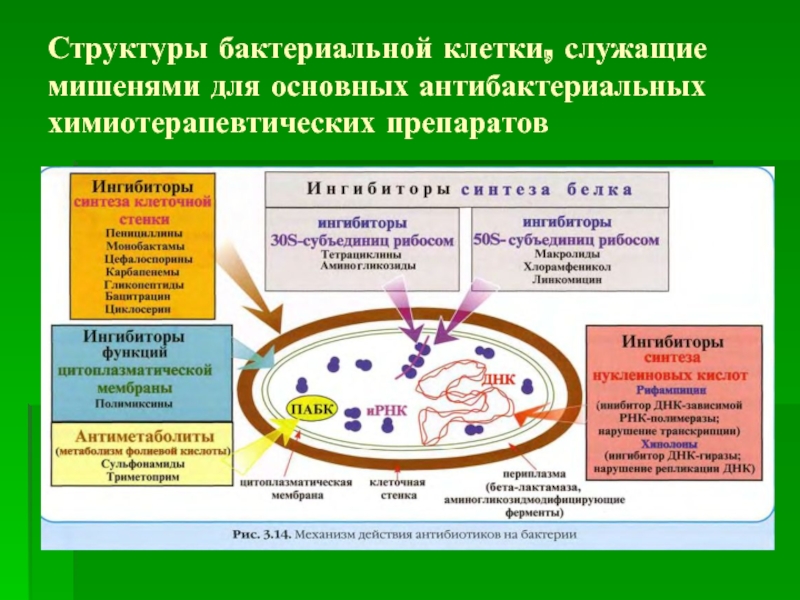
- 9. Структуры бактериальной клетки, служащие мишенями для основных антибактериальных химиотерапевтических препаратов
- 10. Тип продуцента В соответствии с типом продуцента
- 11. Способы получения антибиотиков: • биосинтетические (природные), их
- 12. Механизм действия. Антибиотики подавляют различные процессы:
- 13. Ингибиторы синтеза компонентов клеточной стенки ß-Лактамные
- 14. ß-лактамы обладают общим механизмом действия – подавление
- 15. Механизмы устойчивости Продукция бета-лактамаз Появление ПСБ со
- 16. Классификация бета-лактамаз Класс А 2А – стафилококки,
- 17. 2BE – энтеробактерии. БЛРС. Гидролизуют природные
- 18. 2С - P.aeruginosa, M.catarralis, др. грам-. Гидролизуют
- 19. Класс В Грам -. Гидролизуют практически
- 20. Класс D 2D P.aeruginosa, реже другие
- 21. В настоящее время общепризнано, что штаммы E.coli,
- 22. ПСБ со сниженной активностью к бета-лактамным антибиотикам
- 23. Активное выведение антибиотиков из микробной клетки –
- 24. Пенициллины Биосинтетические пенициллины бензилпенициллин,
- 25. Полусинтетические пенициллины Препараты I поколения отличает узкий
- 26. Препараты II и III поколений отличает широкий
- 27. критерии оценки чувствительности разработаны не для всех
- 28. Карбокси-, уреидо- и ацилпенициллины азлоциллин,
- 29. Потенцированные пенициллины разработаны в связи с увеличением
- 30. Цефалоспорины В соответствии с последовательностью внедрения
- 31. II поколение цефуроксим, цефамандол, цефокситин, цефотетан,
- 32. III поколение цефотаксим, цефтриаксон, цефтазидим,
- 33. III поколение Все цефалоспорины III поколения гидролизуются
- 34. IV поколение цефепим высокоактивен в отношении
- 35. Цефалоспорины активны против многих грамположительных и грамотрицательных
- 36. Монобактамы азтреонам устойчивы к В-лактамазам
- 37. Карбапенемы имипенем меропенем эртапенем дорипенем
- 38. Эртапенем неактивен в отношении P.aeruginosa. Имипенем
- 39. Ингибитор-защищенные бета-лактамы Амоксициллин-клавуланат ампициллин-сульбактам, цефоперазон-сульбактам.
- 40. Гликопептиды Ванкомицин тейкопланин. В спектр
- 41. Ингибиторы функций цитоплазматической мембраны Полимиксины — комплекс полипептидов,
- 42. Ингибиторы синтеза белка Аминогликозиды Препараты I
- 43. Спектр активности включает многие грамположительные и грамотрицательные
- 44. Тетрациклины бактериостатические антибиотики широкого спектра действия,
- 45. Хлорамфеникол Хлорамфеникол (левомицетин, продуцент — Streptomyces venezuelae).
- 46. Макролиды Макролиды— продуцируемые видами Streptomyces антибиотики, спектр
- 47. Линкозамиды линкомицин и клиндамицин По основным показателям
- 48. Оксазолидиноны Линезолид Активен в отношении полирезистентных стафилококков
- 49. Хинолоны Нефторированные налидиксовая кислота,
- 50. Фторированные Не обладающие антипневмококковой активностью эноксацин,
- 51. Антипневмококковые – левофлоксацин, спарфлоксацин,
- 52. У грам - - полная перекрестная резистентность
Слайд 3Ермольева Зинаида Виссарионовна
Первый отечественный пенициллин (крустозин) был получен из P. crustosum в
1942 г.
Слайд 4Критерии эффективности
Терапевтический индекс — частное от деления минимальной токсической дозы соединения на
минимальную дозу, проявляющую антимикробную активность. Более высокие значения терапевтического индекса соответствуют большей эффективности препарата.
Достижимая концентрация в сыворотке крови зависит от массы тела пациента, дозы препарата, пути и схемы введения, а также скорости его выведения из организма.
Достижимая концентрация в сыворотке крови зависит от массы тела пациента, дозы препарата, пути и схемы введения, а также скорости его выведения из организма.
Слайд 5Спектр активности антимикробных средств.
Антимикробные агенты действуют только на вегетирующие клетки, но
не на споры или цисты.
Для реализации своей биологической активности антимикробное средство должно:
• проникнуть в бактериальную клетку;
• связаться с соответствующей мишенью и модифицировать её;
• сохранить при этом свою структуру либо образовать активный метаболит.
Для реализации своей биологической активности антимикробное средство должно:
• проникнуть в бактериальную клетку;
• связаться с соответствующей мишенью и модифицировать её;
• сохранить при этом свою структуру либо образовать активный метаболит.
Слайд 6Препараты узкого спектра активны в отношении небольших групп микроорганизмов.
Препараты широкого спектра
активны в отношении больших групп микроорганизмов.
Слайд 7Антибактериальные, противогрибковые и антипротозойные препараты тормозят рост либо вызывают гибель микроорганизмов.
Противовирусные препараты ингибируют репликацию вирусов, блокируя их адсорбцию на чувствительных клетках, высвобождение вирусного генома либо подавляя вирусоспецифические синтезы.
Активность химиотерапевтических препаратов выражают в единицах действия (ЕД) или в микрограммах (мкг).
Слайд 8К антибактериальным химиотерапевтическим средствам относят антибиотики,
сульфаниламидные препараты,
синтетические антибактериальные средства
различного химического строения,
Противосифилитические,
противотуберкулёзные средства.
Противосифилитические,
противотуберкулёзные средства.
Слайд 9Структуры бактериальной клетки, служащие мишенями для основных антибактериальных химиотерапевтических препаратов
Слайд 10Тип продуцента
В соответствии с типом продуцента выделяют антибиотики, синтезируемые грибами (бензилпенициллин,
гризеофульвин, цефалоспорины),
актиномицетами (стрептомицин, эритромицин)
бактериями (полимиксины).
актиномицетами (стрептомицин, эритромицин)
бактериями (полимиксины).
Слайд 11Способы получения антибиотиков:
• биосинтетические (природные), их продуцентами выступают специальные штаммы микроорганизмов;
• полусинтетические, получаемые химическим соединением природного антибиотика, точнее его «ядра», с различными химическими радикалами (при этом возможно направленное создание препаратов с заданными свойствами);
• синтетические антибиотики , источник их получения — химический синтез, возможный после определения структуры природных препаратов (например, синтетическим путём получают левомицетин).
Слайд 12Механизм действия.
Антибиотики подавляют различные процессы:
синтез компонентов клеточной стенки,
функции цитоплазматической
мембраны,
синтез белка,
транскрипцию и синтез нуклеиновых кислот микроорганизмов.
синтез белка,
транскрипцию и синтез нуклеиновых кислот микроорганизмов.
Слайд 13Ингибиторы синтеза компонентов клеточной стенки
ß-Лактамные антибиотики
К ß-лактамным антибиотикам относят
пенициллины,
цефалоспорины,
монобактамы,
карбапенемы.
Все ß-лактамные антибиотики обладают сходной структурой (содержат ß-лактамное кольцо) и механизмами антимикробного действия
Все ß-лактамные антибиотики оказывают бактерицидное действие.
Слайд 14ß-лактамы обладают общим механизмом действия – подавление синтеза пептидогликана путем ингибиции
ферментов транс- и карбоксипептидаз.
Благодаря способности связываться с пенициллином эти ферменты получили название пенициллинсвязывающих белков (ПСБ)
Благодаря способности связываться с пенициллином эти ферменты получили название пенициллинсвязывающих белков (ПСБ)
Слайд 15Механизмы устойчивости
Продукция бета-лактамаз
Появление ПСБ со сниженной аффинностью к бета-лактамам
Активное выведение антибиотика
из клетки
Нарушение проницаемости внешней мембраны
Нарушение проницаемости внешней мембраны
Слайд 16Классификация бета-лактамаз
Класс А
2А – стафилококки, другие грам+ и грам -.
Гидролизуют
природные и полусинтетические пенициллины, кроме метициллина и оксациллина
2B – Грам – (энтеробактерии).
БЛ широкого спектра. Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1 поколения. Чувствительны к ингибиторам
2B – Грам – (энтеробактерии).
БЛ широкого спектра. Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1 поколения. Чувствительны к ингибиторам
Слайд 172BE – энтеробактерии.
БЛРС. Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1-3
и вменьшей степени 4 поколения. Чувствительны к ингибиторам
2BR – энтеробактерии.
Ингибитор-резистентные БЛ. Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1 поколения. Устойчивы к ингибиторам
2BR – энтеробактерии.
Ингибитор-резистентные БЛ. Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1 поколения. Устойчивы к ингибиторам
Слайд 182С - P.aeruginosa, M.catarralis, др. грам-. Гидролизуют в различной степени природные
и полусинтетическин пенициллины и цефалоспорины. Чувствительны к ингибиторам
2Е - P.vulgaris, C.diversus
Гидролизуют в различной степени природные и полусинтетические пенициллины, цефалоспорины 1-3 поколений. Чувствительны к ингибиторам.
2F Грам -.
Гидролизуют пенициллины, цефалоспорины (в различной степени), карбапенемы. Чувствительность к ингибиторам варьирует
2Е - P.vulgaris, C.diversus
Гидролизуют в различной степени природные и полусинтетические пенициллины, цефалоспорины 1-3 поколений. Чувствительны к ингибиторам.
2F Грам -.
Гидролизуют пенициллины, цефалоспорины (в различной степени), карбапенемы. Чувствительность к ингибиторам варьирует
Слайд 19Класс В
Грам -.
Гидролизуют практически все бета-лактамы, включая карбапенемы. Нечувствительны к
ингибиторам
Класс С
Грам -.
Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1-3 поколений. Нечувствительны к ингибиторам.
Класс С
Грам -.
Гидролизуют природные и полусинтетические пенициллины, цефалоспорины 1-3 поколений. Нечувствительны к ингибиторам.
Слайд 20Класс D
2D P.aeruginosa, реже другие грам-. БЛРС. Гидролизуют пенициллины (включая оксациллин),
в различной степени цефалоспорины 1-3 поколений, в незначительной степени карбапенемы. Малочувствительны к действию ингибиторов
Слайд 21В настоящее время общепризнано, что штаммы E.coli, Klebsiella spp., продуцирующие БЛРС,
необходимо рассматривать как устойчивые к пенициллинам, цефалоспоринам и азтреонаму, независимо от конкретных результатов лабораторной оценки антибиотикочувствительности.
Слайд 22ПСБ со сниженной активностью к бета-лактамным антибиотикам
их появление приводит к
повышению МПК антибиотиков, но далеко не всегда сопровождается появлением клинически значимой устойчивости.
ПСБ со сниженной активностью к бета-лактамным антибиотикам обусловливают устойчивость к этим антибиотикам S.pneumoniae, Staphylococcus spp, N. gonorrhoeae, H.influensae, Enterococcus spp.
ПСБ со сниженной активностью к бета-лактамным антибиотикам обусловливают устойчивость к этим антибиотикам S.pneumoniae, Staphylococcus spp, N. gonorrhoeae, H.influensae, Enterococcus spp.
Слайд 23Активное выведение антибиотиков из микробной клетки – этот механизм чаще всего
проявляется у Pseudomonas.spp.
Нарушение проницаемости внешней мембраны микробной клетки встречается только у грамотрицательных бактерий, чаще всего в сочетании с другими механизмами устойчивости.
Нарушение проницаемости внешней мембраны микробной клетки встречается только у грамотрицательных бактерий, чаще всего в сочетании с другими механизмами устойчивости.
Слайд 24Пенициллины
Биосинтетические пенициллины
бензилпенициллин,
феноксиметилпенициллин
оказывают действие на грамположительные и ограниченное число
грамотрицательных микроорганизмов.
Препараты не проникают в большинство грамотрицательных бактерий и инактивируются бактериальными В-лактамазами (пенициллиназами).
Препараты не проникают в большинство грамотрицательных бактерий и инактивируются бактериальными В-лактамазами (пенициллиназами).
Слайд 25Полусинтетические пенициллины
Препараты I поколения отличает узкий спектр действия, направленный преимущественно в
отношении грамположительных микроорганизмов, включая штаммы-продуценты В-лактамаз
оксациллин,
клоксациллин,
флуклоксациллин
Устойчивость к оксациллину у стафилококков является маркером наличия дополнительного ПСБ – ПСБ 2а, опосредующего устойчивость ко всем бета-лактамам.
MRSA – метициллинрезистентный S.aureus;
MRSS;
MRSE.
оксациллин,
клоксациллин,
флуклоксациллин
Устойчивость к оксациллину у стафилококков является маркером наличия дополнительного ПСБ – ПСБ 2а, опосредующего устойчивость ко всем бета-лактамам.
MRSA – метициллинрезистентный S.aureus;
MRSS;
MRSE.
Слайд 26Препараты II и III поколений отличает широкий спектр действия, но они
инактивируются В-лактамазами.
Аминопенициллины
ампициллин,
амоксициллин
активны в отношении грамположительных кокков и ряда аэробных и факультативно анаэробных грамотрицательных бактерий;
Аминопенициллины
ампициллин,
амоксициллин
активны в отношении грамположительных кокков и ряда аэробных и факультативно анаэробных грамотрицательных бактерий;
Слайд 27критерии оценки чувствительности разработаны не для всех комбинаций микроб-антибиотик.
Для энтеробактерий
ампициллин → амоксициллин.
Слайд 28Карбокси-, уреидо- и ацилпенициллины
азлоциллин,
Пиперациллин
Карбенициллин
активны в отношении грамположительных и
грамотрицательных аэробных и анаэробных бактерий (особенно видов Pseudomonas и Proteus).
Из-за высокой чувствительности к бета-лактамазам область практического применения этих антибиотиков в настоящее время сведена к минимуму.
Реальное значение сохраняет лишь пиперациллин-тазобактам
Из-за высокой чувствительности к бета-лактамазам область практического применения этих антибиотиков в настоящее время сведена к минимуму.
Реальное значение сохраняет лишь пиперациллин-тазобактам
Слайд 29Потенцированные пенициллины
разработаны в связи с увеличением числа бактерий, продуцирующих В-лактамазы, и
возрастанием их роли в патологии человека.
Эти препараты содержат дополнительное В-лактамное кольцо, связывающее В-лактамазы, что защищает молекулу антибиотика от инактивации этими ферментами.
Наибольшее распространение нашли клавулановая кислота и сульбактам.
Эти препараты содержат дополнительное В-лактамное кольцо, связывающее В-лактамазы, что защищает молекулу антибиотика от инактивации этими ферментами.
Наибольшее распространение нашли клавулановая кислота и сульбактам.
Слайд 30Цефалоспорины
В соответствии с последовательностью внедрения в медицинскую практику различают цефалоспорины разных
поколений:
I поколение
цефазолин,
Цефалотин,
цефадроксил,
цефалексин
Активны в отношении Staphylococcus spp., S.pyogenes
I поколение
цефазолин,
Цефалотин,
цефадроксил,
цефалексин
Активны в отношении Staphylococcus spp., S.pyogenes
Слайд 31II поколение
цефуроксим,
цефамандол,
цефокситин,
цефотетан,
цефметазол,
цефаклор
спектр расширен за счет большинства энтеробактерий,
устойчивы
к действию БЛ широкого спектра, однако уровень активности в отношении Enterobacter, Serratia по сравнению с III поколением невысок.
Цефокситин, цефотетан также эффективны при инфекциях, вызванных бактероидами, устойчивы к действию БЛРС
Цефокситин, цефотетан также эффективны при инфекциях, вызванных бактероидами, устойчивы к действию БЛРС
Слайд 32III поколение
цефотаксим,
цефтриаксон,
цефтазидим,
цефоперазон,
цефпирамид,
Цефтибутен
широкий спектр и высокая активность
в отношении всего семейства энтеробактерий.
В отношении грам+ активность несколько меньше, чем у I-II, но клинически значима.
Неактивны в отношении P.aeruginosa цефотаксим и цефтриаксон; активны цефтазидим, цефоперазон, цефпирамид.
В отношении грам+ активность несколько меньше, чем у I-II, но клинически значима.
Неактивны в отношении P.aeruginosa цефотаксим и цефтриаксон; активны цефтазидим, цефоперазон, цефпирамид.
Слайд 33III поколение
Все цефалоспорины III поколения гидролизуются БЛРС, однако скорость гидролиза для
представителей группы разная.
На практике это приводит к тому, что микроорганизм, продуцирующий БЛРС, по формальным критериям может быть отнесен к чувствительным, однако в клинике антибиотик будет неэффективным.
Поэтому – необходимость в проведении дополнительных исследований для детекции БЛРС.
На практике это приводит к тому, что микроорганизм, продуцирующий БЛРС, по формальным критериям может быть отнесен к чувствительным, однако в клинике антибиотик будет неэффективным.
Поэтому – необходимость в проведении дополнительных исследований для детекции БЛРС.
Слайд 34IV поколение
цефепим
высокоактивен в отношении Грам+, энтеробактерий, НФГОМ.
Устойчив к стафилококковым
бета-лактамазам, БЛ широкого спектра грам- бактерий.
Разрушается БЛРС, однако в меньшей степени, чем цефалоспорины III поколения.
Разрушается БЛРС, однако в меньшей степени, чем цефалоспорины III поколения.
Слайд 35Цефалоспорины активны против многих грамположительных и грамотрицательных бактерий и препараты каждого
последующего поколения обычно имеют более широкий спектр действия.
Слайд 36Монобактамы
азтреонам
устойчивы к В-лактамазам
активны в отношении узкого спектра аэробных грамотрицательных
бактерий (виды Pseudomonas и Serratia), проявляющих множественную антибиотикорезистентность.
Слайд 37Карбапенемы
имипенем
меропенем
эртапенем
дорипенем
имеют самый широкий спектр действия среди всех антибиотиков, содержащих
В-лактамное кольцо.
к карбапенемам чувствительны гонококки и штаммы H. influenzae, резистентные к пенициллину и ампициллину.
В спектр активности не входят S.maltophilia (обладает карбапенемазами), MRSS, E.faecium (E.faecalis умеренно устойчив).
к карбапенемам чувствительны гонококки и штаммы H. influenzae, резистентные к пенициллину и ампициллину.
В спектр активности не входят S.maltophilia (обладает карбапенемазами), MRSS, E.faecium (E.faecalis умеренно устойчив).
Слайд 38Эртапенем неактивен в отношении P.aeruginosa.
Имипенем более активен в отношении грамположительных
бактерий,
Меропенем – грамотрицательных.
Приобретенная устойчивость распространена практически только среди P.aeruginosa.
У энтеробактерий – очень редко - перепроверять результаты!
Меропенем – грамотрицательных.
Приобретенная устойчивость распространена практически только среди P.aeruginosa.
У энтеробактерий – очень редко - перепроверять результаты!
Слайд 39Ингибитор-защищенные бета-лактамы
Амоксициллин-клавуланат
ампициллин-сульбактам,
цефоперазон-сульбактам.
Спектр –как у исходных соединений,
преимущество – устойчивость
к БЛ класса А.
Защищенные аминопенициллины – активны против продуцирующих БЛ Staphylococcus, E.coli, Klebsiella, Proteus, а также анаэробов.
Защищенные карбокси-, уреидопенициллины и цефоперазон-сульбактам – активны в отношении наиболее значимых анаэробов и многих продуцентов БЛ широкого и расширенного спектра.
Защищенные аминопенициллины – активны против продуцирующих БЛ Staphylococcus, E.coli, Klebsiella, Proteus, а также анаэробов.
Защищенные карбокси-, уреидопенициллины и цефоперазон-сульбактам – активны в отношении наиболее значимых анаэробов и многих продуцентов БЛ широкого и расширенного спектра.
Слайд 40Гликопептиды
Ванкомицин
тейкопланин.
В спектр входит большинство грамположительных микроорганизмов, реальное значение –
активность в отношении энтерококков и стафилококков, в том числе устойчивых к другим антибиотикам
Вместе с ристомицином, клиндамицином и линкомицином составляют группу антистафилококковых антибиотиков.
Вместе с ристомицином, клиндамицином и линкомицином составляют группу антистафилококковых антибиотиков.
Слайд 41Ингибиторы функций цитоплазматической мембраны
Полимиксины — комплекс полипептидов, синтезируемых Bacillus polymyxa и некоторыми
другими бактериями.
Спектр их бактерицидного эффекта включает грамотрицательную микрофлору (эшерихии, шигеллы, протей, клебсиеллы, псевдомонады и др.).
Препараты токсичны, в медицинской практике применяют лишь полимиксины В и Е (колистин) местно.
Спектр их бактерицидного эффекта включает грамотрицательную микрофлору (эшерихии, шигеллы, протей, клебсиеллы, псевдомонады и др.).
Препараты токсичны, в медицинской практике применяют лишь полимиксины В и Е (колистин) местно.
Слайд 42Ингибиторы синтеза белка
Аминогликозиды
Препараты I поколения
стрептомицин,
канамицин
II поколения
гентамицин,
сизомицин,
тобрамицин;
III поколения
амикацин
показаны при резистентности микроорганизмов к другим препаратам или при необходимости быстрого достижения бактерицидного эффекта.
проявляют синергизм с другими антибиотиками, в первую очередь с В-лактамными, и этот эффект часто используют при терапии инфекций, вызванных бактериями с множественной антибиотикорезистентностью (например, сочетание гентамицина с ампициллином).
Слайд 43Спектр активности включает многие грамположительные и грамотрицательные бактерии;
к аминогликозидам малочувствительны
некоторые стрептококки (пиогенный и зеленящий) и пневмококки, абсолютно резистентны энтерококки, провиденции, бактероиды и прочие анаэробы.
Ряд аминогликозидов (стрептомицин, канамицин) подавляют рост туберкулёзной палочки, а также простейших — амёб, лейшманий, токсоплазм (мономицин, канамицин).
Ряд аминогликозидов (стрептомицин, канамицин) подавляют рост туберкулёзной палочки, а также простейших — амёб, лейшманий, токсоплазм (мономицин, канамицин).
Слайд 44Тетрациклины
бактериостатические антибиотики широкого спектра действия, продуцируемые видами Streptomyces,
биосинтетические тетрациклины
окситетрациклин,
тетрациклин
полусинтетические
доксициклин,
миноциклин.
активны в отношении грамположительных и грамотрицательных бактерий, а также микоплазм и внутриклеточных паразитов — риккетсий, легионелл и хламидий; имеют большое значение в качестве средств лечения холеры, бруцеллёза, туляремии и др.
Для практических целей принято считать, что штаммы микроорганизмов, чувствительные к тетрациклину, чувствительны также к доксициклину и миноциклину.
Слайд 45Хлорамфеникол
Хлорамфеникол (левомицетин, продуцент — Streptomyces venezuelae).
Препарат действует на многие грамотрицательные и
грамположительные бактерии, риккетсии, спирохеты и хламидии и относится к немногим химиотерапевтическим средствам, эффективным в отношении грамотрицательных анаэробов.
Слайд 46Макролиды
Макролиды— продуцируемые видами Streptomyces антибиотики, спектр их действия несколько шире, чем
у бензилпенициллина.
Классификация макролидов основана на их химической структуре.
14-членные –
эритромицин,
олеандомицин,
рокситромицин,
кларитромицин
15-членные –
азитромицин
16-членные –
спирамицин,
мидекамицин,
джозамицин .
Классификация макролидов основана на их химической структуре.
14-членные –
эритромицин,
олеандомицин,
рокситромицин,
кларитромицин
15-членные –
азитромицин
16-членные –
спирамицин,
мидекамицин,
джозамицин .
Слайд 47Линкозамиды
линкомицин и клиндамицин
По основным показателям антибактериальной активности, механизму действия,и резистентности близки
к макролидам
В спектр действия этих антибиотиков входят прежде всего грам+ бактерии (стафилококки, стрептококки).
Активность в отношении некоторых грам- бактерий существенно ниже (нейссерии, гемофилы) и имеет ограниченное клиническое значение.
Исключение – хеликобактер, легионелла. Активны также в отношении хламидий, микоплазм, риккетсий.
В спектр действия этих антибиотиков входят прежде всего грам+ бактерии (стафилококки, стрептококки).
Активность в отношении некоторых грам- бактерий существенно ниже (нейссерии, гемофилы) и имеет ограниченное клиническое значение.
Исключение – хеликобактер, легионелла. Активны также в отношении хламидий, микоплазм, риккетсий.
Слайд 48Оксазолидиноны
Линезолид
Активен в отношении полирезистентных стафилококков и энтерококков.
Из других грамположительных –
бациллюс, коринебактерии, листерии, микобактерии, некоторые виды микоплазм.
Определенный уровень чувствительности проявляют гемофильная палочка, моракселла, легионелла, бордетелла, нейссерии.
Энтеробактерии и псевдомонады – устойчивы.
Активен в отношении анаэробов – клостридии, пептострептококки.
Бактероиды – менее чувствительны.
Определенный уровень чувствительности проявляют гемофильная палочка, моракселла, легионелла, бордетелла, нейссерии.
Энтеробактерии и псевдомонады – устойчивы.
Активен в отношении анаэробов – клостридии, пептострептококки.
Бактероиды – менее чувствительны.
Слайд 49Хинолоны
Нефторированные
налидиксовая кислота,
пипемидиевая кислота,
оксолиниевая кислота
активность в отношении кишечной
палочки, протея, клебсиелл
Слайд 50Фторированные
Не обладающие антипневмококковой активностью
эноксацин,
циноксацин (утратили значение),
норфлоксацин (энтеробактерии),
пефлоксацин, ломефлоксацин,
офлоксацин (энтеробактерии, гемофилы, моракселлы, легионеллы, нейссерии),
ципрофлоксацин (то же ,также псевдомонады, по уровню антиграмнегативной активности превосходит другие, даже более новые)
Активность против грам+ существенно ниже.
ципрофлоксацин (то же ,также псевдомонады, по уровню антиграмнегативной активности превосходит другие, даже более новые)
Активность против грам+ существенно ниже.
Слайд 51Антипневмококковые –
левофлоксацин,
спарфлоксацин,
моксифлоксацин,
гатифлоксацин,
гемифлоксацин
активны в отношении
грам+, в отношении грам- такая же активность как у более ранних.
Слайд 52У грам - - полная перекрестная резистентность между фторхинолонами.
Некоторые уропатогены
могут быть устойчивы к норфлоксацину, но ссохранять чувствительность к другим фторхинолонам.
У грам + - устойчивые к ципрофлоксацину и офлоксацину как правило сохраняют чувствительность к антипневмококковым
У грам + - устойчивые к ципрофлоксацину и офлоксацину как правило сохраняют чувствительность к антипневмококковым