- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОСНОВЫ ТЕРМОДИНАМИКИ презентация
Содержание
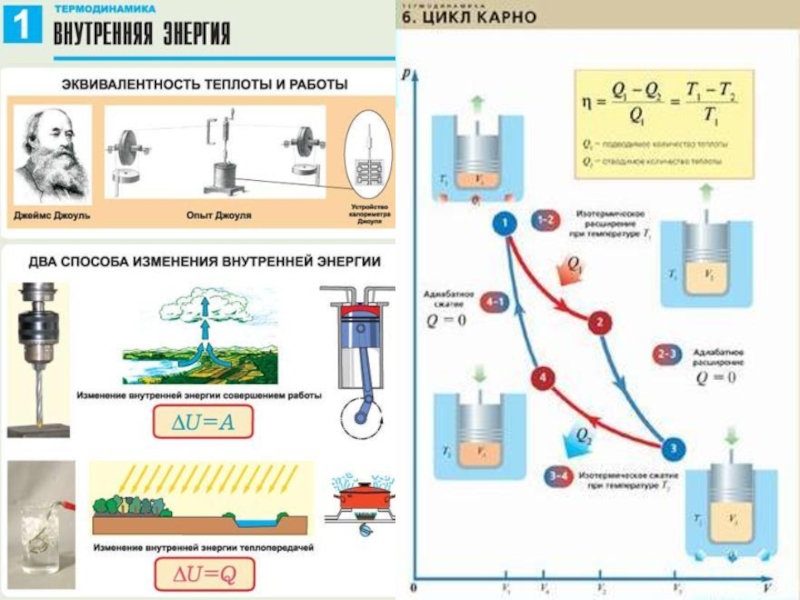
- 1. ОСНОВЫ ТЕРМОДИНАМИКИ
- 2. Термодинамика – теория тепловых процессов, в которой
- 3. Внутренняя энергия макроскопического тела равна сумме кинетических
- 5. Внутренняя энергия идеального одноатомного газа прямо пропорциональна
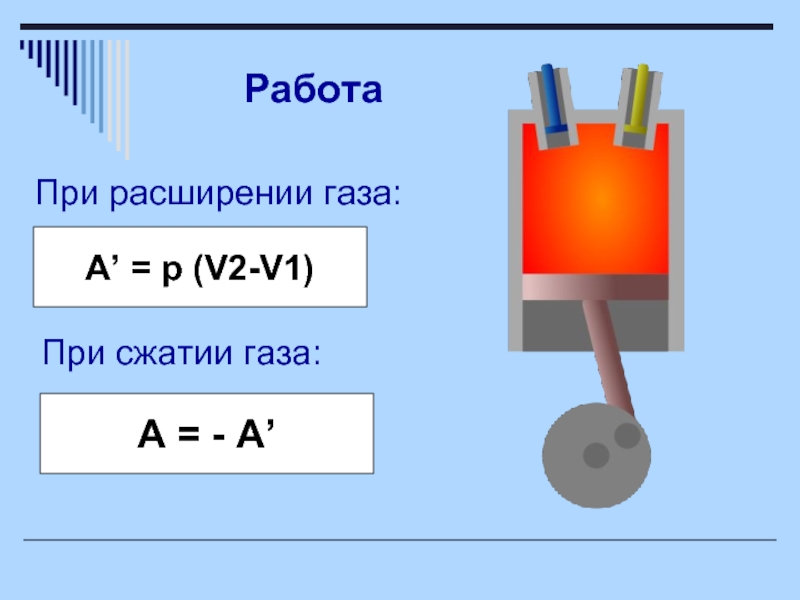
- 6. При расширении газа: Работа A’ = p (V2-V1) При сжатии газа: A = - A’
- 7. Работа внешних сил, действующих на газ: A
- 9. Виды теплопередачи энергии: Излучение – перенос
- 10. Q = Cm (t2 - t1) =
- 11. Закон сохранения энергии: Энергия в природе не
- 13. ЗАКОНЫ ТЕРМОДИНАМИКИ
- 14. I Закон термодинамики: Изменение внутренней энергии
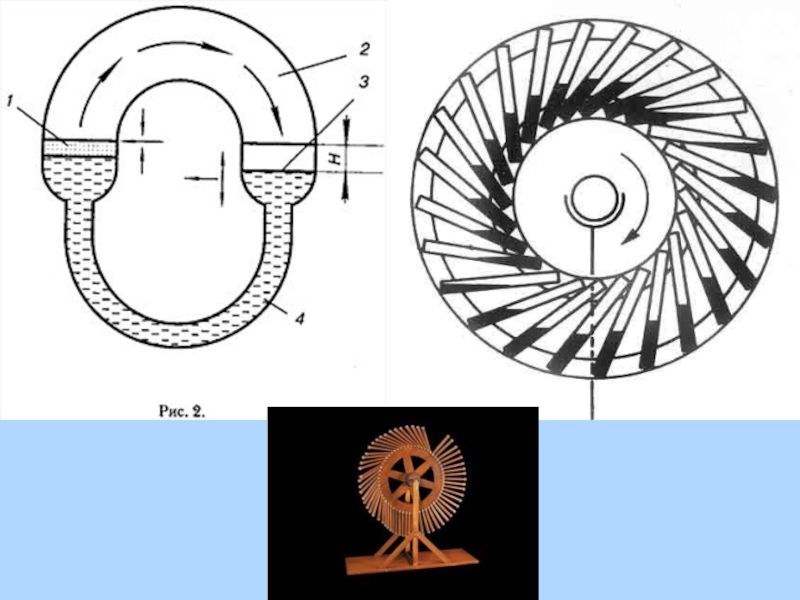
- 17. Вечный двигатель – устройство, способное совершать неограниченное
- 19. Невозможность создания вечного двигателя: Если к системе
- 20. Применение I Закона термодинамики к различным процессам:
- 21. Изобарный процесс: Q = ∆
- 22. Адиабатный процесс: Адиабатный процесс –
- 23. II Закон термодинамики: Невозможно перевести теплоту
- 24. Энергия всегда распространяется
- 25. II Закон термодинамики или конец света
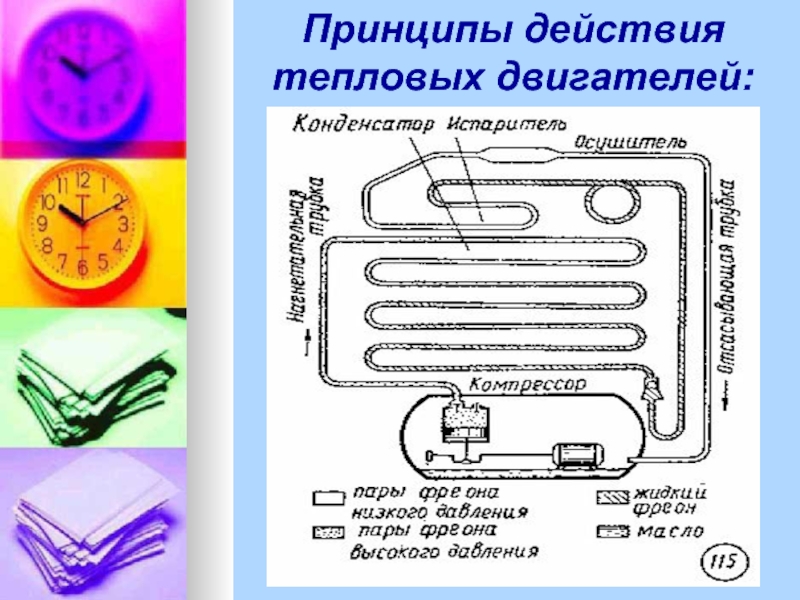
- 26. Принципы действия тепловых двигателей:
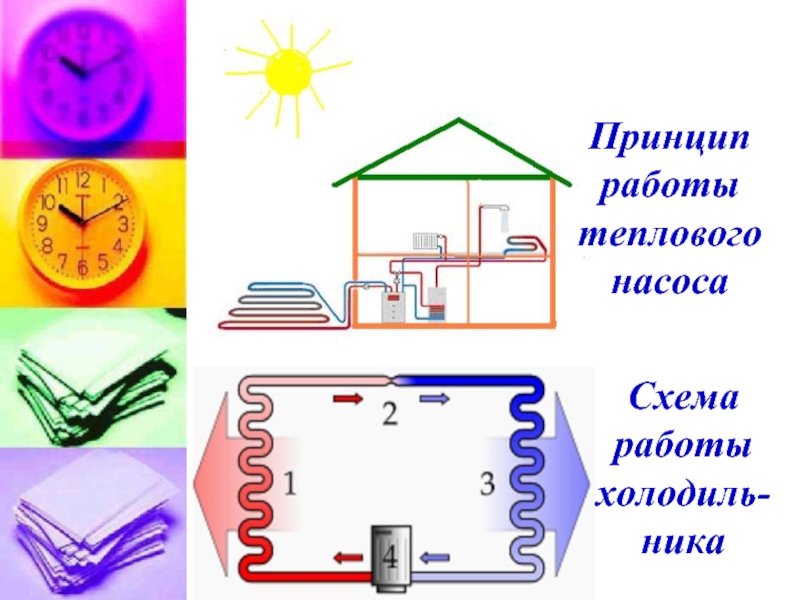
- 27. Принцип работы теплового насоса Схема работы холодиль-ника
- 28. Коэффициент полезного действия (КПД) теплового двигателя Коэффициент
- 29. n (max) = (T1 – T2)
- 30. Спасибо за внимание!
Слайд 2Термодинамика – теория тепловых процессов, в которой не учитывается молекулярное строение
Термодинамика была создана в середине XIX века после открытия закона сохранения энергии. В ее основе лежит понятие внутренняя энергия.
Слайд 3Внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного движения всех
Слайд 5Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре.
U =
Внутренняя энергия зависит от макроскопических параметров: температуры и объема.
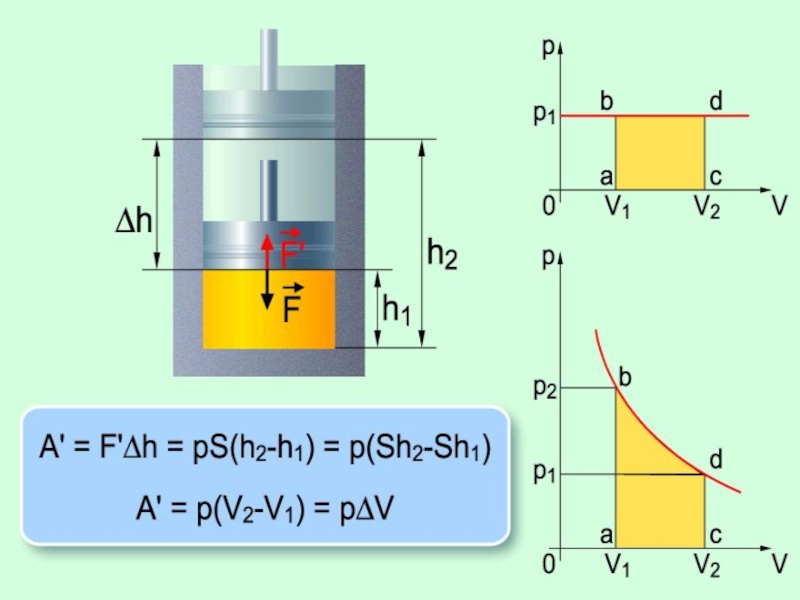
Слайд 7Работа внешних сил, действующих на газ:
A = - A’ = -
Геометрическое истолкование работы:
A’ = p1(V2-V1) = |ab|*|ac|
abdc - прямоугольник
Слайд 9Виды теплопередачи энергии:
Излучение – перенос Е электромагнитными волнами (в вакууме
Конвекция – перенос Е потоками жидкости или газа (теплые слои поднимаются ↑, а холодные опускаются ↓);
Теплопроводность – непосредственный обмен Е(кинетической) между хаотически движущимися частицами соприкасающихся тел и частей одного и того же тела.
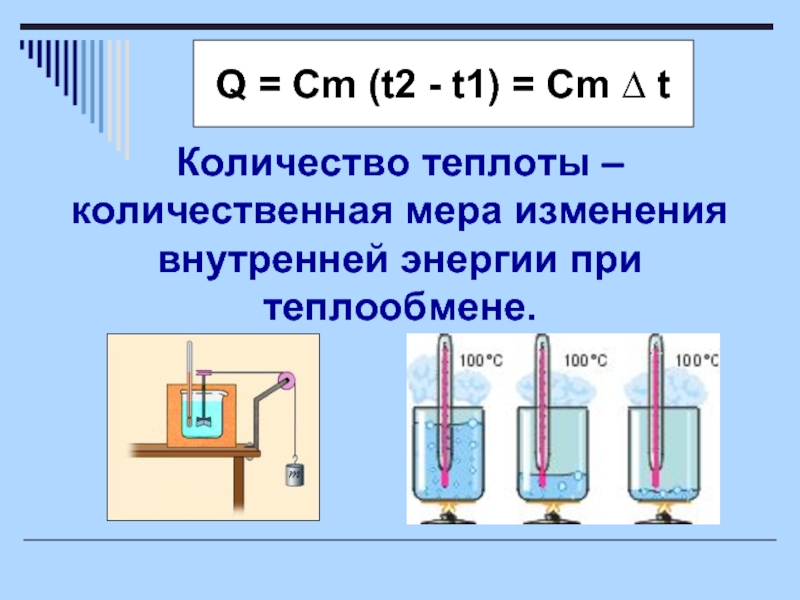
Слайд 10Q = Cm (t2 - t1) = Cm ∆ t
Количество теплоты
Слайд 11Закон сохранения энергии:
Энергия в природе не возникает из ничего и не
Слайд 14I Закон термодинамики:
Изменение внутренней энергии системы при переходе ее из
∆U = A + Q
Слайд 17Вечный двигатель – устройство, способное совершать неограниченное количество работы без затрат
Слайд 19Невозможность создания вечного двигателя:
Если к системе не поступает теплота (Q=0), то
Слайд 20Применение I Закона термодинамики к различным процессам:
Изохорный процесс:
∆ U =
Если газ нагревается, то Q>0 и ∆ U>0,
при охлаждении газа Q<0 и ∆ U = U2-U1<0.
Изотермический процесс:
Q = A’;
Если газ получает теплоту (Q>0), то A’>0,
газ отдает теплоту окружающей среде (термостату), Q<0 и A’<0.
Слайд 21 Изобарный процесс:
Q = ∆ U + A’;
Передаваемое газу количество теплоты
Слайд 22 Адиабатный процесс:
Адиабатный процесс – процесс в теплоизолированной системе.
Q
При расширении газа сам газ совершает положительную работу (A’>0) и внутренняя энергия его уменьшается – газ охлаждается.
Слайд 23II Закон термодинамики:
Невозможно перевести теплоту от более холодной системы к
(немецкий ученый Р. Клаузиус (1822-1888) сформулировал этот закон)
Слайд 28Коэффициент полезного действия (КПД) теплового двигателя
Коэффициент полезного действия (КПД) теплового двигателя
n = A’ / |Q1| =
= (|Q1| - |Q2|) / |Q1| =
= 1 - |Q2| / |Q1|
Слайд 29
n (max) = (T1 – T2) / T1
Главное значение формулы:
любая
(французский инженер и ученый Сади Карно(1796-1832)).