- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Идеальный газ. Давление газа. Основное уравнение МКТ. презентация
Содержание
- 1. Идеальный газ. Давление газа. Основное уравнение МКТ.
- 2. Идеальный газ Давление газа Средняя кинетическая
- 3. Основное уравнение молекулярно-кинетической теории (уравнение Клаузиуса) Закон:
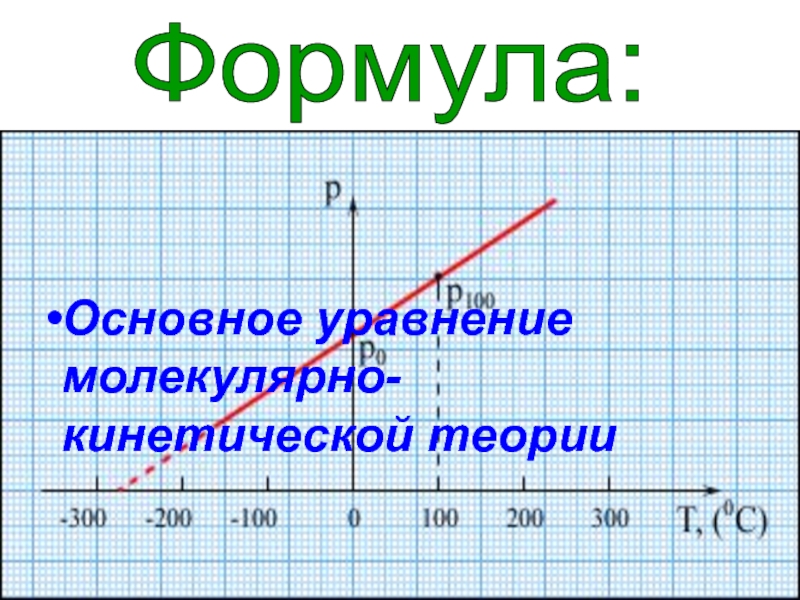
- 4. Формула: Основное уравнение молекулярно-кинетической теории
- 5. Идеальный газ. Давление газа. Основное уравнение молекулярно-кинетической
Слайд 2Идеальный газ
Давление газа
Средняя кинетическая энергия поступательного движения молекул
Концентрация молекул
Понятия и
величины:
Слайд 5Идеальный газ. Давление газа. Основное уравнение молекулярно-кинетической теории.
Идеальный газ –
простейшая физическая модель реального газа.
Газ считается идеальным, если выполнимы следующие допущения:
Размеры молекул ничтожны по сравнению со средним расстоянием между ними (молекула – материальная точка)
Силы притяжения стремятся к нулю, а силы отталкивания проявляются только при соударениях.
Молекулы – абсолютно упругие шары, которые движутся по законам Ньютона.
Идеальным газом называется газ, в котором собственным объемом молекул и межмолекулярным взаимодействием можно пренебречь.
Давление газа – это результат соударений большого числа молекул о стенки сосуда, в котором газ находится, и каждая молекула передает им определенный импульс.
Основное уравнение молекулярно-кинетической теории устанавливает зависимость между параметрами молекул и давлением.
Давление идеального газа p пропорционально произведению массы молекулы m0, концентрации молекул (числу молекул в единице объема) n и квадрату средней квадратичной скорости поступательного движения молекул υ2кв
р = m0∙ n∙ v2кв.
Через среднюю кинетическую энергию молекулы это уравнение записывают в виде
р = n∙E к
Давление газа численно равно двум третям средней кинетической энергии поступательного движения всех молекул, заключенных в единице объема.
Давление идеального газа определяется кинетической энергией его молекул.
Газ считается идеальным, если выполнимы следующие допущения:
Размеры молекул ничтожны по сравнению со средним расстоянием между ними (молекула – материальная точка)
Силы притяжения стремятся к нулю, а силы отталкивания проявляются только при соударениях.
Молекулы – абсолютно упругие шары, которые движутся по законам Ньютона.
Идеальным газом называется газ, в котором собственным объемом молекул и межмолекулярным взаимодействием можно пренебречь.
Давление газа – это результат соударений большого числа молекул о стенки сосуда, в котором газ находится, и каждая молекула передает им определенный импульс.
Основное уравнение молекулярно-кинетической теории устанавливает зависимость между параметрами молекул и давлением.
Давление идеального газа p пропорционально произведению массы молекулы m0, концентрации молекул (числу молекул в единице объема) n и квадрату средней квадратичной скорости поступательного движения молекул υ2кв
р = m0∙ n∙ v2кв.
Через среднюю кинетическую энергию молекулы это уравнение записывают в виде
р = n∙E к
Давление газа численно равно двум третям средней кинетической энергии поступательного движения всех молекул, заключенных в единице объема.
Давление идеального газа определяется кинетической энергией его молекул.