- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Защита границ в действии презентация
Содержание
- 1. Защита границ в действии
- 3. Ворсинки кишечника Альвеола Эпидермис Границы с внешним
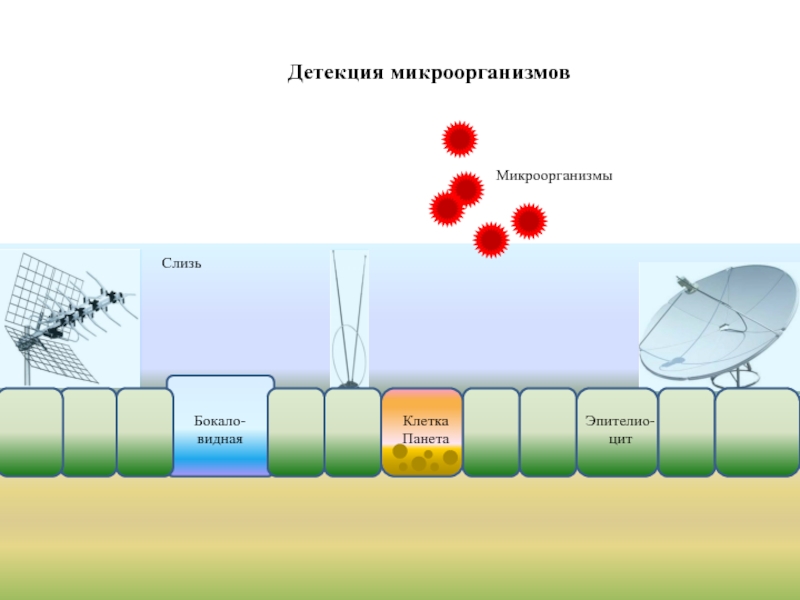
- 4. Детекция микроорганизмов Микроорганизмы Слизь
- 5. нельзя увидеть, услышать, почувствовать на вкус,
- 6. Клетки нашего организма снабжены молекулярными сенсорами инфекций.
- 7. Молекулярные сенсоры на наших клетках могут
- 8. Наши клетки распознают консервативные признаки микроорганизмов, то
- 9. Примеры общих молекулярных признаков всех бактерий: Олигосахаридные
- 10. Олигосахаридные цепочки бактерий заканчиваются
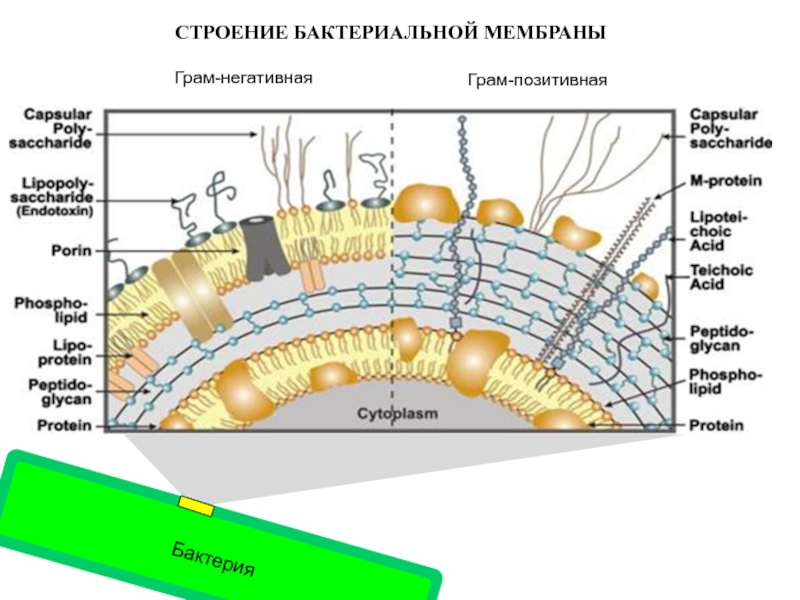
- 11. СТРОЕНИЕ БАКТЕРИАЛЬНОЙ МЕМБРАНЫ Грам-негативная Грам-позитивная
- 12. Бактериальный липополисахарид является общим молекулярным признаком всех Грам-отрицательных бактерий Грам-негативная
- 13. У нас есть рецепторы, разпознающие бактериальный липополисахарид
- 14. Молекулярные сенсоры инфекций и повреждений Toll-like receptors
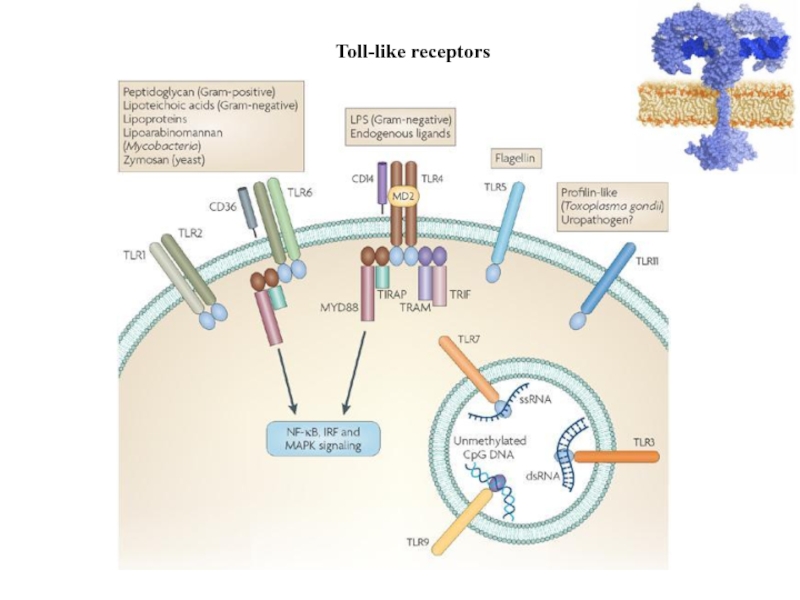
- 15. Toll-like receptors
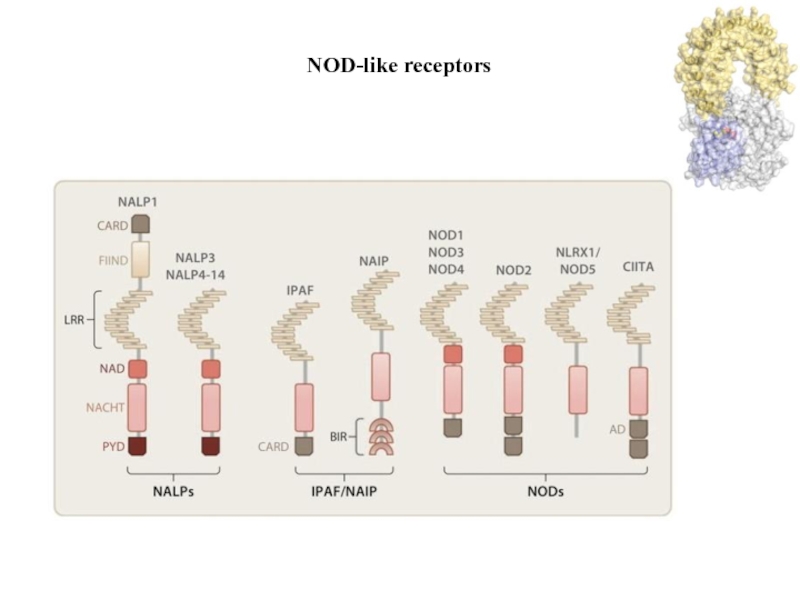
- 16. NOD-like receptors
- 17. RIG-like receptors and cytosolic DNA sensors
- 18. MDA-5 – один из сенсоров семейства RIG-like receptors
- 19. Рецепторы-мусорщики (scavenger receptors) связывают различные вещества
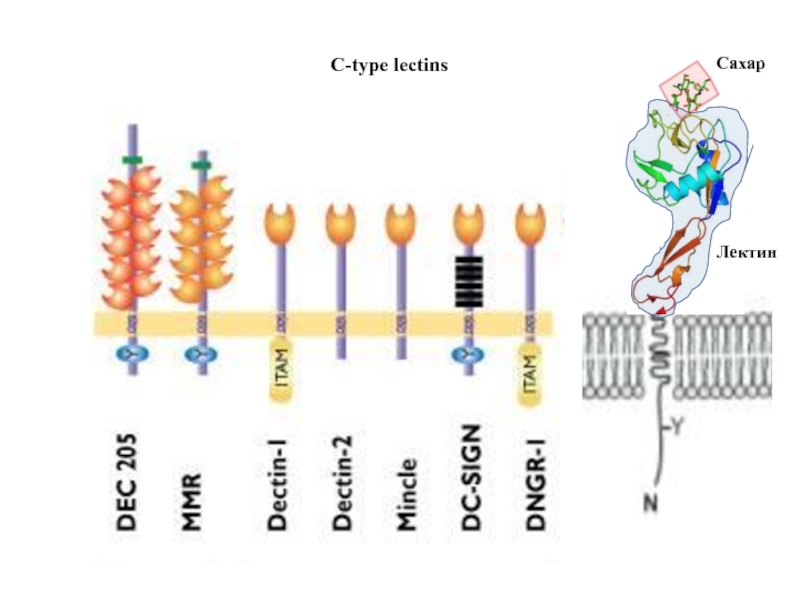
- 20. C-type lectins Лектин Сахар
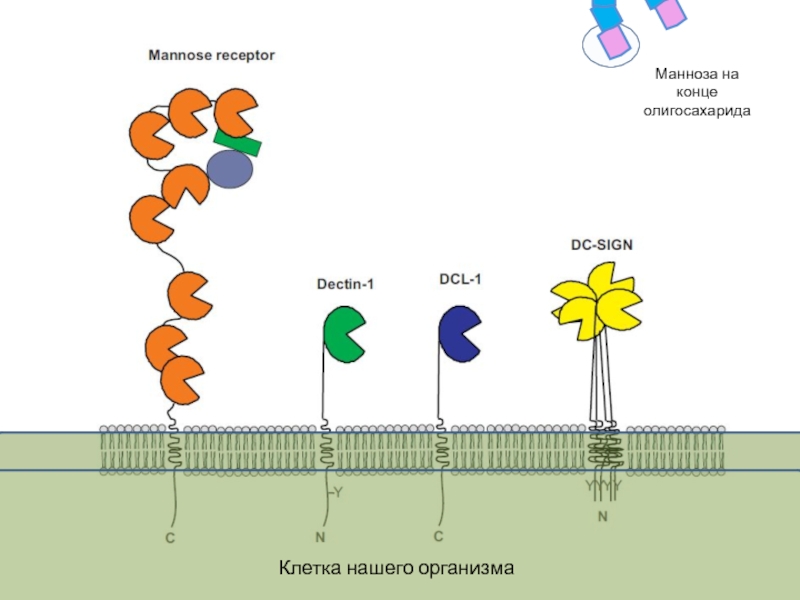
- 21. Манноза на конце олигосахарида Клетка нашего организма
- 22. Figure 1. Structural properties of MR (Mannose
- 23. Любые типы клеток нашего организма (эпителиальные, мышечные,
- 26. Дефенсины Цитокины Реакции первой линии: секреция слизи
- 27. Эндогенные антибиотики – защитные вещества белковой и
- 28. Дефенсин-α5 (красный) и лизоцим (зеленый) в слизистой
- 29. В клетках Панета в ответ на инфекцию
- 30. Содержимое гранул клеток Панета
- 31. Что делают клетки эпителия, встретившись с инфекцией? Защищаются – выделяют антимикробные вещества и слизь
- 33. Клетки рыхлой соединительной ткани (макрофаги, дендритные, тучные,
- 35. Сигналы danger - «Опасность! Готовьтесь к ее
- 36. FIGURE 2. Common transcriptional signature of macrophages
- 37. Макрофаг активируется при контакте с инфекцией (М2
- 38. В активированном фагоците происходит сборка NADPH-оксидазы Везикулы
- 39. Анти-микробные вещества, которые синтезируют фагоциты Супероксид-анион Синглетный кислород Гидроксил-анион OСl-анион Cl-анион Перекись водорода
- 40. Bylund, J. et al. J. Biol. Chem.
- 41. Кинетика ответа клеток на инфекцию и/или цитокины
- 42. Как реагирует макрофаг на инфекцию или
- 44. ХЕМОТАКСИС – движение клетки к источнику
- 45. Movies
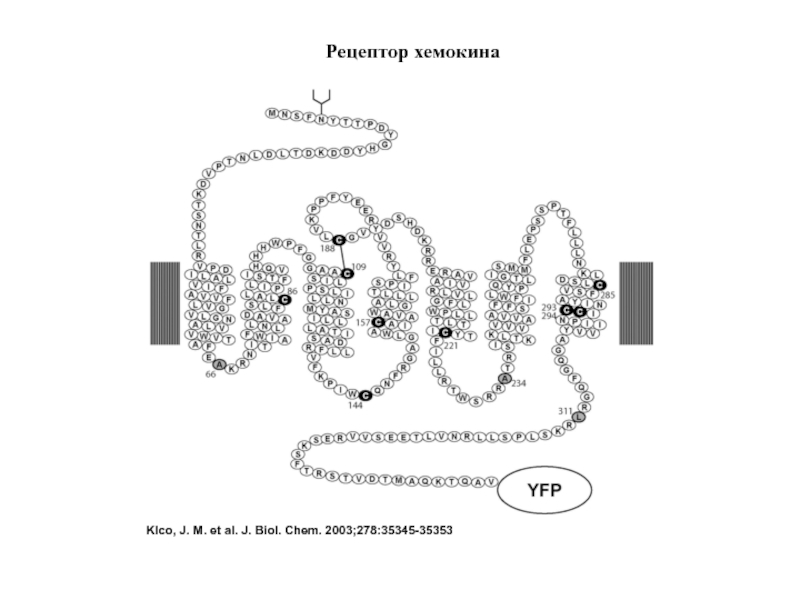
- 47. Klco, J. M. et al. J. Biol. Chem. 2003;278:35345-35353 Рецептор хемокина
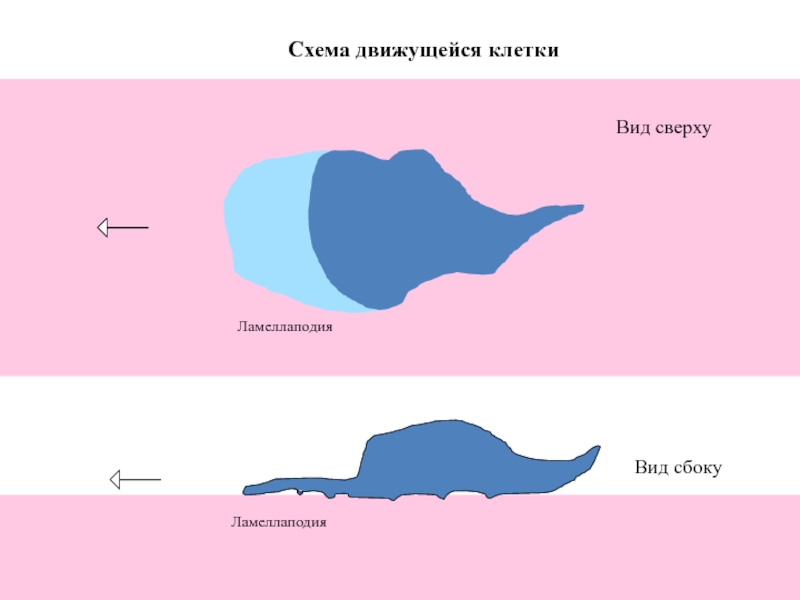
- 48. Схема движущейся клетки Ламеллаподия Вид сверху Вид сбоку Ламеллаподия
- 49. Ламеллоподия заполнена растущими актиновыми филаментами Направление движения клетки Продольный срез ламеллоподии Центральный пучок
- 50. Figure 1 Arrest of a steadily protruding
- 51. Figure 6 Hypothetical scheme of actin network
- 52. Клетка Рецептор хемокина
- 53. Филоподия выпячивается пучком актиновых филамент. Каждая актиновая
- 54. Что важно для движения клетки: Вытягивать филоподии
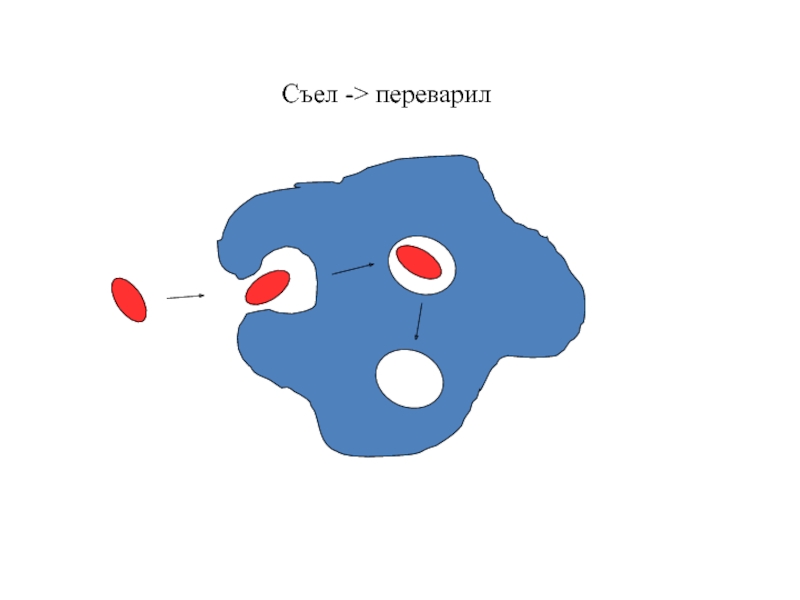
- 56. Фагоцитоз – проглотить врага, убить его и переварить
- 57. Фагоцитоз – поглощение клеткой частицы или другой
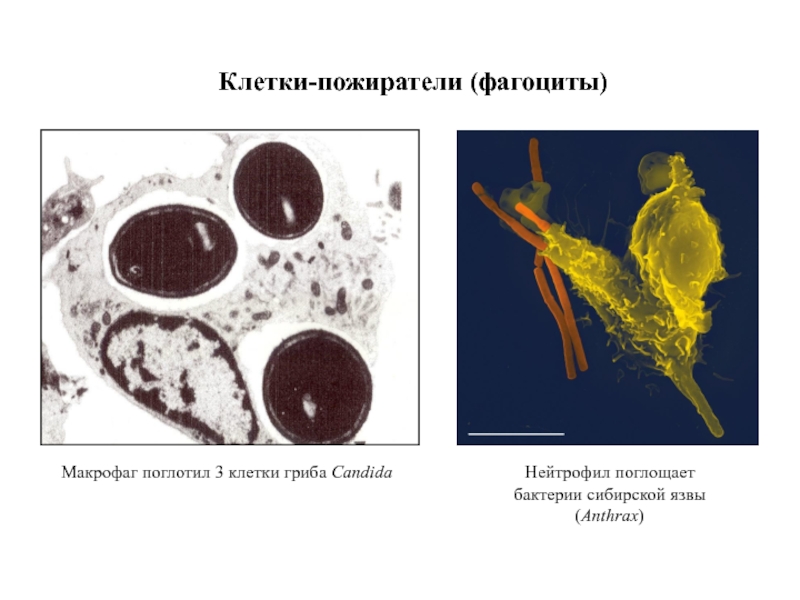
- 58. Клетки-пожиратели (фагоциты) Макрофаг поглотил 3 клетки гриба Candida Нейтрофил поглощает бактерии сибирской язвы (Anthrax)
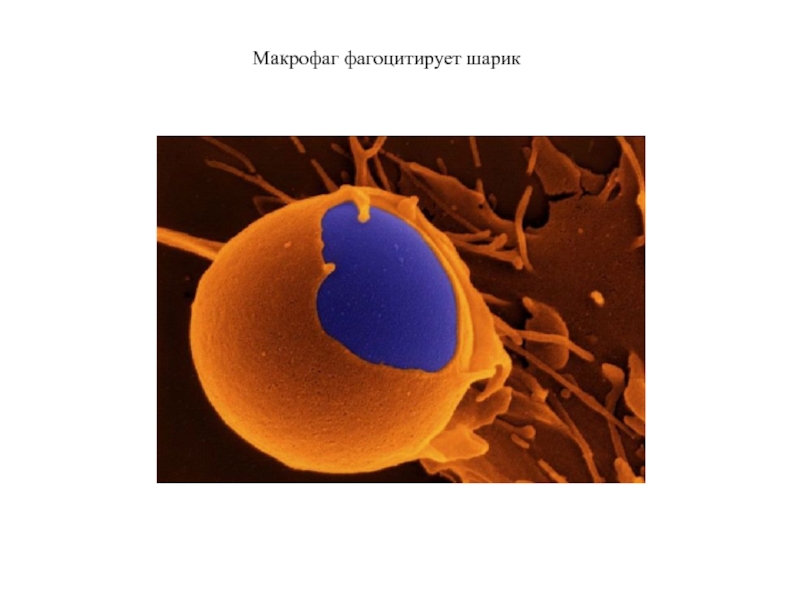
- 59. Макрофаг фагоцитирует шарик
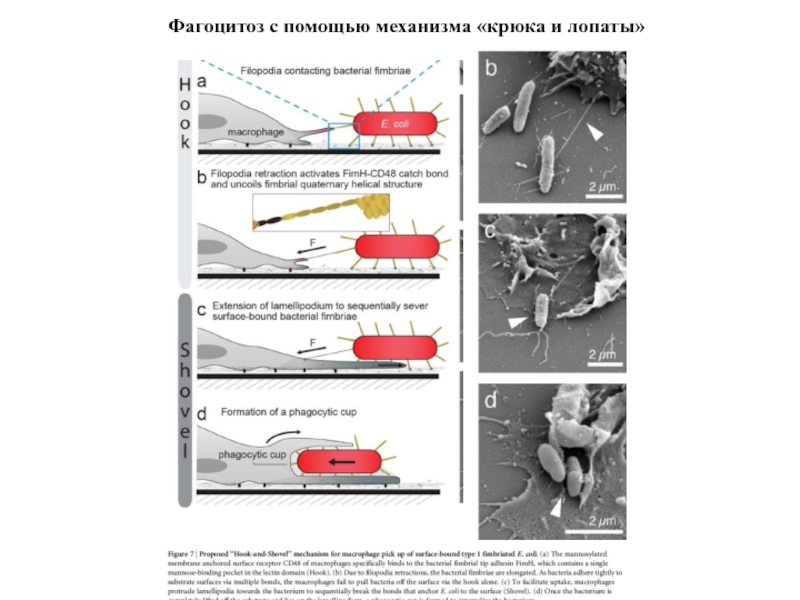
- 60. Фагоцитоз с помощью механизма «крюка и лопаты»
- 61. Phago films
- 66. Chasing bacteria movie
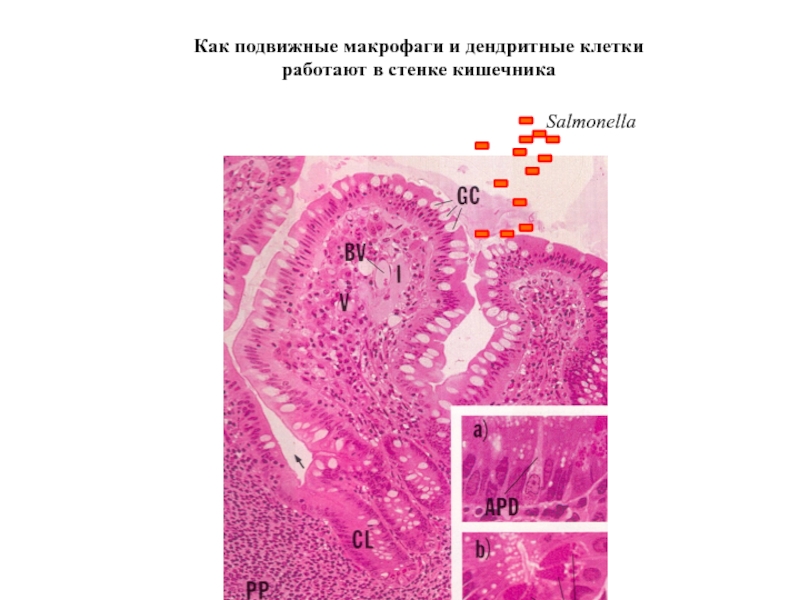
- 67. Как подвижные макрофаги и дендритные клетки работают в стенке кишечника Salmonella
- 68. Прижизненная световая микроскопия ворсинок кишечника 20 мкм
- 69. Кадр из Movie S3. Поверхность нескольких ворсинок
- 70. Стоп-кадры с интервалом 3 сек
- 71. Дендритные клетки выглядят амебоидными и активно ползают,
- 72. Через 30 минут после внесения в просвет
- 73. В ответ на инфекцию дендритные клетки накапливаются
- 74. In vitro дендритные клетки и макрофаги одинаково
- 75. Дендритные клетки и макрофаги захватывают растворимые вещества
- 76. Макрофаги и дендритные клетки эндоцитируют растворимые вещества
- 77. Волна «возбуждения» Клетки первой линии реагирования -
- 78. Почему волна активации клеток, начавшись в очаге инфекции, не распространяется по всему организму?
- 79. Должны быть «тормоза», и они есть: 1.
- 80. Оптимальный сценарий – локальный. Инфекция удалена силами
- 84. Активированные инфекцией дендритные клетки принесут в
- 85. DC облепили лимфатические капилляры (слева), DC
- 86. Чем ближе к лимфатическому капилляру, тем точнее
- 87. Хемокин CCL21 выделяется клетками эндотелия лимфатических капилляров
- 88. Гиалуроновая кислота – гигантский
- 89. Структура гликановой щеточки протеогликанов Дерматан-сульфат Хондроитин-сульфат Гепаран-сульфат
- 91. Appendix
- 92. Типы ответов клеток на инфекцию или
- 93. Макрофаг съел микроба. Кто победил?
- 94. Съел -> переварил
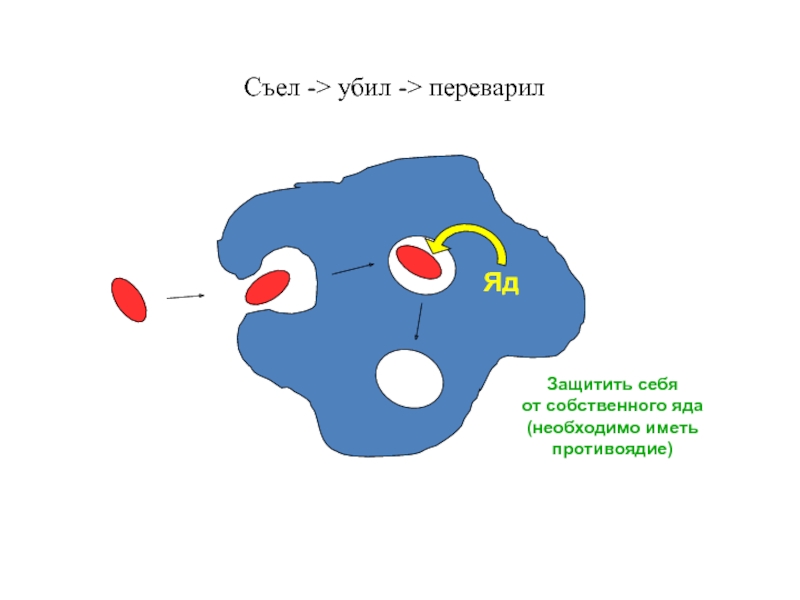
- 95. Съел -> убил
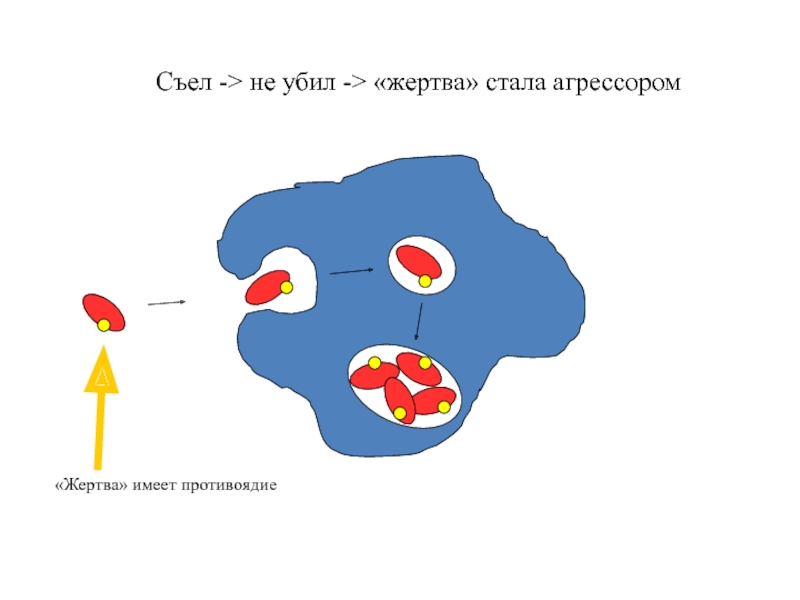
- 96. Съел -> не убил ->
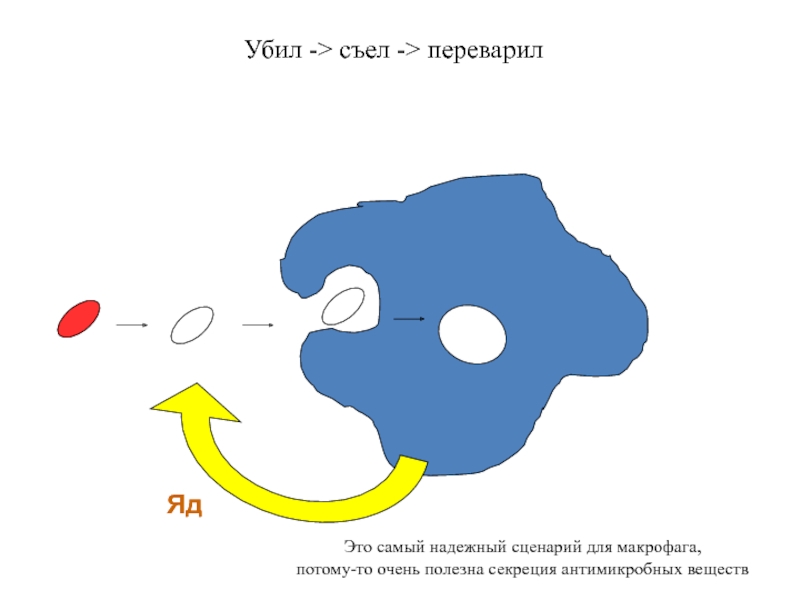
- 97. Убил -> съел ->
Слайд 2
Многоклеточное защищено от вторжения других существ
(вирусов, микробов, простейших, других многоклеточных)
Граница
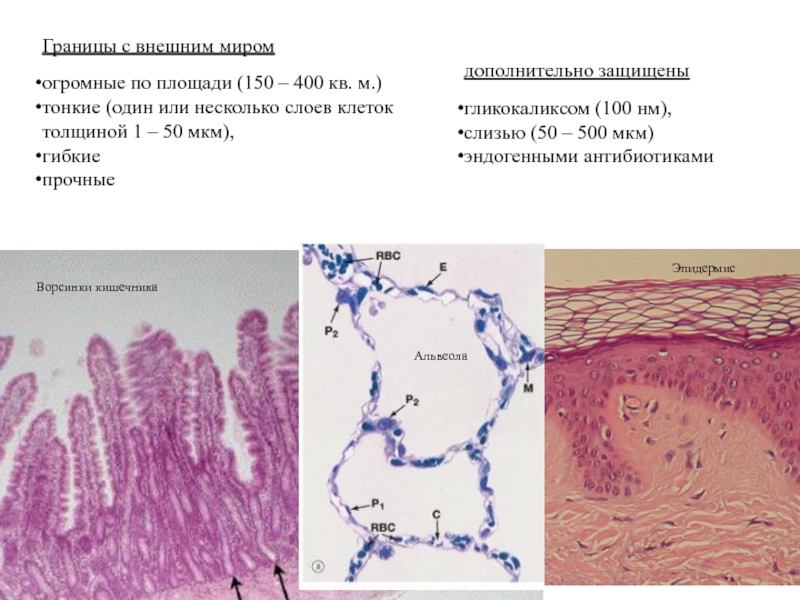
Слайд 3Ворсинки кишечника
Альвеола
Эпидермис
Границы с внешним миром
огромные по площади (150 – 400 кв.
тонкие (один или несколько слоев клеток толщиной 1 – 50 мкм),
гибкие
прочные
дополнительно защищены
гликокаликсом (100 нм),
слизью (50 – 500 мкм)
эндогенными антибиотиками
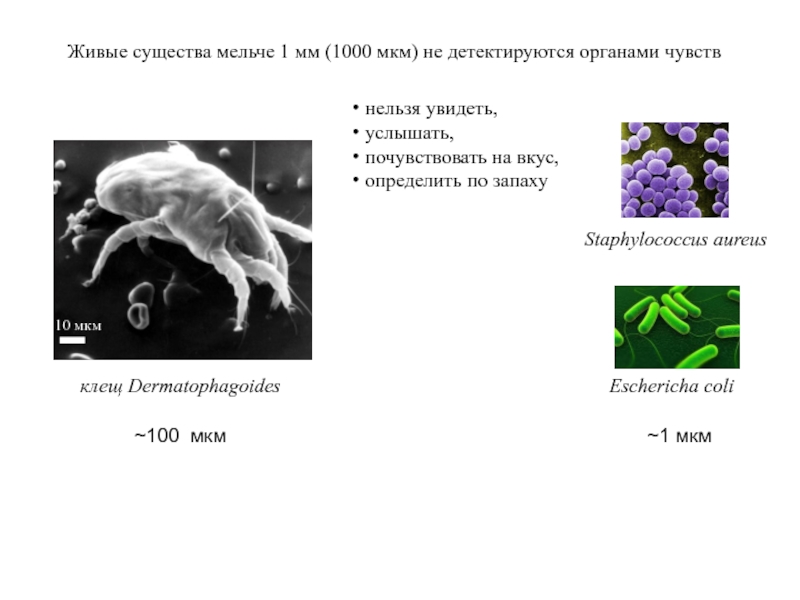
Слайд 5нельзя увидеть,
услышать,
почувствовать на вкус,
определить по запаху
Живые существа мельче 1 мм
10 мкм
Staphylococcus aureus
клещ Dermatophagoides
~100 мкм
~1 мкм
Eschericha coli
Слайд 6Клетки нашего организма снабжены молекулярными сенсорами инфекций.
Разнообразие сенсорных молекул - многие
На каждом типе клеток представлена широкая палитра сенсоров.
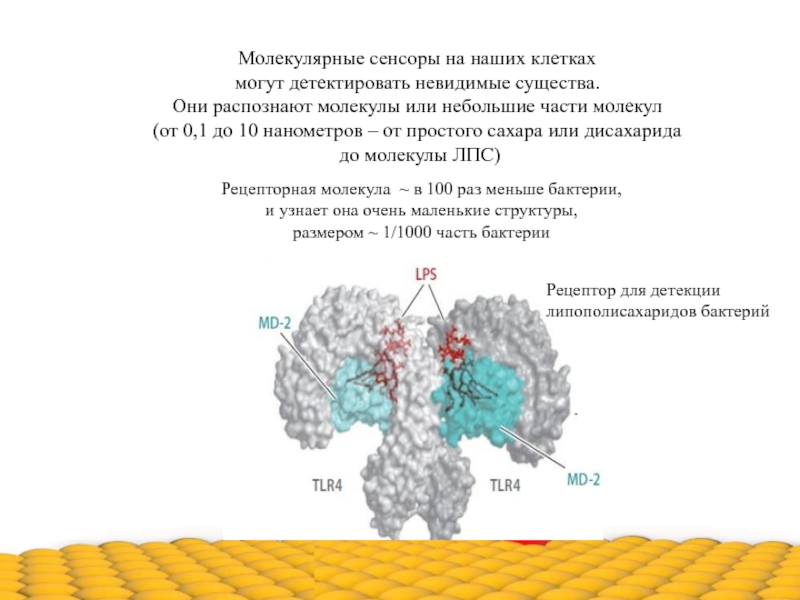
Слайд 7Молекулярные сенсоры на наших клетках
могут детектировать невидимые существа.
Они распознают
(от 0,1 до 10 нанометров – от простого сахара или дисахарида
до молекулы ЛПС)
Рецепторная молекула ~ в 100 раз меньше бактерии,
и узнает она очень маленькие структуры,
размером ~ 1/1000 часть бактерии
Слайд 8Наши клетки распознают консервативные признаки микроорганизмов,
то есть такие молекулярные свойства, которые
царствам микроорганизмов.
Например:
общие свойства всех бактерий,
общие свойства всех Грам-отрицательных бактерий
общие свойства всех Грам-положительных бактерий
общие признаки РНК-содержащих вирусов
общие признаки ДНК-содержащих вирусов
Принцип распознавания консервативных (законсервированных в эволюции)
молекулярных признаков позволяет относительно небольшим количеством
рецепторов детектировать невероятно большое разнообразие бактерий,
грибов, вирусов и других потенциально опасных существ микромира
На всякого мудреца довольно простоты
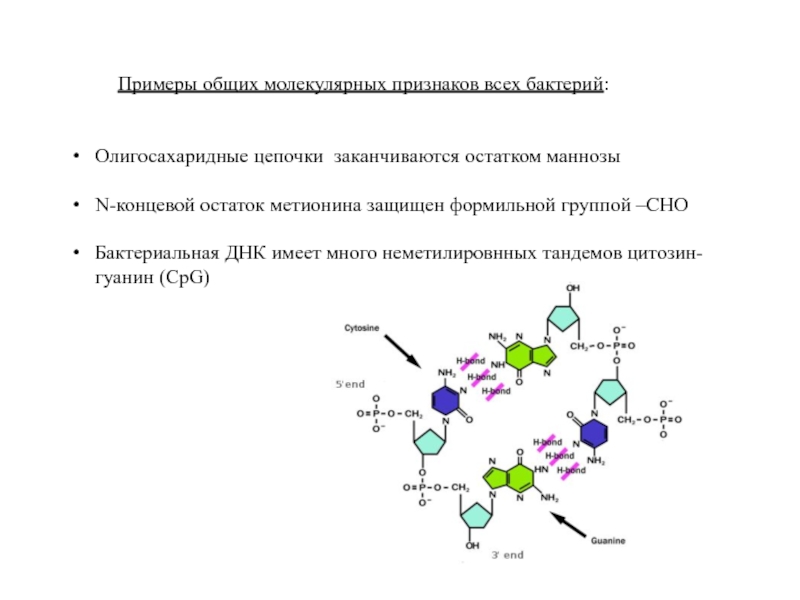
Слайд 9Примеры общих молекулярных признаков всех бактерий:
Олигосахаридные цепочки заканчиваются остатком маннозы
N-концевой остаток
Бактериальная ДНК имеет много неметилировнных тандемов цитозин-гуанин (CpG)
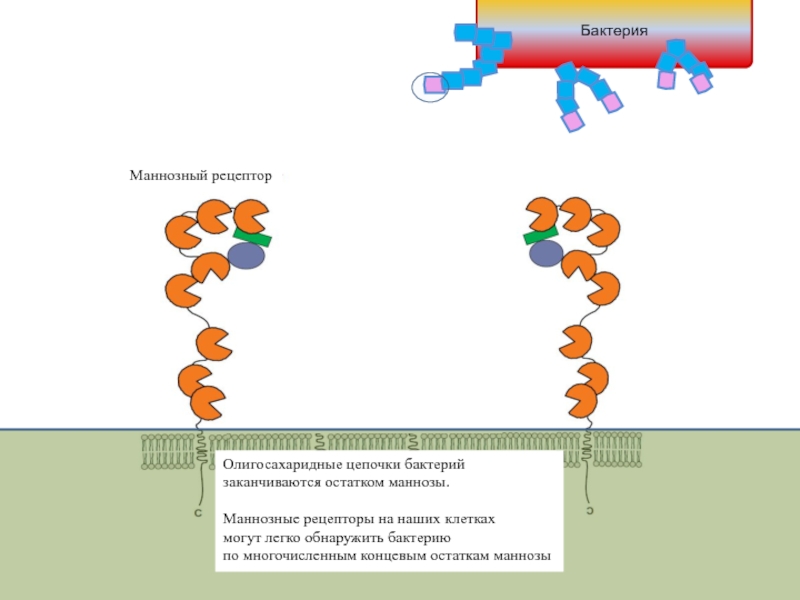
Слайд 10
Олигосахаридные цепочки бактерий
заканчиваются остатком маннозы.
Маннозные рецепторы на наших клетках
могут
по многочисленным концевым остаткам маннозы
Маннозный рецептор
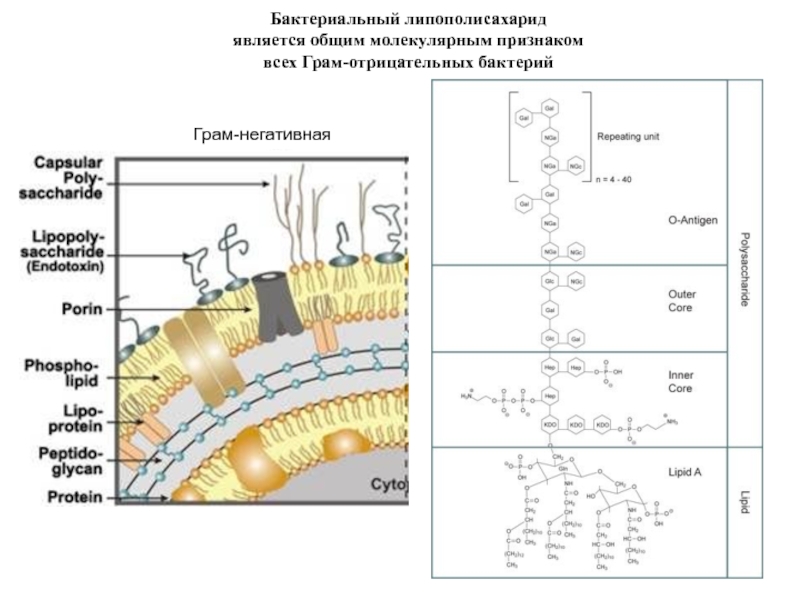
Слайд 12Бактериальный липополисахарид
является общим молекулярным признаком
всех Грам-отрицательных бактерий
Грам-негативная
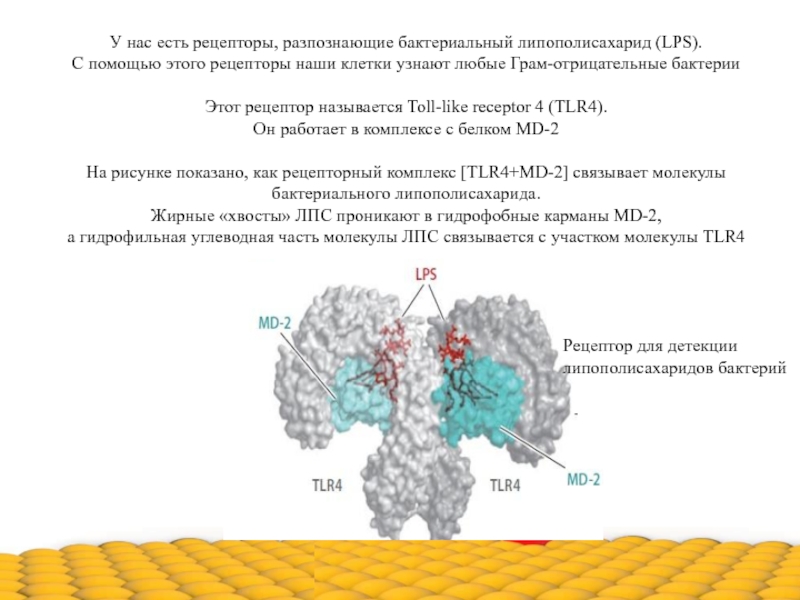
Слайд 13У нас есть рецепторы, разпознающие бактериальный липополисахарид (LPS).
С помощью этого рецепторы
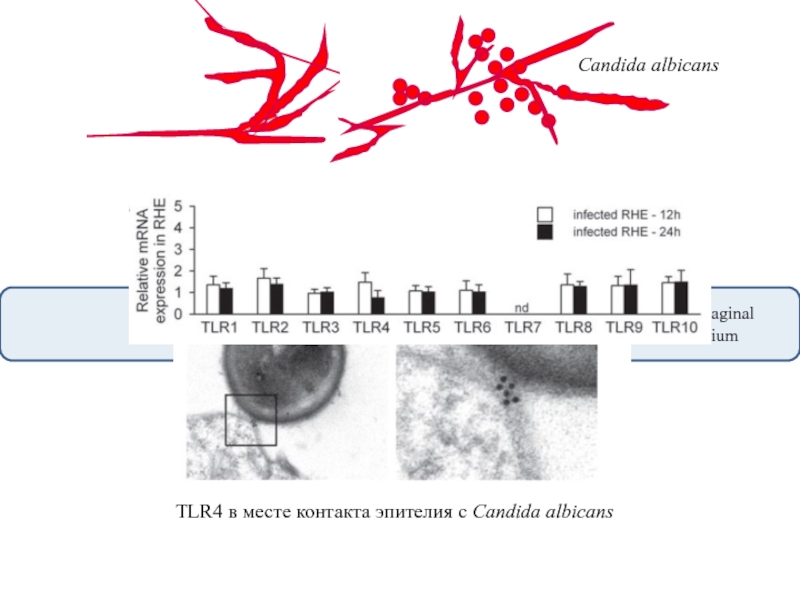
Этот рецептор называется Toll-like receptor 4 (TLR4).
Он работает в комплексе с белком MD-2
На рисунке показано, как рецепторный комплекс [TLR4+MD-2] связывает молекулы бактериального липополисахарида.
Жирные «хвосты» ЛПС проникают в гидрофобные карманы MD-2,
а гидрофильная углеводная часть молекулы ЛПС связывается с участком молекулы TLR4
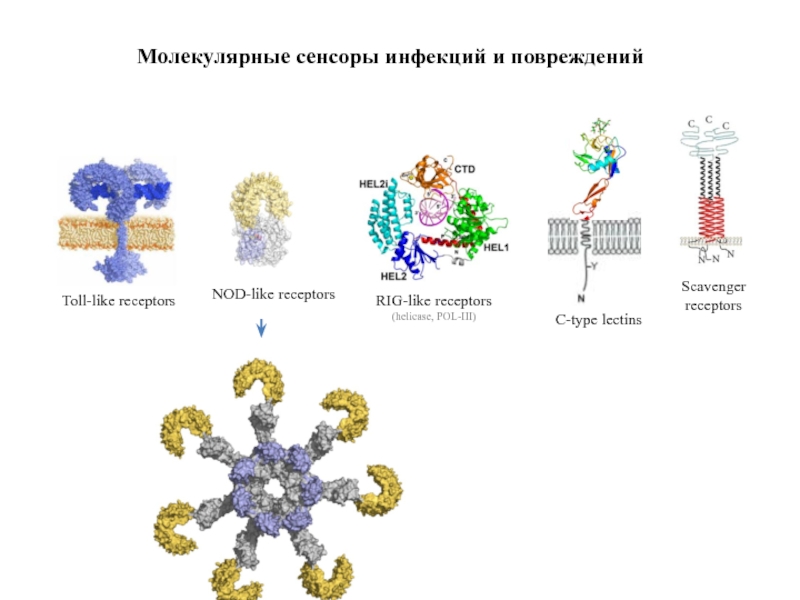
Слайд 14Молекулярные сенсоры инфекций и повреждений
Toll-like receptors
NOD-like receptors
RIG-like receptors
(helicase, POL-III)
C-type lectins
Scavenger
receptors
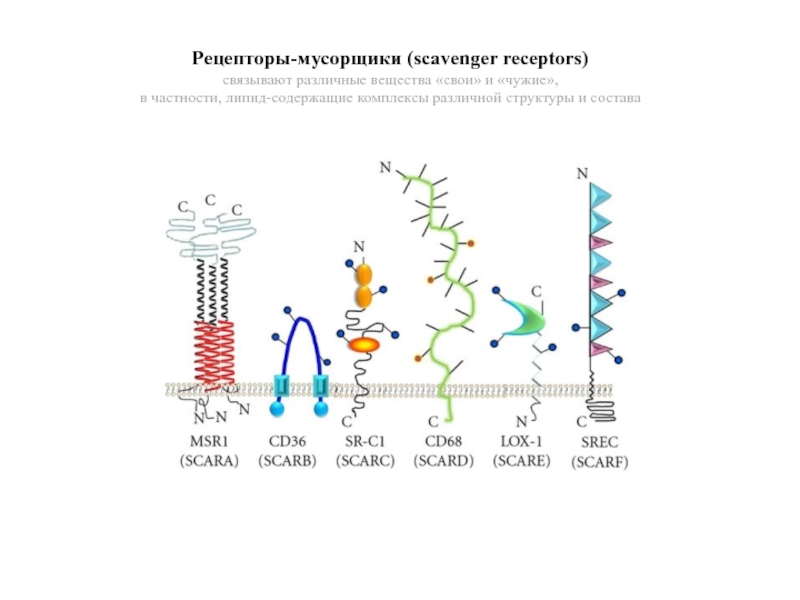
Слайд 19Рецепторы-мусорщики (scavenger receptors)
связывают различные вещества «свои» и «чужие»,
в частности, липид-содержащие
Слайд 22Figure 1. Structural properties of MR (Mannose Receptor).
MR is a type
Коды рецептор-лиганд, как правило, сильно вырожденные
(каждый рецептор связывает не один лиганд)
Вот что может связывать маннозный рецептор:
Патогены:
Вирусы: ВИЧ, Денге вирус, вирус гепатита B
Грибы: Candida albicans, Pneumocystis carinii
Бактерии: Mycobacterium tuberculosis, Klebsiella pneumoniae (LPS),
Streptococcus pneumoniae (капсульный полисахарид)
Гельминты: Schistosoma mansoni (soluble egg antigens),
Trichurus muris (secretory proteins)
Эндогенные лиганды:
лизосомальные гидролазы, миелопероксидаза,
тканевой активатор плазминогена, металлопротеиназа Adam-13,
ростовой фактор гепатоцитов, тироглобулин
Коллагены I, II, III, IV >>>> V типов
Слайд 23Любые типы клеток нашего организма (эпителиальные, мышечные,
нервные, лейкоциты и др.)
инфекцию.
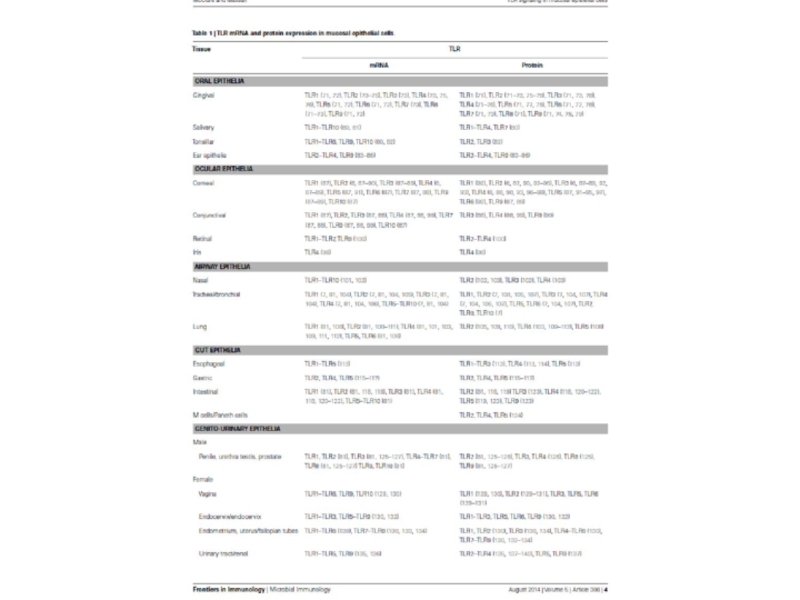
В качестве примера на следующем слайде дана таблица
наличия Toll-like рецепторов на разных эпителиях.
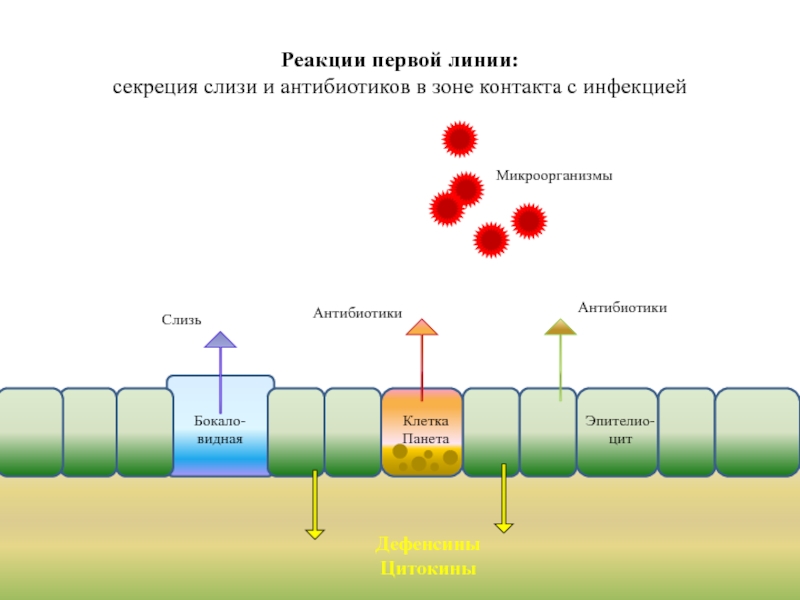
Слайд 26Дефенсины
Цитокины
Реакции первой линии:
секреция слизи и антибиотиков в зоне контакта с инфекцией
Микроорганизмы
Слизь
Антибиотики
Антибиотики
Слайд 27Эндогенные антибиотики –
защитные вещества белковой и пептидной природы:
дефенсины
кателицидины
гистатины
лактоферрин
лизоцим
псориазин
дермцидин
и многие
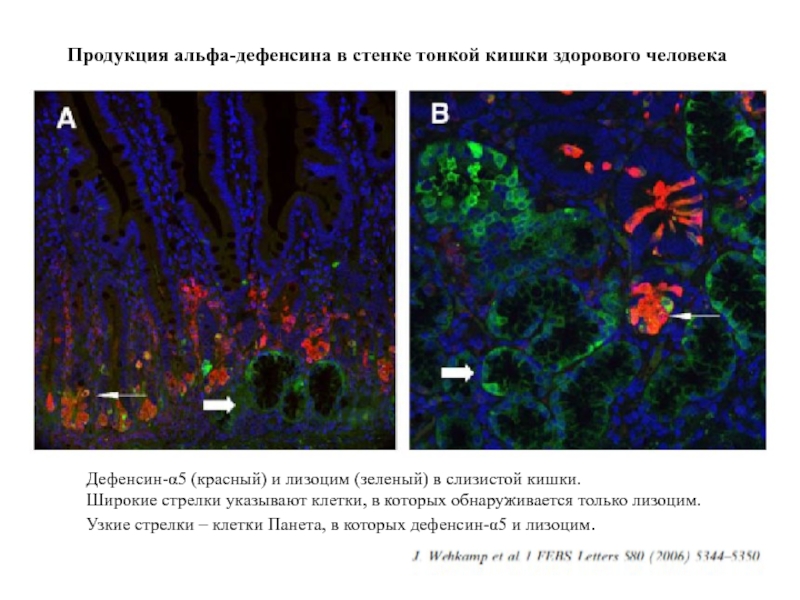
Слайд 28Дефенсин-α5 (красный) и лизоцим (зеленый) в слизистой кишки.
Широкие стрелки указывают
Узкие стрелки – клетки Панета, в которых дефенсин-α5 и лизоцим.
Продукция альфа-дефенсина в стенке тонкой кишки здорового человека
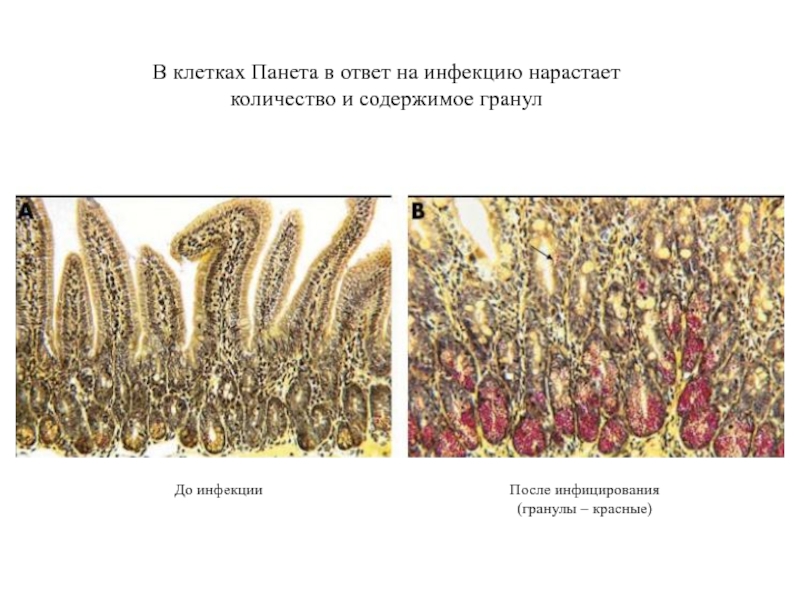
Слайд 29В клетках Панета в ответ на инфекцию нарастает
количество и содержимое гранул
До
После инфицирования
(гранулы – красные)
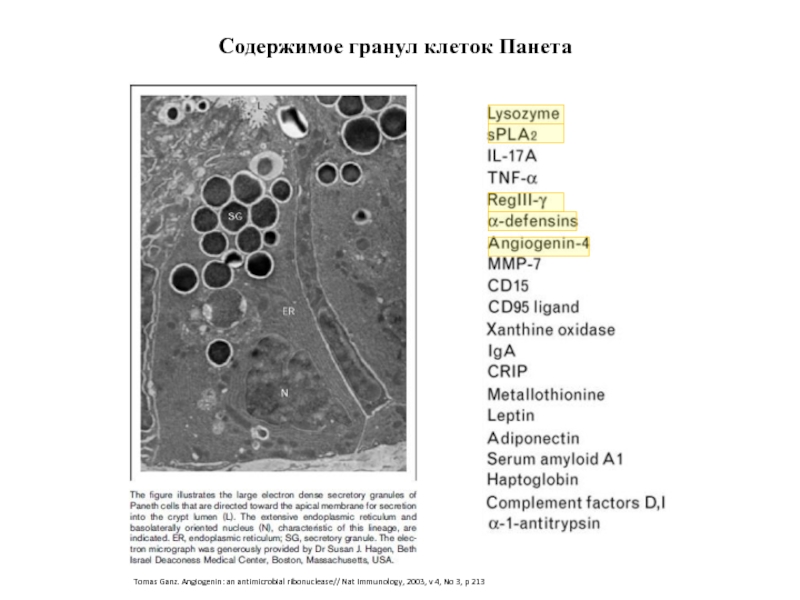
Слайд 30Содержимое гранул клеток Панета
Tomas Ganz. Angiogenin: an antimicrobial ribonuclease// Nat Immunology,
Слайд 31Что делают клетки эпителия, встретившись с инфекцией?
Защищаются – выделяют антимикробные вещества
Слайд 33Клетки рыхлой соединительной ткани (макрофаги, дендритные, тучные, фибробласты) активируются:
(а) под
(б) в результате контакта с веществами инфекционной природы
Реакции второй линии:
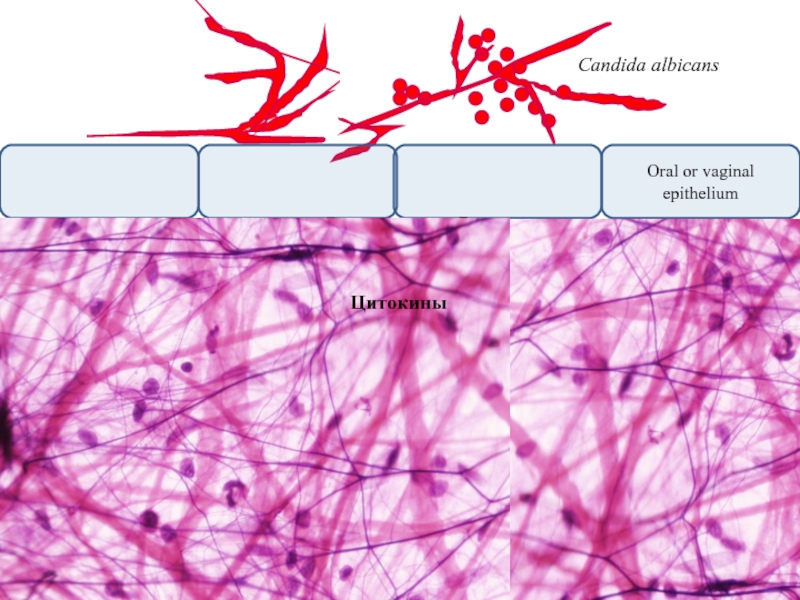
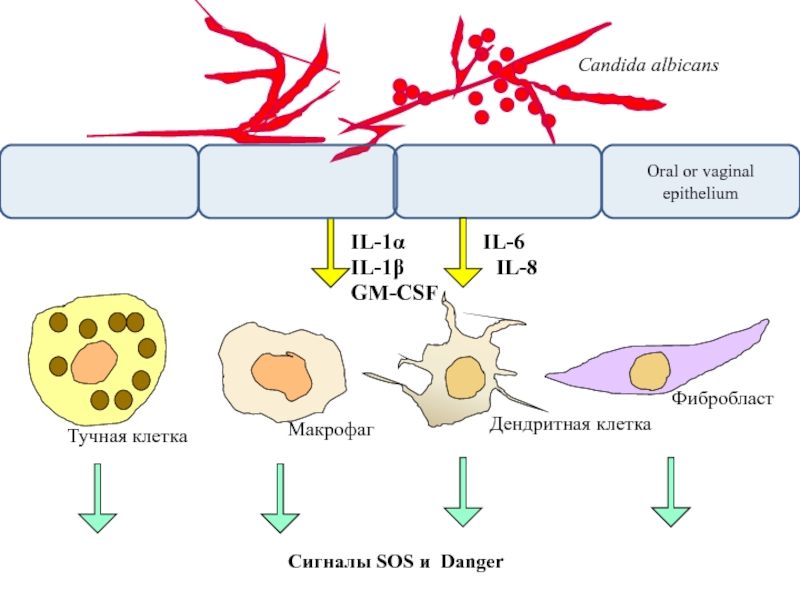
Слайд 34
Candida albicans
IL-1α
IL-1β
IL-6
IL-8
GM-CSF
Фибробласт
Макрофаг
Дендритная клетка
Тучная клетка
Сигналы SOS и Danger
Слайд 35Сигналы danger - «Опасность! Готовьтесь к ее отражению!!»
Примеры: интерфероны, heat-shock proteins
Сигналы
Примеры: все хемокины и факторы, обладающие эффектами хемокинов (дефенсин)
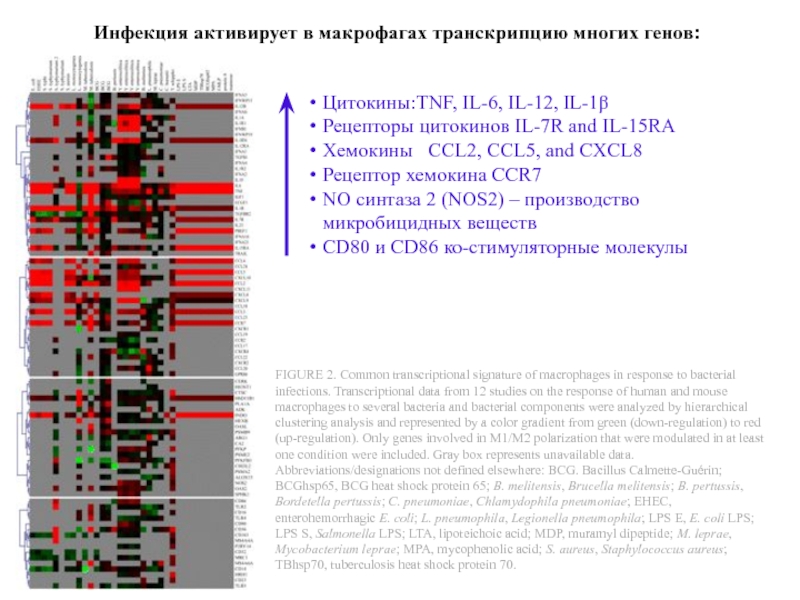
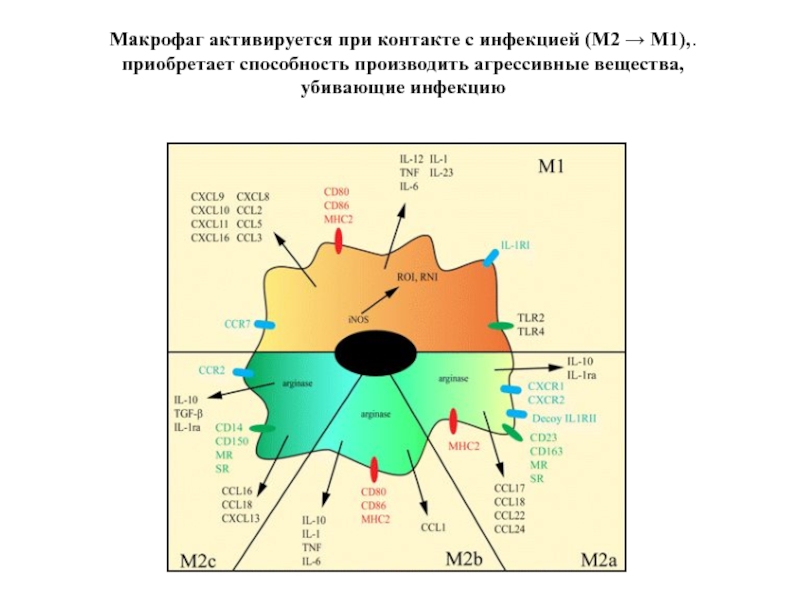
Слайд 36FIGURE 2. Common transcriptional signature of macrophages in response to bacterial
Инфекция активирует в макрофагах транскрипцию многих генов:
Цитокины:TNF, IL-6, IL-12, IL-1β
Рецепторы цитокинов IL-7R and IL-15RA
Хемокины CCL2, CCL5, and CXCL8
Рецептор хемокина CCR7
NO синтаза 2 (NOS2) – производство микробицидных веществ
CD80 и CD86 ко-стимуляторные молекулы
Слайд 37Макрофаг активируется при контакте с инфекцией (М2 → M1),.
приобретает способность производить
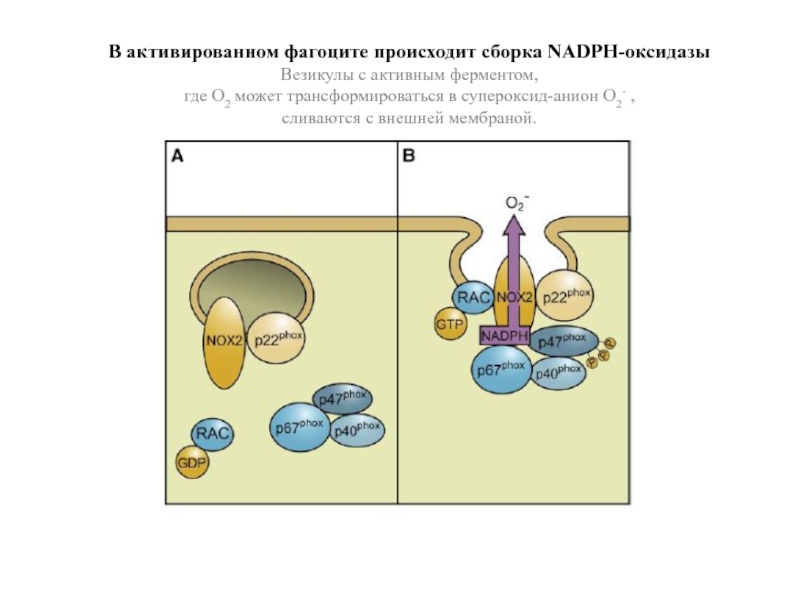
Слайд 38В активированном фагоците происходит сборка NADPH-оксидазы
Везикулы с активным ферментом,
где O2
сливаются с внешней мембраной.
Слайд 39Анти-микробные вещества, которые синтезируют фагоциты
Супероксид-анион
Синглетный кислород
Гидроксил-анион
OСl-анион
Cl-анион
Перекись водорода
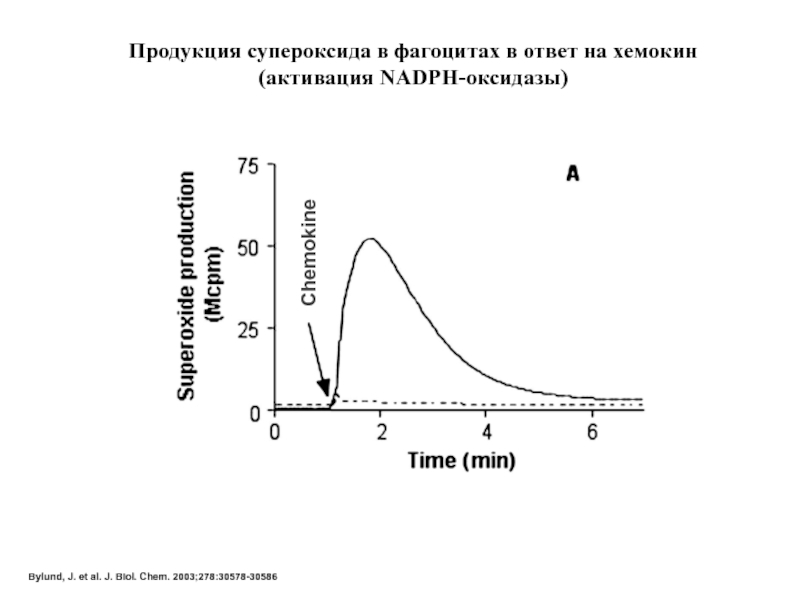
Слайд 40Bylund, J. et al. J. Biol. Chem. 2003;278:30578-30586
Продукция супероксида в фагоцитах
(активация NADPH-оксидазы)
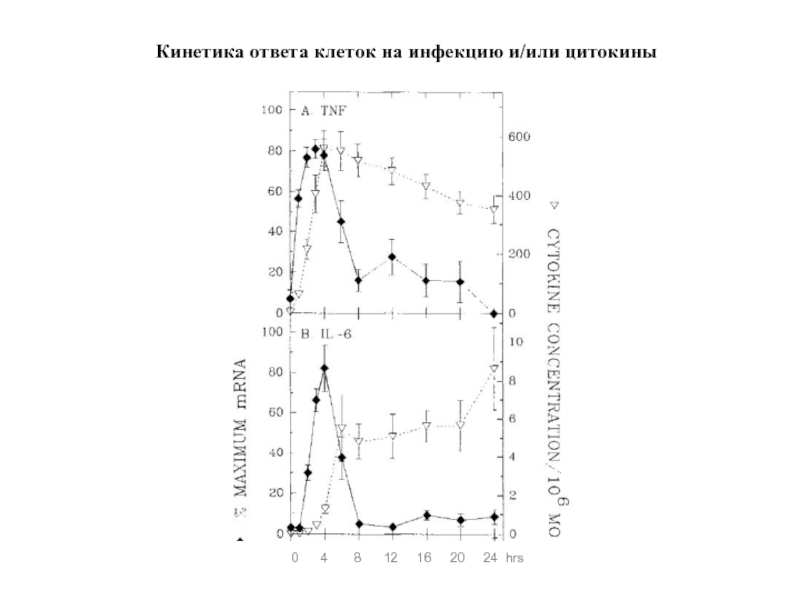
Слайд 42Как реагирует макрофаг на инфекцию
или сигналы от других клеток, встретившихся
В течение первых минут макрофаг начинает выбрасывать готовые и
синтезировать новые противомикробные вещества.
Кроме противомикробных веществ, вырабатываются сигнальные молекулы,
задача которых активировать защитные свойства соседних клеток
и привлечь в зону бедствия дополнительных бойцов
Макрофаг, реагирующий на инфекцию или сигналы других клеток,
встретивших инфекцию, сильно меняется –
в нем активируется транскрипция ~200-300 ранее молчавших генов
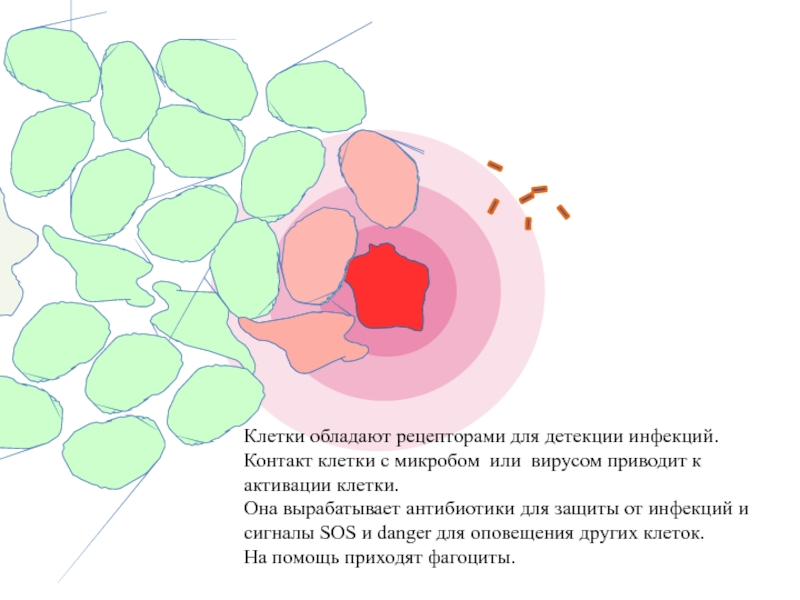
Слайд 43
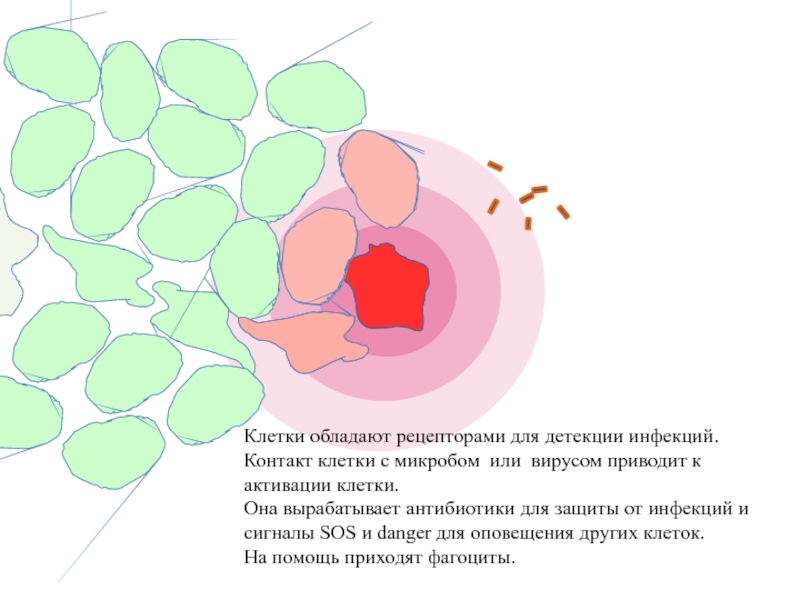
Клетки обладают рецепторами для детекции инфекций.
Контакт клетки с микробом или вирусом
Она вырабатывает антибиотики для защиты от инфекций и сигналы SOS и danger для оповещения других клеток.
На помощь приходят фагоциты.
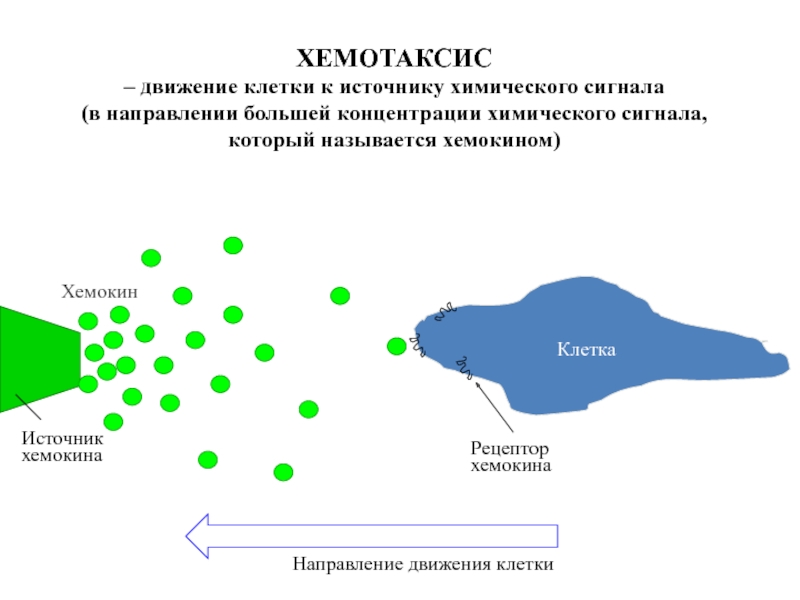
Слайд 44ХЕМОТАКСИС
– движение клетки к источнику химического сигнала
(в направлении большей концентрации
который называется хемокином)
Клетка
Рецептор
хемокина
Источник
хемокина
Направление движения клетки
Хемокин
Слайд 49Ламеллоподия заполнена растущими актиновыми филаментами
Направление движения клетки
Продольный срез ламеллоподии
Центральный пучок
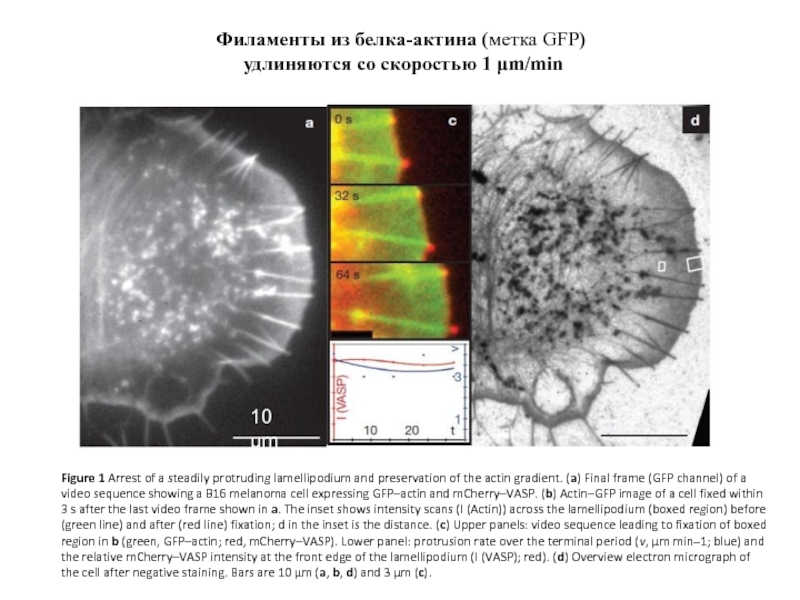
Слайд 50Figure 1 Arrest of a steadily protruding lamellipodium and preservation of
Филаменты из белка-актина (метка GFP)
удлиняются со скоростью 1 μm/min
Слайд 51Figure 6 Hypothetical scheme of actin network generation in lamellipodia. In
membrane. We suggest that WAVE, VASP and formins associate in different combinations in multimolecular complexes to regulate the balance between network and bundle formation. Possible schemes are indicated. (a) Single actin filaments are nucleated by the docking of the Arp2/3 complex onto the WAVE complex. (b) Filaments elongate, initially tethered via the WAVE WH2 domain, with the Arp2/3 complex on the filament minus end. (c) VASP molecules associated with the WAVE complex take over the role of filament elongation (as oligomers) through common binding partners, releasing WAVE
for further nucleation events. (d) Some growing actin plus ends tethered by VASP oligomers and associated proteins come together by lateral flow in the membrane and (e) initiate the formation of a filament pair through recruitment of an actin-bundling protein (X-linker). (f) Filament pairs could also be nucleated and elongated directly by formins (a doublet making up one ring) in combination with a bundling protein. Finally, long cross-linking proteins (such as filamin and α‑actinin) stabilize the network by forming filament interconnections (not shown). For clarity, the filament density in the scheme is lower than in the real cell.
NATURE CELL BIOLOGY, Vol 12 | NUMBER 5 | MAY 2010
Как актиновые филаменты вытягиваются внутри ламеллоподии на переднем фронте движущейся клетки
Слайд 52Клетка
Рецептор
хемокина
G-protein
PI3-kinase
PI3-P
GEF
Rac
Arp2/3
Хемокин
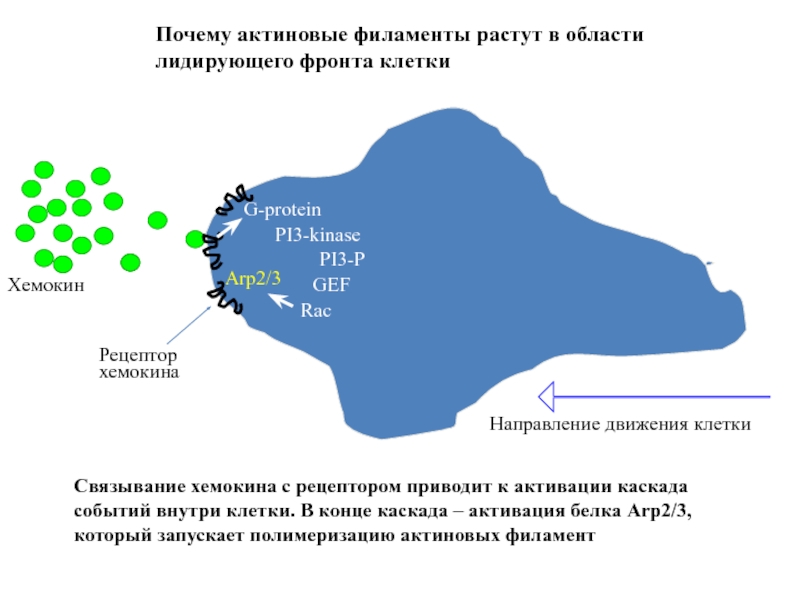
Связывание хемокина с рецептором приводит к активации каскада событий внутри
Почему актиновые филаменты растут в области
лидирующего фронта клетки
Направление движения клетки
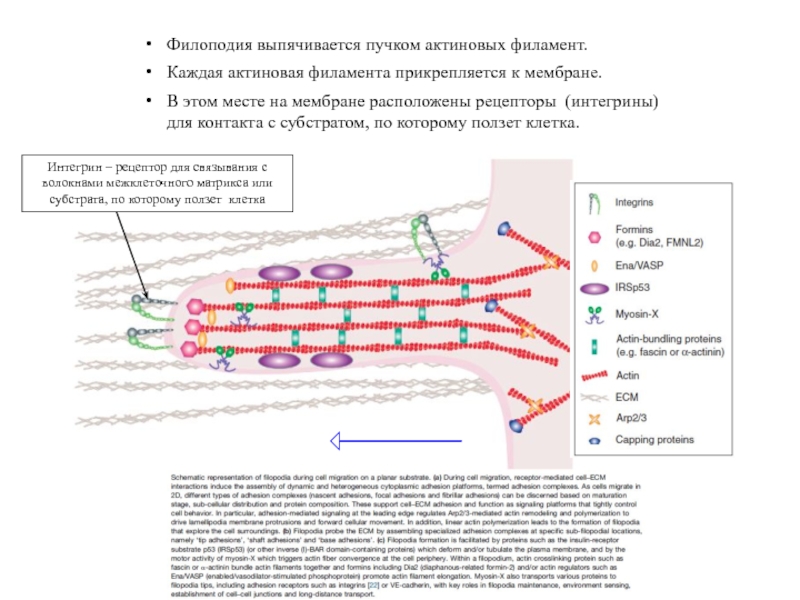
Слайд 53Филоподия выпячивается пучком актиновых филамент.
Каждая актиновая филамента прикрепляется к мембране.
В этом
Интегрин – рецептор для связывания с волокнами межклеточного матрикса или субстрата, по которому ползет клетка
Слайд 54Что важно для движения клетки:
Вытягивать филоподии
Закрепиться вытянутой филоподией за субстрат
Из
Подтянуть тело клетки
Вектор движения задается химическими сигналами хемотаксиса
(хемокины, молекулы инфекционной природы) . Без вектора движение клетки будет беспорядочным.
Слайд 55
Клетки обладают рецепторами для детекции инфекций.
Контакт клетки с микробом или вирусом
Она вырабатывает антибиотики для защиты от инфекций и сигналы SOS и danger для оповещения других клеток.
На помощь приходят фагоциты.
Слайд 57Фагоцитоз – поглощение клеткой частицы или другой клетки
Recently at the Medical
William Osler,
канадский врач и исследователь,
описал захват частиц угля
клетками легкого в 1876 г
The Osler slide, a demonstration of phagocytosis from 1876: Reports of phagocytosis before Metchnikoff’s 1880 paper.// Cellular Immunology, 2006, v 240, issue 1, p 1-4
Илья Ильич Мечников
Явление фагоцитоза было открыто William Osler. Несколькими годами позже И.И.Мечников обнаружил этот процесс в опытах с морскими звездами и дафниями, вводя в их организмы инородные тела.
Когда Мечников поместил в тело дафнии спору грибка, он заметил, что на нее нападают особые подвижные клетки. Когда он ввел слишком много спор, клетки не успели поглотить все споры, и животное погибло. Клетки, защищавшие организм от спор, бактерий и грибов, Мечников назвал фагоцитами.
Слайд 58
Клетки-пожиратели (фагоциты)
Макрофаг поглотил 3 клетки гриба Candida
Нейтрофил поглощает бактерии сибирской язвы
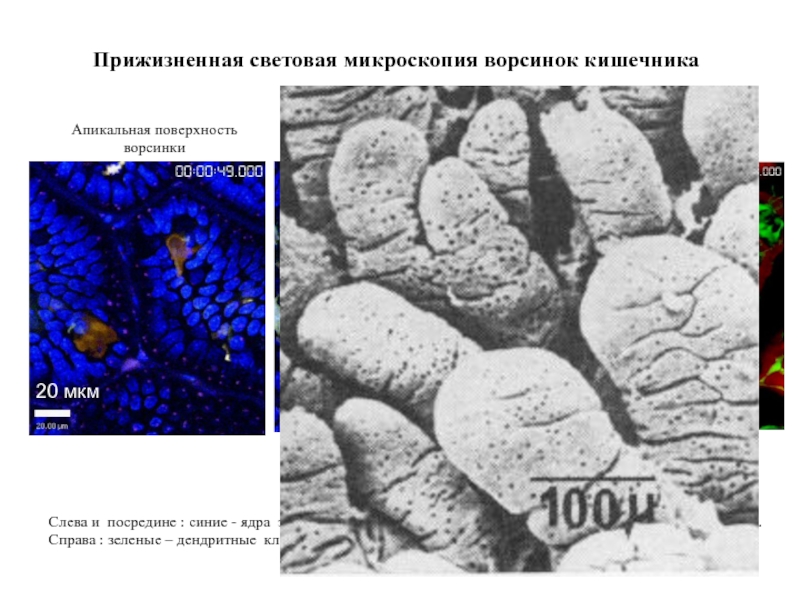
Слайд 68Прижизненная световая микроскопия ворсинок кишечника
20 мкм
20 мкм
50 мкм
Слева и посредине :
Справа : зеленые – дендритные клетки, красные – кровяные капилляры.
Чуть глубже, 10-20 мкм
Апикальная поверхность
ворсинки
Еще глубже, 30-40 мкм
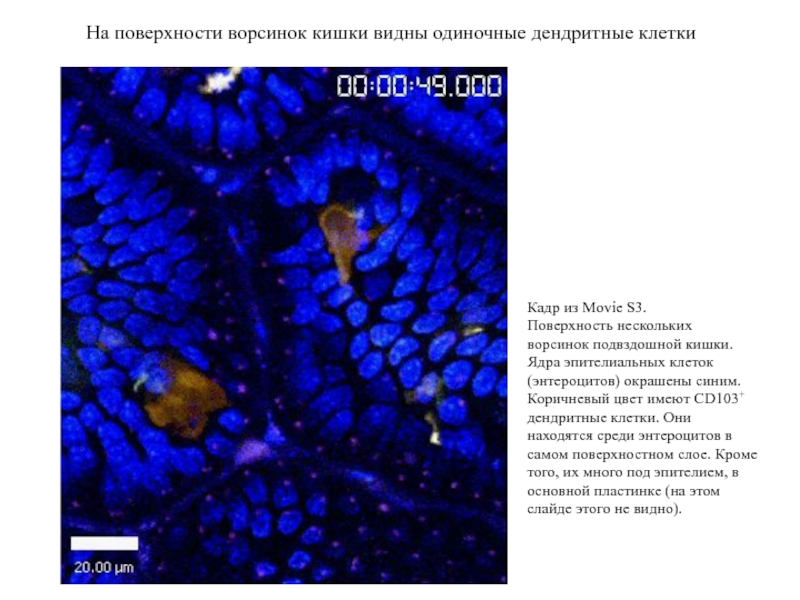
Слайд 69Кадр из Movie S3.
Поверхность нескольких ворсинок подвздошной кишки.
Ядра эпителиальных клеток
На поверхности ворсинок кишки видны одиночные дендритные клетки
Слайд 70
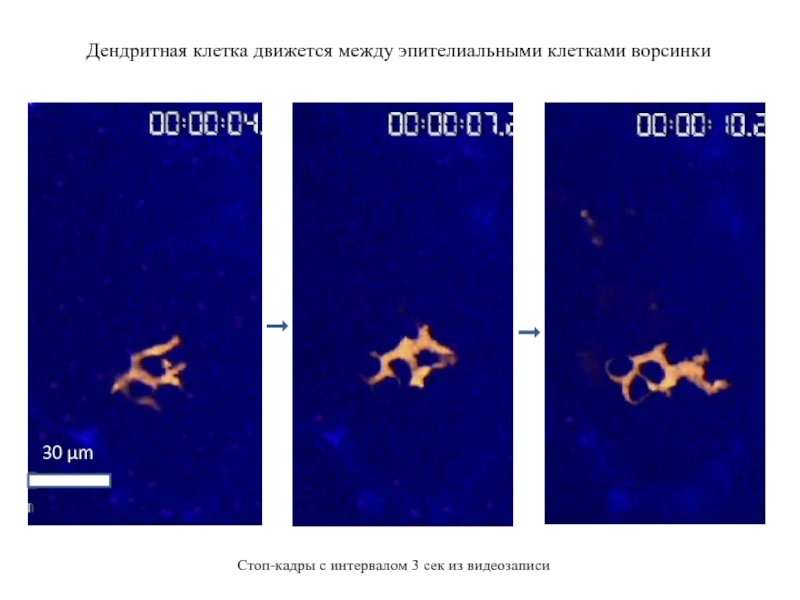
Стоп-кадры с интервалом 3 сек из видеозаписи
Дендритная клетка движется между эпителиальными
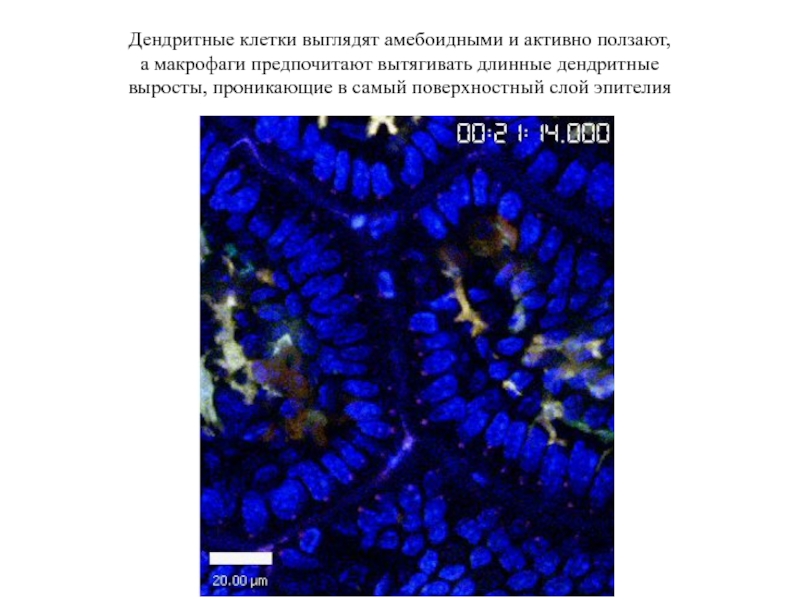
Слайд 71Дендритные клетки выглядят амебоидными и активно ползают,
а макрофаги предпочитают вытягивать
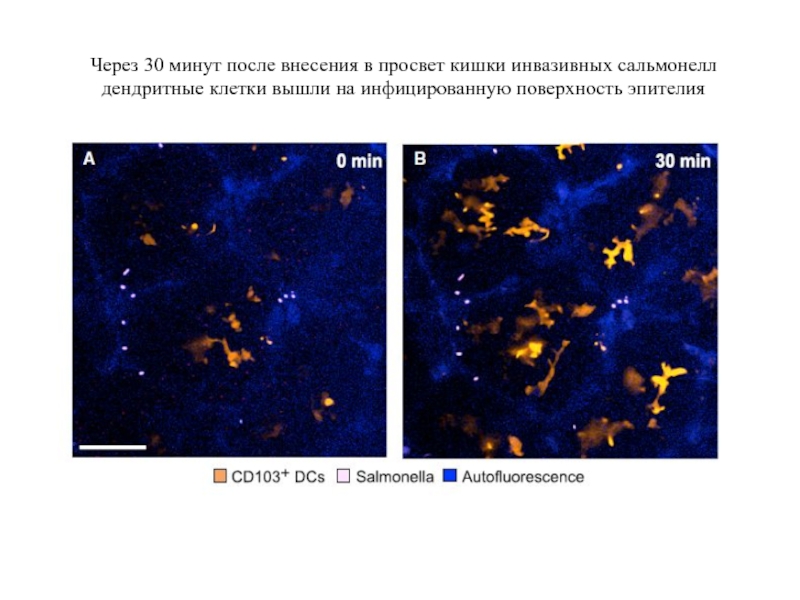
Слайд 72Через 30 минут после внесения в просвет кишки инвазивных сальмонелл
дендритные клетки
Слайд 73В ответ на инфекцию дендритные клетки накапливаются
в поверхностном слое эпителия
Обозначения:
Epithelium –
LP (lamina propria ) ткань под эпителием, внутренняя ткань ворсинки,
где обитает большое количество макрофагов и дендритных клеток
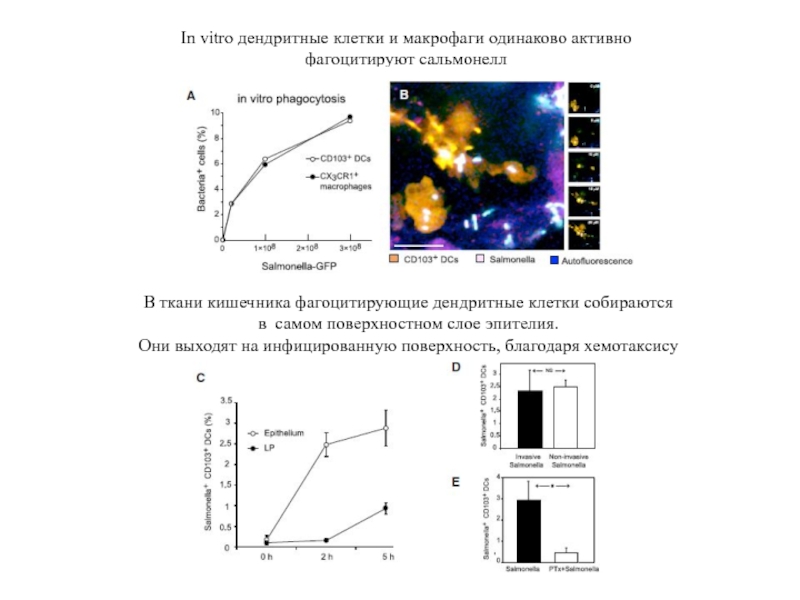
Слайд 74In vitro дендритные клетки и макрофаги одинаково активно фагоцитируют сальмонелл
В ткани
в самом поверхностном слое эпителия.
Они выходят на инфицированную поверхность, благодаря хемотаксису
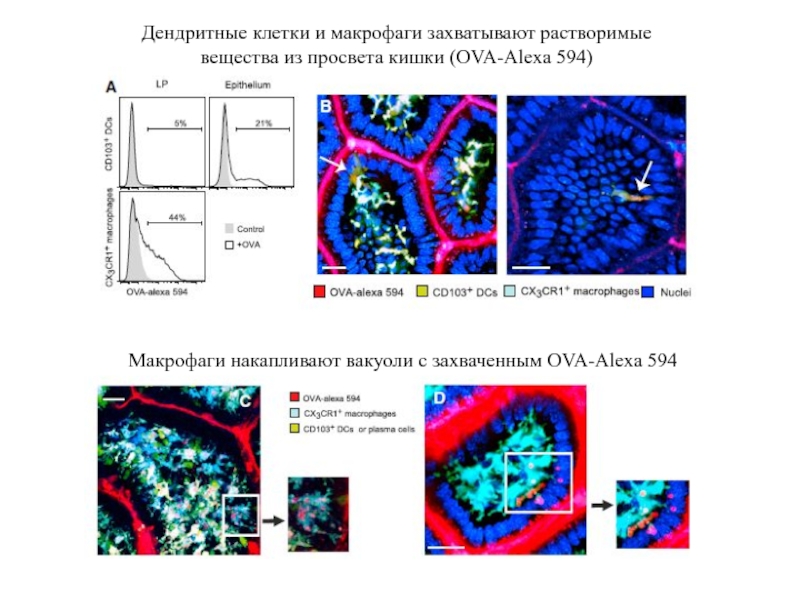
Слайд 75Дендритные клетки и макрофаги захватывают растворимые вещества из просвета кишки (OVA-Alexa
Макрофаги накапливают вакуоли с захваченным OVA-Alexa 594
Слайд 76Макрофаги и дендритные клетки эндоцитируют растворимые вещества и
фагоцитируют микробные клетки
Дендритные клетки
Слайд 77Волна «возбуждения»
Клетки первой линии реагирования - эпителий
Клетки второй линии реагирования –
Клетки третьей линии реагирования – новые макрофаги (хемотаксис), эндотелий сосудов и др.
Что дальше?
Если активация распространится на все клетки организма, то наступит смерть!
Слайд 78Почему волна активации клеток, начавшись в очаге инфекции,
не распространяется по
Слайд 79Должны быть «тормоза»,
и они есть:
1. Вслед за активаторами производятся ингибиторы
2. Рецепторы
3. После активации клетка вступает в фазу ареактивности
(например, эпигенетические изменения закрывают транскрипцию)
4. Активируются специальные «тормозные» типы клеток (супрессоры) или цитокины (SOCS и др.).
Слайд 80Оптимальный сценарий – локальный. Инфекция удалена силами пограничников.
Это происходит несметное
Не очень благоприятный сценарий – генерализованный. Пограничники не справились даже с помощью дополнительных приграничных сил (хемотаксис).
Для удаления инфекции придется прибегнуть к помощи всего организма
(это - болезнь).
Защита по этому сценарию будет рассматриваться в следующих лекциях
Рассмотрели пограничную защиту в действии
Слайд 84Активированные инфекцией дендритные клетки принесут
в лимфатический узел инфекционные антигены.
Здесь они
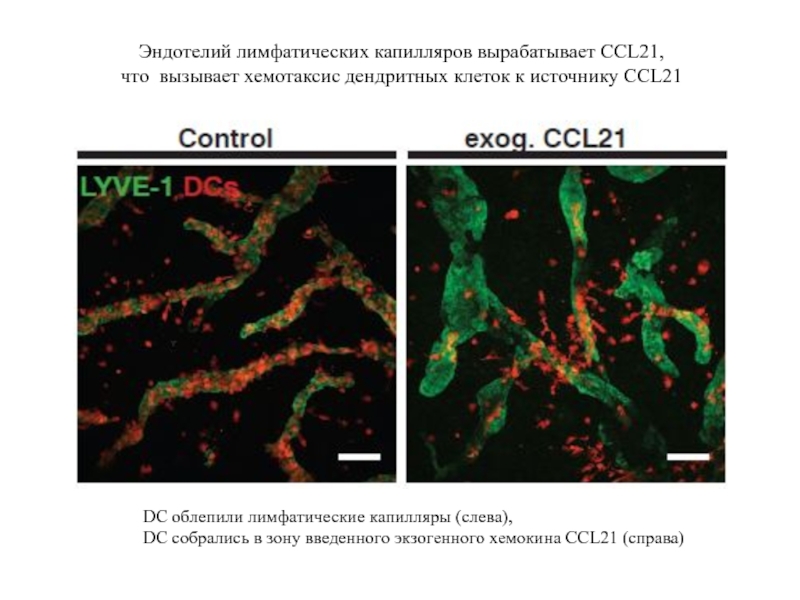
Слайд 85DC облепили лимфатические капилляры (слева),
DC собрались в зону введенного экзогенного
Эндотелий лимфатических капилляров вырабатывает CCL21,
что вызывает хемотаксис дендритных клеток к источнику CCL21
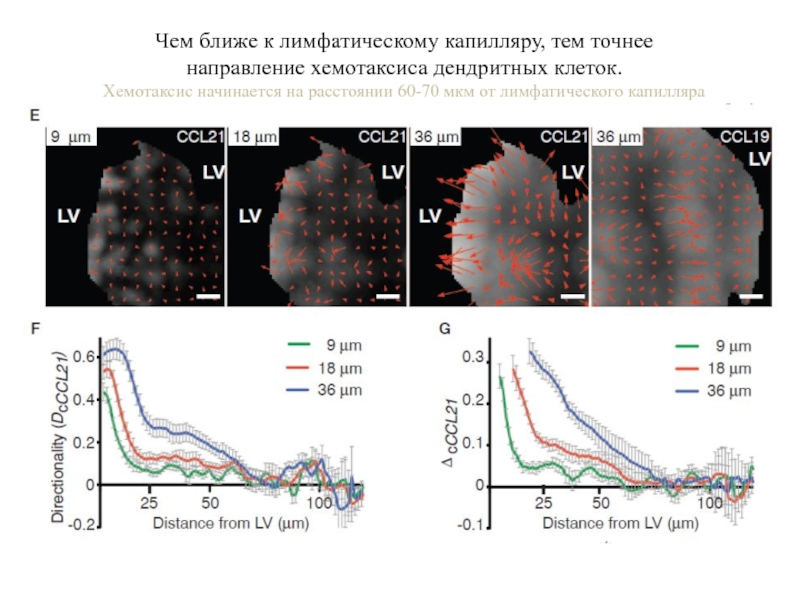
Слайд 86Чем ближе к лимфатическому капилляру, тем точнее
направление хемотаксиса дендритных клеток.
Хемотаксис начинается на расстоянии 60-70 мкм от лимфатического капилляра
Слайд 87Хемокин CCL21 выделяется клетками эндотелия лимфатических капилляров и иммобилизируется на гепарансульфате
То есть градиент хемокина - в виде градиента концентрации иммобилизованного вещества
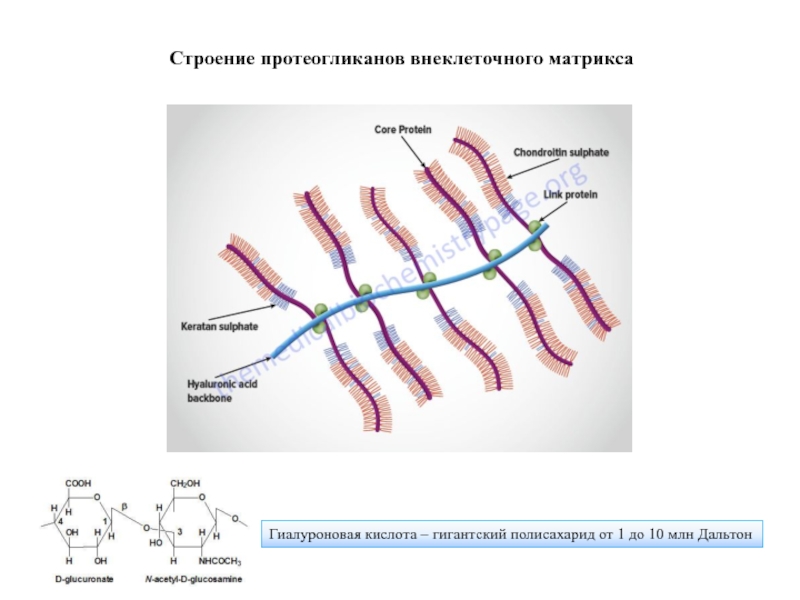
Слайд 88
Гиалуроновая кислота – гигантский полисахарид от 1 до 10 млн Дальтон
Строение
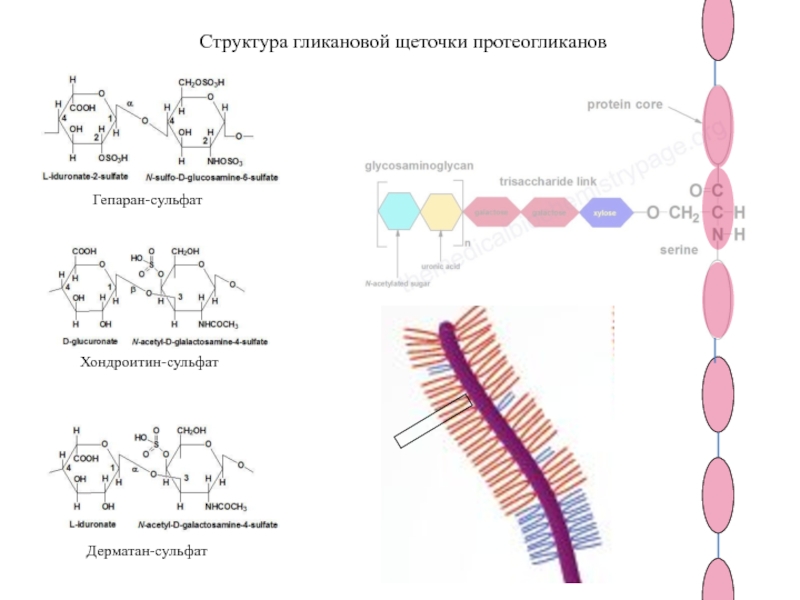
Слайд 89
Структура гликановой щеточки протеогликанов
Дерматан-сульфат
Хондроитин-сульфат
Гепаран-сульфат
Слайд 92Типы ответов клеток на инфекцию
или цитокины, индуцированные инфекцией:
Активация транскрипции
Изменение трансляции
Пост-трансляционные
Секреция
Экспрессия мембранных молекул
Деление клетки
Движение клетки
Изменение формы и адгезионных свойств клетки