М
Алашбеков Ж
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Цитокины, основные характеристики, роль в регуляции иммунного ответа презентация
Содержание
- 1. Цитокины, основные характеристики, роль в регуляции иммунного ответа
- 2. ЦИТОКИНЫ В развитии иммунного
- 3. К группе цитокинов относятся: интерлейкины – макромолекулы,
- 4. К цитокинам относят интерфероны, колониестимулирующие факторы (КСФ),
- 5. КЛАССИФИКАЦИЯ ЦИТОКИНОВ ПО СТРОЕНИЮ.
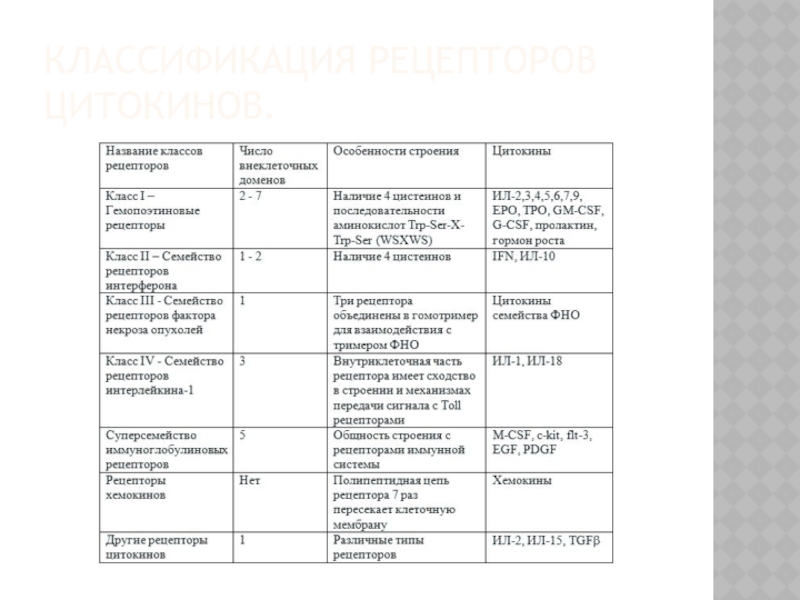
- 6. КЛАССИФИКАЦИЯ РЕЦЕПТОРОВ ЦИТОКИНОВ.
- 7. ИНТЕРЛЕЙКИНЫ (ИЛ) цитокины, ответственные за межклеточные взаимодействия между лейкоцитами Описано ок. 20 интерлейкинов.
- 8. ИЛ 1 Ил-1 продуцируется гл. обр. макрофагами
- 9. ИЛ 2; ИЛ 3; ИЛ 4
- 10. ИЛ 5; ИЛ 6; ИЛ 7; ИЛ
- 11. ИЛ 9; ИЛ 10; ИЛ 11; ИЛ
- 12. ИЛ 13; ИЛ 14; ИЛ 15
- 13. ИЛ 16; ИЛ 17; ИЛ 18
- 14. ФАКТОРЫ ВЗАИМОДЕЙСТВИЯ ЛИМФОЦИТ-МАКРОФАГ. Макрофаги человека являются акцепторами
- 15. Основными антигенпредставляющими клетками являются дендритные клетки Лангерганса,
- 16. Моноциты и тканевые макрофаги являются ведущими клетками
- 17. В-СИСТЕМА ЛИМФОЦИТОВ В костном мозге
- 18. Степень зрелости В-лимфоцитов определяется наличием на их
- 19. В лимфатических узлах В-лимфоциты располагаются в тимуснезависи-мых
- 20. Т-СИСТЕМА ЛИМФОЦИТОВ Тимус, как и
- 21. На мембране тимических Т-лимфоцитов экспрессируется специфический
- 22. Таким образом, для CD4- и СD8-Т-лимфоцитов характерно
- 23. РОЛЬ ИНТЕРФЕРОНОВ В ИММУННОМ ОТВЕТЕ. Интерферон а
- 24. Противовирусное действие интерферонов опосредовано по меньшей мере
- 25. ГЕНЕТИЧЕСКИЙ КОНТРОЛЬ ИММУННОГО ОТВЕТА. генетическое детерминирование иммунного
- 26. Иммунный ответ любого организма антигенспецифичен, конкретен, но
- 27. Например, для носителей HLA-В8, DR3 и А2,
- 29. ИНТЕРПРЕТАЦИЯ ИММУНОГРАММ С ВКЛЮЧЕНИЕМ ЦИТОКИНОВ Спектр иммунологических
- 30. ФУНДАМЕНТАЛЬНЫЕ ПРИНЦИПЫ ИНТЕРПРЕТАЦИИ ИММУНОГРАММЫ: 1. Полноценный клинический
- 31. 5. Анализ иммунограммы в динамике (особенно в
Слайд 1ТЕМА :ЦИТОКИНЫ, ОСНОВНЫЕ ХАРАКТЕРИСТИКИ, РОЛЬ В РЕГУЛЯЦИИ ИММУННОГО ОТВЕТА
Выполнили: Гайдукова
Слайд 2ЦИТОКИНЫ
В развитии иммунного ответа важную роль играют цитокины. Они
действуют как на малых, так и больших расстояниях, обеспечивают взаимодействие между разными категориями иммунокомпетентных клеток, а также выполняют роль эффекторных молекул иммунных реакций. Они являются теми посредниками, которые обеспечивают связь иммунной системы с гемопоэзом (стволовыми кроветворными клетками), с эндокринной и нервной системами. Через них иммунная система оказывает регуляторное влияние на различные органы и ткани, может активировать или подавлять их функции, регулировать метаболизм, процессы физиологической и репаративной регенерации.
Слайд 3К группе цитокинов относятся: интерлейкины – макромолекулы, продуцируемые лимфоцитами; монокины, продуцируемые
моноцитами/ макрофагами; интерфероны; факторы некроза опухоли; хемокины, которые способны регулировать хемотаксис и активность лейкоцитов, а также воспалительные реакции. Многие цитокины принадлежат к семейтсву гемопоэтинов: ГМ-КСФ, Г-КСФ, ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-11, ИЛ-12, ИЛ-13, ИЛ-15.
Таким образом, цитокины – это низкомолекулярные белки с регулятор-ными свойствами.
Таким образом, цитокины – это низкомолекулярные белки с регулятор-ными свойствами.
Слайд 4К цитокинам относят интерфероны, колониестимулирующие факторы (КСФ), хемокины, трансформирующие ростовые факторы;
фактор некроза опухолей; интерлейкины со сложившимися исторически порядковыми номерами и некоторые другие эндогенные медиаторы. Интерлейкины, имеющие порядковые номера, начиная с 1, не относятся к одной подгруппе цитокинов, связанных общностью функций. Они в свою очередь могут быть разделены на провоспалительные цитокины, ростовые и дифференцировочные факторы лимфоцитов, отдельные регуляторные цитокины.
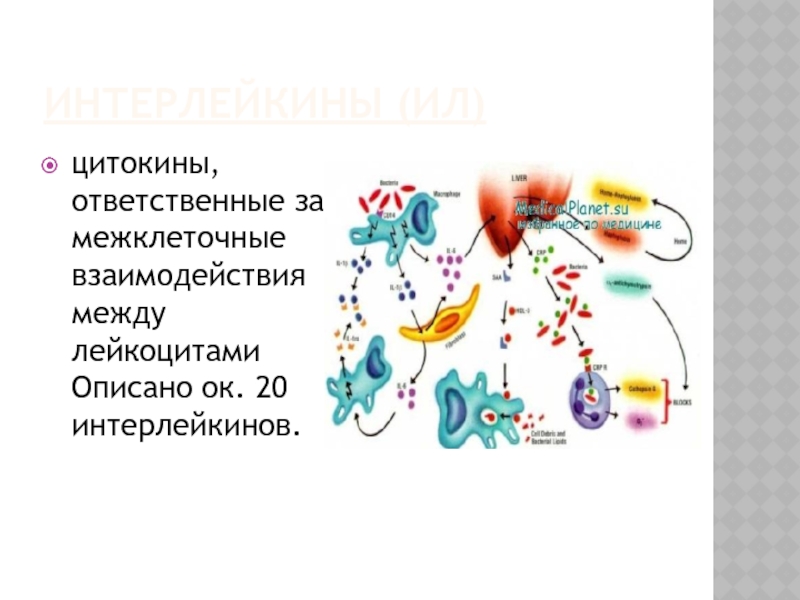
Слайд 7ИНТЕРЛЕЙКИНЫ (ИЛ)
цитокины, ответственные за межклеточные взаимодействия между лейкоцитами Описано ок. 20
интерлейкинов.
Слайд 8ИЛ 1
Ил-1 продуцируется гл. обр. макрофагами и в меньшей степени дендритными
клетками, эндотелиоцитами, фибробластами, NK, кератиноцитами, некоторыми клонами Th2. Он стимулирует продукцию Т-хелперами ИЛ-2, способствует проявлению рецепторов к ИЛ-2 на Т-лимфоцитах, влияет на созревание В-лимфоцитов, стимулирует образование молекул МНС, а также оказывает провоспалительное и пирогенное действие. Стимулирует образование гепатоцитами белков острой фазы, усиливает функции нейтрофилов, NK, обеспечивает взаимосвязь иммунной, нервной и эндокринной систем. Оказывает провоспалительное и пирогенное действие, обеспечивает взаимосвязь иммунной, нервной и эндокринной систем.
Слайд 9ИЛ 2; ИЛ 3; ИЛ 4
Ил-2 вырабатывается Т-лимфоцитами, гл. обр. Thl,
а также цитотоксическими лимфоцитами (CD8+) 1 порядка. Он активирует дифференцировку Thl и Т-киллеров, стимулирует NK и синтез иммуноглобулинов В-лимфоцитами.
Ил-3 продуцируется Т-лимфоцитами и стволовыми клетками. Является ростовым фактором стволовых и ранних предшественников гемопоэтических клеток.
Ил-4 продуцируется гл. обр. Th2. Он стимулирует дифференцировку Th0 в Th2, стимулирует синтез иммуноглобулинов В-лимфоцитами, подавляет генерацию цитотоксических лимфоцитов, NK, а также продукцию ИФН-g и противоопухолевую активность макрофагов.
Ил-3 продуцируется Т-лимфоцитами и стволовыми клетками. Является ростовым фактором стволовых и ранних предшественников гемопоэтических клеток.
Ил-4 продуцируется гл. обр. Th2. Он стимулирует дифференцировку Th0 в Th2, стимулирует синтез иммуноглобулинов В-лимфоцитами, подавляет генерацию цитотоксических лимфоцитов, NK, а также продукцию ИФН-g и противоопухолевую активность макрофагов.
Слайд 10ИЛ 5; ИЛ 6; ИЛ 7; ИЛ 8
Ил-5 синтезируется Th2. Способстует
пролиферации и дифференцировке стимулированных В-лимфоцитов, усиливает продукцию IgA, активирует эозинофилы.
Ил-6 вырабатывается макрофагами, Т- и В-лимфоцитами. Стимулирует пролиферацию тимоцитов, В-лимфоцитов, активирует предшественников цитотоксических лимфоцитов, гранулоцитов и макрофагов, стимулирует образование гепатоцитами белков острой фазы, оказывает провоспалительное действие, обеспечивает взаимосвязь иммунной, нервной и эндокринной систем.
ИЛ-7 продуцируется стромальными клетками костного мозга. Является ростовым фактором пре-В- и пре-Т-лимфоцитов.
ИЛ-8 синтезируется моноцитами, макрофагами, фибробластами. Вызывает миграцию нейтрофилов и базофилов в очаг воспаления и их дегрануляцию, выделение супероксидного радикала. Стимулирует ангиогенез.
Ил-6 вырабатывается макрофагами, Т- и В-лимфоцитами. Стимулирует пролиферацию тимоцитов, В-лимфоцитов, активирует предшественников цитотоксических лимфоцитов, гранулоцитов и макрофагов, стимулирует образование гепатоцитами белков острой фазы, оказывает провоспалительное действие, обеспечивает взаимосвязь иммунной, нервной и эндокринной систем.
ИЛ-7 продуцируется стромальными клетками костного мозга. Является ростовым фактором пре-В- и пре-Т-лимфоцитов.
ИЛ-8 синтезируется моноцитами, макрофагами, фибробластами. Вызывает миграцию нейтрофилов и базофилов в очаг воспаления и их дегрануляцию, выделение супероксидного радикала. Стимулирует ангиогенез.
Слайд 11ИЛ 9; ИЛ 10; ИЛ 11; ИЛ 12
ИЛ-9 продуцируется гл. обр. Т-лимфоцитами.
Стимулирует пролиферацию Т-лимфоцитов, активирует тучные клетки, усиливает эффекты эритропоэтина.
ИЛ-10 синтезируется Th2 а также цитотоксическими Т-лимфоцитами второго порядка и макрофагами. Стимулирует пролиферацию и дифференцировку В-лимфоцитов, подавляет синтез ИЛ-2 и ИФН-у клетками Thl, угнетает продукцию провоспалительных цитокинов.
ИЛ-11 продуцируется стромальными клетками костного мозга. Стимулирует деление и дифференцировку предшественников гемопоэза, колониеобразование мегакариоцитов, увеличивает количество тромбоцитов и эритроцитов в периферической крови. Угнетает продукцию провоспалительных цитокинов.
ИЛ-12 продуцируют моноциты, макрофаги и, в меньшей степени, В-лимфоциты и дендритные клетки. Стимулирует рост и дифференцировку Th (Th0 => Thl), Т-киллеров, NK. Индуцирует продукцию ИФН-g Т-лимфоцитами и NK, угнетает апоптоз Thl, синтез IgE. Вместе с ИЛ-4 регулирует баланс Thl и Th2.
ИЛ-10 синтезируется Th2 а также цитотоксическими Т-лимфоцитами второго порядка и макрофагами. Стимулирует пролиферацию и дифференцировку В-лимфоцитов, подавляет синтез ИЛ-2 и ИФН-у клетками Thl, угнетает продукцию провоспалительных цитокинов.
ИЛ-11 продуцируется стромальными клетками костного мозга. Стимулирует деление и дифференцировку предшественников гемопоэза, колониеобразование мегакариоцитов, увеличивает количество тромбоцитов и эритроцитов в периферической крови. Угнетает продукцию провоспалительных цитокинов.
ИЛ-12 продуцируют моноциты, макрофаги и, в меньшей степени, В-лимфоциты и дендритные клетки. Стимулирует рост и дифференцировку Th (Th0 => Thl), Т-киллеров, NK. Индуцирует продукцию ИФН-g Т-лимфоцитами и NK, угнетает апоптоз Thl, синтез IgE. Вместе с ИЛ-4 регулирует баланс Thl и Th2.
Слайд 12ИЛ 13; ИЛ 14; ИЛ 15
ИЛ-13 синтезируется Th2. Стимулирует рост и
дифференцировку В-лимфоцитов, подавляет функцию моноцитов/макрофагов, в частности секрецию провоспалительных цитокинов.
ИЛ-14 продуцируется в основном Т-лимфоцитами. Усиливает пролиферацию В-лимфоцитов и подавляет продукцию иммуноглобулинов.
ИЛ-15 вырабатывается моноцитами, эпителиоцитами и гладкомышечными клетками. По действию на Т-лимфоциты ИЛ-15 сходен с ИЛ-2, что объясняется способностью специфически связываться с ИЛ-2-рецепторами. Активирует NK и В-лимфоциты.
ИЛ-14 продуцируется в основном Т-лимфоцитами. Усиливает пролиферацию В-лимфоцитов и подавляет продукцию иммуноглобулинов.
ИЛ-15 вырабатывается моноцитами, эпителиоцитами и гладкомышечными клетками. По действию на Т-лимфоциты ИЛ-15 сходен с ИЛ-2, что объясняется способностью специфически связываться с ИЛ-2-рецепторами. Активирует NK и В-лимфоциты.
Слайд 13ИЛ 16; ИЛ 17; ИЛ 18
ИЛ-16 синтезируется эозинофилами и CD8+ Т-лимфоцитами. Является
хемоаттрактантом для CD4+ лимфоцитов.
ИЛ-17 продуцируется активированными CD4 Т-лимфоцитами. Основными клетками-мишенями цитокина являются эпителиоциты, эндотелиоциты и фибробласты. Он усиливает выработку ИЛ-б, ИЛ-8, гранулоцитарного КСФ, простатландина Е2, увеличивает экспрессию ICAM-1, стимулирует активность фибробластов.
ИЛ-18 образуется активированными макрофагами, а также гепатоцитами. Стимулирует синтез Т-лимфоцитами ИФН-g, макрофагами - ИЛ-1, ИЛ 8 и ФНО. Кроме того, он активирует NK.
ИЛ-17 продуцируется активированными CD4 Т-лимфоцитами. Основными клетками-мишенями цитокина являются эпителиоциты, эндотелиоциты и фибробласты. Он усиливает выработку ИЛ-б, ИЛ-8, гранулоцитарного КСФ, простатландина Е2, увеличивает экспрессию ICAM-1, стимулирует активность фибробластов.
ИЛ-18 образуется активированными макрофагами, а также гепатоцитами. Стимулирует синтез Т-лимфоцитами ИФН-g, макрофагами - ИЛ-1, ИЛ 8 и ФНО. Кроме того, он активирует NK.
Слайд 14ФАКТОРЫ ВЗАИМОДЕЙСТВИЯ ЛИМФОЦИТ-МАКРОФАГ.
Макрофаги человека являются акцепторами любого внешнего воздействия: бактериальных и
вирусных инфекций, лучевого и химиотерапевтического воздействия, а также эндогенных раздражителей (вторичные инфекции опухолей, сапрофитная флора, продукты клеточного распада). Спектр патогенов, с которыми взаимодействуют макрофаги, необыкновенно широк. Макрофаги обладают чрезвычайно чувствительными рецепторами, позволяющими им распознавать чужеродные молекулы, и толерантностью к нормальным клеткам собственного организма. Если
Т - лимфоцитам для приобретения толерантности к "своему" необходим специальный инструктаж в процессе онтогенеза, то толерантность МФ по отношению к собственным клеткам организма можно считать врожденной.
Т - лимфоцитам для приобретения толерантности к "своему" необходим специальный инструктаж в процессе онтогенеза, то толерантность МФ по отношению к собственным клеткам организма можно считать врожденной.
Слайд 15Основными антигенпредставляющими клетками являются дендритные клетки Лангерганса, фолликулярные дендритные клетки зародышевых
цен-тров лимфатических узлов, интердигитирующие клетки тимуса.
Касаясь значимости клеток мононуклеарной фагоцитирующей системы в развитии межклеточного взаимодействия на фоне антигенной стимуляции, необходимо отметить не только их фагоцитарную и антигенпредставляющую функции, но и способность к продукции комплекса биологически активных соединений - монокинов.
Монокины - гетерогенная группа соединений с различной биологической активностью. К числу монокинов относятся следующие группы веществ:
Медиаторы воспаления и иммуномодуляции (интерлейкин 1, фактор нек-роза опухоли, интерферон, лизоцим, фактор активации нейтрофилов, компо-ненты системы комплемента С1, С2, С3, С5, а также интерлейкины -3, 6, 8, 10, 12, 15).
Факторы свертывающей системы крови,активаторы и ингибиторы фибри-нолиза (активатор плазминогена, ингибиторы плазминогена и плазмина, V, VII, IX, Х плазменные факторы свертываемости крови).
Факторы роста, в частности,различные колониестимулирующие фак-торы, активизирующие гемопоэз в костном мозге, фактор роста фибробластов.
Касаясь значимости клеток мононуклеарной фагоцитирующей системы в развитии межклеточного взаимодействия на фоне антигенной стимуляции, необходимо отметить не только их фагоцитарную и антигенпредставляющую функции, но и способность к продукции комплекса биологически активных соединений - монокинов.
Монокины - гетерогенная группа соединений с различной биологической активностью. К числу монокинов относятся следующие группы веществ:
Медиаторы воспаления и иммуномодуляции (интерлейкин 1, фактор нек-роза опухоли, интерферон, лизоцим, фактор активации нейтрофилов, компо-ненты системы комплемента С1, С2, С3, С5, а также интерлейкины -3, 6, 8, 10, 12, 15).
Факторы свертывающей системы крови,активаторы и ингибиторы фибри-нолиза (активатор плазминогена, ингибиторы плазминогена и плазмина, V, VII, IX, Х плазменные факторы свертываемости крови).
Факторы роста, в частности,различные колониестимулирующие фак-торы, активизирующие гемопоэз в костном мозге, фактор роста фибробластов.
Слайд 16Моноциты и тканевые макрофаги являются ведущими клетками иммунно-го ответа организма, обеспечивая
переработку антигенов и их презентацию (особенно при вторичном иммунном ответе) Т-хелперам в комплексе с Iа-антигеном. Последний является продуктом Ir генов II класса МНС. Подобная презентация необходима для запуска иммунного ответа на многие Т-зависимые антигены.
Продуцируемый клетками мононуклеарной фагоцитирующей системы цитокин-интерлейкин-I в комплексе с антигеном, ассоциированным с I-а бел-ками, стимулирует продукцию Т-хелперами интерлейкина-II.
Связь между Т-хелперами и макрофагами обеспечивается при участии ад-гезивных молекул, синтез которых, в свою очередь, зависит от интенсивно-сти продукции макрофагами ИЛ-I,ИЛ-6,ФНО.
В последние годы несколько изменились представления о различных суб-популяциях Т- и В- систем лимфоцитов и их значимости в развитии иммун-ного ответа.
В связи с этим представляется целесообразным остановиться на совре-менных знаниях о центральных и периферических органах иммунной систе-мы и особенностях функционирования различных субпопуляций лимфоцитов на фоне антигенной стимуляци
Продуцируемый клетками мононуклеарной фагоцитирующей системы цитокин-интерлейкин-I в комплексе с антигеном, ассоциированным с I-а бел-ками, стимулирует продукцию Т-хелперами интерлейкина-II.
Связь между Т-хелперами и макрофагами обеспечивается при участии ад-гезивных молекул, синтез которых, в свою очередь, зависит от интенсивно-сти продукции макрофагами ИЛ-I,ИЛ-6,ФНО.
В последние годы несколько изменились представления о различных суб-популяциях Т- и В- систем лимфоцитов и их значимости в развитии иммун-ного ответа.
В связи с этим представляется целесообразным остановиться на совре-менных знаниях о центральных и периферических органах иммунной систе-мы и особенностях функционирования различных субпопуляций лимфоцитов на фоне антигенной стимуляци
Слайд 17В-СИСТЕМА ЛИМФОЦИТОВ
В костном мозге под влиянием микроокружения стромальных костно-мозговых клеток осуществляется
дифференцировка большей части В-лимфоцитов, относящихся к В2- субпопуляции клеток.
В1-субпопуляция лимфоцитов еще в эмбриональном периоде покидает костный мозг. Физиологическая регенерация В1-лимфоцитов в течение жиз-ни человека поддерживается преимущественно в брюшной и плевральной полостях.
В1- и В2-субпопуляции лимфоцитов отличаются по своей функцио-нальной значимости и экспонируемым на поверхности мембраны маркерам.
В процессе дифференцировки В2-лимфоцитов на их мембране экспо-нируются рецепторы иммуноглобулиновой природы, причем незрелые В2-лимфоциты экспрессируют IgМ и небольшое количество молекул главного комплекса гистосовместимости класса II , часть из которых представляет со-бой так называемые Iа белки или Ia-антигены. По мере созревания В2-лимфоцитов на их поверхности экспрессируются молекулы иммуноглобули-нов всех 5 классов, а также увеличивается плотность Ia-антигенов. В то же время появляются рецепторы для различных компонентов комплемента и другие маркерные молекулы, в частности,СD19, СD21, СD23, СD35. Анти-генчувствительными рецепторами В-лимфо-цитов являются мембраносвя-занный мономер IgМ, а возможно, и IgD.
В1-субпопуляция лимфоцитов еще в эмбриональном периоде покидает костный мозг. Физиологическая регенерация В1-лимфоцитов в течение жиз-ни человека поддерживается преимущественно в брюшной и плевральной полостях.
В1- и В2-субпопуляции лимфоцитов отличаются по своей функцио-нальной значимости и экспонируемым на поверхности мембраны маркерам.
В процессе дифференцировки В2-лимфоцитов на их мембране экспо-нируются рецепторы иммуноглобулиновой природы, причем незрелые В2-лимфоциты экспрессируют IgМ и небольшое количество молекул главного комплекса гистосовместимости класса II , часть из которых представляет со-бой так называемые Iа белки или Ia-антигены. По мере созревания В2-лимфоцитов на их поверхности экспрессируются молекулы иммуноглобули-нов всех 5 классов, а также увеличивается плотность Ia-антигенов. В то же время появляются рецепторы для различных компонентов комплемента и другие маркерные молекулы, в частности,СD19, СD21, СD23, СD35. Анти-генчувствительными рецепторами В-лимфо-цитов являются мембраносвя-занный мономер IgМ, а возможно, и IgD.
Слайд 18Степень зрелости В-лимфоцитов определяется наличием на их мембране следующих рецепторов: антигенспецифических
иммуноглобулиновой при-роды, к Fc-фрагменту Ig, к комплементу, к поликлональным В-активаторам, липополисахаридам и монопротеазам. В2-лим-фоциты являются предшест-венниками клеток- плазмоцитов, обеспечивающих синтез иммуноглобулинов в ответ на антигенную стимуляцию. Необходимым условием их трансформа-ции в клетки-продуценты антител является их взаимодействие с Т-лимфоцитами-хелперами.
В связи с этим очевидно, что В2-лимфоциты ответственны за развитие гуморального ответа на тимусзависимые антигены.
В связи с этим очевидно, что В2-лимфоциты ответственны за развитие гуморального ответа на тимусзависимые антигены.
Слайд 19В лимфатических узлах В-лимфоциты располагаются в тимуснезависи-мых зонах фолликулов, составляя лишь
35% всех лимфоцитов. В-лимфоциты находятся в кортикальной зоне в покоящемся состоянии и образуют так на-зываемые первичные фолликулы. На фоне антигенной стимуляции они фор-мируют вторичные фолликулы.
Важным компонентом системы иммунопоэза является селезенка, в кото-рой содержание В-лимфоцитов достигает 65%, что обеспечивает быстрое на-копление антителпродуцирующих плазматических клеток на фоне антиген-ной стимуляции.
При внутривенном введении антигена антитела образуются преимущест-венно в селезенке.
Лимфоидные образования червеобразного отростка, а также групповые лимфатические фолликулы - пейеровы бляшки - участвуют в синтезе антител класса IgA, тем самым обеспечивая иммунитет слизистых.
В миндалинах глоточного кольца имеются Т- и В-лимфоциты, обеспечи-вающие клеточный и гуморальный механизмы защиты, в частности, синтез антител класса IgA и IgG. В связи с этим тонзиллэктомия, проведенная в раннем возрасте, снижает противоинфекционную защиту глоточного кольца.
Важным компонентом системы иммунопоэза является селезенка, в кото-рой содержание В-лимфоцитов достигает 65%, что обеспечивает быстрое на-копление антителпродуцирующих плазматических клеток на фоне антиген-ной стимуляции.
При внутривенном введении антигена антитела образуются преимущест-венно в селезенке.
Лимфоидные образования червеобразного отростка, а также групповые лимфатические фолликулы - пейеровы бляшки - участвуют в синтезе антител класса IgA, тем самым обеспечивая иммунитет слизистых.
В миндалинах глоточного кольца имеются Т- и В-лимфоциты, обеспечи-вающие клеточный и гуморальный механизмы защиты, в частности, синтез антител класса IgA и IgG. В связи с этим тонзиллэктомия, проведенная в раннем возрасте, снижает противоинфекционную защиту глоточного кольца.
Слайд 20Т-СИСТЕМА ЛИМФОЦИТОВ
Тимус, как и костный мозг, является центральным, или первичным орга-ном
лимфоидной ткани. В составе тимуса имеются несколько долек, каждая из которых представлена эпителиальными клетками, дендритными клетками, макрофагами, лимфоцитами и другими клетками. Эпителиальные клетки ти-муса синтезируют такие пептидные гормоны, как тимолин, тимозины, тимо-поэтин. Крупные эпителиальные клетки коркового вещества выполняют роль «клеток-кормилиц» для лимфоцитов. Эпителиальные клетки коркового ве-щества имеют разветвленные отростки с большим количеством молекул главного комплекса гистосовместимости. В то же время на поверхности от-ростков эпителиальных клеток мозгового вещества тимуса представлены мо-лекулы главного комплекса гистосовместимости классов II и I.
Продвигаясь из коркового вещества в мозговое, предшественники Т-лимфоцитов дифференцируются в Т-лимфоциты под влиянием тими-ческих гормонов. В то же время секретируемые в кровь гормоны тимуса обеспечи-вают дозревание Т-лимфоцитов в периферических лимфатических органах – селезенке и лимфатических узлах.
Продвигаясь из коркового вещества в мозговое, предшественники Т-лимфоцитов дифференцируются в Т-лимфоциты под влиянием тими-ческих гормонов. В то же время секретируемые в кровь гормоны тимуса обеспечи-вают дозревание Т-лимфоцитов в периферических лимфатических органах – селезенке и лимфатических узлах.
Слайд 21
На мембране тимических Т-лимфоцитов экспрессируется специфический рецептор для распознавания антигена. В
отличие от антиген-распознающего рецептора В-лимфоцитов иммуноглобулиновой природы специфический ре-цептор Т-лимфоцита является гетеродимером, состоящим из - и -цепей, обеспечивающих распознавание специфичности антигена, а также молекулы CD3. Последняя состоит из трех пептидных цепей и обеспечивает передачу сигнала о взаимодействии антигенраспознающих пептидных цепей , с ан-тигеном в глубь клетки. Таким образом, полная структура рецептора Т-лимфоцитов представляется комплексом из пяти пептидов, включающих ге-теродимер и молекулу CD3. Поверхностными антигенными маркерами Т-лимфоцитов являются CD3-рецепторы
Слайд 22Таким образом, для CD4- и СD8-Т-лимфоцитов характерно распознавание чужеродного антигена лишь
в комплексе с аутологичным мембранным бел-ком, кодируемым главным комплексом гистосовместимости. Подобные клет-ки, способные к одновременному распознаванию чужеродного антигена в комплексе с продуктами собственных МНС-генов, подвергаются положи-тельной селекции в тимусе. Эти клетки мигрируют из тимуса в кровь, а также в ткани. После встречи Т-лимфоцитов в периферических тканях с антигеном начинается 2-й этап дифференцировки Т-лимфоцита-иммуногенез. Контакт лимфоцитов с антигеном может происходить в регионарных лимфатических узлах при проникновении антигена через покровные барьерные ткани, а так-же в селезенке при проникновении антигенов в кровоток. В случае энтераль-ного поступления антигена его взаимодействие с лимфоцитами осуществля-ется в брыжеечных лимфатических узлах. Миграция лимфоцитов из крови в ткани происходит преимущественно через кубовидный эндотелий постка-пиллярных венул при участии адгезивных молекул, экспрессируемых на их поверхности, в частности, L-селектинов.
Содержание Т-лимфоцитов в периферической крови достигает 50-65% всех лимфоцитов крови, в грудном лимфатическом протоке - 85% лимфоци-тов.
Уровень Т-лимфоцитов в селезенке составляет 35%, в лимфатических уз-лах - 65%, где они занимают паракортикальные или тимусзависимые зоны.
Содержание Т-лимфоцитов в периферической крови достигает 50-65% всех лимфоцитов крови, в грудном лимфатическом протоке - 85% лимфоци-тов.
Уровень Т-лимфоцитов в селезенке составляет 35%, в лимфатических уз-лах - 65%, где они занимают паракортикальные или тимусзависимые зоны.
Слайд 23РОЛЬ ИНТЕРФЕРОНОВ В ИММУННОМ ОТВЕТЕ.
Интерферон а — это собирательное название Для
целой группы белков, которых уже известно не менее 15; синтез этих белков индуцируют вирусы, бактерии и опухолевые клетки. Интерферон а синтезируется в основном макрофагами и В-лимфоцитами. Синтез интерферона (3 происходит в фибробластах, макрофагах и эпителиальных клетках и запускается вирусами и другими чужеродными нуклеиновыми кислотами. Интерферон у вырабатывается преимущественно Т-лимфоцитами в ответ на антигены и митогены; по-видимому, он оказывает скорее иммуномодулирующее, чем противовирусное дайствие. Этот интерферон сильнее, чем другие интерфероны, по-давляет внутриклеточно паразитирующих бактерий (например, некоторых риккетсий, листерий)
Слайд 24Противовирусное действие интерферонов опосредовано по меньшей мере двумя механизмами: разрушением вирусной
РНК путем активации рибонуклеазы L и подавлением синтеза белка в зараженной клетке путем индукции синтеза протеинкиназы PKR, которая блокирует фактор инициации трансляции eIF2a. Иммуномодулирующее действие интерферонов заключается в регуляции синтеза иммуноглобулинов, цитокинов и экспрессии антигенов HLA. Кроме того, интерферон у стимулирует макрофаги.
Слайд 25ГЕНЕТИЧЕСКИЙ КОНТРОЛЬ ИММУННОГО ОТВЕТА.
генетическое детерминирование иммунного ответа организма индивидуума на воздействие
антигена (специфичности, интенсивности и типа). Он осуществляется рядом генетических систем. К таким системам относятся гены иммуноглобулинов, Т-клеточного рецептора, молекул ГКГ, цитокинов, системы комплемента и другие методы контрацепции.
Слайд 26Иммунный ответ любого организма антигенспецифичен, конкретен, но вариабелен по силе и
направленности. В популяциях человека и животных можно выделить группы людей или особей высоко, умеренно, слабо и оппозитно реагирующих на определенный антиген (вакцину). В то же время следует отметить, что иммунная система конкретного индивидуума по-разному реагирует на различные антигены.
Слайд 27Например, для носителей HLA-В8, DR3 и А2, B12 характерен сильный тип
клеточного иммунного ответа, а для HLA-В7, В18, В35 — слабый. Низкий тип гуморального иммунного ответа на столбнячный анатоксин ассоциируется с HLA-A24, BS2, DR2. Высокий тип гуморального иммунного ответа на вирус краснухи отмечается при наличии в HLA фенотипе антигена В15, а низкий — В5, В22. Дефицит некоторых компонентов комплемента и наличие определенного комплотипа также влияют на уровень гуморального и клеточного иммунного ответа.
Генетически детерминированные различия индивидуумов по силе иммунного ответа не меняются в течение жизни. Ряд иммунопатологических заболеваний в высокой степени ассоциируются с носительством определенных генов иммунного ответа.
Генетически детерминированные различия индивидуумов по силе иммунного ответа не меняются в течение жизни. Ряд иммунопатологических заболеваний в высокой степени ассоциируются с носительством определенных генов иммунного ответа.
Слайд 29ИНТЕРПРЕТАЦИЯ ИММУНОГРАММ С ВКЛЮЧЕНИЕМ ЦИТОКИНОВ
Спектр иммунологических лабораторных исследований, проведенных больному, составляет
его иммунограмму. Все основные принципы интерпретации иммунограмм разработаны на основе накопленного опыта использования общего анализа крови в повседневной врачебной практике с 20-х годов прошлого столетия и опыта использования иммунограммы клиницистами за последние 30 лет. В основу диагностики и прогнозирования следует всегда ставить совокупность изменений всех показателей лейкограммы и иммунограммы. Один и тот же конечный результат иммунной реакции при одинаковых условиях может быть получен разным количественным и качественным сочетанием компонентов иммунной системы.
Слайд 30ФУНДАМЕНТАЛЬНЫЕ ПРИНЦИПЫ ИНТЕРПРЕТАЦИИ ИММУНОГРАММЫ:
1. Полноценный клинический анализ иммунограммы может быть проведен
лишь в комплексе с оценкой клинической картины заболевания у данного пациента и данных его анамнеза. Делать клинический вывод на основании лишь иммунограммы нельзя, так как одни и те же измения показателей иммунограммы могут наблюдаться при принципиально разных патологических процессах.
2. Комплексный анализ иммунограммы более информативен, нежели оценка любого показателя в отдельности. Одинаковые изменения определенного показателя в разные фазы острого воспалительного процесса могут рассматриваться как благоприятный и неблагоприятный признак.
3. Реальную информацию об изменениях иммунограммы дают значительные нарушения показателей в иммунограмме (40-50% от нормы и более). В связи с лабильностью показателей иммунограммы их незначительные колебания возможны у совершенно здоровых лиц.
4. Клинические данные играют решающую роль, а иммунограмма несет вспомогательное диагностическое и прогностическое значение. Отсутствие сдвигов в иммунограмме при наличии клинической картины патологии требует изучения функции компонентов отдельных звеньев иммунной системы.
Слайд 315. Анализ иммунограммы в динамике (особенно в сопоставлении с клинической динамикой)
более информативен с точки зрения как диагностики, так и прогноза течения заболевания, помогает избежать ошибочного трактования.
6. Диагностическое и прогностическое значение имеют индивидуальные показатели нормы у данного пациента (с учетом возраста и наличия сопутствующих хронических заболеваний, действия вредных факторов, медикаментозной терапии).
7. Первоочередное значение при оценке иммунограммы имеет соотношение показателей иммунограммы, а не их абсолютные значения.
8. При оценке показателей иммунограммы следует учитывать возможность их колебаний, в связи с принятием пищи, физическими нагрузками, ощущением страха, временем суток.
9. Несоответствие сдвигов показателей иммунограммы и клинической картины заболевания (синдром диссоциации) свидетельствует о неблагоприятном развитии процесса.
10. Чем выше антигенность чужеродного фактора и больше зона его проникновения, тем ярче будет воспалительный процесс. Поэтому более выраженными должны быть и сдвиги в иммунограмме, что будет свидетельствовать в пользу адекватности реакции иммунной системы. Отсутствие указанных изменений в лейко- и иммунограмме – неблагоприятный симптом, который свидетельствует о неадекватности роботы иммунной системы.