- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2) презентация
Содержание
- 1. Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2)
- 2. * доцент Свергун В.Т. Содержание
- 4. * доцент Свергун В.Т. Пути метаболизма
- 5. * доцент Свергун В.Т.
- 6. * доцент Свергун В.Т.
- 7. * доцент Свергун В.Т. Г л
- 8. * доцент Свергун В.Т. Анаэробный гликолиз
- 9. * доцент Свергун В.Т. Г е
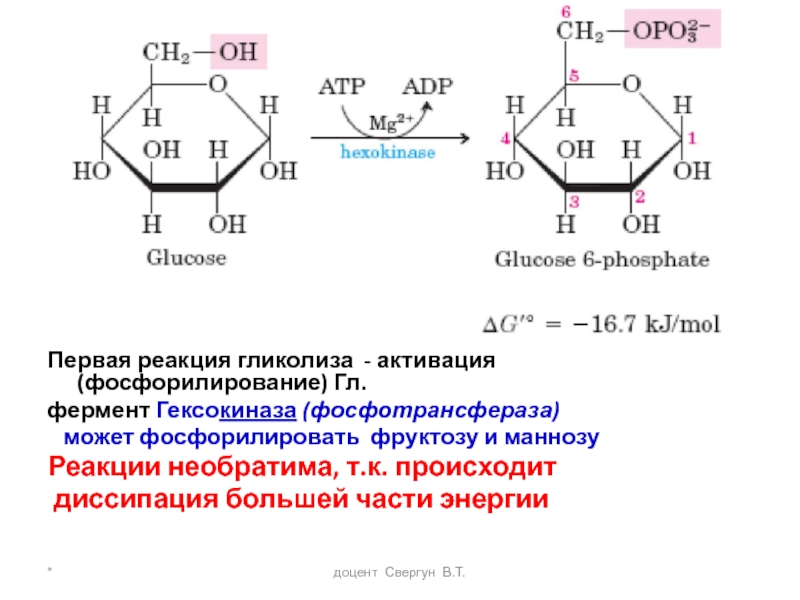
- 10. * доцент Свергун В.Т. Первая реакция
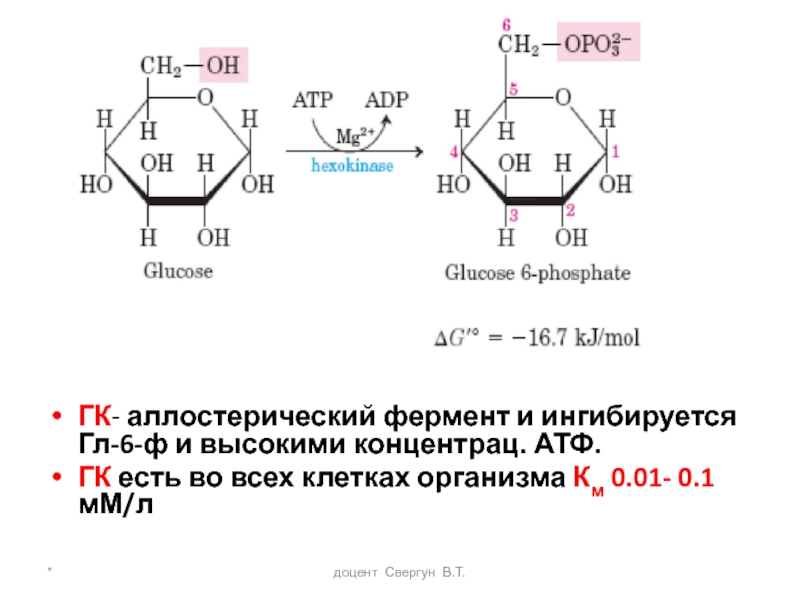
- 11. * доцент Свергун В.Т. ГК- аллостерический
- 12. * доцент Свергун В.Т.
- 13. * доцент Свергун В.Т.
- 14. * доцент Свергун В.Т.
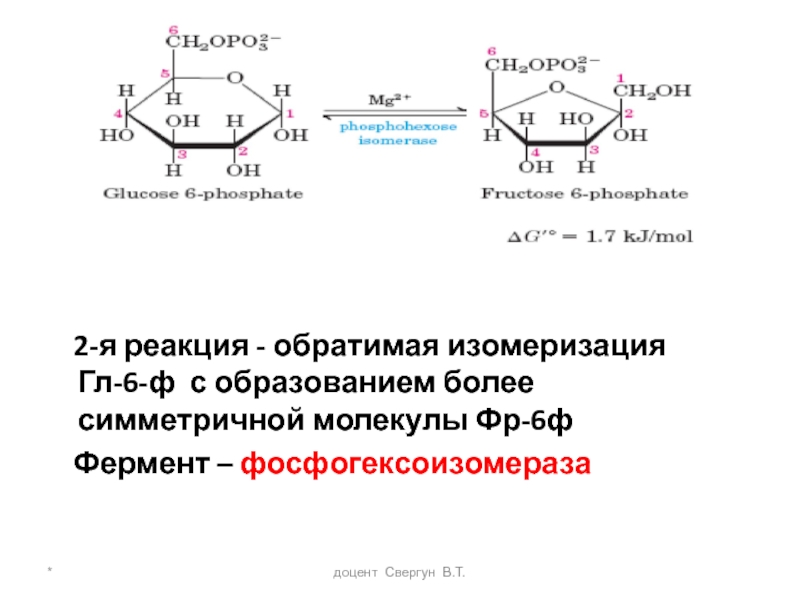
- 15. * доцент Свергун В.Т. ФФК -
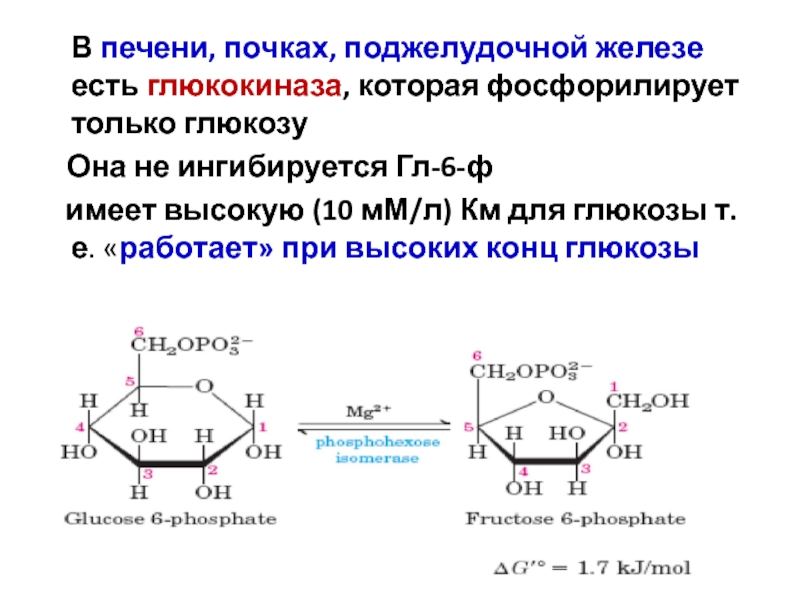
- 16. * доцент Свергун В.Т. Регуляция активности
- 17. * доцент Свергун В.Т. Регуляция активности
- 18. * доцент Свергун В.Т.
- 19. * доцент Свергун В.Т. 4-я реакция.
- 20. * доцент Свергун В.Т.
- 21. * доцент Свергун В.Т. Характеристика альдолазы
- 22. * доцент Свергун В.Т. Эти триозы
- 23. * доцент Свергун В.Т. 3ФГА затем
- 24. * доцент Свергун В.Т. 3ФГА затем
- 25. * доцент Свергун В.Т.
- 26. * доцент Свергун В.Т.
- 27. * доцент Свергун В.Т.
- 28. * доцент Свергун В.Т. Следующие реакции
- 29. * доцент Свергун В.Т. и последующего
- 30. * доцент Свергун В.Т.
- 31. * доцент Свергун В.Т.
- 32. * доцент Свергун В.Т. Суммарное уравнение гликолиза
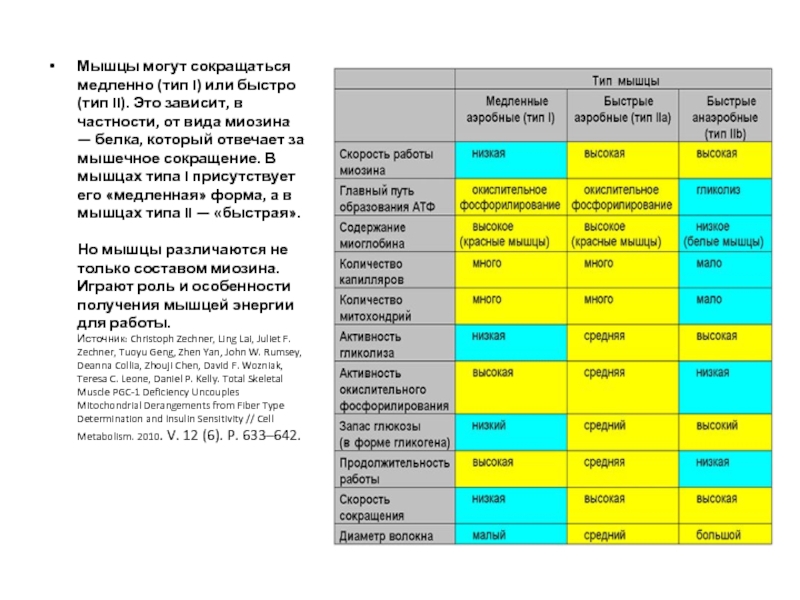
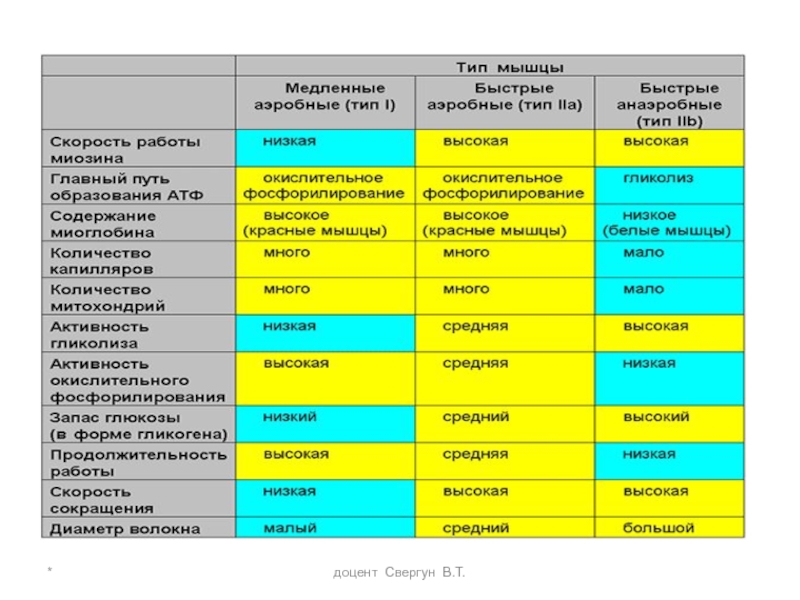
- 33. Мышцы могут сокращаться медленно (тип I) или
- 34. * доцент Свергун В.Т.
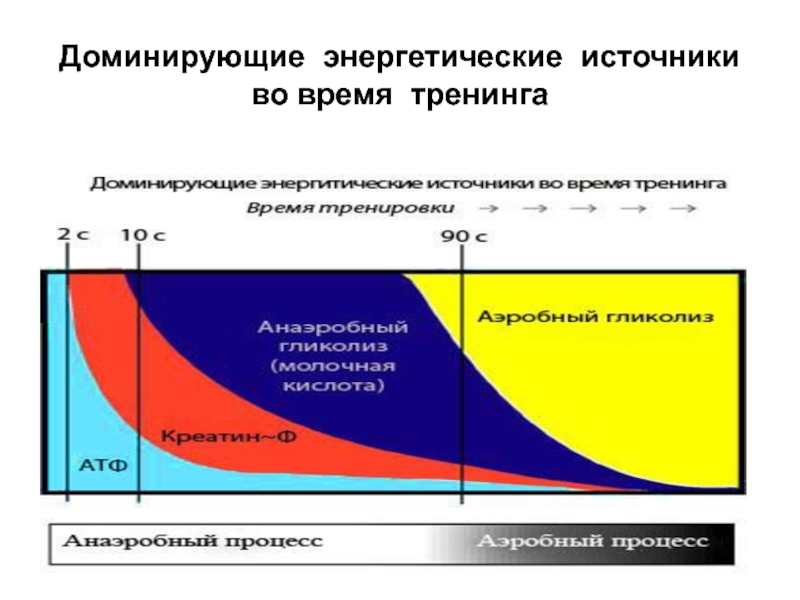
- 35. Доминирующие энергетические источники во время тренинга
- 36. * доцент Свергун В.Т. Лактат ДГ
- 37. * доцент Свергун В.Т. При гликолизе
- 38. * доцент Свергун В.Т. Ферменты гликолиза
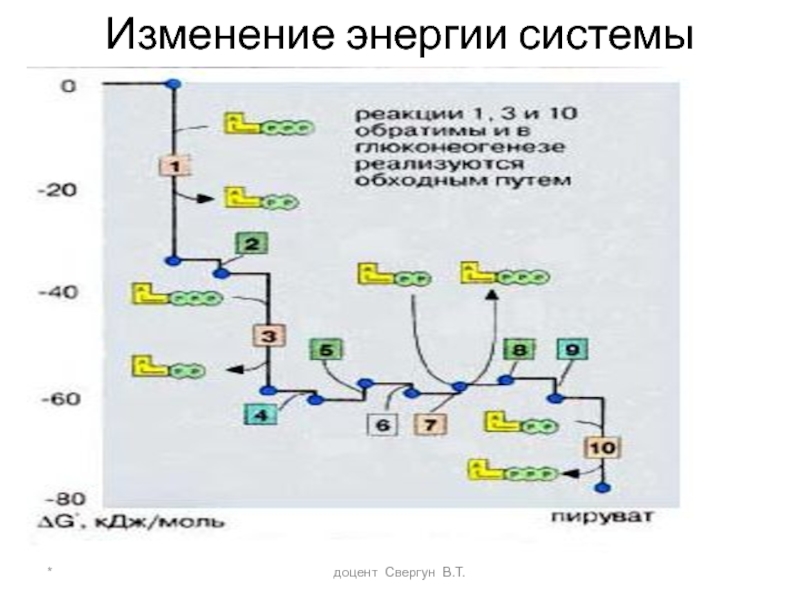
- 39. * доцент Свергун В.Т. Изменение энергии системы
- 40. * доцент Свергун В.Т.
- 41. * доцент Свергун В.Т. М е
- 42. * доцент Свергун В.Т. М е
- 43. * доцент Свергун В.Т. М е
- 44. * доцент Свергун В.Т. МЭОС
- 45. * доцент Свергун В.Т.
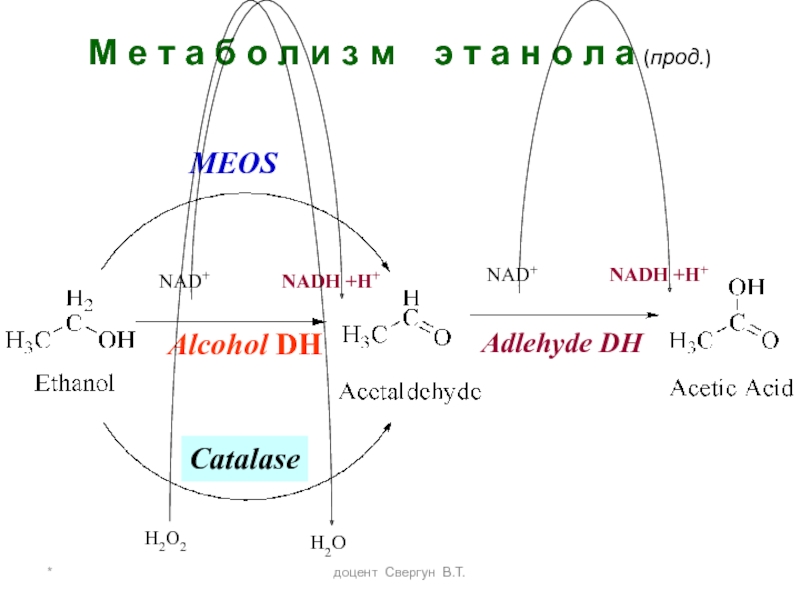
- 46. * доцент Свергун В.Т. Метаболизм этанола
- 47. * доцент Свергун В.Т. М е
- 48. * доцент Свергун В.Т. Метаболизм ацетальдегида
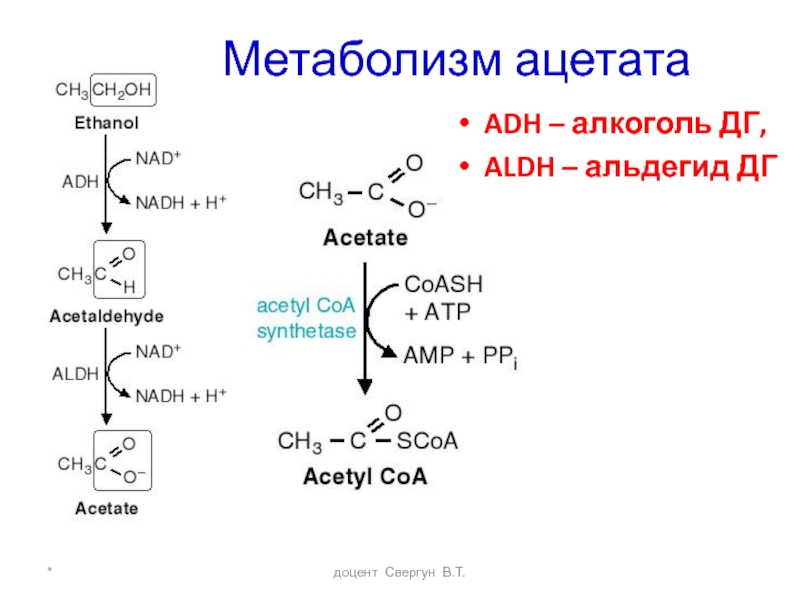
- 50. * доцент Свергун В.Т. Метаболизм ацетата ADH – алкоголь ДГ, ALDH – альдегид ДГ
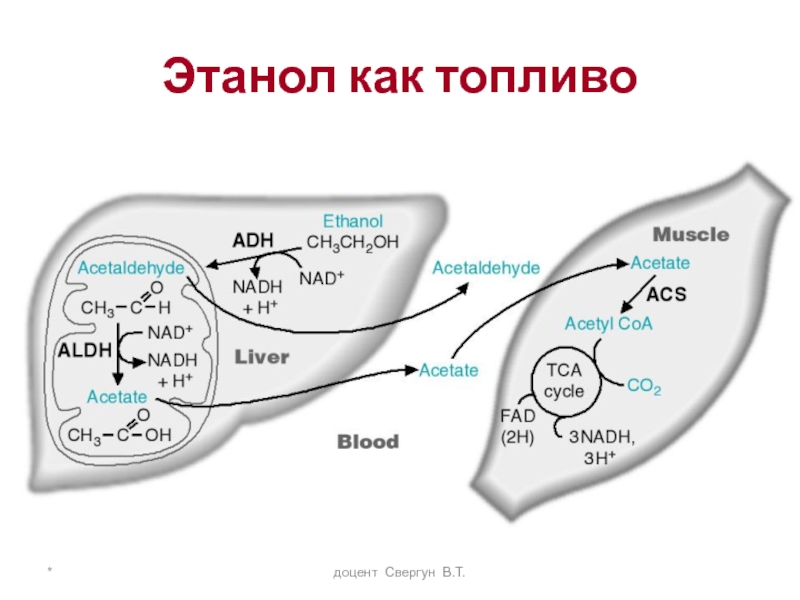
- 51. * доцент Свергун В.Т. Этанол как топливо
- 52. * доцент Свергун В.Т. Метабол.
- 53. * доцент Свергун В.Т. Метабол.
- 54. * доцент Свергун В.Т. Метабол. механизмы
- 55. * доцент Свергун В.Т. Факторы воздействия этанола
- 56. * доцент Свергун В.Т. Первичный метаболит
- 57. * доцент Свергун В.Т.
- 58. * доцент Свергун В.Т. 40% азиатского
- 59. * доцент Свергун В.Т.
- 60. * доцент Свергун В.Т.
- 61. * доцент Свергун В.Т. Метабол. механизмы
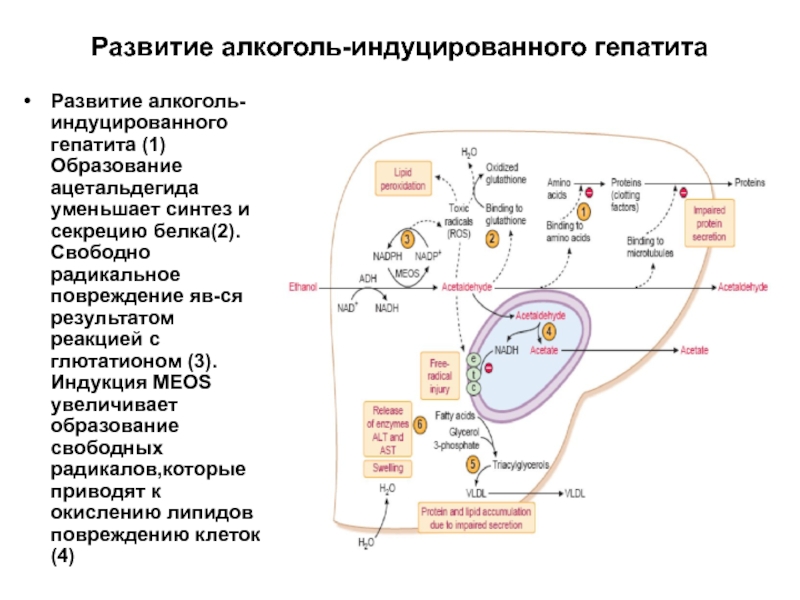
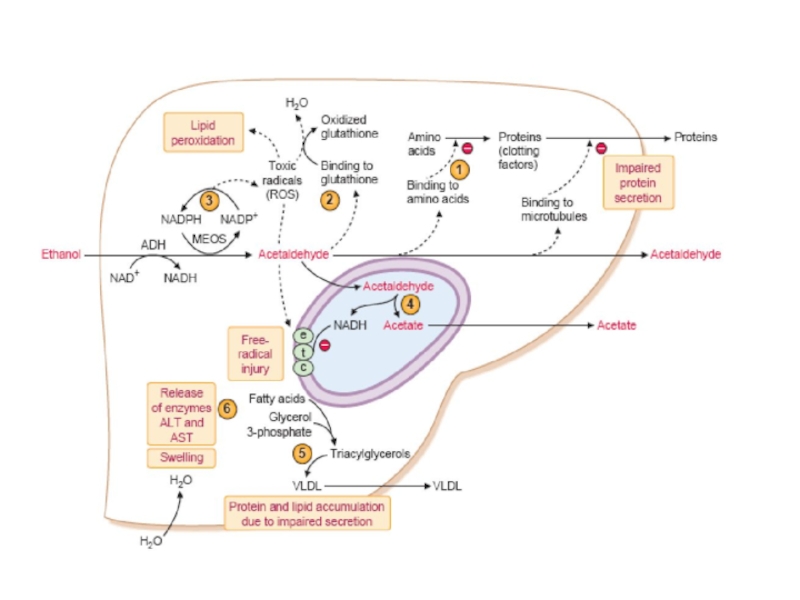
- 62. Развитие алкоголь-индуцированного гепатита Развитие алкоголь-индуцированного гепатита (1)
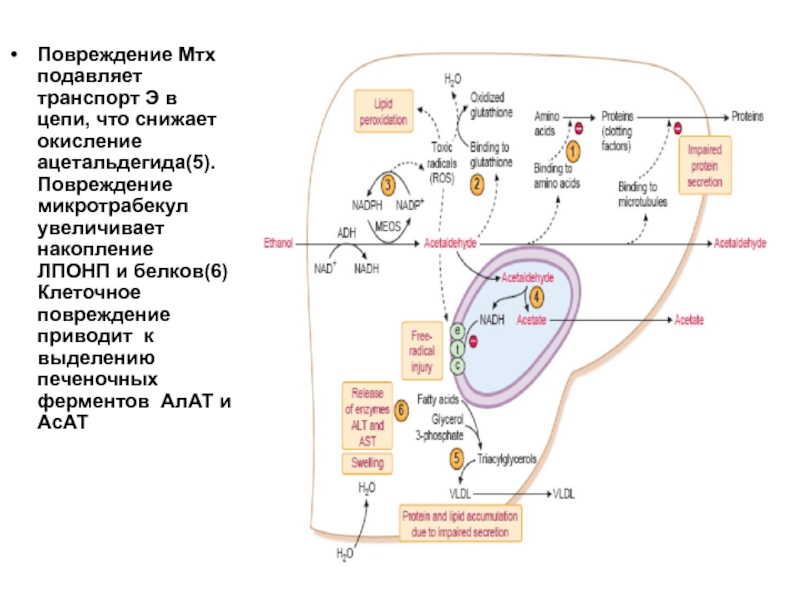
- 64. Повреждение Мтх подавляет транспорт Э в цепи,
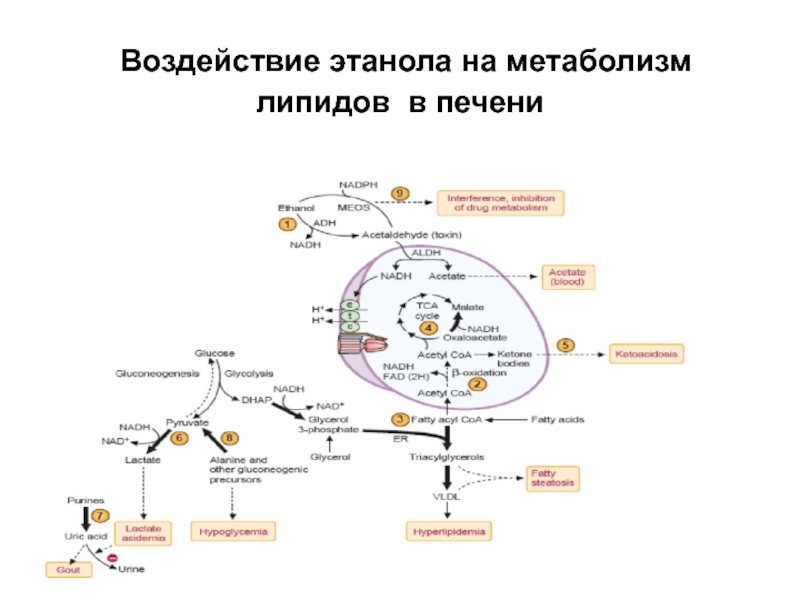
- 65. Воздействие этанола на метаболизм липидов в печени
- 67. * доцент Свергун В.Т.
- 68. * доцент Свергун В.Т.
- 69. * доцент Свергун В.Т.
Слайд 2*
доцент Свергун В.Т.
Содержание
1. Пути обмена глюкозо-6 фосфата в
2. Анаэробное расщепление глюкозы
3. Спиртовое брожение
4. Метаболизм этанола
5. Регуляция гликолиза и гликогенолиза
6. Энергетический баланс окисления
углеводов.
Слайд 4*
доцент Свергун В.Т.
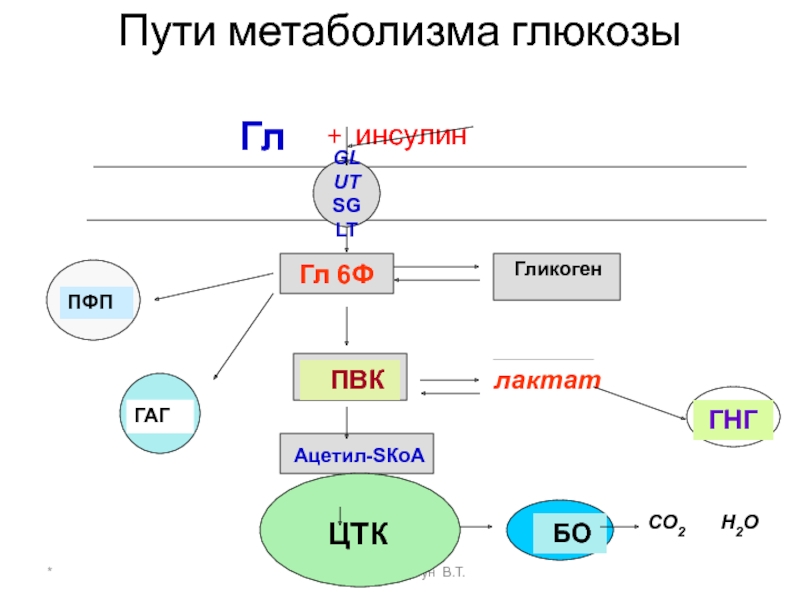
Пути метаболизма глюкозы
Гл + инсулин
GLUT
SGLT
Гл
ПВК
лактат
ГНГ
Гликоген
ПФП
ГАГ
Ацетил-SКоА
ЦТК
БО
СО2
Н2О
Слайд 5*
доцент Свергун В.Т.
Гликолиз и
Гликолиз (греч. glykys-сладкий, lysis-распад)-процесс распада глюкоз (аэробный или анаэробный)
Брожение – анаэробный гликолиз с образованием АТФ и различных в-в (спирта, лактата, ацетата, пропионата, бутирата)
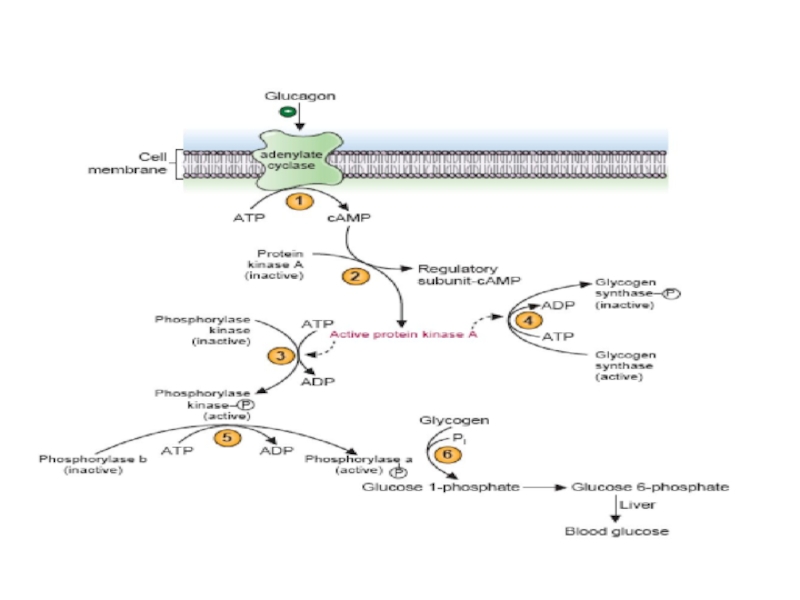
Гликогенолиз- процесс распада гликогена
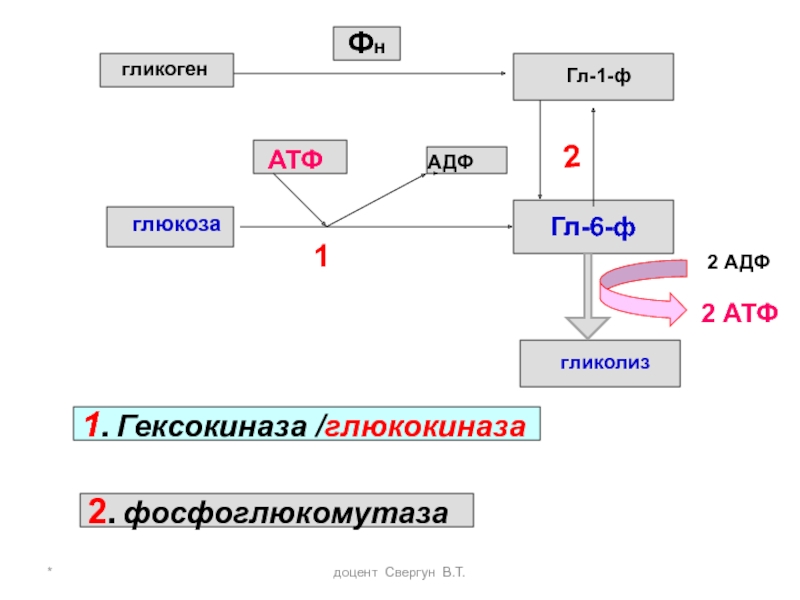
В фосфоглюкомутазной реакции образуется Г-6ф, после чего пути гликолиза и гликогенолиза полностью совпадают
В гликогенолизе образуется 3 молекулы АТФ, а не 2, (Г-6ф образуется без затраты АТФ)
Во время синтеза гликогена расходуется АТФ, сл-но оба процесса энергетически равноценны
Слайд 6*
доцент Свергун В.Т.
гликоген
Фн
Гл-1-ф
глюкоза
2
Гл-6-ф
АТФ
АДФ
1. Гексокиназа /глюкокиназа
2. фосфоглюкомутаза
гликолиз
2 АДФ
2 АТФ
Слайд 7*
доцент Свергун В.Т.
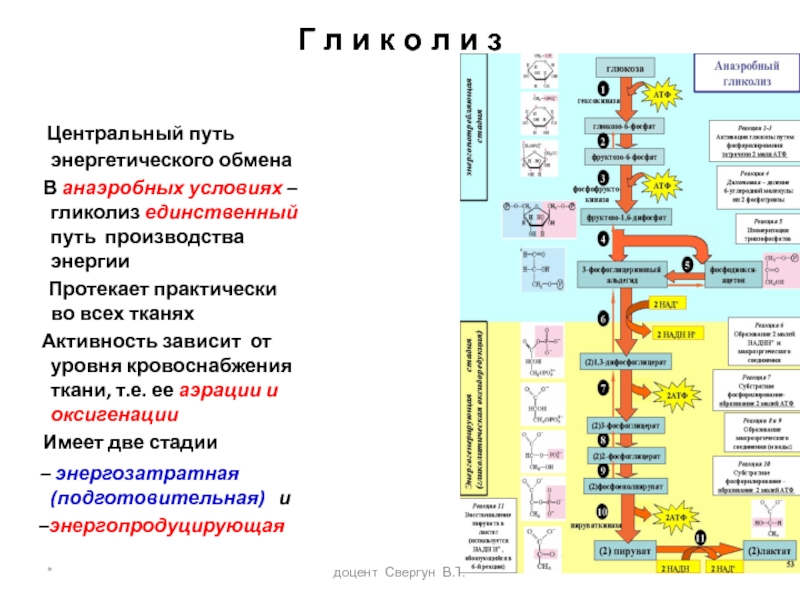
Г л и к о л и з
Центральный путь энергетического обмена
В анаэробных условиях –гликолиз единственный путь производства энергии
Протекает практически во всех тканях
Активность зависит от уровня кровоснабжения ткани, т.е. ее аэрации и оксигенации
Имеет две стадии
– энергозатратная (подготовительная) и
–энергопродуцирующая
Слайд 8*
доцент Свергун В.Т.
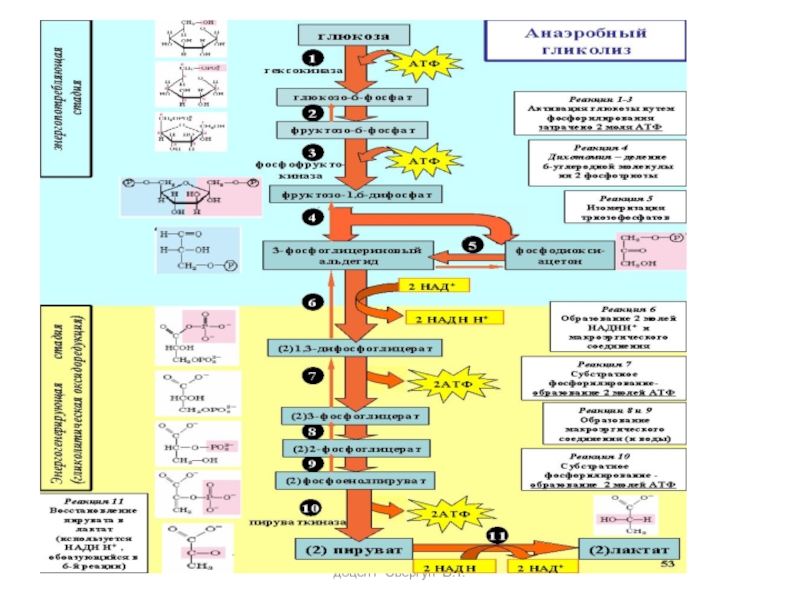
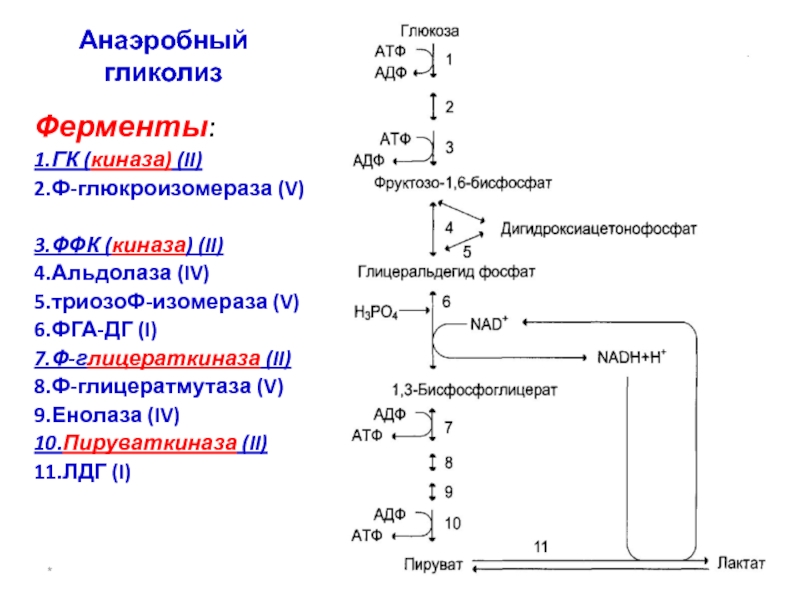
Анаэробный гликолиз
Ферменты:
1.ГК (киназа) (II)
2.Ф-глюкроизомераза (V)
3.ФФК (киназа) (II)
4.Альдолаза (IV)
5.триозоФ-изомераза
6.ФГА-ДГ (I)
7.Ф-глицераткиназа (II)
8.Ф-глицератмутаза (V)
9.Енолаза (IV)
10.Пируваткиназа (II)
11.ЛДГ (I)
Слайд 10*
доцент Свергун В.Т.
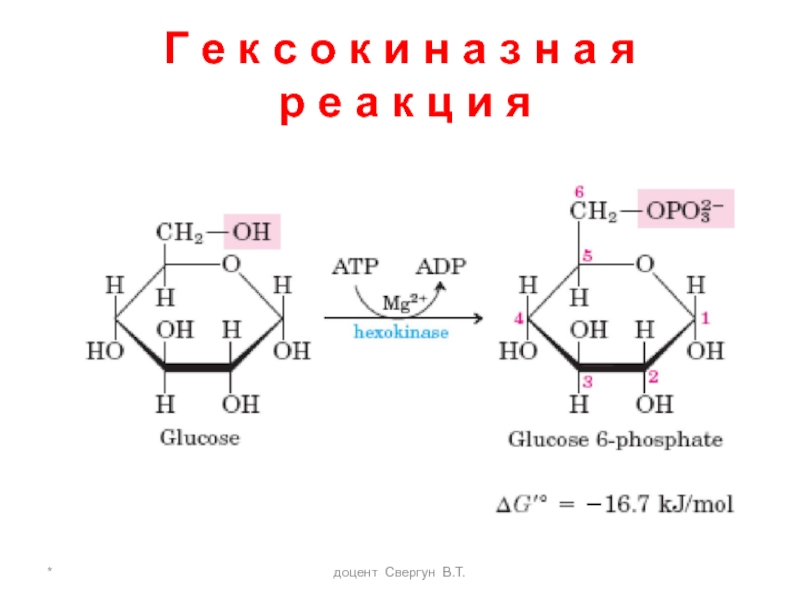
Первая реакция гликолиза - активация (фосфорилирование) Гл.
фермент Гексокиназа
может фосфорилировать фруктозу и маннозу
Реакции необратима, т.к. происходит
диссипация большей части энергии
Слайд 11*
доцент Свергун В.Т.
ГК- аллостерический фермент и ингибируется Гл-6-ф и высокими
ГК есть во всех клетках организма Км 0.01- 0.1 мМ/л
Слайд 12*
доцент Свергун В.Т.
В печени, почках, поджелудочной железе есть
Она не ингибируется Гл-6-ф
имеет высокую (10 мМ/л) Км для глюкозы т.е. «работает» при высоких конц глюкозы
Слайд 13*
доцент Свергун В.Т.
2-я реакция - обратимая
Фермент – фосфогексоизомераза
Слайд 14*
доцент Свергун В.Т.
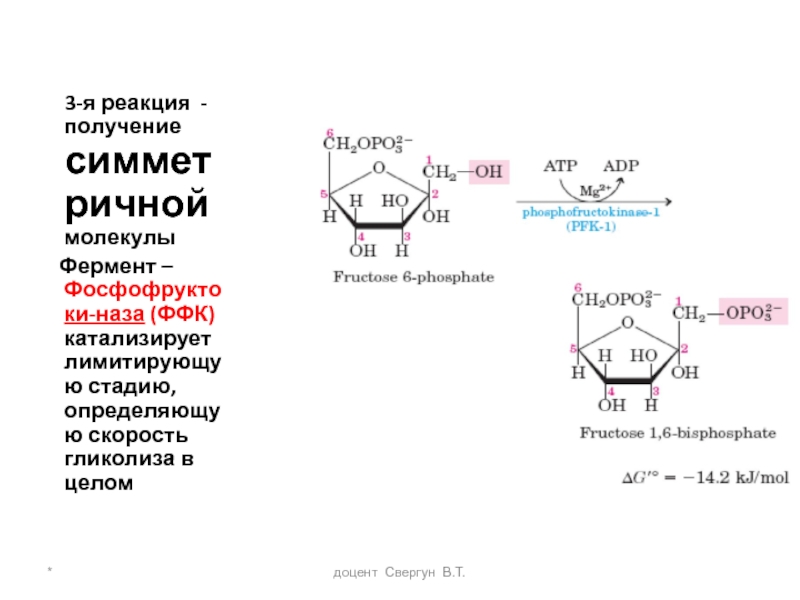
3-я реакция -
Фермент – Фосфофруктоки-наза (ФФК) катализирует лимитирующую стадию, определяющую скорость гликолиза в целом
Слайд 15*
доцент Свергун В.Т.
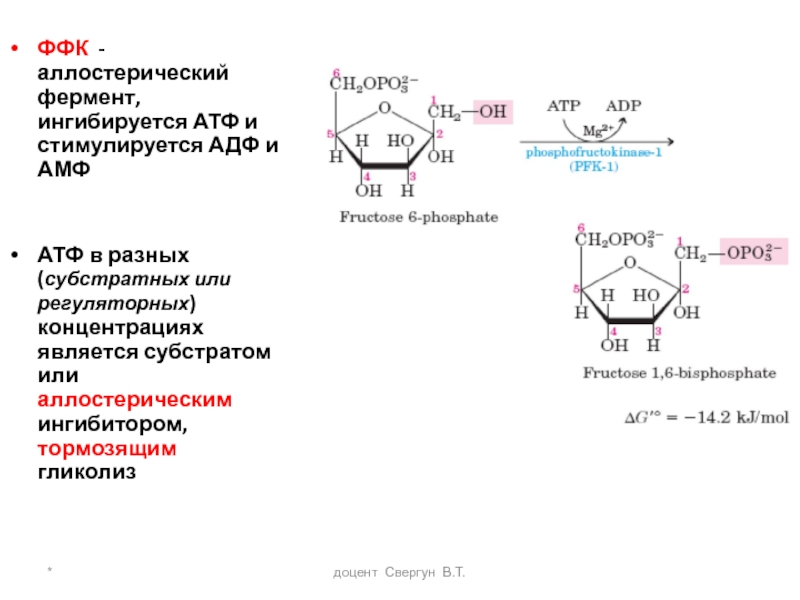
ФФК - аллостерический фермент, ингибируется АТФ и стимулируется
АТФ в разных (субстратных или регуляторных) концентрациях является субстратом или аллостерическим ингибитором, тормозящим гликолиз
Слайд 16*
доцент Свергун В.Т.
Регуляция активности ФФК и скорости гликолиза
Км
При накоплении [ АТФ],
отношение АТФ/АДФ ↑↑ ↑↑, активность ФФК и гликолиза снижается,
например в неработающей мышце
При снижении [ АТФ] - обратная реакция
Слайд 17*
доцент Свергун В.Т.
Регуляция активности ФФК и скорости гликолиза (прод)
ФФК -
ФФК и гликолиз:
ингибируется цитратом, ЖК и их ацил-КоА.
При увеличении АТФ/АДФ, скорость ЦТК снижается → [цитрат] который ингибирует гликолиз
активируются ионами Са++ - вторичный мессенджер (активатор многих функций клетки) например при мышечном сокращении
Слайд 19*
доцент Свергун В.Т.
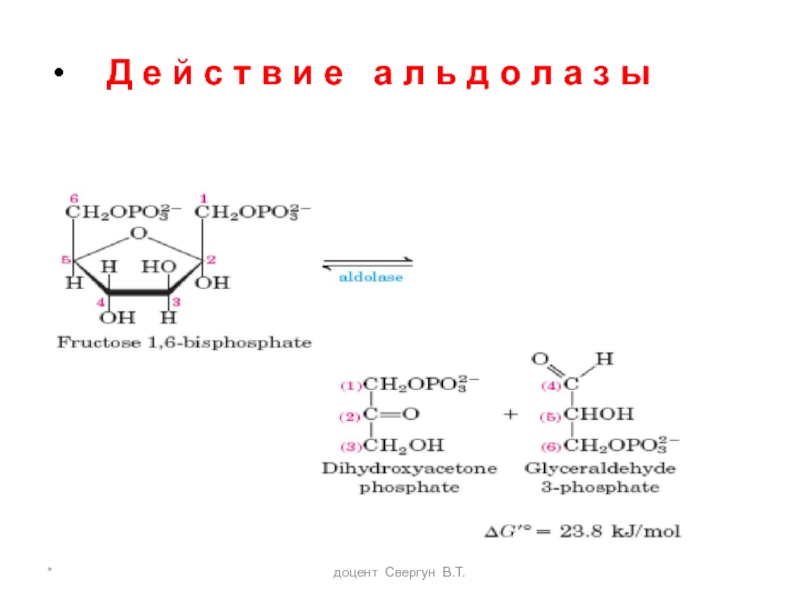
4-я реакция. Фермент-альдолаза (лиаза)
Разрыв связи происходит
Слайд 20*
доцент Свергун В.Т.
Равновесие реакции сдвинуто в
Т. О. завершается первый этап гликолиза, связанный с расходом энергии 2 мол. АТФ на активацию субстратов
Слайд 21*
доцент Свергун В.Т.
Характеристика альдолазы (см. учебник)
Определение активности альдолазы используют в
остром гепатите активность этого фермента может увеличиваться в 5-20 раз,
инфаркте миокарда – в 3-10 раз,
миодистрофии – в 4-10 раз.
Слайд 22*
доцент Свергун В.Т.
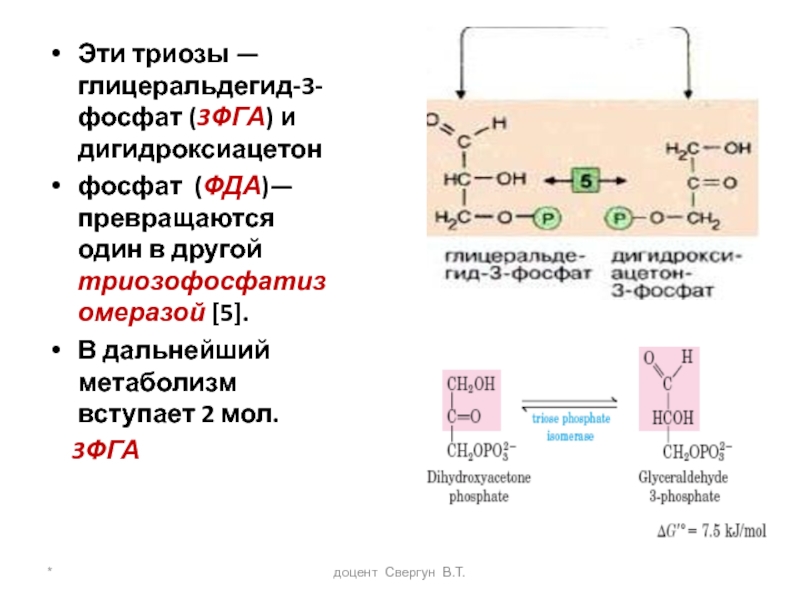
Эти триозы — глицеральдегид-3-фосфат (3ФГА) и дигидроксиацетон
фосфат (ФДА)—
В дальнейший метаболизм вступает 2 мол.
3ФГА
Слайд 23*
доцент Свергун В.Т.
3ФГА затем окисляется ферментом -глицеральдегид-З-фосфатдегидрогеназой [6] с образованием
Процесс называется гликолитической оксидоредукцией
В этой обратимой реакции в молекулу включается Фн (для последующего «субстратного фосфорилирования»,) с образованием 1,3-диФГК
Слайд 24*
доцент Свергун В.Т.
3ФГА затем окисляется ферментом -глицеральдегид-З-фосфатдегидрогеназой [6] с образованием
Процесс называется гликолитической оксидоредукцией
В этой обратимой реакции в молекулу включается Фн (для последующего «субстратного фосфорилирования»,) с образованием 1,3-диФГК.
1,3-диФГК содержит фосфо~ангидридную связь, расщепление которой сопряжено с образованием АТФ
Слайд 26*
доцент Свергун В.Т.
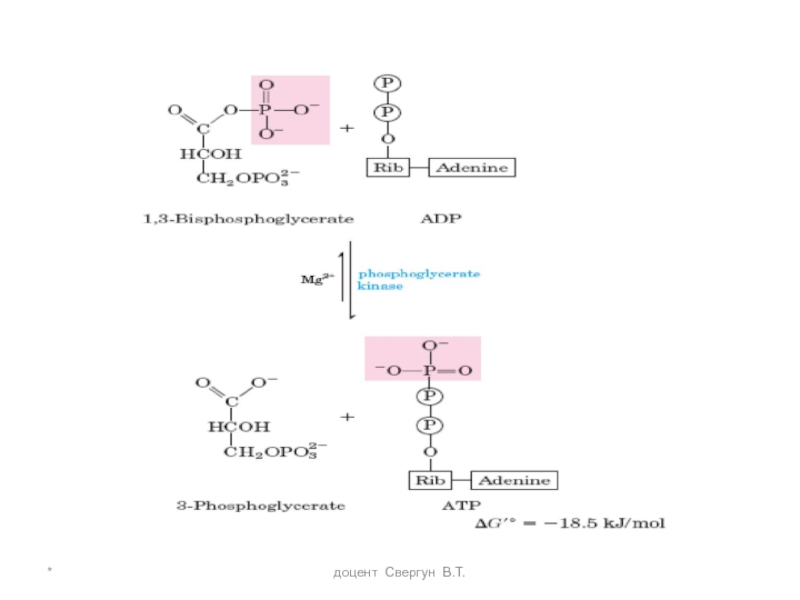
На следующей стадии (катализируе-мой фосфоглицераткиназой [7])
Слайд 28*
доцент Свергун В.Т.
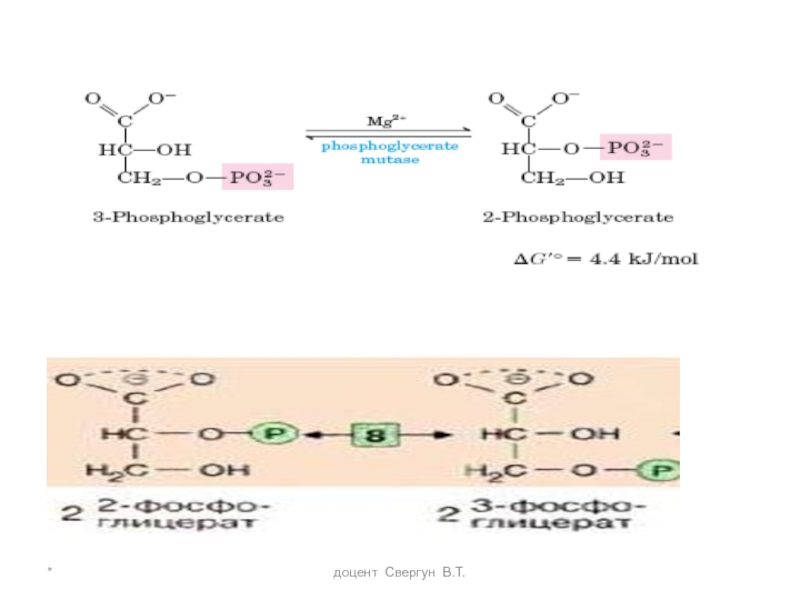
Следующие реакции -изомеризации 3-ФГК, полученного в результате реакции
в 2-фосфоглицерат (фермент: фосфоглицератмутаза [8])
Слайд 29*
доцент Свергун В.Т.
и последующего отщепления воды (фермент: енолаза - лиаза[9])
Продукт представляет собой сложный эфир фосфорной кислоты и енольной формы пирувата и потому называется фосфоенол-пируватом (ФЕП)
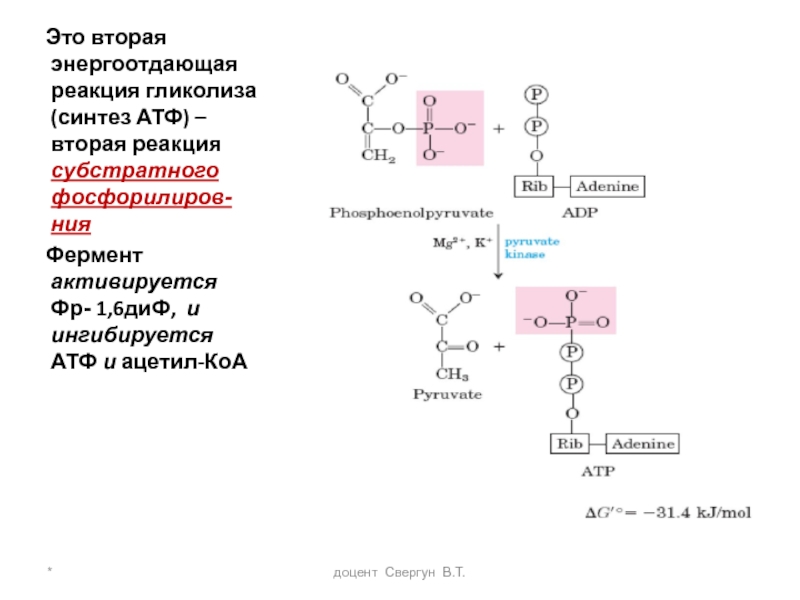
Слайд 30*
доцент Свергун В.Т.
На предпоследней стадии, которая катализируется пируваткиназой
Это вторая энергоотдающая реакция гликолиза (синтез АТФ) – вторая реакция субстратного фосфорилирования
Фермент активируется Фр- 1,6диФ, и ингибируется АТФ и ацетил-КоА
Слайд 31*
доцент Свергун В.Т.
Это вторая энергоотдающая реакция гликолиза (синтез
Фермент активируется Фр- 1,6диФ, и ингибируется АТФ и ацетил-КоА
Слайд 33Мышцы могут сокращаться медленно (тип I) или быстро (тип II). Это
Слайд 36*
доцент Свергун В.Т.
Лактат ДГ реакция
Завершающий стадией гликолиза является
Стадия регенерации NAD+ и образования лактата
ПВК + NADH+H+ лактат +NAD+
Слайд 37*
доцент Свергун В.Т.
При гликолизе на активацию одной молекулы глюкозы потребляется
В то же время при метаболическом превращении каждого С3-фрагмента образуются 2 молекулы АТФ
В результате выигрыш энергии составляет 2 моля АТФ на моль глюкозы
Слайд 40*
доцент Свергун В.Т.
Анаэробный распад глюкозы с образованием этанола
Все
Различие:
ПВК Ацетальдегид Этанол
ПВК декарбоксилаза (IV) кофермент ТПФ
Алкоголь ДГ кофермент NADH
С п и р т о в о е б р о ж е н и е
Слайд 41*
доцент Свергун В.Т.
М е т а б о л и
Небольшая амфифильная молекула (R ≈0.43нм), хорошо растворима в водной и гидрофобной фазах
В организме образуется эндогенный этанол – 20-200 мкМ/л (0.0004 – 0.001 г/л) – буфер ацетальдегида – мощного регулятора О-В процессов
У животных с низким содержанием эндогенного этанола его метаболизм и выведение повышены
У Hs при стрессе, старении, голодании, авитаминозах и т.д. возрастает потребность в экзогенном этаноле,что м.б. связано со снижением его эндогенного уровня
Слайд 42*
доцент Свергун В.Т.
М е т а б о л и
3 пути метаболизма:
Алкоголь ДГ (КФ 1.1.1.1) – низкоспецифичный NAD-завис. фермент цитоплазмы (до 80% экз. этанола)
Этанол +NAD+ Ац-альдегид + NADH + H+
≈ 80% монголоидов и 5-20% европеоидов имеют
АДГ2 2-1 (β2β1) и АДГ2 2(β2β2) с высокой активностью (быстрый токсич. эффект)
Слайд 43*
доцент Свергун В.Т.
М е т а б о л и
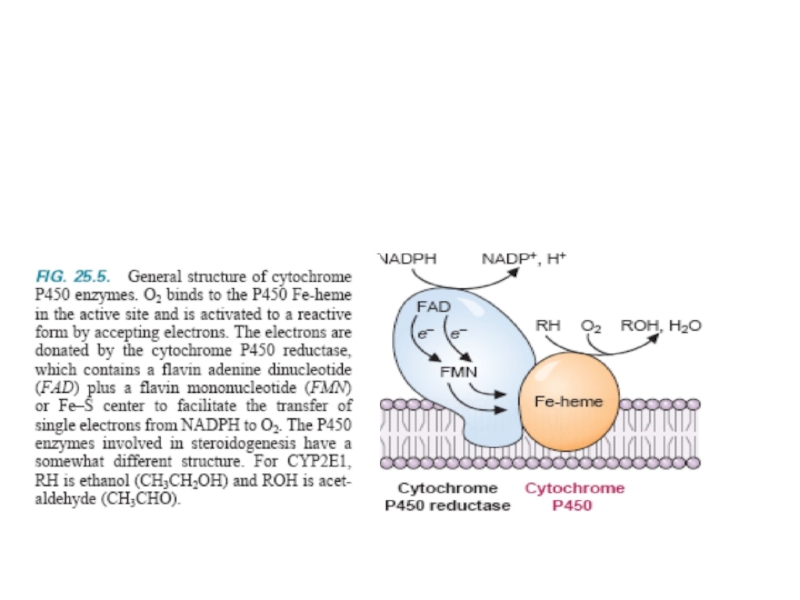
2. МЭОС (MEOS) – микросомальная этанолокисляющая система до - 10-20% экз. этанола (н.у.)
Этанол + О2 + NADPH+H+ Ац альд +NADP+ + 2Н2О
Индуцибельная система под действием спиртов, и др. ксенобиотиков
Слайд 44*
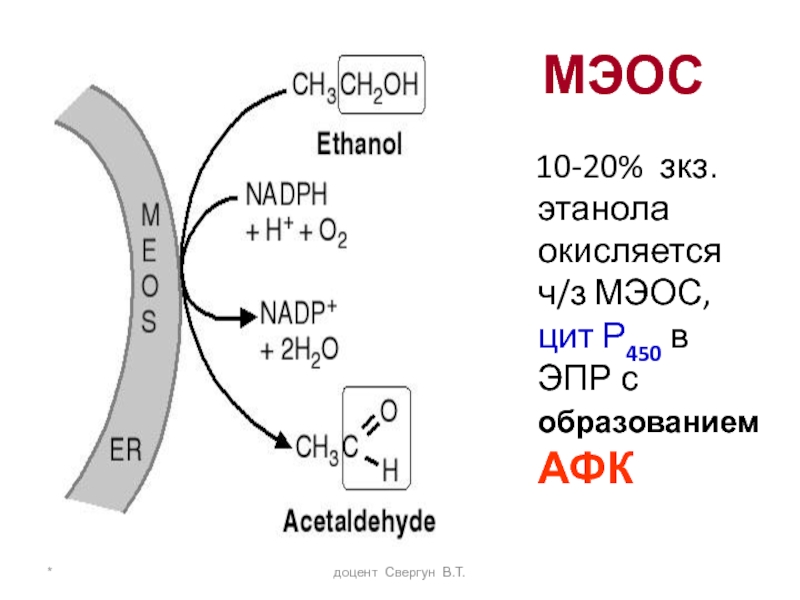
доцент Свергун В.Т.
МЭОС
10-20% зкз. этанола окисляется ч/з
Слайд 45*
доцент Свергун В.Т.
У алкоголиков в МЭОС поступает до
Более высокая Км чем у АДГ (работает при более высоких конц Этанола)
Попутно образуются АФК, повреждающие разные ткани – печень, миокард, ЖКТ и др
Слайд 46*
доцент Свергун В.Т.
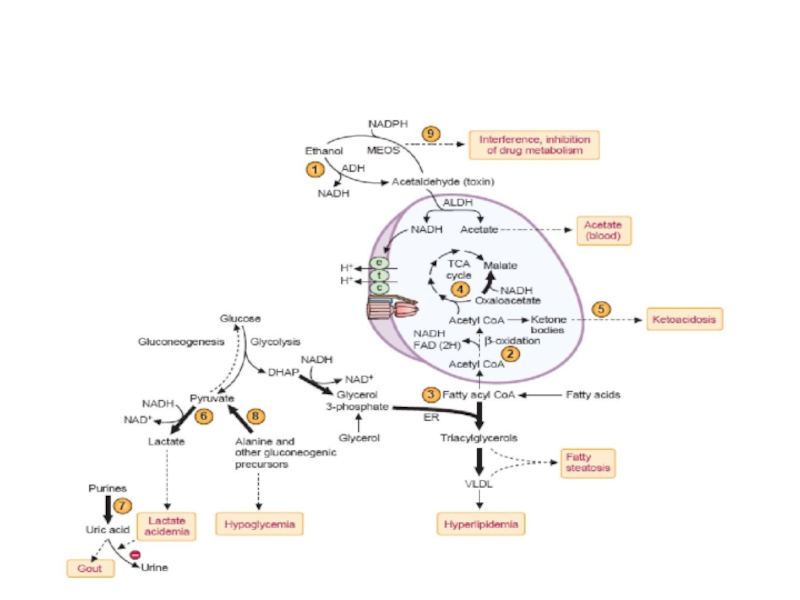
Метаболизм этанола (прод.)
3. Минорный каталазный путь (до 2%)
Наиболее активен в мозге и пероксисомах печени
Слайд 48*
доцент Свергун В.Т.
Метаболизм ацетальдегида (Ац)
Ацетальдегид окисляется до ацетата 2 путями
минорный альдегидоксидазный:
Ац + О2 + FADH2 + Н2О2+ FAD+
при этом образуются различные АФК, вызывающие пероксидный стресс и поражение внутренних органов
Ацетальдегид-ДГ обнаружена в разных органах (печень до 40%, почки, ЖКТ, эритроциты):
Ац + Н2О +NAD+ ацетат + NADH+H+
Слайд 52*
доцент Свергун В.Т.
Метабол. эффекты Э (100-150 г.)
Увеличение в цитоплазме
Ингибирование NAD-зависимых ДГ (ЦТК, ДЦ, окисление ЖК), что еще более увеличивает [NADH+H+] – лактат-ацидоз
окисления ЖК и синтеза эндогенных ТГ – жировая инфильтрация и дегенерация внутр. органов (жировая печень, тигровое сердце и др.)
Активация продукции и окисления эндогенного сукцината
Слайд 53*
доцент Свергун В.Т.
Метабол. эффекты Э (прод.)
Снижение скорости ТД и
Метаболизм этанола и высокая [NADH+H+ ] инициирует образование АФК и пероксидный стресс, ПОЛ – изменение вязкости мембран их повреждение, а также белков, ДНК и др.
Апоптоз, дегенеративные повреждение внутр. органов
Слайд 54*
доцент Свергун В.Т.
Метабол. механизмы формирования зависимости
Катехоламиновая эйфория
Снижение скорости потребления О2 появление – (низкоэнергетического состояния) - образование в Головном Мозге медиаторов торможения ГАМК, ГОМК
Взаимодействие Ац и биогенных аминов и образование морфиноподобных в-в (сальсолинол, β-карболины, тетрагидропапаверолины)
Слайд 56*
доцент Свергун В.Т.
Первичный метаболит этанола- токсичный ацетальдегид, в умеренных и
Лица, у которых длительно сохраняется высокий уровень ацетальдегида в крови
( метаболическая особенность- зависит от активности Альдегиддегидрогеназы) наблюдается крайне плохое самочувствие после приема алкоголя.
Это резко снижает вероятность его систематического употребления
Слайд 57*
доцент Свергун В.Т.
АДГ- метаболизирует примерно - 12 г
Ацетальдегид быстро разрушается под действием ацетальдегидегидрогеназы (АцДГ- митохон. фермент) и кодируется генетическим аллелем АлДГ 2-1.
10% азиатского населения( японцы, китайцы, корейцы) продуцируют только неактивную форму АлДГ,контролируемую ДОМИНАНТНЫМ аллелем АлДГ 2-2.
Поэтому у азиатского населения уровень ацетальдегида КРАЙНЕ ВЫСОК даже при употреблении небольших доз спирта и риск развития алкоголизма равен нулю
Слайд 58*
доцент Свергун В.Т.
40% азиатского населения- гетерозиготы ( их геном содержит
Уровень ацетальдегида у них умеренно повышен, и симптомы интоксикации после приема алкоголя более выражены
Риск развития алкоголизма меньше, чем у нормально метаболизирующих, но значительно ↑ ↑ ↑ ↑ ↑ при попадании в среду, где традиционно пьют
Слайд 59*
доцент Свергун В.Т.
Аллели, которые кодируют высокоэффективные формы
Кластер генов,кодирующих разные изоформы АДГ, располагается на 4-й хромосоме.
Полиморфизм характерен для всех генов АДГ
АДГ1А,
АДГ1В,
АДГ1С,
АДГ4,
АДГ5,
АДГ6,
АДГ7
Слайд 60*
доцент Свергун В.Т.
Некоторые из вариантов аллелей связывают
Некоторые варианты аллелей, кодирующие изоформы АДГ1В и АДГ1С,
обеспечивают образование белков с исключительно высокой ферментативной активностью и снижают риск развития алкоголизма
У жителей Азии часто встречаются комбинации более эффективной АДГ и менее эффективной АлДГ
Слайд 61*
доцент Свергун В.Т.
Метабол. механизмы формирования зависимости
1. Истощение и нарушение
2.Гипогликемия из-за алиментарных нарушений и торможения ГНГ
3.Снижение продукции половых гормонов импотенция у мужчин и фригидность у женщин (депрессия)








![*доцент Свергун В.Т. 3ФГА затем окисляется ферментом -глицеральдегид-З-фосфатдегидрогеназой [6] с образованием NADH + H+Процесс называется](/img/tmb/6/510681/0a159600302cdf35196e770ca3512233-800x.jpg)
![*доцент Свергун В.Т. 3ФГА затем окисляется ферментом -глицеральдегид-З-фосфатдегидрогеназой [6] с образованием NADH + H+Процесс называется](/img/tmb/6/510681/993558700c7d4fda9bf4d9b9caaf211f-800x.jpg)
![*доцент Свергун В.Т. На следующей стадии (катализируе-мой фосфоглицераткиназой [7]) перенос фосфата этого соединения сопряжен](/img/tmb/6/510681/fd5e8aca6e74f8c94ee817e8adbc2d30-800x.jpg)
![*доцент Свергун В.Т. Следующие реакции -изомеризации 3-ФГК, полученного в результате реакции [7], в 2-фосфоглицерат (фермент:](/img/tmb/6/510681/6df121e4afb1bc19e05c09e1103d55c5-800x.jpg)
![*доцент Свергун В.Т. и последующего отщепления воды (фермент: енолаза - лиаза[9]) Продукт представляет собой сложный](/img/tmb/6/510681/7b14d6a2cc3fbc92d5f4516b875b4fe7-800x.jpg)
![*доцент Свергун В.Т. На предпоследней стадии, которая катализируется пируваткиназой [10], образуются ПВК и АТФ.](/img/tmb/6/510681/eaba9a63d11e6611c160526885dc7505-800x.jpg)











![*доцент Свергун В.Т. Метабол. эффекты Э (100-150 г.) Увеличение в цитоплазме и Мтх [Ацетальдегида], [NADH+H+](/img/tmb/6/510681/09b18e477765f3b34437a5d1cccf7356-800x.jpg)