- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Острые лейкозы презентация
Содержание
- 1. Острые лейкозы
- 2. ОСТРЫЙ ЛЕЙКОЗ ≥20% бластов в крови или
- 3. КЛИНИЧЕСКАЯ КАРТИНА Пролиферация опухолевого клона Нейтропения
- 4. ЭКСТРАМЕДУЛЯРНЫЕ ПОРАЖЕНИЯ По мере развития ОЛ клетки
- 7. ОСТРЫЕ ЛЕЙКОЗЫ Миелоидные (нелимфобластные) Лимфобластные
- 9. КЛИНИЧЕСКИЕ ФАЗЫ И СТАДИИ Активная фаза Ремиссия Минимальная остаточная болезнь Рецидив
- 10. ОМЛ Одна мутировавшая клетка дает после деления
- 11. ЭПИДЕМИОЛОГИЯ Заболеваемость ОЛ составляет в среднем 5
- 12. ЭТИОЛОГИЯ По всей вероятности, существует комплекс
- 13. ПАТОГЕНЕЗ
- 14. ПАТОГЕНЕЗ Блок дифференцировки клетки-предшественника того или иного
- 15. группа острых миелобластных лейкозов возникших
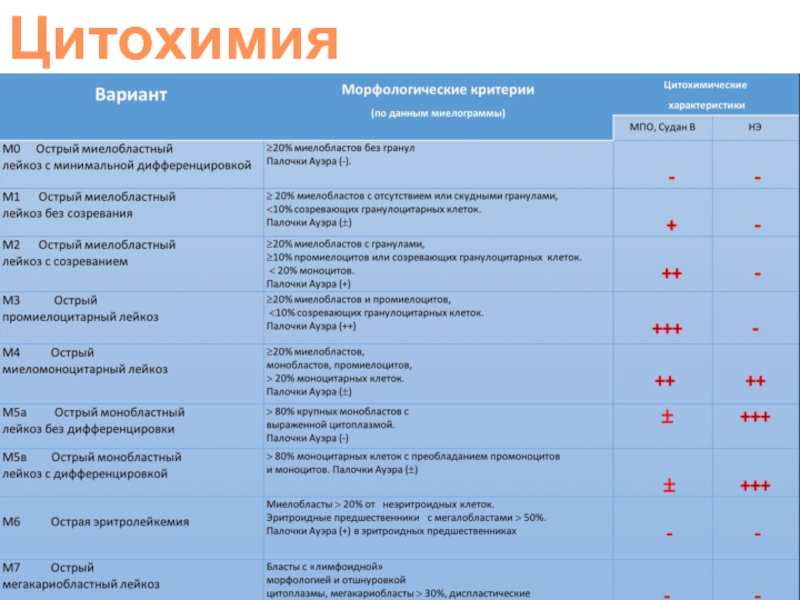
- 16. КЛАССИФИКАЦИЯ ОМЛ FAB ВОЗ
- 17. FAB классификация 1976
- 18. Цитохимическая диагностика AML Пероксидаза является лизосомальным
- 19. Диффузно-гранулярная PAS-реакция в бластах (М5). РАS-реакция
- 20. МОРФОЛОГИЯ Для диагностики ОМЛ необходимо выявление 20%
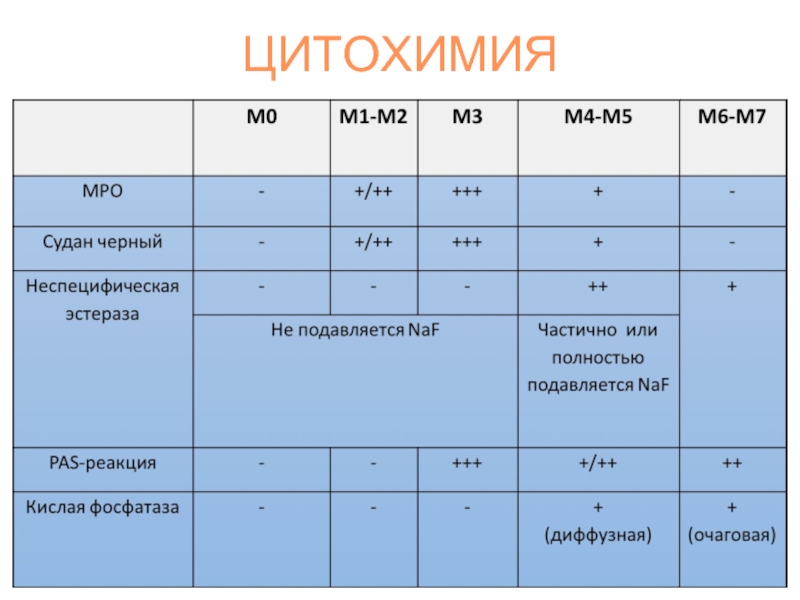
- 21. ЦИТОХИМИЯ
- 22. Цитохимия
- 23. FAB классификация 1982
- 24. Классификация ОМЛ (FAB 1976-85 гг.)
- 25. WHO 2008 г Основана на:
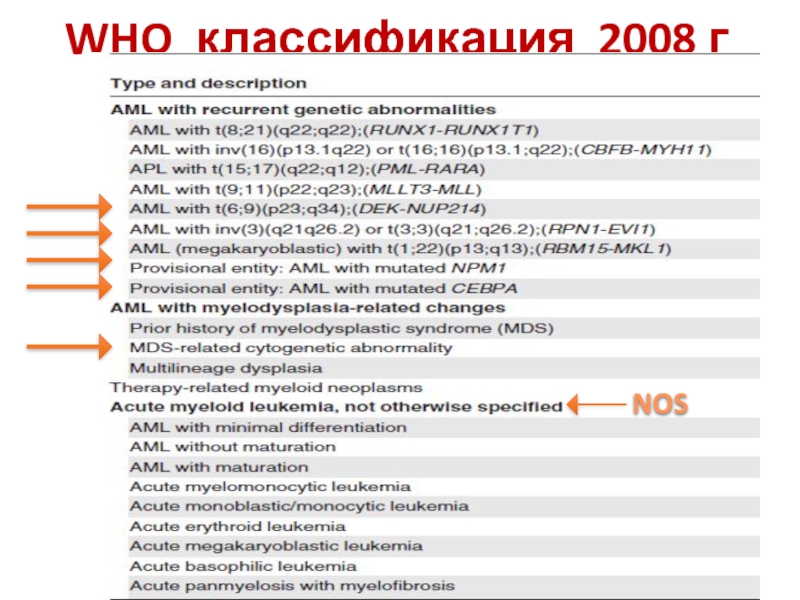
- 26. WHO классификация 2008 г NOS
- 27. ГРУППЫ РИСКА ОМЛ Цитогенетические поломки Мутации Ответ
- 28. ГРУППЫ ЦИТОГЕНЕТИЧЕСКОГО РИСКА Recommendations from an international
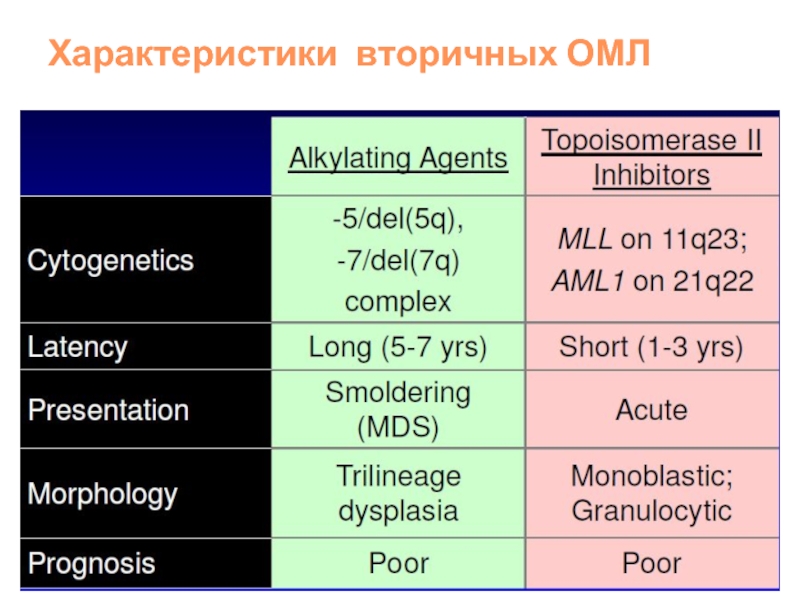
- 29. Характеристики вторичных ОМЛ
- 30. Лабораторно - инструментальные исследования перед началом
- 31. ТЕРАПЕВТИЧЕСКАЯ ТАКТИКА Индукция ремиссии Постремиссионный этап
- 32. ПРИНЦИПЫ ТЕРАПИИ Комбинация Ara-C и даунорубицина Высокие
- 33. ВОЗРАСТ
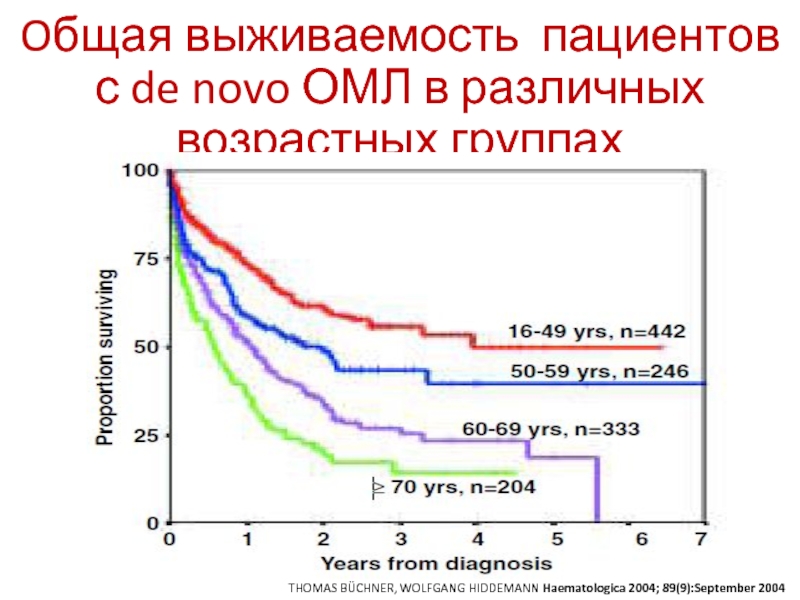
- 34. Oбщая выживаемость пациентов с de novo ОМЛ
- 35. ОСТРЫЕ ЛИМФОБЛАСТНЫЕ ЛЕЙКОЗЫ
- 37. ЭПИДЕМИОЛОГИЯ США 1,6 случаев на 100000
- 38. КЛИНИЧЕСКАЯ КАРТИНА Лейкоцитоз (лейкопения), тромбоцитопения, анемия В-симптомы
- 39. ДИАГНОСТИКА ОЛЛ Морфологическое и цитохимическое исследования
- 40. КЛАССИФИКАЦИЯ FAB, 1976 г. – морфологические критерии
- 41. КЛАССИФИКАЦИЯ ВОЗ, 2016
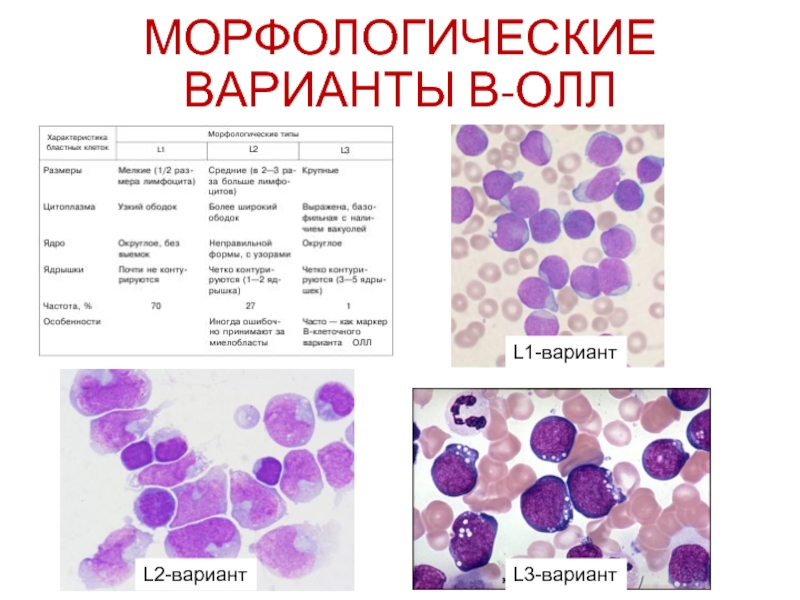
- 42. МОРФОЛОГИЧЕСКИЕ ВАРИАНТЫ В-ОЛЛ L3-вариант L1-вариант L2-вариант
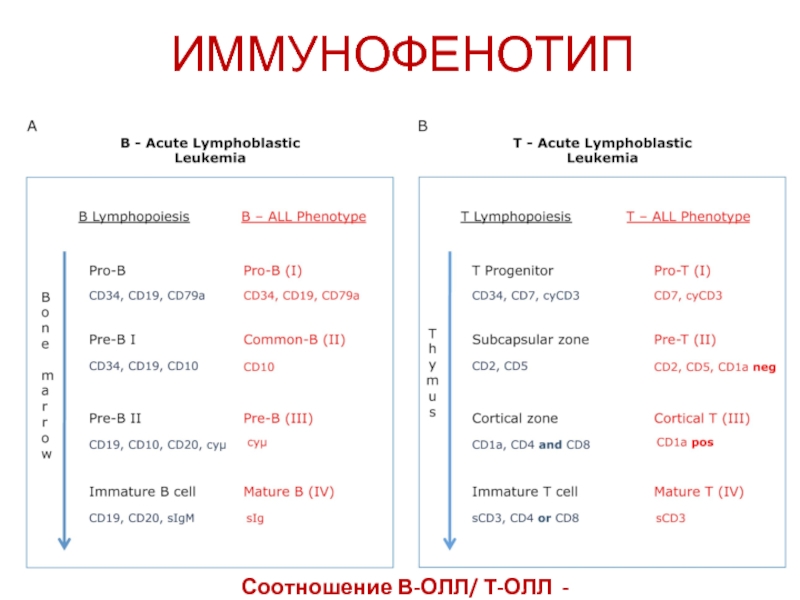
- 43. ИММУНОФЕНОТИП Соотношение В-ОЛЛ/ Т-ОЛЛ - 3/1
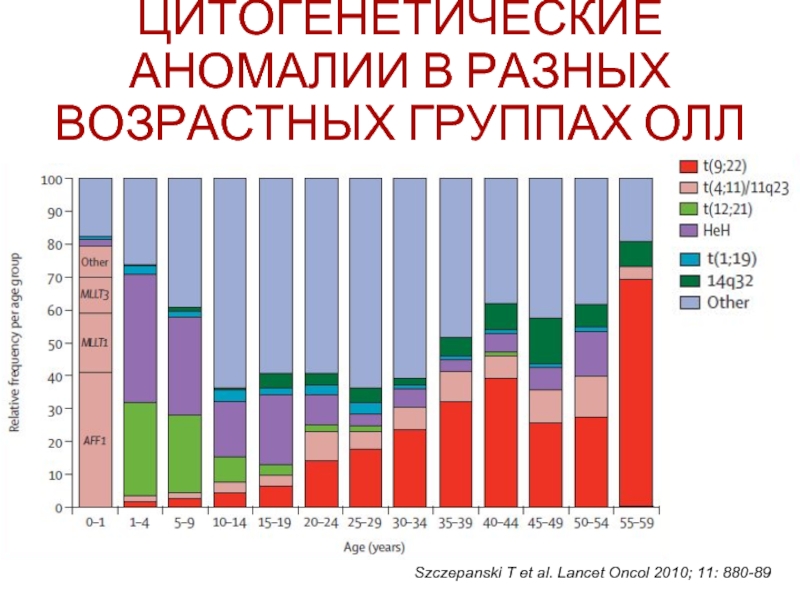
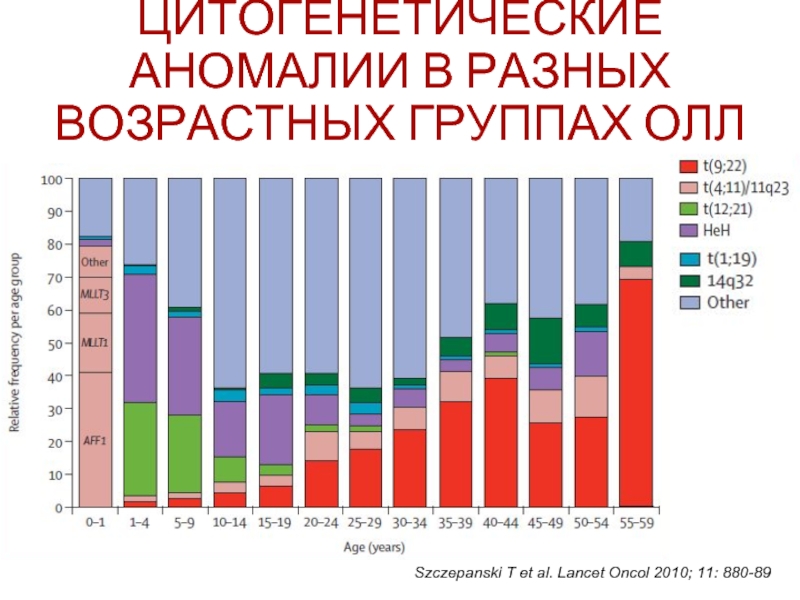
- 44. ЦИТОГЕНЕТИЧЕСКИЕ АНОМАЛИИ В РАЗНЫХ ВОЗРАСТНЫХ ГРУППАХ ОЛЛ
- 45. ПРОГНОСТИЧЕСКИЕ ФАКТОРЫ СТРАТИФИКАЦИЯ НА ГРУППЫ РИСКА Группа
- 46. СТРАТЕГИЯ ТЕРАПИИ ОЛЛ
- 47. ТЕРАПИЯ ОЛЛ Химиотерапевтическое воздействие Мониторинг
- 48. ПОЛИХИМИОТЕРАПИЯ ОЛЛ исторически 3 основных принципа КУРСЫ РЕИНДУКЦИИ повтор модифицированной индукционной терапии
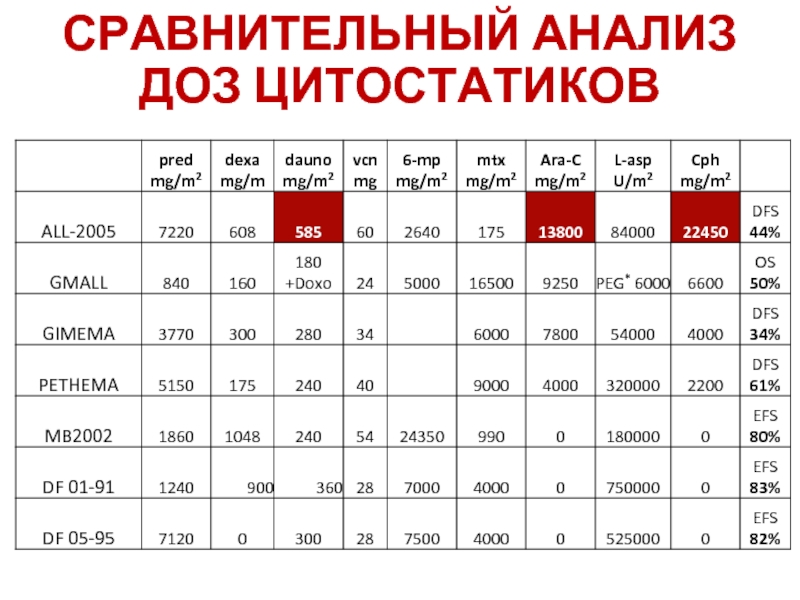
- 49. СРАВНИТЕЛЬНЫЙ АНАЛИЗ ДОЗ ЦИТОСТАТИКОВ
- 50. Основной принцип терапии ОЛЛ – непрерывность лечения
- 51. ИНДУКЦИЯ смена глюкокортикостероидной терапии в зависимости
- 52. КОНСОЛИДАЦИЯ И РЕИНДУКЦИЯ общая продолжительность лечения с
- 53. Консолидация и Реиндукция основы курсов химиотерапии:
- 54. ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ непрерывная терапия антиметаболитами с короткими
- 55. на протяжении всей терапии (2,5 года) необходимо
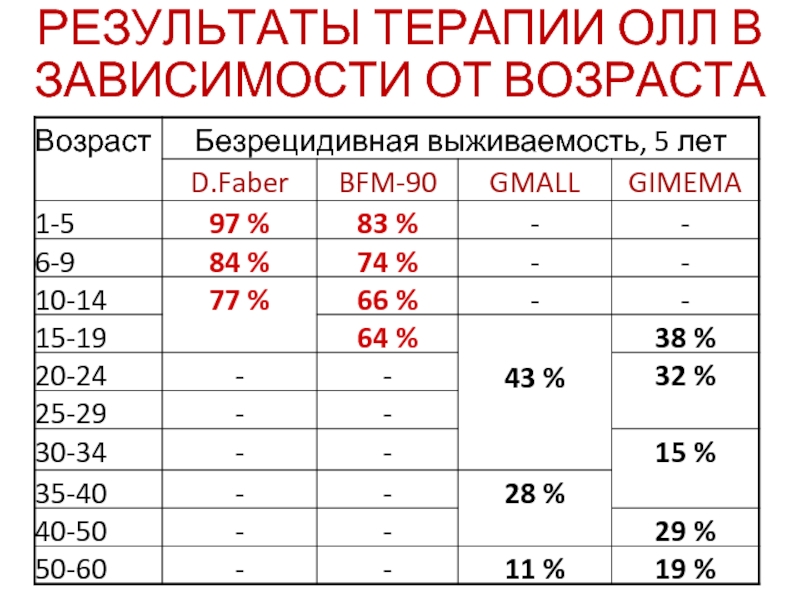
- 56. РЕЗУЛЬТАТЫ ТЕРАПИИ ОЛЛ В ЗАВИСИМОСТИ ОТ ВОЗРАСТА
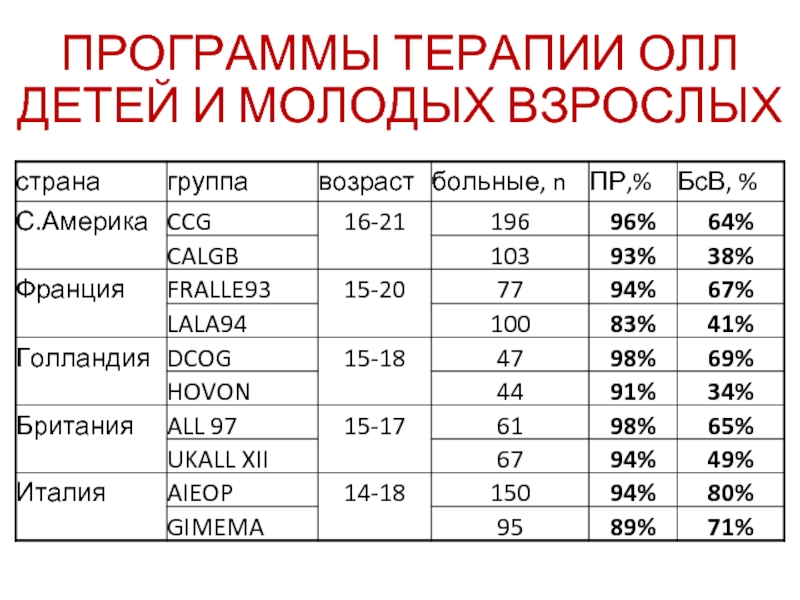
- 57. ПРОГРАММЫ ТЕРАПИИ ОЛЛ ДЕТЕЙ И МОЛОДЫХ ВЗРОСЛЫХ
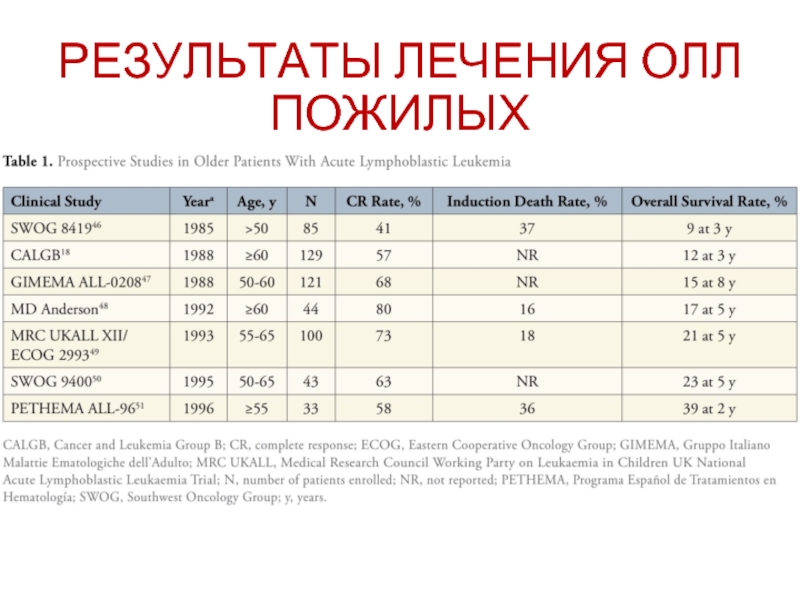
- 58. РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ ОЛЛ ПОЖИЛЫХ
- 59. Ph+ ОСТРЫЕ ЛИМФОБЛАСТНЫЕ ЛЕЙКОЗЫ
- 60. ЦИТОГЕНЕТИЧЕСКИЕ АНОМАЛИИ В РАЗНЫХ ВОЗРАСТНЫХ ГРУППАХ ОЛЛ
- 61. РЕЗУЛЬТАТЫ ТЕРАПИИ Ph+ ОЛЛ ДО ЭРЫ
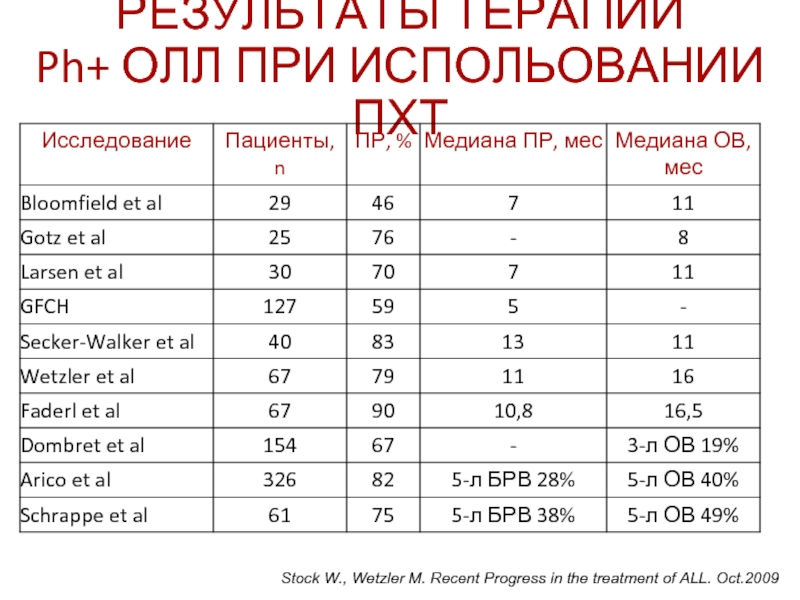
- 62. РЕЗУЛЬТАТЫ ТЕРАПИИ Ph+ ОЛЛ ПРИ ИСПОЛЬОВАНИИ
- 63. ИМАТИНИБ В ТЕРАПИИ Ph+ ОЛЛ Увеличение ПР
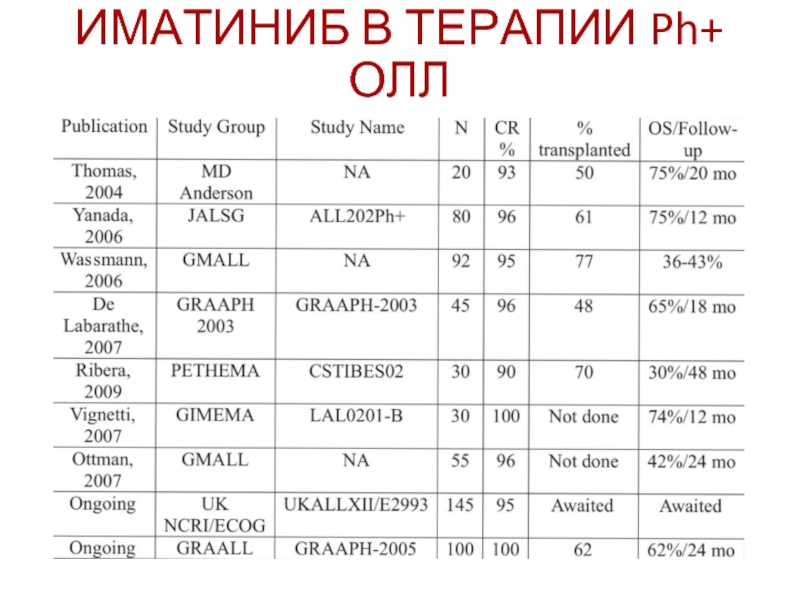
- 64. ИМАТИНИБ В ТЕРАПИИ Ph+ ОЛЛ
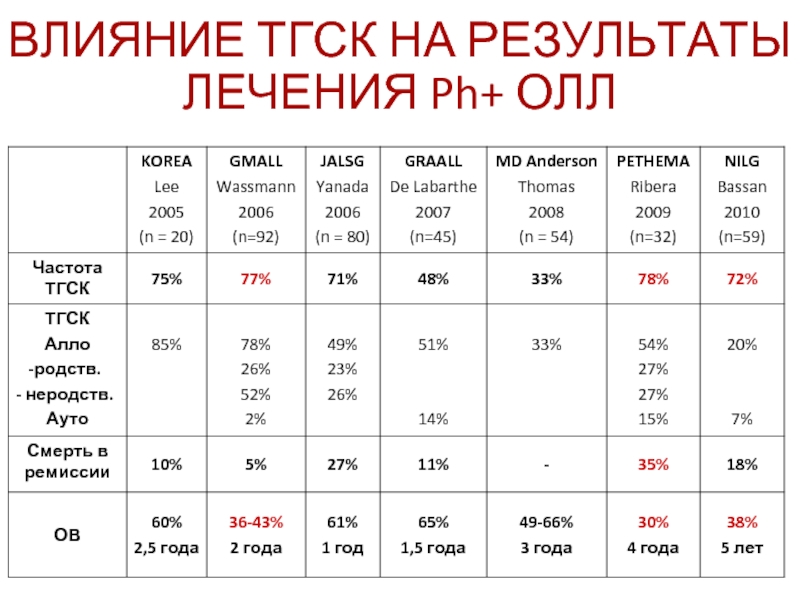
- 65. ВЛИЯНИЕ ТГСК НА РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ Ph+ ОЛЛ
Слайд 2ОСТРЫЙ ЛЕЙКОЗ
≥20% бластов в крови или костном мозге
Количество лейкоцитов крови ↑↓
При низком количестве лейкоцитов бласты в периферической крови могут не обнаруживаться
Обычно в гемограмме:
Лейкоцитоз, бластемия
Нейтропения, hiatus keukemicus
Нормохромная анемия
Тромбоцитопения
Слайд 3КЛИНИЧЕСКАЯ КАРТИНА
Пролиферация опухолевого клона
Нейтропения
Тромбоцитопения
Анемия
Инфильтрация органов
Опухолевая интоксикация
Лейкостаз
Геморрагический синдром (ДВС)
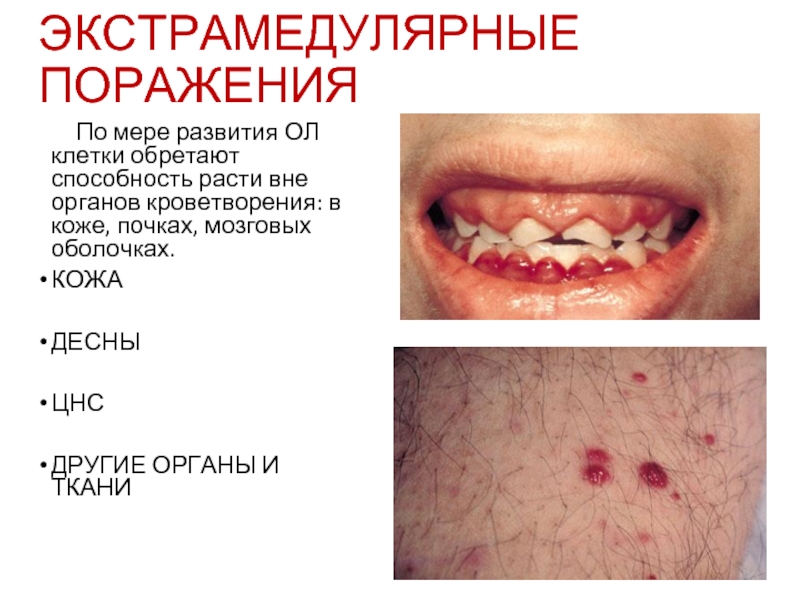
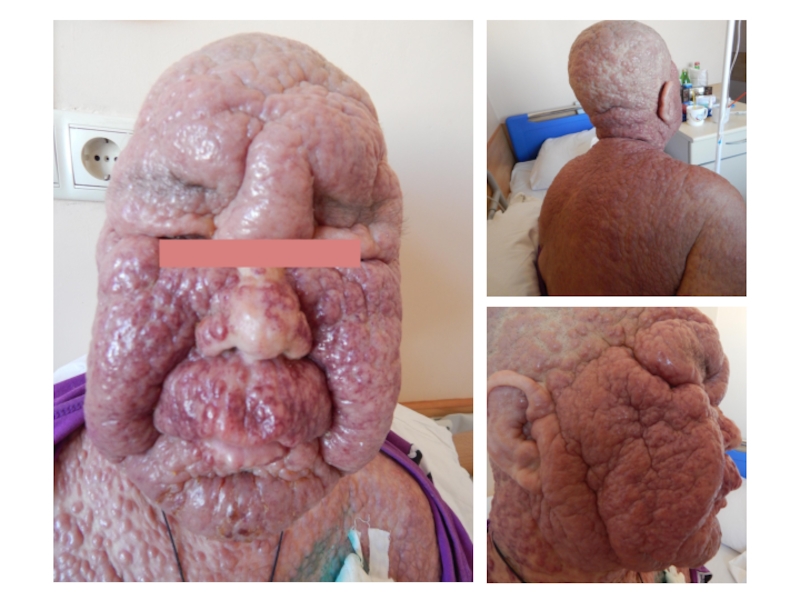
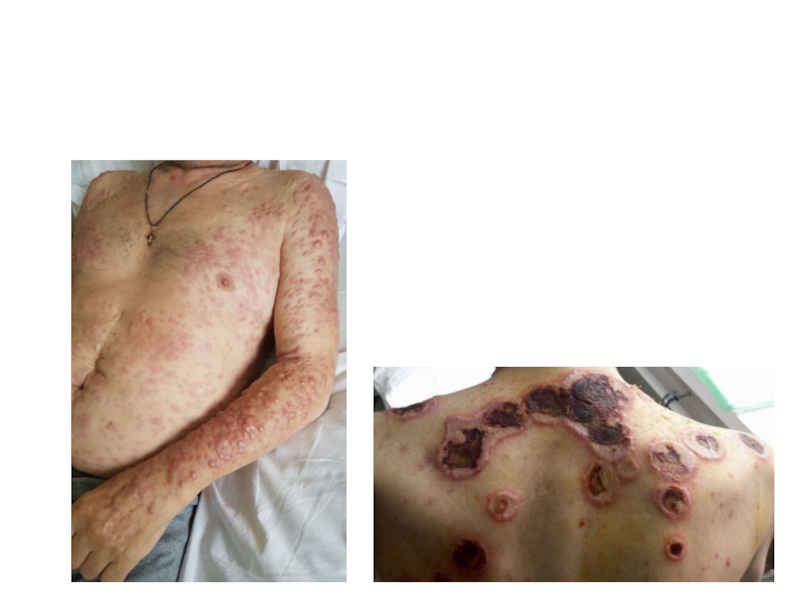
Слайд 4ЭКСТРАМЕДУЛЯРНЫЕ ПОРАЖЕНИЯ
По мере развития ОЛ клетки обретают способность расти вне органов
КОЖА
ДЕСНЫ
ЦНС
ДРУГИЕ ОРГАНЫ И ТКАНИ
Слайд 10ОМЛ
Одна мутировавшая клетка дает после деления огромное количество клеток (за 3
Слайд 11ЭПИДЕМИОЛОГИЯ
Заболеваемость ОЛ составляет в среднем 5 случаев на 100 000 населения
75% всех случаев диагностируется у взрослых.
среднее соотношение ОМЛ и ОЛЛ составляет 6:1.
Встречаемость ОМЛ 2,7 на 100 000 населения и увеличивается с возрастом:
дети 6-8 случаев на 1 000 000 населения в год
взрослые 12-20 случаев на 1 000 000 населения в год
пожилые 40-60 случаев на 1 000 000 населения в год
Средний возраст больных данным заболеванием составляет 65 лет.
Выявлено, что вероятность развития лейкоза
у 50-летнего человека составляет 1 к 50000
у 70-летнего - 1 к 7000.
Острый миелоидный лейкоз наиболее распространен среди мужчин. У женщин данное заболевание встречается намного реже.
Слайд 12ЭТИОЛОГИЯ
По всей вероятности, существует комплекс причин, приводящих к развитию лейкоза.
Хромосомные
ионизирующего излучения
электромагнитного поля
химических веществ (бензин, пестициды, гербециды)
химио- и радиотерапии по поводу других опухолей
курение (Ряд исследователей предполагает, что около 20% ОМЛ являются следствием курения)
Генетические заболевания: синдром Дауна, анемия Фанкони, атаксия-телеангиоэктазия, синдром Вискотта-Олдрича, нейрофиброматоз, синдром Кляйнфельтера, синдром Патау, синдром Швахмана, синдром Костмана.
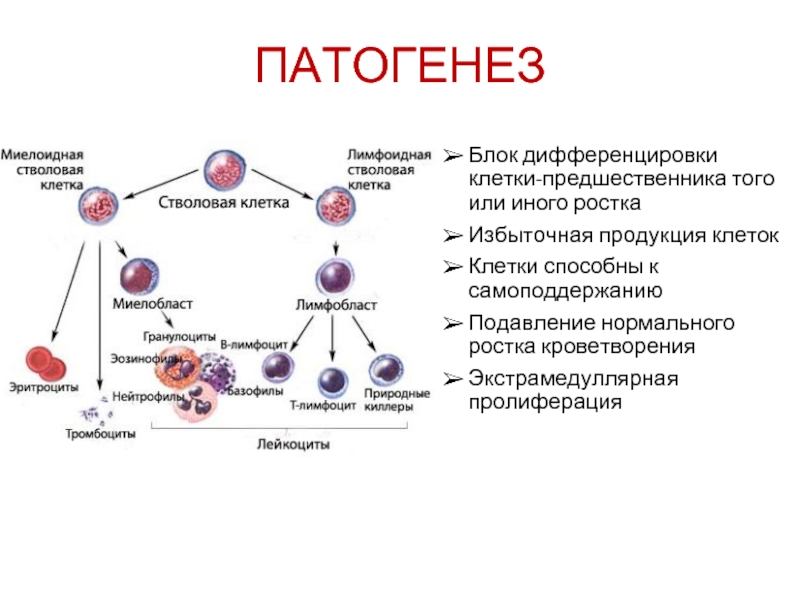
Слайд 14ПАТОГЕНЕЗ
Блок дифференцировки клетки-предшественника того или иного ростка
Избыточная продукция клеток
Клетки способны к
Подавление нормального ростка кроветворения
Экстрамедуллярная пролиферация
Слайд 15 группа острых миелобластных лейкозов возникших из клетки-предшественницы миелопоэза различаются
морфологическими
цитохимическими
иммунофенотипическими
цитогенетическими
молекулярно-биологическими характеристиками.
Слайд 17FAB классификация 1976
основана на:
морфологии
цитохимических характеристиках
(
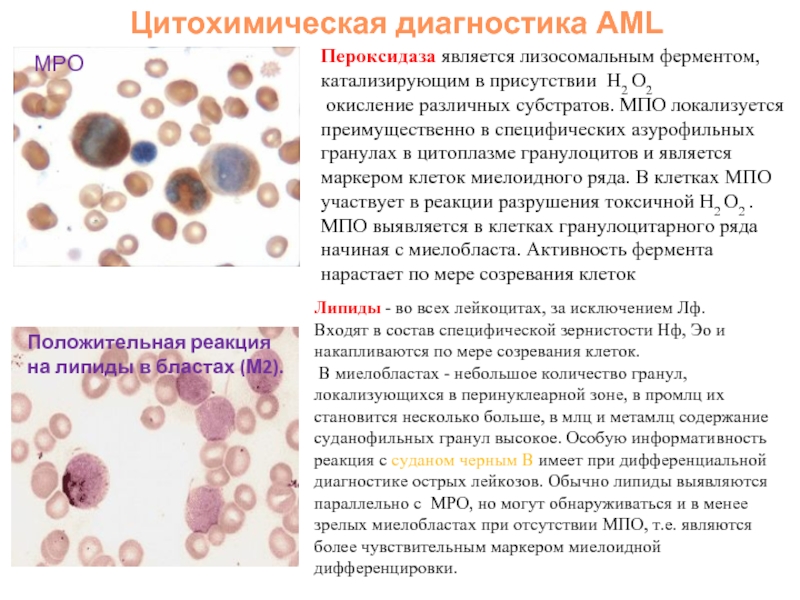
Слайд 18Цитохимическая диагностика AML
Пероксидаза является лизосомальным ферментом, катализирующим в присутствии H2
окисление различных субстратов. МПО локализуется преимущественно в специфических азурофильных гранулах в цитоплазме гранулоцитов и является маркером клеток миелоидного ряда. В клетках МПО участвует в реакции разрушения токсичной H2 O2 . МПО выявляется в клетках гранулоцитарного ряда начиная с миелобласта. Активность фермента нарастает по мере созревания клеток
Липиды - во всех лейкоцитах, за исключением Лф.
Входят в состав специфической зернистости Нф, Эо и накапливаются по мере созревания клеток.
В миелобластах - небольшое количество гранул, локализующихся в перинуклеарной зоне, в промлц их становится несколько больше, в млц и метамлц содержание суданофильных гранул высокое. Особую информативность реакция с суданом черным В имеет при дифференциальной диагностике острых лейкозов. Обычно липиды выявляются параллельно с MPO, но могут обнаруживаться и в менее зрелых миелобластах при отсутствии МПО, т.е. являются более чувствительным маркером миелоидной дифференцировки.
Положительная реакция на липиды в бластах (М2).
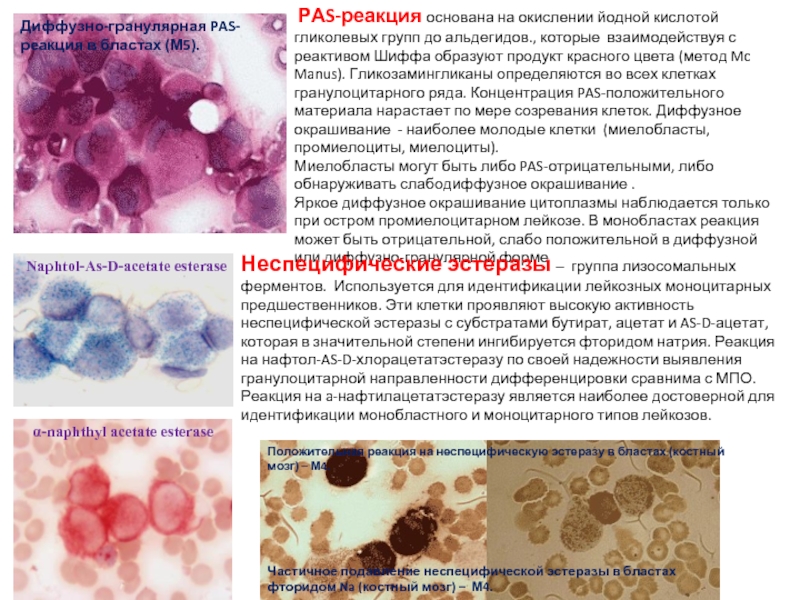
Слайд 19Диффузно-гранулярная PAS-реакция в бластах (М5).
РАS-реакция основана на окислении йодной кислотой
Миелобласты могут быть либо PAS-отрицательными, либо обнаруживать слабодиффузное окрашивание .
Яркое диффузное окрашивание цитоплазмы наблюдается только при остром промиелоцитарном лейкозе. В монобластах реакция может быть отрицательной, слабо положительной в диффузной или диффузно-гранулярной форме
Неспецифические эстеразы – группа лизосомальных ферментов. Используется для идентификации лейкозных моноцитарных предшественников. Эти клетки проявляют высокую активность неспецифической эстеразы с субстратами бутират, ацетат и AS-D-ацетат, которая в значительной степени ингибируется фторидом натрия. Реакция на нафтол-AS-D-хлорацетатэстеразу по своей надежности выявления гранулоцитарной направленности дифференцировки сравнима с МПО. Реакция на a-нафтилацетатэстеразу является наиболее достоверной для идентификации монобластного и моноцитарного типов лейкозов.
Положительная реакция на неспецифическую эстеразу в бластах (костный мозг) – М4.
Частичное подавление неспецифической эстеразы в бластах фторидом Na (костный мозг) – М4.
Слайд 20МОРФОЛОГИЯ
Для диагностики ОМЛ необходимо выявление 20% и более бластов в костном
Исключение: ОМЛ с t(15;17), t(8;21), inv(16) и некоторых случаев эритролейкемии. В этих случаях диагноз ОМЛ устанавливается на основании данных цитогенетики
Миелобласты, монобласты и мегакариобласты включаются в подсчет бластов.
В ОМЛ с моноцитоидной или миеломоноцитоидной дифференцировкой, монобласты и промоноциты считаются как эквивалент бластов.
Эритробласты не подсчитываются как бласты, кроме редких случаев эритроидной лейкемии.
Перерасчет процента бластов в костном мозге на неэритроидные ядросодержащие клетки производится, если процент ядросодержащих неэритроидных клеток достигает 50 или более.
Слайд 24
Классификация ОМЛ (FAB 1976-85 гг.)
M0 - острый недифференцированный лейкоз
М1 - острый
М2 -острый миелобластный лейкоз с признаками созревания, >10% зрелых, <20% моноцитов
M2baso – базофильно-клеточный
М3 - острый промиелоцитарный лейкоз
гранулярный вариант (М3)
гипогранулярный вариант (М3v)
М4 - острый миеломонобластный лейкоз моноцитов - >20% но <80%
M4eos – с >5% эзинофилией
М5 - острый монобластный лейкоз, монобластов >50%
М5а - монобластный без признаков созревания
М5b – монобластный с признаками созревания
М6 - острый эритробластный лейкоз (эритробласты ≥50% и миелобласты ≥30% от неэритроидных клеток)
М7 - острый мегакариобластный лейкоз
Слайд 25WHO 2008 г
Основана на:
-
- цитохимии
- иммунофенотипе
- ЦГ
-предшествующей истории
-молекулярной биологии
Слайд 27ГРУППЫ РИСКА
ОМЛ
Цитогенетические поломки
Мутации
Ответ на лечение
Вторичный ОЛ
ОЛЛ
1) возраст
2) гиперлейкоцитоз
3) Иммунофенотип
4) цитогенетика
5) ответ
6) коэкспрессия миелоидных маркеров
7) нейролейкоз
Слайд 28ГРУППЫ ЦИТОГЕНЕТИЧЕСКОГО РИСКА
Recommendations from an international expert panel on behalf of
Слайд 30
Лабораторно - инструментальные исследования перед началом лечения ОМЛ
Миелограмма (+ клеточность).
Цитохимическое исследование костного мозга (пероксидаза, гликоген, альфа- нафтилэстераза, PAS реакция)
Цитогенетическое исследование костного мозга
Молекулярно-генетическое исследование
Иммунофенотипирование костного мозга
Клинический анализ крови + Ретикулоциты, СОЭ
Биохимическое исследование
Коагулограмма
Микробиологическое, вирусологическое , серологическое исследование
12-канальное ЭКГ, ЭХО – КГ
УЗИ органов брюшной полости
Рентгенограмма грудной клетки\ КТ органов грудной клетки
Общий анализ мочи
Анализ крови на Ф-50, RW, HBs Ag, antiHCV
Группа крови, Rh, определение аутоантител к эритроцитам
Для женщин детородного возраста – тест на беременность.
Диагностическая люмбальная пункция. (гиперлейкоцитоз, М4-М5 варианты ОМЛ по FAB- классификации – лечебно-диагностическая)
Оценка ECOG-статуса, индекса коморбидности.
УЗДГ сосудов шеи и подключичных сосудов (при наличии в анамнезе катетеризации центральных вен или указаний на анатомические особенности)
HLA-типирование
Слайд 31ТЕРАПЕВТИЧЕСКАЯ ТАКТИКА
Индукция ремиссии
Постремиссионный этап
Консолидация ремиссии
Поддерживающая терапия
Терапия рецидива
терапия молекулярного рецидива
Слайд 32ПРИНЦИПЫ ТЕРАПИИ
Комбинация Ara-C и даунорубицина
Высокие дозы Ara-C
Аллогенная трансплантация костного мозга
Максимальная эрадикация-
Контроль- количественный PCR
Слайд 34Oбщая выживаемость пациентов с de novo ОМЛ в различных возрастных группах
THOMAS
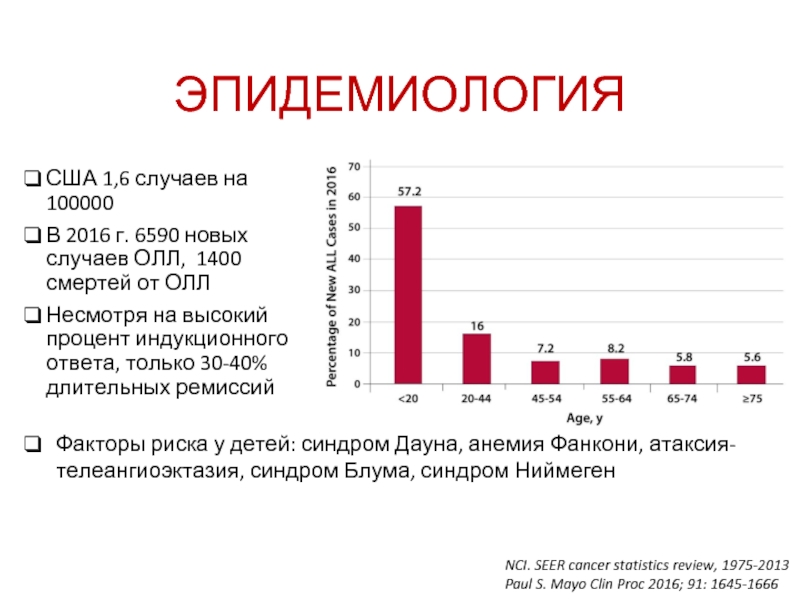
Слайд 37ЭПИДЕМИОЛОГИЯ
США 1,6 случаев на 100000
В 2016 г. 6590 новых случаев
Несмотря на высокий процент индукционного ответа, только 30-40% длительных ремиссий
NCI. SEER cancer statistics review, 1975-2013
Paul S. Mayo Clin Proc 2016; 91: 1645-1666
Факторы риска у детей: синдром Дауна, анемия Фанкони, атаксия-телеангиоэктазия, синдром Блума, синдром Ниймеген
Слайд 38КЛИНИЧЕСКАЯ КАРТИНА
Лейкоцитоз (лейкопения), тромбоцитопения, анемия
В-симптомы
Инфекционные осложнения, геморрагический синдром
Лимфаденопатия
Спленомегалия и /или гепатомегалия
Нейролейкемия (оболочки, реже ЧМН) 5-8%
Вовлечение медиастинальных лимфоузлов, синдром ВПВ (Т-ОЛЛ)
Яички
Слайд 39ДИАГНОСТИКА ОЛЛ
Морфологическое и цитохимическое исследования
Иммунофенотипирование бластных клеток
Цитогенетическое исследование
Определение маркеров минимальной резидуальной болезни (МРБ)
Слайд 40КЛАССИФИКАЦИЯ
FAB, 1976 г. – морфологические критерии (L1, L2, L3)
WHO, 1997 г.
WHO, 2008 г. – В-ОЛЛ
- В-ОЛЛ с доп хромосомными аномалиями
- Лейкоз Беркитта перенесен в лимфома/лейкоз Беркитта
Bennet J.M. Br J Haematol 1976;33: 451-458
Harris N. J Clin Oncol 1999; 17: 3835-3849
Vardiman J.W. Blood 2009; 114: 937-951
Arber D.A. Blood 2016; 127: 2391-2405
Слайд 44ЦИТОГЕНЕТИЧЕСКИЕ АНОМАЛИИ В РАЗНЫХ ВОЗРАСТНЫХ ГРУППАХ ОЛЛ
Szczepanski T et al. Lancet
Слайд 45ПРОГНОСТИЧЕСКИЕ ФАКТОРЫ
СТРАТИФИКАЦИЯ НА ГРУППЫ РИСКА
Группа риска
иммунофенотип common-В-ОЛЛ пре-пре-В,
пре-В-ОЛЛ, ранний Т-ОЛЛ,
тимический Т-ОЛЛ зрелый Т-ОЛЛ,
билинейный
лейкоциты В-ОЛЛ < 30 х 109/л > 30 x 109/л
лейкоциты Т-ОЛЛ < 100 х 109/л >100 х 109/л
ЛДГ < 960 ед > 960 ед
t (9;22), t (4;11) - +
% бластов в КМ / 7д < 25% > 25%
ремиссия 35 день > 35 дня
Слайд 47ТЕРАПИЯ ОЛЛ
Химиотерапевтическое воздействие
Мониторинг минимальной резидуальной болезни (МРБ)
Трансплантация стволовых
Тагетная терапия (моноклональные антитела)
Новые цитостатические препараты
Дифференцированные подходы лечения
Слайд 48ПОЛИХИМИОТЕРАПИЯ ОЛЛ
исторически 3 основных принципа
КУРСЫ РЕИНДУКЦИИ
повтор модифицированной индукционной терапии
Слайд 50Основной принцип терапии ОЛЛ – непрерывность лечения с модификацией доз цитостатических
Интенсивное применение L-аспаргиназы, дексаметазона, винкристина, метотрексата, пури-нетола (6-МР)
ПРИНЦИПЫ ТЕРАПИИ ОЛЛ
Слайд 51ИНДУКЦИЯ
смена глюкокортикостероидной терапии в зависимости от чувствительности опухолевых клеток. Низкая
ХТ воздействие во время восстановления КМ после агранулоцитоза с помощью ГКС + Аспарагиназы.
Слайд 52КОНСОЛИДАЦИЯ И РЕИНДУКЦИЯ
общая продолжительность лечения с момента начала индукции и до
низкодозное ежедневное воздействие на опухолевый клон
важна непрерывность терапии вместо агрессивной консолидации
фоновым препаратом является 6-МР с необходимой модифакации его дозы в зависимости от миелосупрессии
эффективность курсов реиндукции = необходимо на этапе постремиссионной терапии повторить курс терапии с ГКС, антрациклинами и винкристином
Слайд 53Консолидация и Реиндукция
основы курсов химиотерапии:
курс с Метотрексатом в высоких дозах
курс с Цитарабином в высоких дозах ?
курс с Циклофосфаном и Цитарабином (невысокодозным) на фоне Пуринетола
в течение всей консолидации около 6 введений ПЭГ-аспарагиназы
Желательно в первой линии терапии использование ПЭГ- аспарагиназы для уменьшения вероятности развития аллергической реакции
КОНСОЛИДАЦИЯ И РЕИНДУКЦИЯ
Слайд 54ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ
непрерывная терапия антиметаболитами с короткими пульсами дексаметазона
еженедельное применение метотрексата для
импульсное применение L-аспаргиназы, использование синергизма Аспарагиназы с Метотрексатом на фоне пури-нетола
длительная терапия Аспарагиназой для накопительной суммарной дозы
продолжительность поддерживающей терапии 2 года
Слайд 55на протяжении всей терапии (2,5 года) необходимо предусмотреть 15-16 интратекальных пункций
во
во время поддерживающей терапии профилактика нейролейкемии каждые 3 месяца
включать ли в профилактику нейролейкемии краниальное облучение? => Необходим анализ случаев нейрорецидивов
При использовании курсов с Метотрексатом и Цитарабином в высоких дозах от краниального облучения можно отказаться
ПРОФИЛАКТИКА НЕЙРОЛЕЙКЕМИИ
Слайд 60ЦИТОГЕНЕТИЧЕСКИЕ АНОМАЛИИ В РАЗНЫХ ВОЗРАСТНЫХ ГРУППАХ ОЛЛ
Szczepanski T et al. Lancet
Слайд 61РЕЗУЛЬТАТЫ ТЕРАПИИ
Ph+ ОЛЛ ДО ЭРЫ ИМАТИНИБА
Полная ремиссия ≈ 70%
Общая 5-летняя
Общая выживаемость при выполнении ТКМ ≈ 30-35%
Слайд 62РЕЗУЛЬТАТЫ ТЕРАПИИ
Ph+ ОЛЛ ПРИ ИСПОЛЬОВАНИИ ПХТ
Stock W., Wetzler M. Recent
Слайд 63ИМАТИНИБ В ТЕРАПИИ Ph+ ОЛЛ
Увеличение ПР с 65-75% до 95%
Повышение количества
Снижение смертности в индукции
Смертность в ПР 5-16%
Как ТГСК изменяет результаты терапии?