- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основы противоопухолевой химиотерапии презентация
Содержание
- 1. Основы противоопухолевой химиотерапии
- 2. Определения Карциномы — злокачественные опухоли, происходящие из
- 3. Основные свойства опухолевой клетки Опухолевая прогрессия —
- 4. Регуляция клеточного цикла и ее нарушения в опухолевых клетках
- 5. Периоды клеточного цикла G1 (9 ч). Увеличение размеров
- 6. Регуляция клеточного цикла: циклинзависимые киназы Молекула киназы
- 7. Регуляция клеточного цикла: сигнальные пути Сигнальные пути
- 8. Механизм действия комплексов «циклин-Cdk» Комплексы G1-фазы обеспечивают:
- 9. Нарушения контроля клеточного цикла в опухолевых клетках
- 10. Регуляция апоптоза и ее нарушения в опухолевых клетках
- 11. Апоптоз: биологическая роль Уничтожение дефектных клеток. Уничтожение
- 12. Апоптоз: пусковые факторы Апоптоз «изнутри» Чрезмерные (нерепарируемые)
- 13. Эффекторы апоптоза Каспазы. Сериновые протеазы, разрывают пептидные
- 14. Примерная схема апоптоза 1. Повреждение хромосом или мембран.
- 15. Изменения регуляции апоптоза в опухолевых клетках Потеря
- 16. Основные группы противоопухолевых препаратов
- 17. Основные пути поиска и разработки новых противоопухолевых
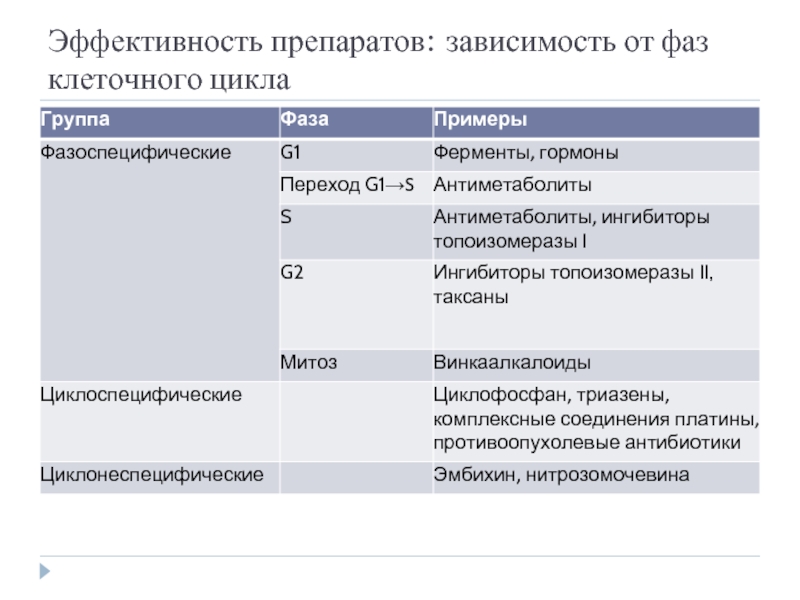
- 18. Классификация противоопухолевых препаратов Алкилирующие агенты Антиметаболиты Противоопухолевые
- 19. 1. Алкилирующие агенты Механизм действия: образуют положительно
- 20. Алкилирующие агенты: хлорэтиламины Сернистый иприт, sulfur mustard
- 21. Алкилирующие агенты: этиленимины Тиофосфамид (тиотэф), 1950 г. Гексаметилмеламин (алтретамин), 1960-е гг.
- 22. Алкилирующие агенты: эфиры алкилсульфокислот Бусульфан,
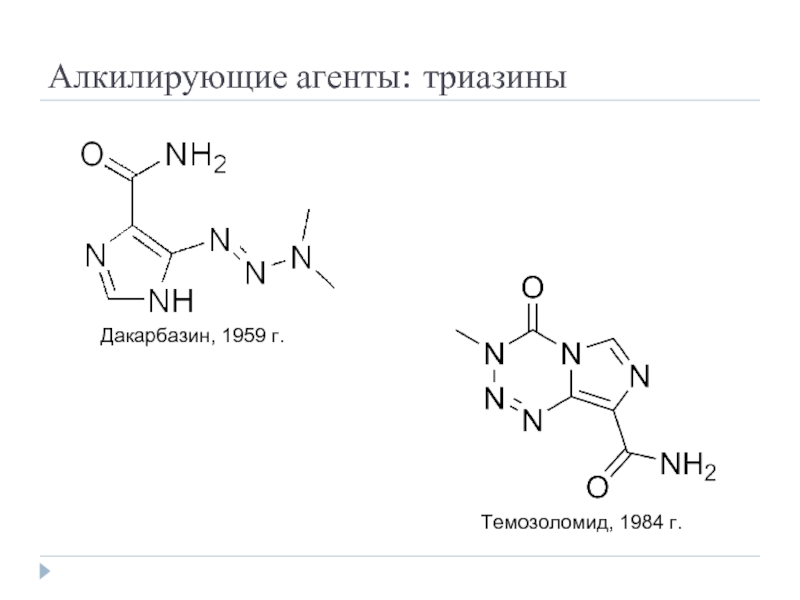
- 23. Алкилирующие агенты: триазины Дакарбазин, 1959 г. Темозоломид, 1984 г.
- 24. Алкилирующие агенты: производные нитрозомочевины Нитрозометилмочевина, 1878 г.
- 25. Алкилирующие агенты: комплексные соединения платины Цисплатин, 1968 г. Карбоплатин Оксалиплатин Сатраплатин, 1993 г.
- 26. 2. Антиметаболиты Механизм действия: клетки их не
- 27. Антиметаболиты фолиевой кислоты Метотрексат, 1947 г., Ингибирует
- 28. Антиметаболиты пуринов 6-меркаптопурин. Серосодержащий аналог гипоксантина. Флударабин. Производное аденина
- 29. Антиметаболиты пиримидинов 5-фторурацил, 1957 г. Метаболизируется
- 30. Антиметаболиты пиримидинов-2 Капецитабин 1995 г. «Селективно-активируемая»
- 31. Антиметаболиты пиримидинов-3: аналоги цитидина Цитозин-арабинозид, 1961 г. Гемцитабин, 1988 г.
- 32. 3. Противоопухолевые антибиотики Механизм действия: до конца не изучен Интеркаляторы Ингибиторы топоизомеразы II
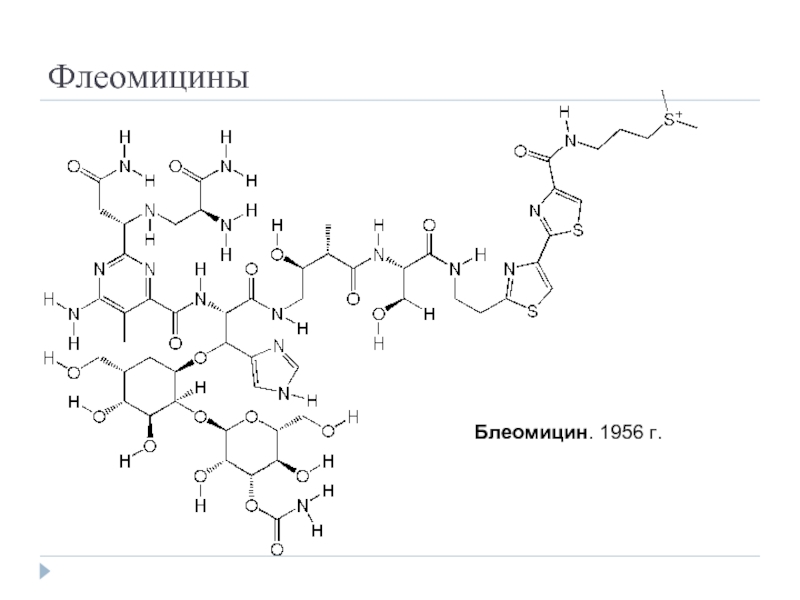
- 33. Флеомицины Блеомицин. 1956 г.
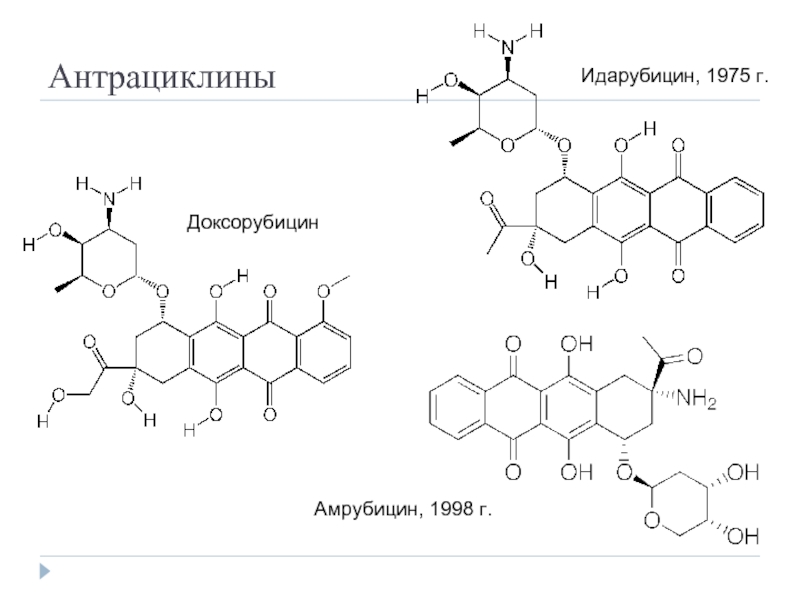
- 34. Антрациклины Доксорубицин Идарубицин, 1975 г. Амрубицин, 1998 г.
- 35. 4. Ферментные препараты Механизм действия: ферменты, расщепляющие
- 36. L-аспарагиназа
- 37. 5. Препараты растительного происхождения Механизм действия:
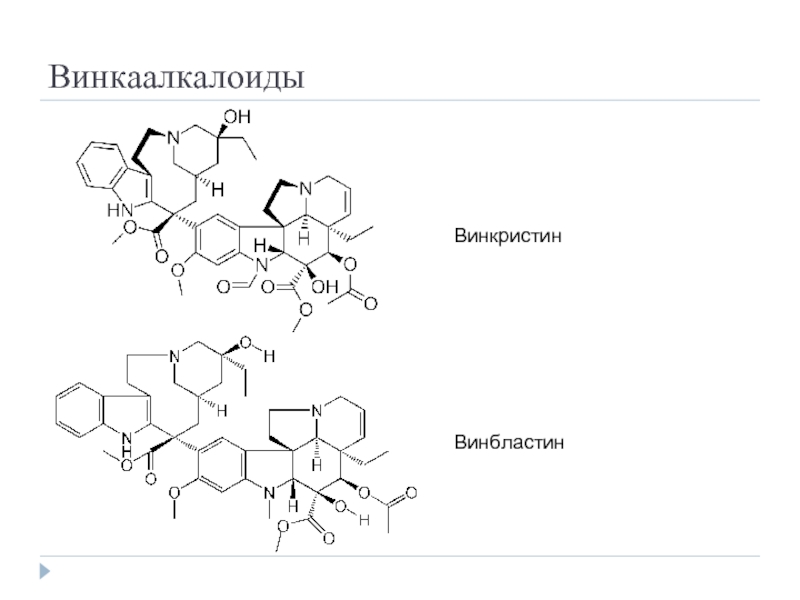
- 38. Винкаалкалоиды Винкристин Винбластин
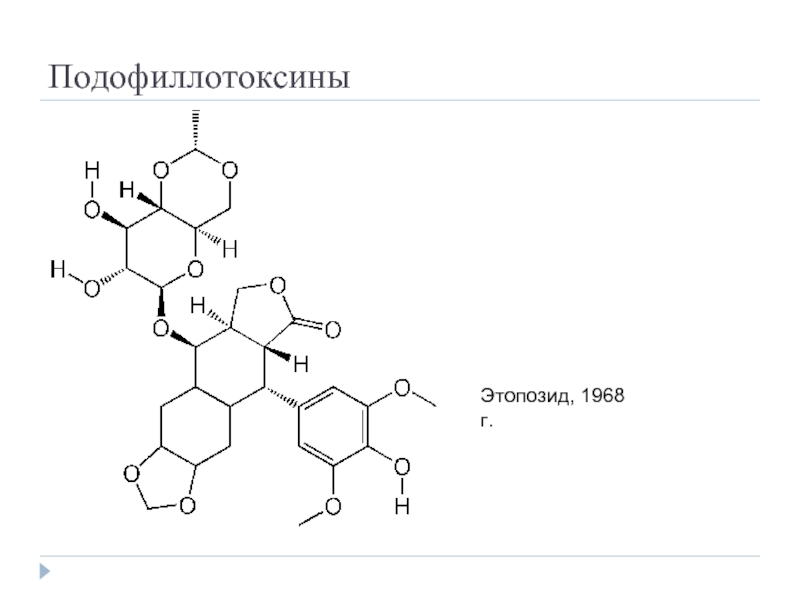
- 39. Подофиллотоксины Этопозид, 1968 г.
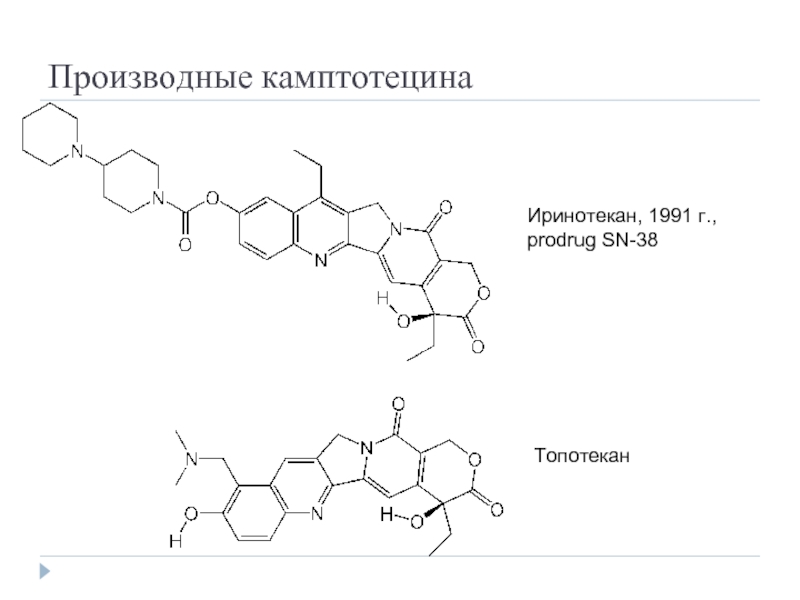
- 40. Производные камптотецина Иринотекан, 1991 г., prodrug SN-38 Топотекан
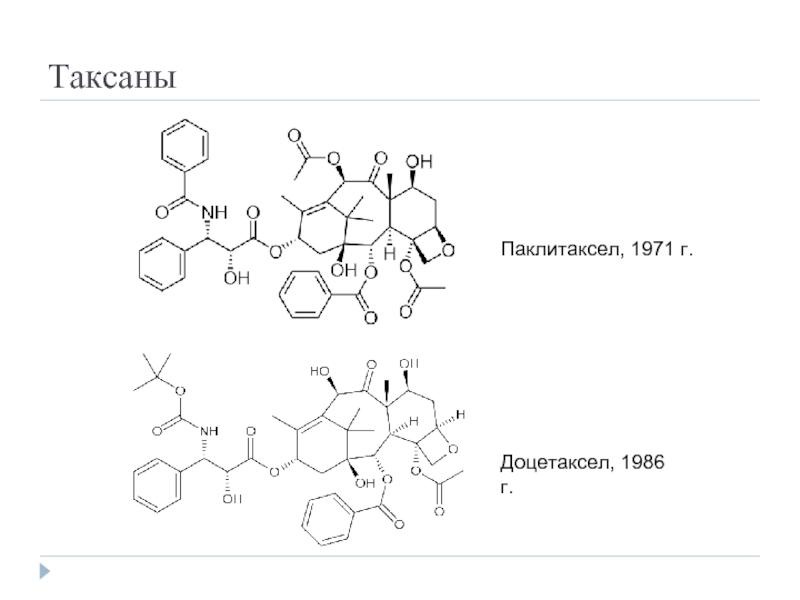
- 41. Таксаны Паклитаксел, 1971 г. Доцетаксел, 1986 г.
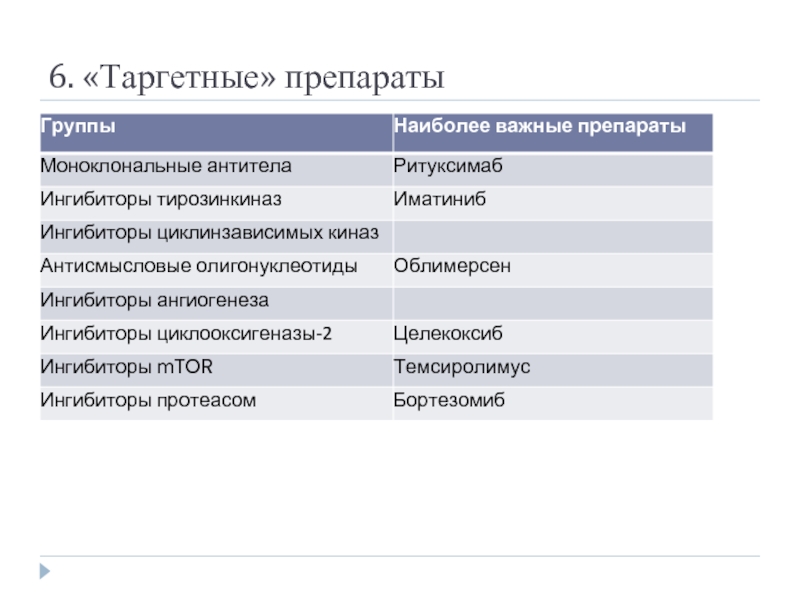
- 42. 6. «Таргетные» препараты
- 43. Моноклональные антитела Механизм действия Комплемент-зависимая цитотоксичность Антитело-зависимая
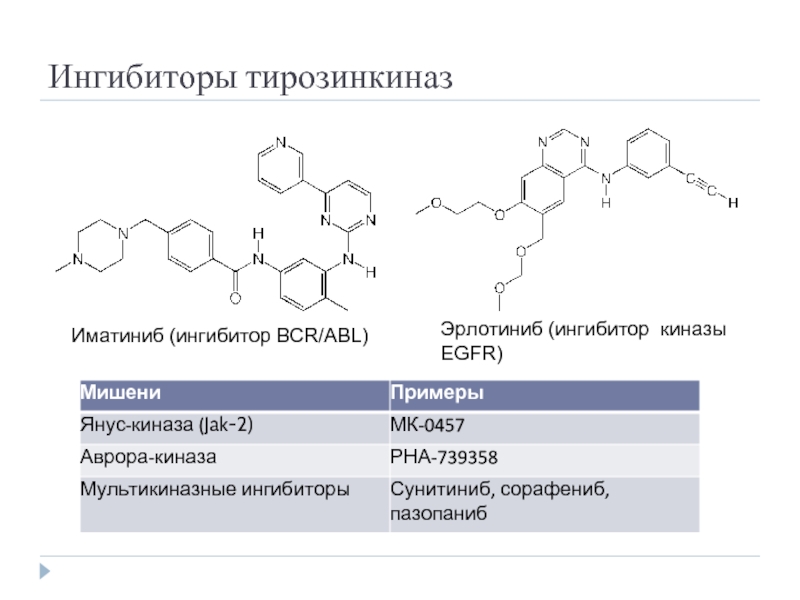
- 44. Ингибиторы тирозинкиназ Иматиниб (ингибитор BCR/ABL) Эрлотиниб (ингибитор киназы EGFR)
- 45. Ингибиторы ангиогенеза Прямые ингибиторы ангиогенеза - препараты,
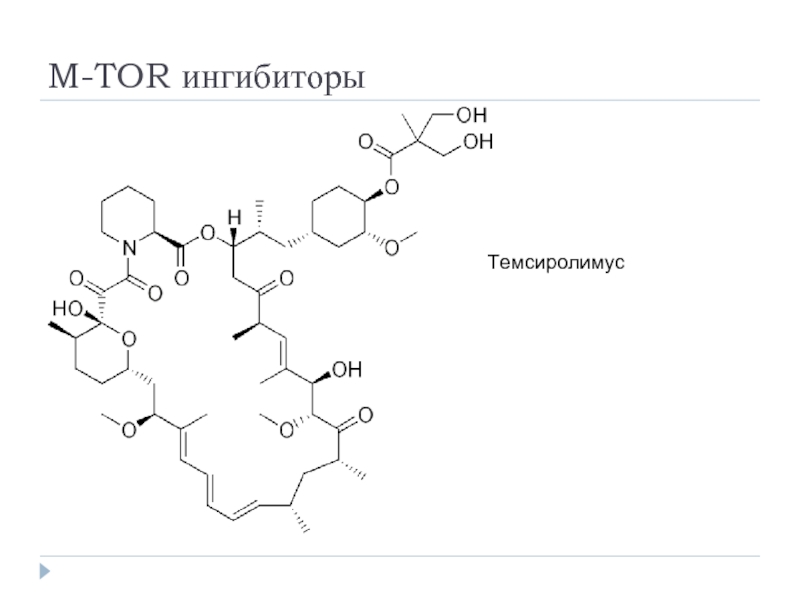
- 46. M-TOR ингибиторы Темсиролимус
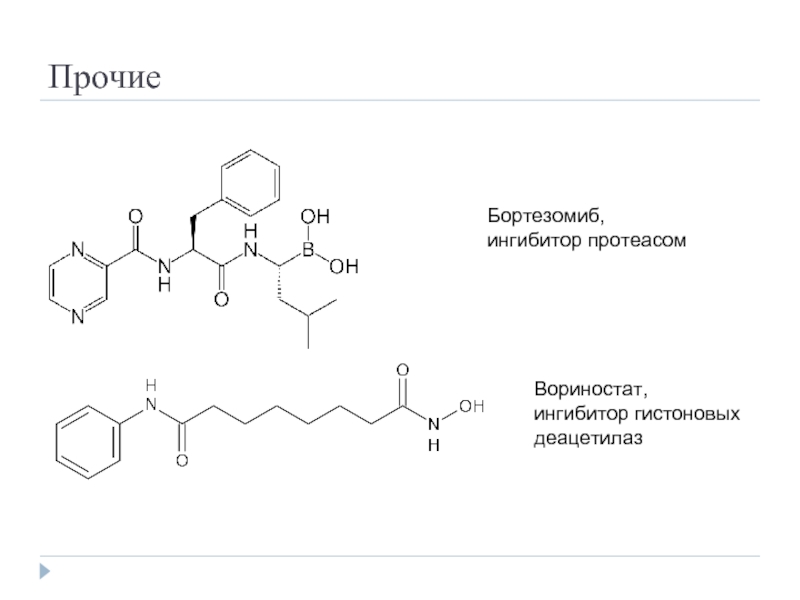
- 47. Прочие Бортезомиб, ингибитор протеасом Вориностат, ингибитор гистоновых деацетилаз
- 48. Сравнительная характеристика антител и химически синтезированных таргетных
- 49. 7. Индукторы дифференцировки I. Витамины и их аналоги
- 50. Эффективность препаратов: зависимость от фаз клеточного цикла
- 51. Заболевания, при которых с помощью химиотерапии удается
- 52. Важные онкологические заболевания, слабо подвергающиеся фармакологическому лечению
Слайд 2Определения
Карциномы — злокачественные опухоли, происходящие из эпителия
Аденокарциномы — злокачественные опухоли, происходящие
Саркомы — злокачественные опухоли, происходящие из тканей мезенхимного происхождения (соединительные, костные, хрящевые)
Лейкоз ― (от греч. leukós — белый), лейкемия, белокровие, опухолевое системное заболевание кроветворной ткани
Протоонкоген — ген нормального генома человека, участвует в регуляции пролиферации клеток. В результате мутаций протоонкоген может стать онкогеном (вирусным или клеточным)
Онкоген — измененный ген, кодирующий белок, обеспечивающий пролиферацию и дифференцировку клеточных популяций (протеинкиназы, ГТФазы, факторы роста)
Вирусный онкоген — вирусный ген, при встраивании/интеграции в геном вызывает опухолевое перерождение
Онкосупрессор — ген, тормозящий пролиферацию опухолевых клеток. При выключении функции гена возможна опухолевая трансформация
Слайд 3Основные свойства опухолевой клетки
Опухолевая прогрессия — появление и селекция все более
Самодостаточность в пролиферативных сигналах
Отсутствие (снижение) чувствительности к ростсупрессирующим сигналам
Неограниченность репликативного потенциала
Ослабление индукции апоптоза
Стимуляция неоангиогенеза (в опухоли диаметром более 2–4 мм образуются сосуды)
Изменение морфологии
Инвазия и метастазирование
Блок клеточной дифференцировки
Генетическая нестабильность
Метаболический атипизм
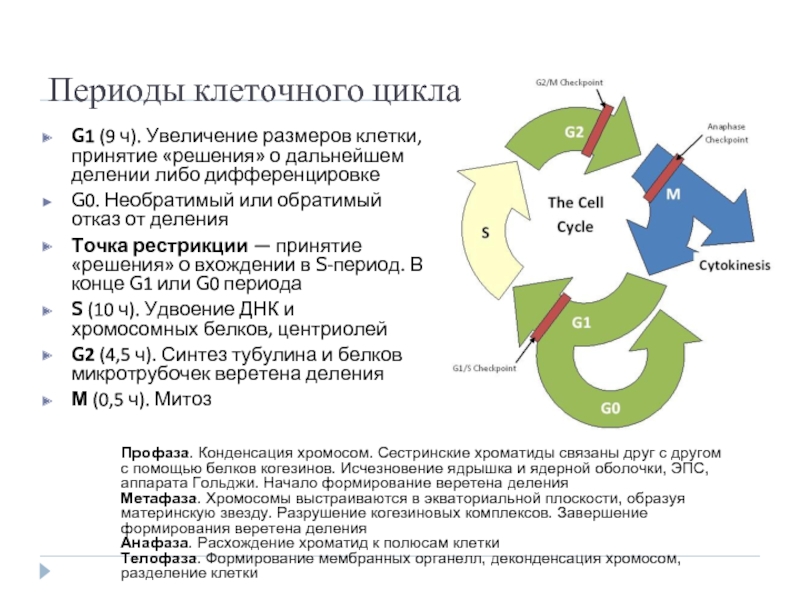
Слайд 5Периоды клеточного цикла
G1 (9 ч). Увеличение размеров клетки, принятие «решения» о дальнейшем
G0. Необратимый или обратимый отказ от деления
Точка рестрикции — принятие «решения» о вхождении в S-период. В конце G1 или G0 периода
S (10 ч). Удвоение ДНК и хромосомных белков, центриолей
G2 (4,5 ч). Синтез тубулина и белков микротрубочек веретена деления
М (0,5 ч). Митоз
Профаза. Конденсация хромосом. Сестринские хроматиды связаны друг с другом с помощью белков когезинов. Исчезновение ядрышка и ядерной оболочки, ЭПС, аппарата Гольджи. Начало формирование веретена деления
Метафаза. Хромосомы выстраиваются в экваториальной плоскости, образуя материнскую звезду. Разрушение когезиновых комплексов. Завершение формирования веретена деления
Анафаза. Расхождение хроматид к полюсам клетки
Телофаза. Формирование мембранных органелл, деконденсация хромосом, разделение клетки
Слайд 6Регуляция клеточного цикла: циклинзависимые киназы
Молекула киназы (Cdk) состоит из одной неактивной
Циклин D–Cdk4/Cdk6 функционирует в начале G1-периода, способствует прохождению клеткой точки рестрикции.
Циклин E–Cdk2 — вторая половина G1-периода.
Циклин А–Cdk2 — S-период.
Циклин В–Cdk2 — S-период.
Циклин В–Cdk1 — G2-период, вводит клетку в митоз (MPF — митозстимулирующий фактор).
Слайд 7Регуляция клеточного цикла: сигнальные пути
Сигнальные пути «нацелены» в большинстве случаев на
Условия, необходимые для деления клетки:
прикрепление к поверхности
действие ростового фактора
отсутствие контакта с другими клетками
Сигналы:
действие митогенов (от рецепторов эпидермального фактора роста [стволовые клетки эпителия] или антигенпредставляющей клетки [Т-хелперы]))
действие антимитогенов (ФНО, ТФРβ)
прикрепление клетки к матриксу (интегрины)
контактное торможение пролиферации
Слайд 8Механизм действия комплексов «циклин-Cdk»
Комплексы G1-фазы обеспечивают:
образование компонентов комплексов последующих стадий, и
образование субстратов и ферментов, необходимых для репликации ДНК
Комплексы S- и G2-фазы обеспечивают:
безошибочную репликацию ДНК
образование компонентов митоз-стимулирующего фактора («циклин В–Cdk1»)
торможение активности митоз-стимулирующего фактора во избежание преждевременного начала митоза
Слайд 9Нарушения контроля клеточного цикла в опухолевых клетках
Генетические изменения, вызывающие перманентную стимуляцию
Нарушения в пути передачи сигналов, опосредующих активацию чекпойнтов в ответ на ростингибирующие сигналы. Чаще ― мутации в генах-супрессорах
Блокирование или извращение дифференцировки
Слайд 11Апоптоз: биологическая роль
Уничтожение дефектных клеток.
Уничтожение «ненужных» клеток.
Гибель клеток куколки в ходе
Редукция пронефроса и мезонефрального канала в эмбриогенезе.
Исчезновение межпальцевых «перепонок» при морфогенезе.
Инволюция органов у горбуш после нереста.
Гибель клеток функционального слоя эндометрия накануне менструации.
Гибель лактоцитов молочных желез после прекращения лактации.
Селекция клеток иммунной системы.
Уничтожение аутореактивных клонов Т- и В-лимфоцитов.
Гибель стимулированных антигеном лимфоцитов при длительном отсутствии антигена.
Селекция половых клеток.
Гибель ооцитов атрезирующих фолликулов.
Регуляция численности клеток.
Слайд 12Апоптоз: пусковые факторы
Апоптоз «изнутри»
Чрезмерные (нерепарируемые) повреждения хромосом (разрывы ДНК, нарушения конформации,
Повреждение внутриклеточных мембран (перекисное окисление липидов)
Нарушение питания
Апоптоз «по команде»
Действие негативного сигнала.
Гибель лимфоцитов под действием глюкокортикоидов
Fas-лиганд Т-киллера
Сигнал от кадгеринов при контактном торможении
Прекращение действия подкрепляющего сигнала.
Гибель клеток-предшественников крови при отсутствии КСФ
Гибель клеток эндометрия из-за изменения гормонального фона
Гибель клеток при потере связи с опорой (нет сигнала от интегринов)
Слайд 13Эффекторы апоптоза
Каспазы. Сериновые протеазы, разрывают пептидные связи, образованные с участием остатка
Эндонуклеазы
Ca2+–Mg2+-зависимая эндонуклеаза: активируется под действием каспаз и внутриядерных белков.
Подобная ДНКазе-I ядерная ДНКаза — катализирует начальные стадии распада хроматина на очень крупные фрагменты.
Сильные окислители. При действии на клетку ФНО в ней активируется ген iNO-синтазы, что приводит к увеличению проницаемости мембран, в т.ч. мембран митохондрий. При апоптозе также инактивируются гены ферментов антиоксидантной системы (супероксиддисмутаза, каталаза, пероксидаза).
Слайд 14Примерная схема апоптоза
1. Повреждение хромосом или мембран.
2. Передача сигналов на белок р53.
3. Повышение проницаемости
4. Включение каспазного каскада.
5. Частичный протеолиз каспазами белков-мишеней.
→ конденсация хроматина
→ активация ядерных эндонуклеаз
→ изменение липидного состава плазмолеммы
6. Постепенная фрагментация хроматина.
7. Образование апоптозных телец и их фагоцитоз.
Слайд 15Изменения регуляции апоптоза в опухолевых клетках
Потеря экспрессии на поверхности клетки рецептора
Нарушение проведения апоптогенного сигнала к митохондриям (инактивация p53 и PTEN)
Ингибирование проницаемости митохондриальной мембраны для цитохрома С и AIF из-за изменения экспрессии белков Bcl2
Блокирование активации эффекторных каспаз (потеря экспресии гена Apaf-1 при метилировании)
Резкое уменьшение жизни каспаз при связывании их с белками-ингибиторами
Слайд 17Основные пути поиска и разработки новых противоопухолевых агентов
Основные группы мишеней
ДНК и процесс ее синтеза
Белки-посредники на различных путях передачи сигнала (регуляция клеточного цикла, апоптоз)
Слайд 18Классификация противоопухолевых препаратов
Алкилирующие агенты
Антиметаболиты
Противоопухолевые антибиотики
Препараты растительного происхождения
Ингибиторы митоза (винкаалкалоиды и таксаны)
Ингибиторы
Ферментные препараты
Гормональные и антигормональные препараты
Таргетные препараты
Моноклональные антитела к мембранным белкам
Низкомолекулярные соединения
Модификаторы биологических реакций
Слайд 191. Алкилирующие агенты
Механизм действия: образуют положительно заряженные группы, которые связываются с
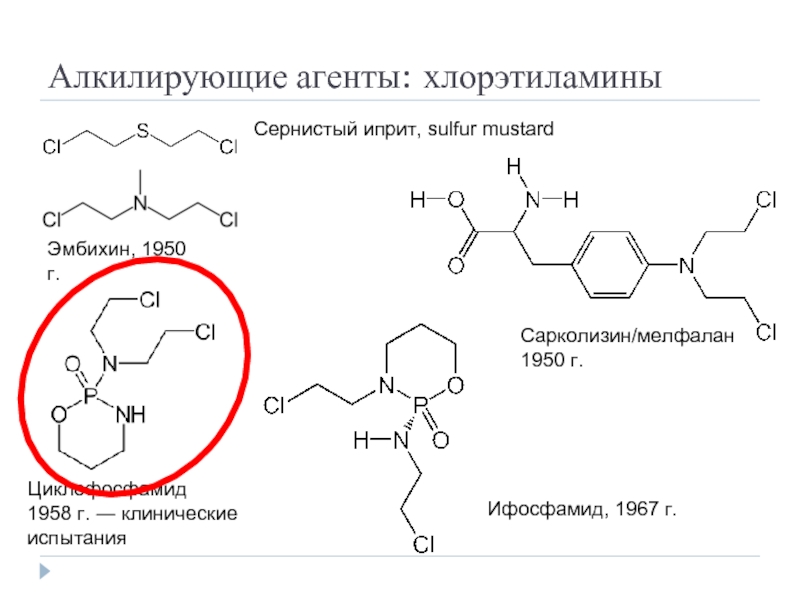
Слайд 20Алкилирующие агенты: хлорэтиламины
Сернистый иприт, sulfur mustard
Эмбихин, 1950 г.
Циклофосфамид
1958 г. ―
Сарколизин/мелфалан1950 г.
Ифосфамид, 1967 г.
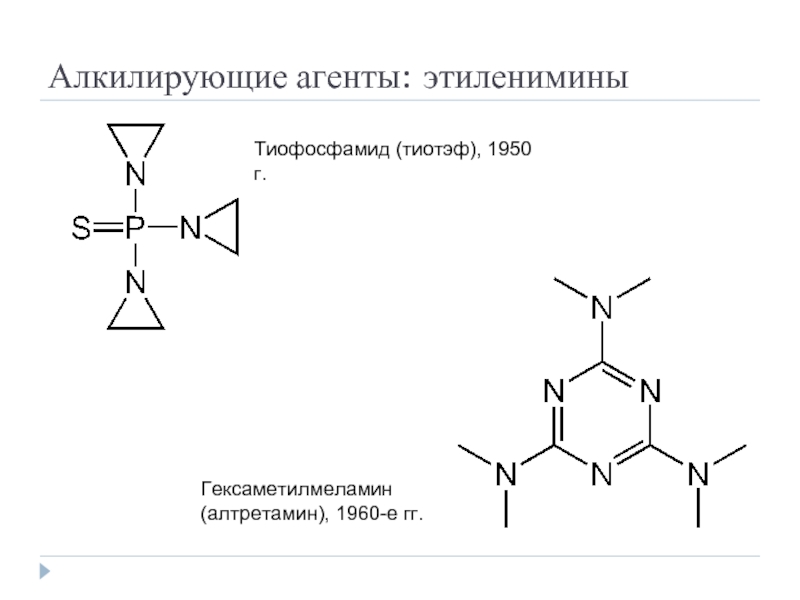
Слайд 21Алкилирующие агенты: этиленимины
Тиофосфамид (тиотэф), 1950 г.
Гексаметилмеламин
(алтретамин), 1960-е гг.
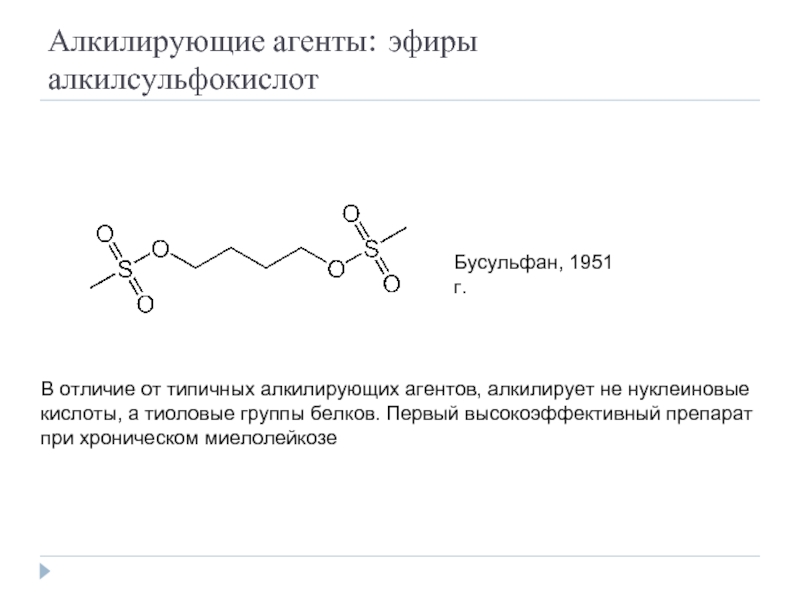
Слайд 22Алкилирующие агенты: эфиры алкилсульфокислот
Бусульфан, 1951 г.
В отличие от типичных алкилирующих
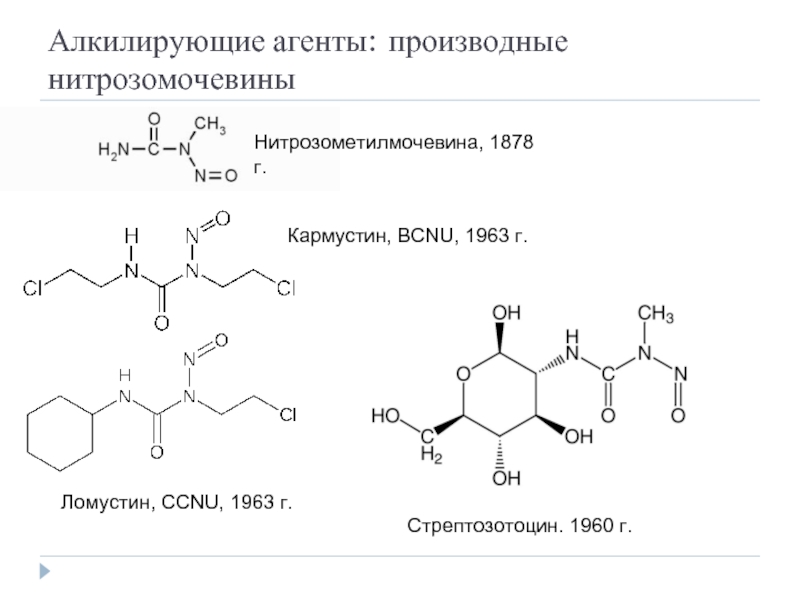
Слайд 24Алкилирующие агенты: производные нитрозомочевины
Нитрозометилмочевина, 1878 г.
Кармустин, BCNU, 1963 г.
Стрептозотоцин. 1960 г.
Ломустин, СCNU, 1963 г.
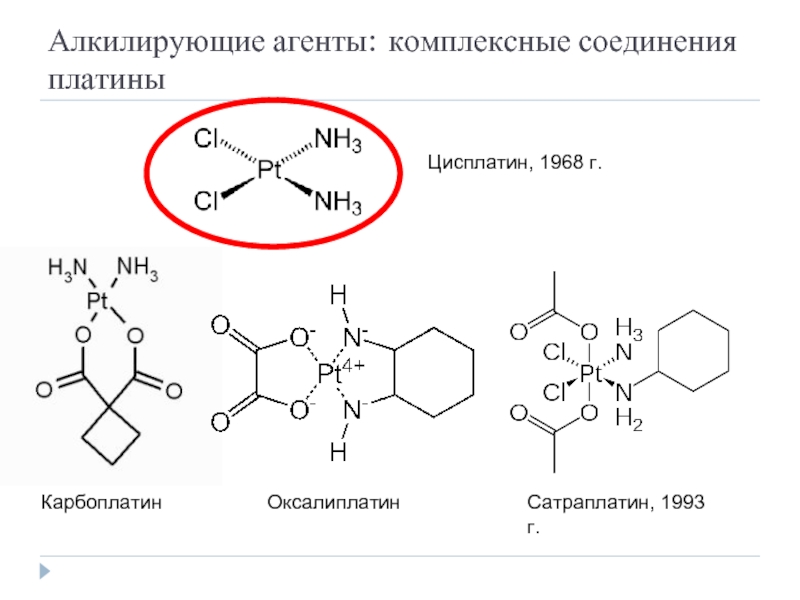
Слайд 25Алкилирующие агенты: комплексные соединения платины
Цисплатин, 1968 г.
Карбоплатин
Оксалиплатин
Сатраплатин, 1993 г.
Слайд 262. Антиметаболиты
Механизм действия: клетки их не распознают и утилизируют как обычные
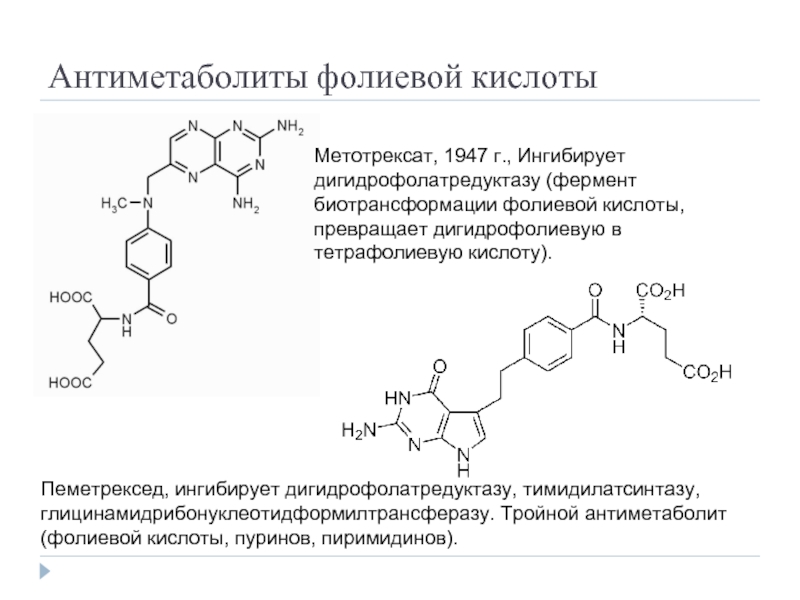
Слайд 27Антиметаболиты фолиевой кислоты
Метотрексат, 1947 г., Ингибирует дигидрофолатредуктазу (фермент биотрансформации фолиевой кислоты,
Пеметрексед, ингибирует дигидрофолатредуктазу, тимидилатсинтазу, глицинамидрибонуклеотидформилтрансферазу. Тройной антиметаболит (фолиевой кислоты, пуринов, пиримидинов).
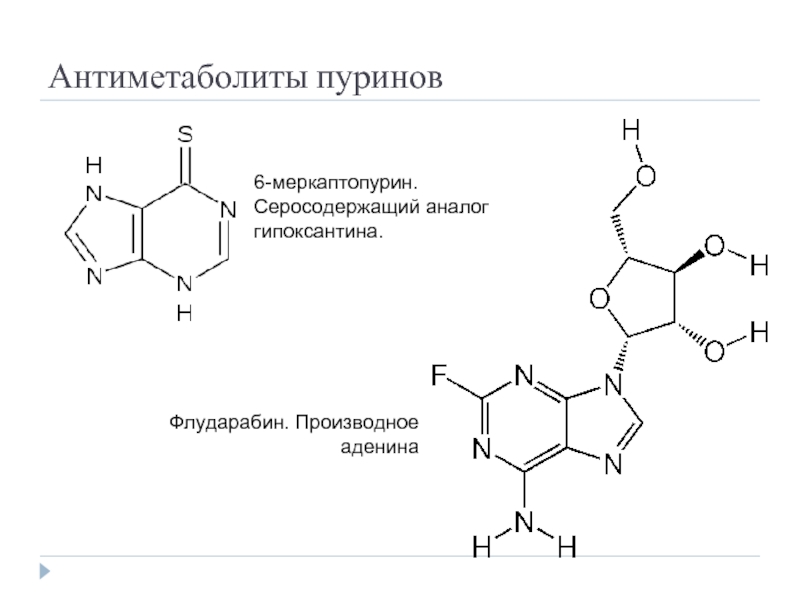
Слайд 28Антиметаболиты пуринов
6-меркаптопурин. Серосодержащий аналог гипоксантина.
Флударабин. Производное аденина
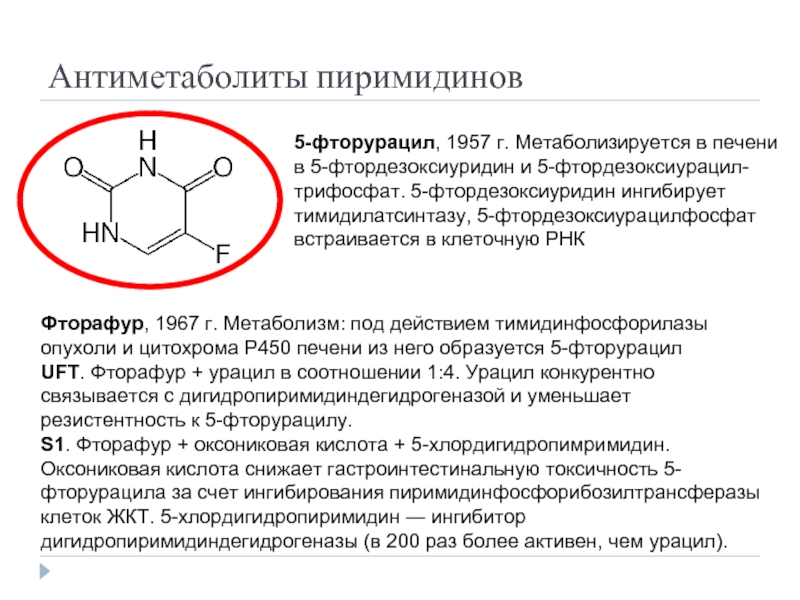
Слайд 29Антиметаболиты пиримидинов
5-фторурацил, 1957 г. Метаболизируется в печени в 5-фтордезоксиуридин и 5-фтордезоксиурацил-трифосфат.
Фторафур, 1967 г. Метаболизм: под действием тимидинфосфорилазы опухоли и цитохрома Р450 печени из него образуется 5-фторурацил
UFT. Фторафур + урацил в соотношении 1:4. Урацил конкурентно связывается с дигидропиримидиндегидрогеназой и уменьшает резистентность к 5-фторурацилу.
S1. Фторафур + оксониковая кислота + 5-хлордигидропимримидин. Оксониковая кислота снижает гастроинтестинальную токсичность 5-фторурацила за счет ингибирования пиримидинфосфорибозилтрансферазы клеток ЖКТ. 5-хлордигидропиримидин ― ингибитор дигидропиримидиндегидрогеназы (в 200 раз более активен, чем урацил).
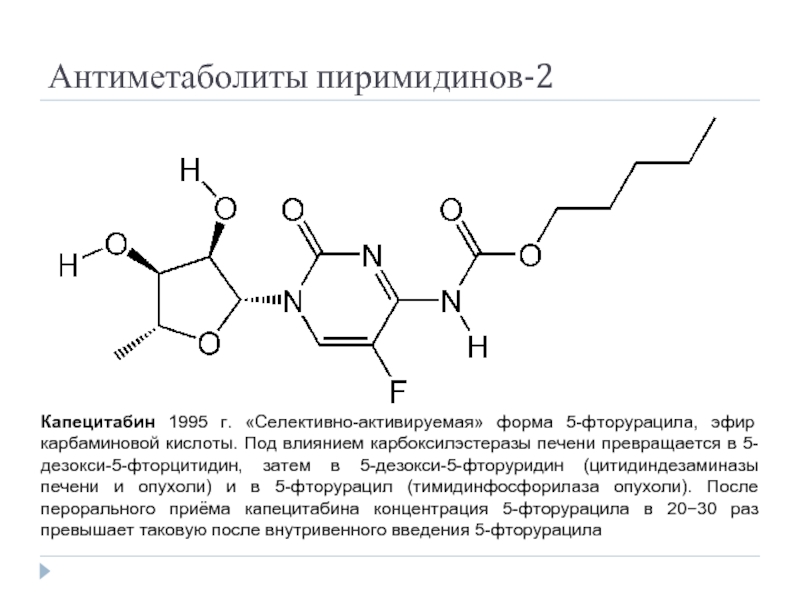
Слайд 30Антиметаболиты пиримидинов-2
Капецитабин 1995 г. «Селективно-активируемая» форма 5-фторурацила, эфир карбаминовой кислоты. Под
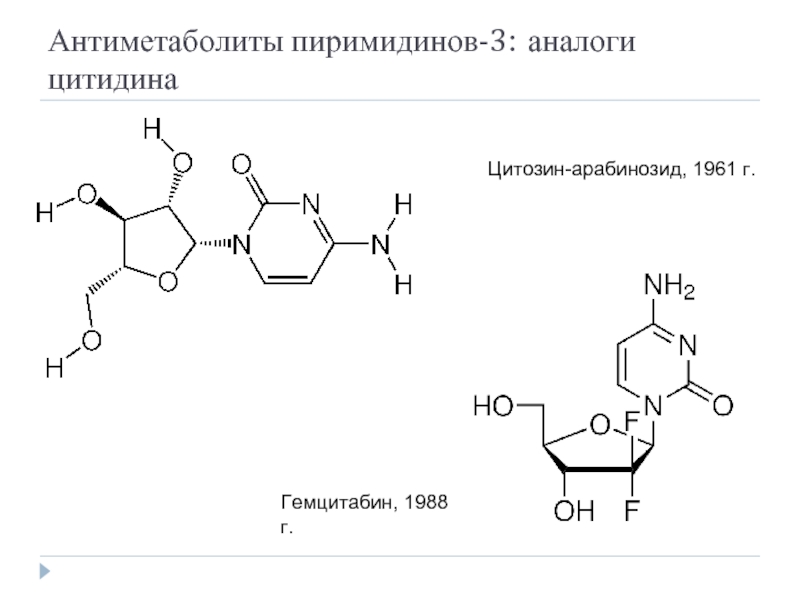
Слайд 31Антиметаболиты пиримидинов-3: аналоги цитидина
Цитозин-арабинозид, 1961 г.
Гемцитабин, 1988 г.
Слайд 323. Противоопухолевые антибиотики
Механизм действия: до конца не изучен
Интеркаляторы
Ингибиторы топоизомеразы II
Слайд 354. Ферментные препараты
Механизм действия:
ферменты, расщепляющие аминокислоты, необходимые для роста опухолевых клеток
ферменты, разрушающие РНК опухолевых клеток (ранпирназа и др.).
Слайд 375. Препараты растительного происхождения
Механизм действия:
винкаалкалоиды: cвязываются с белком микротрубочек тубулином,
таксаны: усиливают полимеризацию тубулина, стабилизируя микротрубочки и прерывая процесс деполимеризации;
подофиллотоксины: ингибиторы топоизомеразы II, ингибиторы полимеризации тубулина, приводят к накоплению клеток в поздней S и G2 фазе;
производные камптотецина: ингибиторы топоизомеразы I.
Слайд 43Моноклональные антитела
Механизм действия
Комплемент-зависимая цитотоксичность
Антитело-зависимая клеточная цитотоксичность
Индукция апоптоза
Ингибирование сигнальной трансдукции
Блокада рецепторов (антирецепторы)
Особые
Химерные. Содержат 30−35% мышиных и 65−70% антител
Гуманизированные. 90% человеческих, 10% мышиных антител
Основные представители
Ритуксимаб (мабтера). Анти-CD20. Химерное моноклональное
Трастузумаб (герцептин). Гуманизированное моноклональное к Her2/neu
Цетуксимаб. Химерное антитело к EGFR
Бевацизумаб. Гуманизированное моноклональное антитело к VEGF
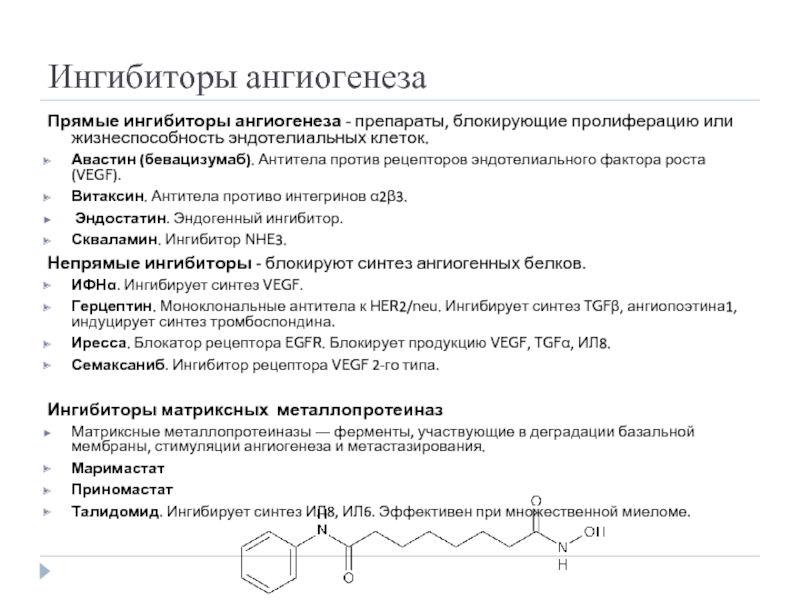
Слайд 45Ингибиторы ангиогенеза
Прямые ингибиторы ангиогенеза - препараты, блокирующие пролиферацию или жизнеспособность эндотелиальных
Авастин (бевацизумаб). Антитела против рецепторов эндотелиального фактора роста (VEGF).
Витаксин. Антитела противо интегринов α2β3.
Эндостатин. Эндогенный ингибитор.
Скваламин. Ингибитор NHE3.
Непрямые ингибиторы - блокируют синтез ангиогенных белков.
ИФНα. Ингибирует синтез VEGF.
Герцептин. Моноклональные антитела к HER2/neu. Ингибирует синтез TGFβ, ангиопоэтина1, индуцирует синтез тромбоспондина.
Иресса. Блокатор рецептора EGFR. Блокирует продукцию VEGF, TGFα, ИЛ8.
Семаксаниб. Ингибитор рецептора VEGF 2-го типа.
Ингибиторы матриксных металлопротеиназ
Матриксные металлопротеиназы ― ферменты, участвующие в деградации базальной мембраны, стимуляции ангиогенеза и метастазирования.
Маримастат
Приномастат
Талидомид. Ингибирует синтез ИЛ8, ИЛ6. Эффективен при множественной миеломе.
Слайд 48Сравнительная характеристика антител и химически синтезированных таргетных препаратов
Перспективные мишени:
геномная нестабильность;
киназы (EGFR/HER1, BCR/ABL, KIT, mTOR, SRC, LCK, YES, FYN, EPHA2…);
процессы ангиогенеза;
и др.
Слайд 497. Индукторы дифференцировки
I. Витамины и их аналоги
Политрансретиноевая кислота: острый промиелоцитарный лейкоз.
Витамин D3.
II. Цитокины
ИФНα2
ФНО: на стадии изучения.
III. Низкомолекулярные соединения
Гексаметилбисацетамд
Форболовый эфир
Бутираты
Пептиды (дикарбамин)
IV. Противоопухолевые антибиотики (в малых дозах)
Актиномицин D
Митомицин С
Слайд 51Заболевания, при которых с помощью химиотерапии удается вылечить большинство больных
Лимфома Ходжкина
Опухоли
Герминогенные опухоли яичка, яичников, внегонадные герминогенные опухоли
Острый лимфобластный лейкоз
Острый промиелоцитарный лекоз
Слайд 52Важные онкологические заболевания, слабо подвергающиеся фармакологическому лечению
Практически нечувствительные
Рак поджелудочной железы
Мезотелиома плевры
Рак
Гепатоцеллюлярный рак
Саркомы мягких тканей
Рак шейки матки
Существуют чувствительные популяции клеток
Немелкоклеточный рак легкого
Рак желудка
Рак почки
Рак мочевого пузыря
Меланома
Папиллярный рак щитовидной железы
Глиомы низкой и промежуточной степени злокачественности