- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Миастения, аутоиммунное нервномышечное заболевание презентация
Содержание
- 1. Миастения, аутоиммунное нервномышечное заболевание
- 2. Миастения Миастения - аутоиммунное нервно-мышечное заболевание, клинически
- 3. Эпидемиология Распространенность - 5-10 человек на 100
- 4. Этиология Врожденная – дефект ацетилхолинэстеразы, дефект ацетилхолиновых
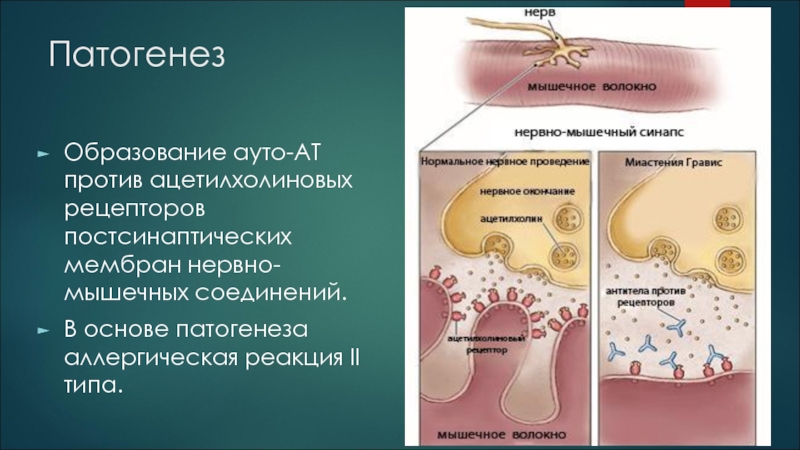
- 5. Патогенез Образование ауто-АТ против ацетилхолиновых рецепторов постсинаптических
- 6. Патогенез Большое значение имеют вилочковые нарушения.
- 7. Патогенез У большинства больных миастенией тимусы содержат
- 8. Классификация По возрасту: МГ новорожденных – материнские
- 9. По течению: миастенические эпизоды — кратковременные миастенические
- 10. прогрессирующее течение наблюдается у большинства больных. Начало
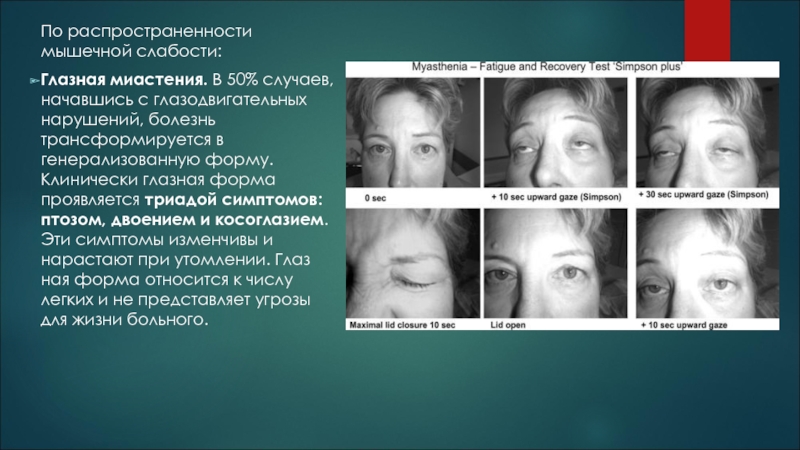
- 11. По распространенности мышечной слабости: Глазная миастения. В
- 12. Глоточно-лицевая миастения по частоте встречаемости не превышает
- 13. Скелетно-мышечная форма встречается в 6—7% случаев. При
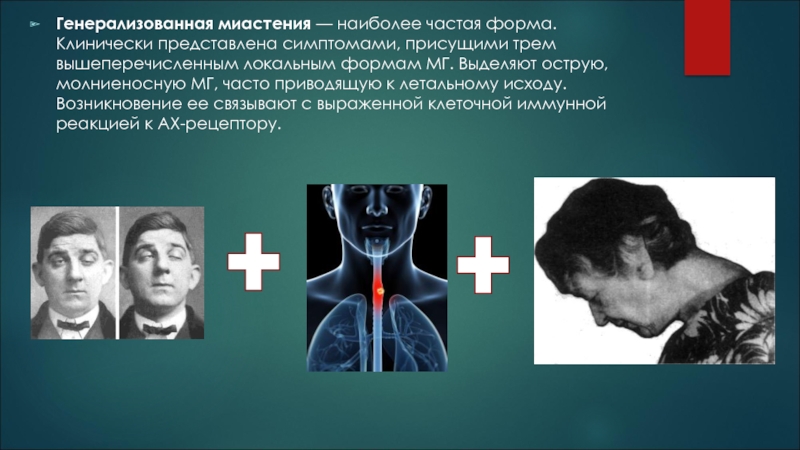
- 14. Генерализованная миастения — наиболее частая форма. Клинически
- 15. Диагностика Клинический осмотр и выяснение истории болезни.
- 16. 1. Анамнез: кратковременные эпизоды слабости и утомляемости
- 17. ЭНМГ Декремент-тест – метод электрофизиологического исследования, в
- 19. Фармакологический тест. Используют неостигмина метилсульфат (прозерин) или
- 20. Лабораторные данные Обнаружение: 1. АутоАТ к АХ-рецептору.
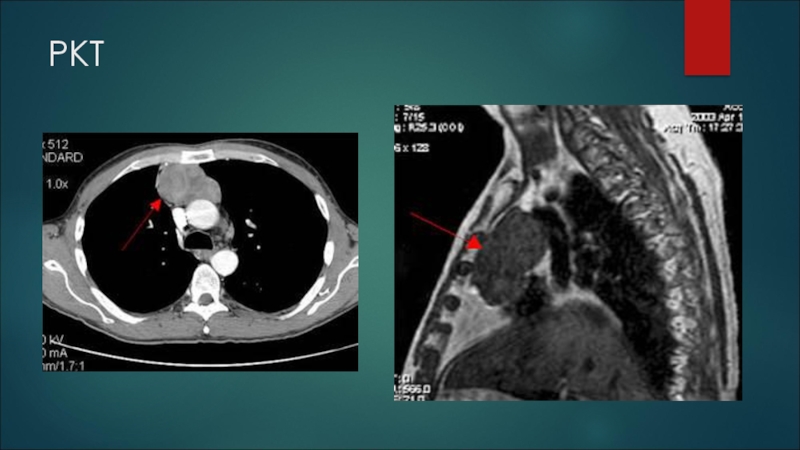
- 21. РКТ
- 22. Дифференциальная диагностика 1. Бульбарные явления: сосудистые и
- 23. Дифференциальная диагностика 3. Дыхательные расстройства и кризы
- 24. Дифференциальная диагностика 5. Синдром Ламберта-Итона. Феномен «врабатывания»-нарастание
- 25. Лечение Этапность Сочетание компенсирующей, патогенетической и неспецефической терапии Учет фазы течения заболевания
- 26. Первый этап АХЭП. Калимин в максимальной суточной
- 27. Второй этап Недостаточная эфыективность препаратов первого этапа.
- 28. Третий этап При недостаточной эффективности или при
- 29. Оперативное лечение: Тимэктомия. Оценка результатов операции по
- 30. Миастенический криз МК — угрожающее жизни быстро
- 31. 1. Миастенический криз- прогрессирование расстройства дыхания (минуты-часы)
- 32. 2. Холинергический криз - из-за избытка ацетилхолина
- 33. 3. Смешанный криз - самый тяжелый вариант,
- 34. Дифференциальная диагностика кризов
- 35. Неотложная помощь при МК Этап 1: если
- 36. Этап 2: если нет реакции на АХЭ-препараты
- 37. Больным миастенией нельзя: - Загорать - Тяжело
- 38. Спасибо за внимание
Слайд 2Миастения
Миастения - аутоиммунное нервно-мышечное заболевание, клинически проявляющееся в виде слабости и
Слайд 3Эпидемиология
Распространенность - 5-10 человек на 100 000 населения.
Возраст – любой,
Пол – Чаще женщины в возрасте 20-40 лет. Соотношение женщин и мужчин 3:1. В пожилом возрасте соотношение выравнивается.
Слайд 4Этиология
Врожденная – дефект ацетилхолинэстеразы, дефект ацетилхолиновых рецепторов (мутации в генах)
Приобретенная –
Слайд 5Патогенез
Образование ауто-АТ против ацетилхолиновых рецепторов постсинаптических мембран нервно-мышечных соединений.
В основе патогенеза
Слайд 6Патогенез
Большое значение имеют вилочковые нарушения.
В тимусе происходит созревание и обучение
Слайд 7Патогенез
У большинства больных миастенией тимусы содержат В-лимфоциты, продуцирующие антитела против АХ-рецепторов.
У
Слайд 8Классификация
По возрасту:
МГ новорожденных – материнские АТ
Юношеская МГ – возникает в среднем
МГ взрослых - наиболее распространенная.
Поздняя МГ - старше 60 лет.
Слайд 9По течению:
миастенические эпизоды — кратковременные миастенические симптомы (глазодвигательные, генерализованные или дыхательные),
стационарное течение наблюдается у 10% больных. Эта форма, нередко возникнув остро, в дальнейшем под влиянием лечения приобретает не прогрессирующий характер со склонностью к ремиссиям;
Слайд 10прогрессирующее течение наблюдается у большинства больных. Начало может быть молниеносным, острым
злокачественное течение наблюдается у 7—9,2% больных и характеризуется чаще всего острым началом и склонностью к дыхательным нарушениям.
Слайд 11По распространенности мышечной слабости:
Глазная миастения. В 50% случаев, начавшись с глазодвигательных
Слайд 12Глоточно-лицевая миастения по частоте встречаемости не превышает 8—10%. Одна из злокачественных
Гехт Б.М. Санадзе А.Г. << Миастения>> 2012 г.
Слайд 13Скелетно-мышечная форма встречается в 6—7% случаев. При этой форме в 8—10%
Слайд 14Генерализованная миастения — наиболее частая форма. Клинически представлена симптомами, присущими трем
Слайд 15Диагностика
Клинический осмотр и выяснение истории болезни.
Функциональная проба на выявление синдрома патологической
Прозериновая проба
Повторный декремент-тест для выявления реакции на прозерин
Клинический осмотр для выявления обратимости миастенических изменений на фоне прозерина
Анализ крови на антитела к ацетилхолиновым рецепторам.
Компьютерная томография органов переднего средостения
Слайд 161. Анамнез: кратковременные эпизоды слабости и утомляемости в прошлом, диплопия и
2. Физикальное обследование: усиление слабости при повторных движениях или статическом напряжении.
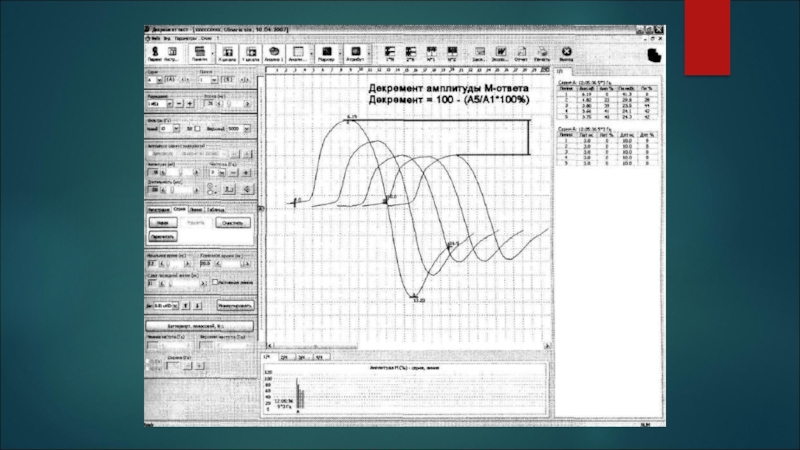
Слайд 17ЭНМГ
Декремент-тест – метод электрофизиологического исследования, в ходе которого оценивают способность нервно-мышечного
Постепенное снижение амплитуды М-волн по сравнению с первой (более чем на 10%) позволяет заподозрить миастению.
После чего вводят прозерин 0,05% 1-3 мл п/к. через 30 мин повторное исследование. Для истинной миастении характерно повторное увеличение амплитуды (снижение декремента).
Слайд 19Фармакологический тест.
Используют неостигмина метилсульфат (прозерин) или пиридостигмина бромид (калимин). Оценка результатов
Полная компенсация - восстановление мышечной силы до нормальных значений (5 баллов) независимо от степени исходного снижения - 15% пациентов
Неполная компенсация - увеличение мышечной силы на 2-3 балла, но не до нормы - 75% пациентов.
Частичная компенсация - увеличение мышечной силы на 1 балл в отдельных мышцах, когда в других мышцах она не изменяется
Проба позитивная при полной и неполной компенсации, проба сомнительная при частичной компенсации, проба негативная при отсутствии реакции.
Слайд 20Лабораторные данные
Обнаружение:
1. АутоАТ к АХ-рецептору.
2. К титин-белку (у больных с
3. К мышечно-специфической тирозинкиназе (при серонегативной миастении)
Слайд 22Дифференциальная диагностика
1. Бульбарные явления: сосудистые и опухолевые поражения мозга, для которых
2. БАС - возможны симптомы миастении, нарушение нервно-мышечной передачи и реакция на АХЭП. При БАС - признаки денервации и реиннервации, большое количество потенциальов фасцикуляций.
Слайд 23Дифференциальная диагностика
3. Дыхательные расстройства и кризы – Синдром Гийена-Барре. При СГБ
4. Слабость мышц туловища и конечностей - миопатии. Нет поражения экстраокулярной и бульбарной мускулатруры, нет дыхательных расстройств, часто атрофии и снижение или отсутствие сухожильных рефлексов
Слайд 24Дифференциальная диагностика
5. Синдром Ламберта-Итона. Феномен «врабатывания»-нарастание силы после некоторого утомления. Реакция
6. Ботулизм. Отсутствие эффекта от АХЭП, характерны экстраокулярные бульбарные дыхательные нарушения. Гипо или арефлексия. На ЭМГ инкремент. Анамнез.
Слайд 25Лечение
Этапность
Сочетание компенсирующей, патогенетической и неспецефической терапии
Учет фазы течения заболевания
Слайд 26Первый этап
АХЭП. Калимин в максимальной суточной дозе 240-360 мг. (30 мг
Препараты калия
Калийсберегающие диуретики. Спиронолактон перорально в дозе 25-50 мг 3-4 раза в день
Слайд 27Второй этап
Недостаточная эфыективность препаратов первого этапа.
Перед подготовкой к операции (тимэктомии) –
Эффективность до 80%.
Преднизолон по схеме через день. Доза 1мг/кг/сут, но не менее 50 мг.
Слайд 28Третий этап
При недостаточной эффективности или при выраженных побочных эффетах применяют цитостатические
Циклоспорин 3 мг/кг. Эффект появляется черз 1-2 мес, максимум через 3-4 мес.
Слайд 29Оперативное лечение:
Тимэктомия. Оценка результатов операции по схеме G. Keynes
А – отличный
В – хороший эффект - значительное улучшение состояния, практически полное восстановление двигательной функции и работоспособности при уменьшении суточной дозы калимина по сравнению с дооперационной в 2 раза и более и отсутствии необходимости в иммуносупрессивной терапии.
С -удовлетворительный эффект — незначительное улучшение двигательной функции при постоянном приеме калимина и иногда преднизолона, отсутствие прогрессирования заболевания.
D – отсутствие эффекта.
Е – летальность.
Слайд 30Миастенический криз
МК — угрожающее жизни быстро развивающееся и нарастающее нарушение жизненно
Под МК подразумевается состояние больного с миастенией, требующее интубации пациента вследствие дыхательных нарушений. При МК жизненная емкость легких падает до 1л и меньше.
Слайд 311. Миастенический криз- прогрессирование расстройства дыхания (минуты-часы) - дыхание частое поверхностное
Слайд 322. Холинергический криз - из-за избытка ацетилхолина гиперполяризация и десенситизация ах-рецепторов.
Слайд 333. Смешанный криз - самый тяжелый вариант, встречается часто. Сочетание клинической
Ломкий криз.
Дифф диагностика - проба с АХЭП. Миастенический криз - +, холинергический - -, Смешанный - частичная или неполная компенсация.
Слайд 35Неотложная помощь при МК
Этап 1: если есть реакция на АХЭ-препараты.
1) Подбор адекватных
2) Немедленно начать патогенетическую терапию: пульс-терапия преднизолоном в/в капельно по 1000—2000 мг через день + 300—500 мг в/в во 2-й день.
3) Далее — преднизолон перорально ежедневно по 1,5—2 мг/кг массы тела по схеме большая/малая доза.
4) Препараты калия — в/в по 3 г /сут.
5) Плазмаферез или иммуноглобулины человека G.
NB! Пульс-терапия относительно противопоказана при холинергическом и смешанном кризах из-за десентитизации АХЭ.
Слайд 36Этап 2: если нет реакции на АХЭ-препараты
1) Интубация и ИВЛ и
2) Через 36 часов: прозерин и попытка отключения ИВЛ.
3) При восстановлении дыхания, не экстубируя больного, п/к прозерин каждые 3—4 ч. При устойчивом состоянии — экстубировать пациента.
4) Если остаются дыхательная недостаточность и нарушение глотания — вновь подключить ИВЛ и больше АХЭ-препараты не вводить.
5) На следующий день — п/к прозерин и снова попытаться отключить ИВЛ.
6) Если дыхание не нормализуется через 3 сут — трахеостома. Продолжать или начать патогенетическую терапию.
7) Плазмаферез или иммуноглобулины G.
8) Психотерапия и разъяснительная работа для профилактики передозировки АХЭ-препаратов, а также для отключения ИВЛ обязательны!
Введение АХЭ-препаратов при МК на фоне ИВЛ считается грубой ошибкой!