- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Клеточные технологии и современная медицина презентация
Содержание
- 1. Клеточные технологии и современная медицина
- 2. Механизмы реализации лечебного действия клеточной терапии 1.
- 3. ПУТИ КОМПЕНСАЦИИ НЕДОСТАТОЧНОСТИ ФУНКЦИИ ПОРАЖЕННОГО ОРГАНА ДОНОРСКИМИ
- 4. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ЭФФЕКТИВНОСТЬ КЛЕТОЧНОЙ ТЕРАПИИ ПОРАЖЕННОГО ОРГАНА
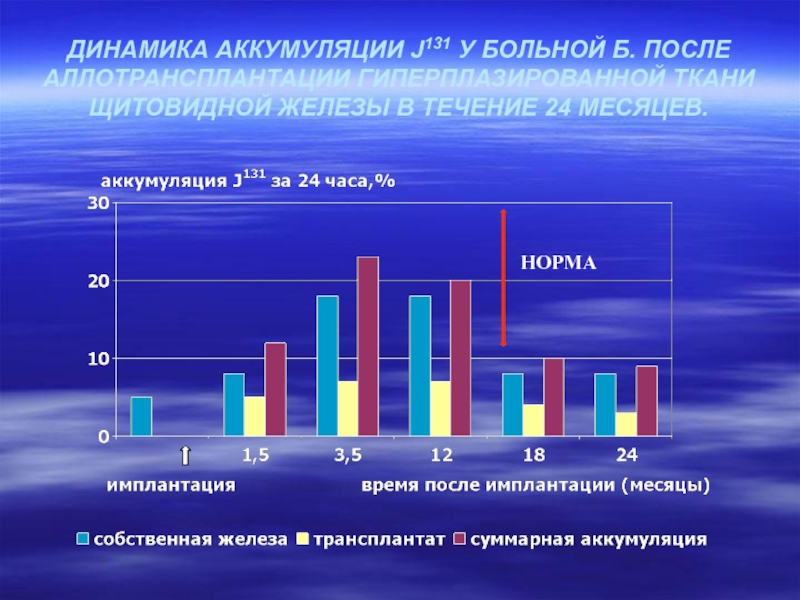
- 5. ДИНАМИКА АККУМУЛЯЦИИ J131 У БОЛЬНОЙ Б. ПОСЛЕ
- 6. ПРЕИМУЩЕСТВА ФЕТАЛЬНЫХ ОРГАНОВ ПЕРЕД ОРГАНАМИ ВЗРОСЛЫХ
- 7. Свойства стволовых клеток способность к многократному делению;
- 8. Факторы препятствующие использованию эмбриональных стволовых клеток в
- 9. Сравнительная характеристика
- 10. Источники взрослых стволовых клеток для клинического применения
- 11. Достоинства костного мозга как источника СК Относительно
- 12. СК костного мозга Пунктат костного мозга
- 13. Пластичность Недифференцированные стромальные СК Остеогенная дифференцировка Миогенная дифференцировка Адипоцитарная дифференцировка
- 14. Кардиомиоцитоподобная клетка из костного мозга in vitro.
- 15. Динамика различной пролиферативной активности ММСК у животных
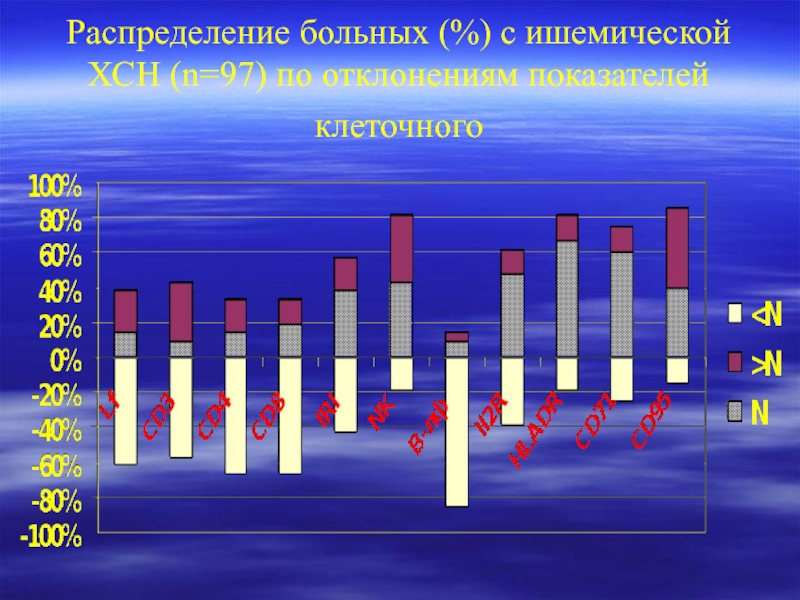
- 16. Распределение больных (%) с ишемической ХСН (n=97) по отклонениям показателей клеточного
- 17. Взаимосвязь между содержанием CD25+ лимфоцитов в крови
- 18. Взаимосвязь между содержанием CD95+ лимфоцитов в крови
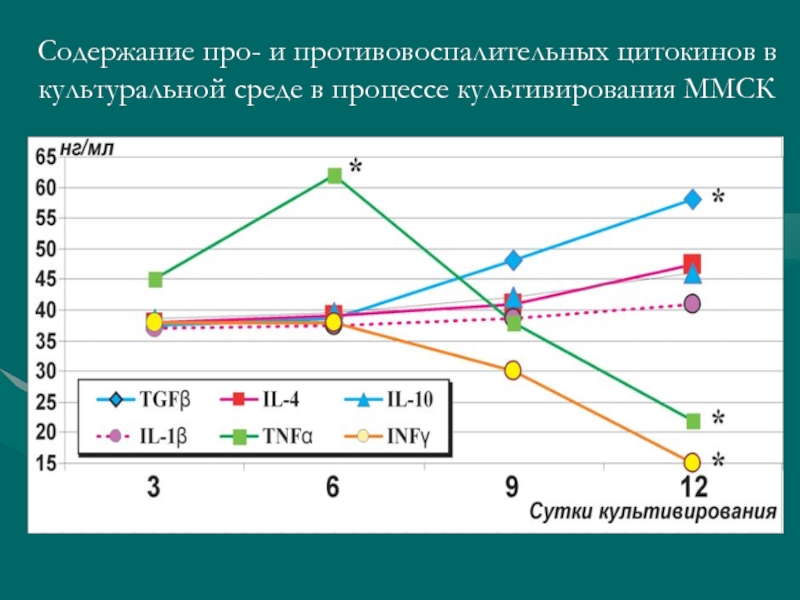
- 19. Содержание про- и противовоспалительных цитокинов в культуральной среде в процессе культивирования ММСК
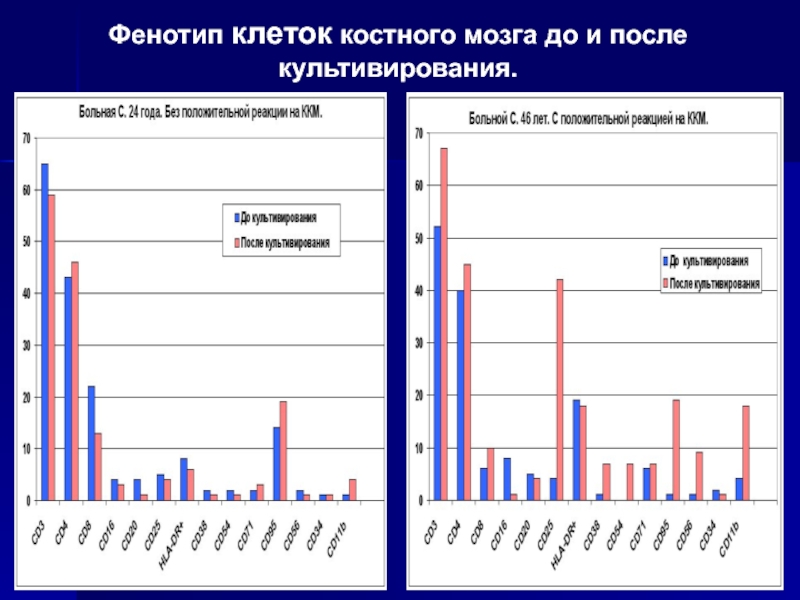
- 20. Фенотип клеток костного мозга до и после культивирования.
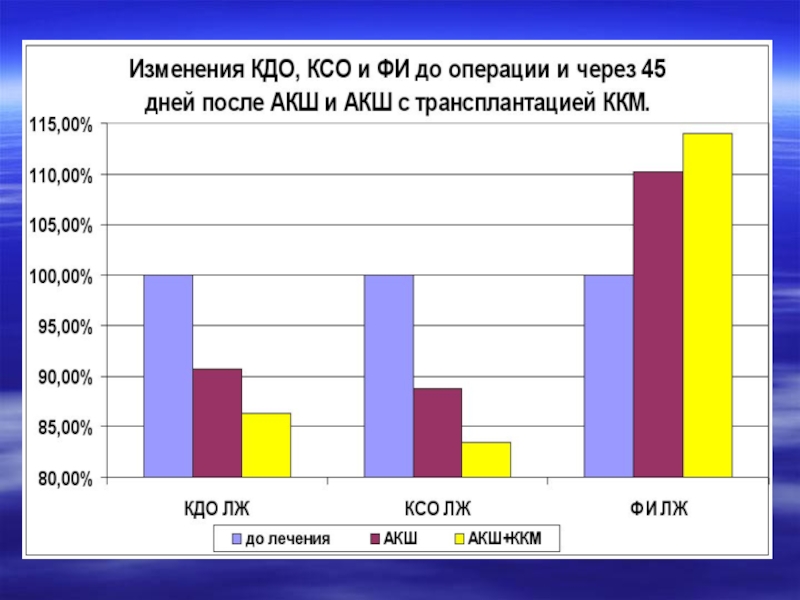
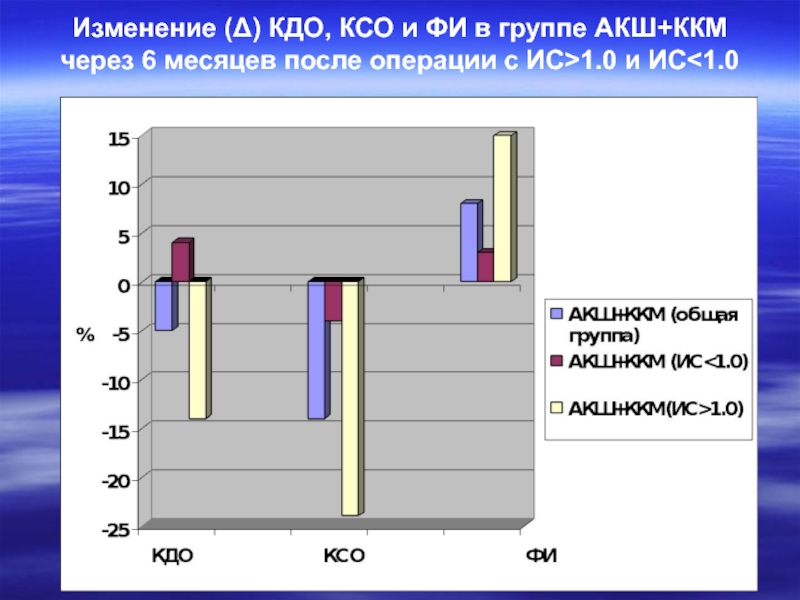
- 22. Изменение (Δ) КДО, КСО и ФИ в
- 23. Микрососуды брыжейки тонкой кишки у интактной крысы.
- 24. Микрососуды брыжейки тонкой кишки через 4 месяца
- 25. Микрососуды брыжейки тонкой кишки крыс с сахарным
- 26. Микрососуды брыжейки тонкой кишки крыс с СД
- 27. Морфология ткани селезенки крыс с СД I
- 28. МСК Нео ангиогенез Дифференцировка в специализированные клетки
Слайд 1Клеточные технологии и современная медицина
Н.А. Онищенко
(лекция)
НИИ ТРАНСПЛАНТОЛОГИИ И ИСКУССТВЕННЫХ ОРГАНОВ
Слайд 2Механизмы реализации лечебного действия клеточной терапии
1. Возмещается дефицит отсутствующих клонов специализированных
2. Стимулируется резерв внутриклеточной регенерации и пролиферации в сохранившихся клетках органа.
Слайд 3ПУТИ КОМПЕНСАЦИИ НЕДОСТАТОЧНОСТИ ФУНКЦИИ ПОРАЖЕННОГО ОРГАНА ДОНОРСКИМИ КЛЕТКАМИ
При трансплантации - за
При экстракорпоральном подключении - за счет увеличения мощности импульсных регуляторных сигналов донорских клеток и реализации их системного воздействия на восстановительные процессы в пораженном органе.
Слайд 4ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ ЭФФЕКТИВНОСТЬ КЛЕТОЧНОЙ ТЕРАПИИ ПОРАЖЕННОГО ОРГАНА
Масса жизнеспособной ткани в пораженном
Масса биологической активности донорских клеток должна быть достаточной для индукции регуляторной перестройки в клетках пораженного органа.
Слайд 5ДИНАМИКА АККУМУЛЯЦИИ J131 У БОЛЬНОЙ Б. ПОСЛЕ АЛЛОТРАНСПЛАНТАЦИИ ГИПЕРПЛАЗИРОВАННОЙ ТКАНИ ЩИТОВИДНОЙ
НОРМА
Слайд 6ПРЕИМУЩЕСТВА ФЕТАЛЬНЫХ ОРГАНОВ ПЕРЕД ОРГАНАМИ ВЗРОСЛЫХ
ДОНОРОВ
Клетки фетальных органов имеют слабо
Преобладает содержание стволовых и бластных клеток, обладающих мощным потенциалом пролиферации.
Стволовые и бластные клетки продуцируют уникальный комплекс цитокинов и ростовых факторов.
Слайд 7Свойства стволовых клеток
способность к многократному делению;
способность при делении воспроизводить себе подобные
способность дифференцироваться в один или более тип клеток.
Слайд 8Факторы препятствующие использованию эмбриональных стволовых клеток в клеточной терапии
Технические трудности в
Недостаток информации об индукции их дифференцировки in vitro;
Наличие ряда биоэтических вопросов, возникающих при использовании ЭСК, выделенной из эмбриональной ткани с применением технологии переноса ядра;
Опасность индукции канцирогенеза при использовании ЭСК;
Иммунологические проблемы отторжения.
Слайд 9Сравнительная характеристика ЭСК
Хорошо размножаются
Тоти-, плюрипотентны
Сложная техника получения и культивирования
Получение порождает этические проблемы
Аутологичная трансплантация возможна только в случае реализации терапевтического клонирования
Высокий риск канцерогенеза
Пролиферативный потенциал ниже, чем у ЭСК
Уни-, би-, мультипотентны, редко – плюрипотентны
Более доступный процессинг
Нет этических проблем
Возможность аутологичной трансплантации
Онкогенность минимальна
Слайд 10Источники взрослых стволовых клеток для клинического применения
Фетальная печень (гемопоэтические СК)
Мозг фетуса
Пуповинная кровь (гемопоэтические СК)
Костный мозг взрослого человека (гемопоэтические и стромальные СК)
Слизистая оболочка носоглотки в районе обонятельной луковицы (нейральные СК)
Жировая ткань(мезенхимальные СК)
Пульпа молочных зубов
Слайд 11Достоинства костного мозга как источника СК
Относительно большое количество СК в пунктате
Несколько видов СК в пунктате (высокая пластичность СК костного мозга)
Возможность аутологичной трансплантации
Доступность
Относительно низкая стоимость получения и культивирования
Отсутствие онкогенности
Отсутствие этических проблем
Слайд 12СК костного мозга
Пунктат костного мозга
Мононуклеарная фракция
Гемопоэтические СК Стромальные СК
CD34+, 1–2%
CD14-, < 0.05%
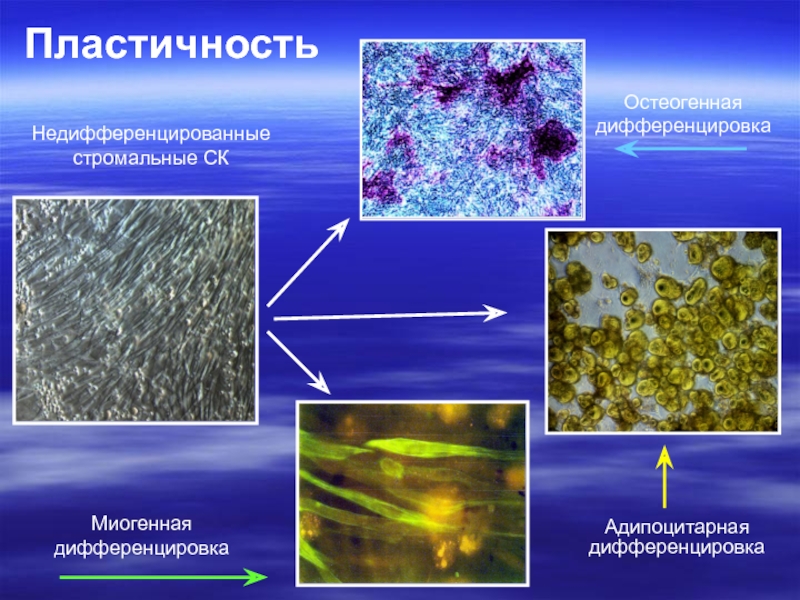
Слайд 13Пластичность
Недифференцированные стромальные СК
Остеогенная дифференцировка
Миогенная дифференцировка
Адипоцитарная
дифференцировка
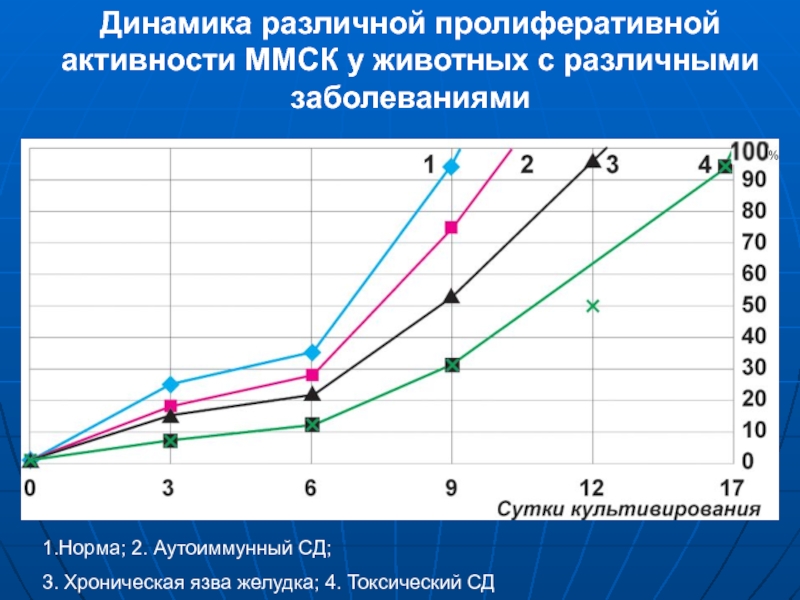
Слайд 15Динамика различной пролиферативной активности ММСК у животных с различными заболеваниями
1.Норма; 2.
3. Хроническая язва желудка; 4. Токсический СД
Слайд 17Взаимосвязь между содержанием CD25+ лимфоцитов в крови и количеством колониеформирующих единиц
Слайд 18Взаимосвязь между содержанием CD95+ лимфоцитов в крови и количеством колонеформирующих единиц
Слайд 19Содержание про- и противовоспалительных цитокинов в культуральной среде в процессе культивирования
Слайд 22Изменение (Δ) КДО, КСО и ФИ в группе АКШ+ККМ через 6
Слайд 23Микрососуды брыжейки тонкой кишки у интактной крысы.
Импрегнация азотнокислым серебром по Куприянову
Ув.
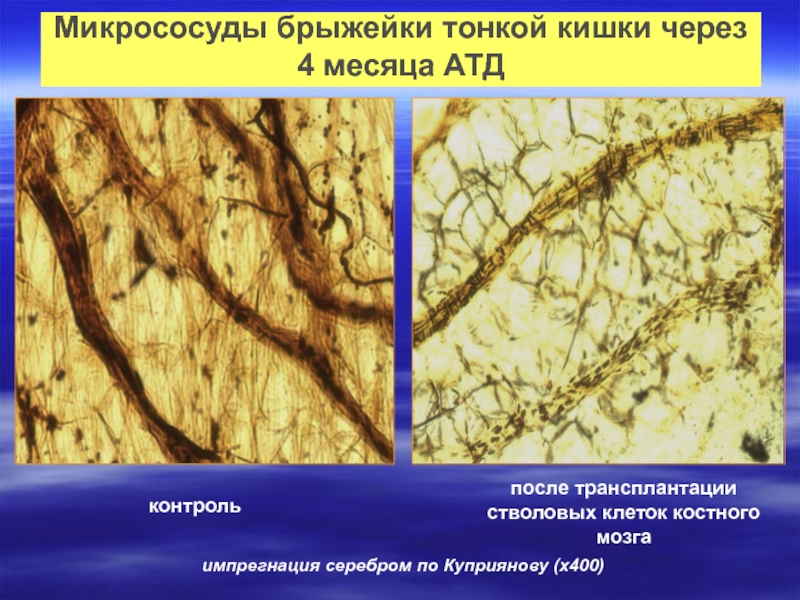
Слайд 24Микрососуды брыжейки тонкой кишки через 4 месяца АТД
контроль
после трансплантации стволовых клеток
импрегнация серебром по Куприянову (х400)
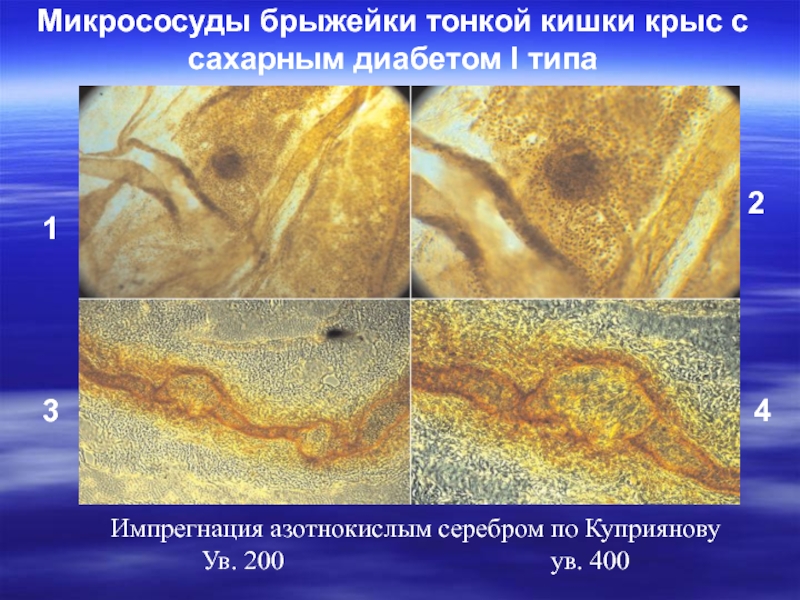
Слайд 25Микрососуды брыжейки тонкой кишки крыс с сахарным диабетом I типа
1
2
3
4
Импрегнация азотнокислым
Ув. 200 ув. 400
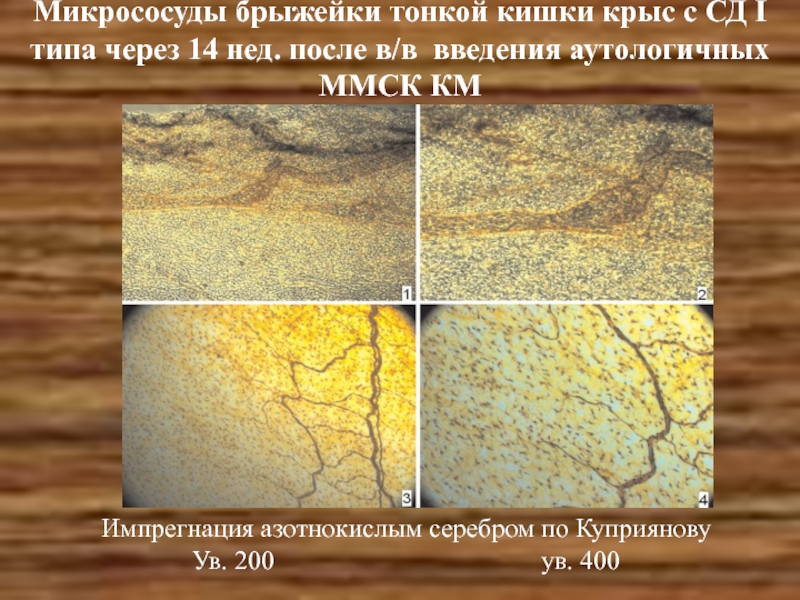
Слайд 26Микрососуды брыжейки тонкой кишки крыс с СД I типа через 14
Импрегнация азотнокислым серебром по Куприянову
Ув. 200 ув. 400
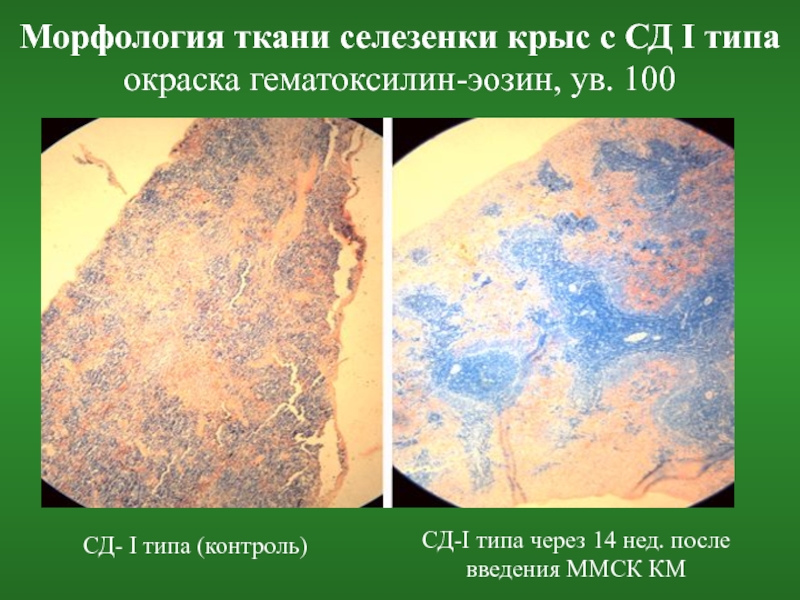
Слайд 27Морфология ткани селезенки крыс с СД I типа
окраска гематоксилин-эозин, ув. 100
СД-
СД-I типа через 14 нед. после введения ММСК КМ
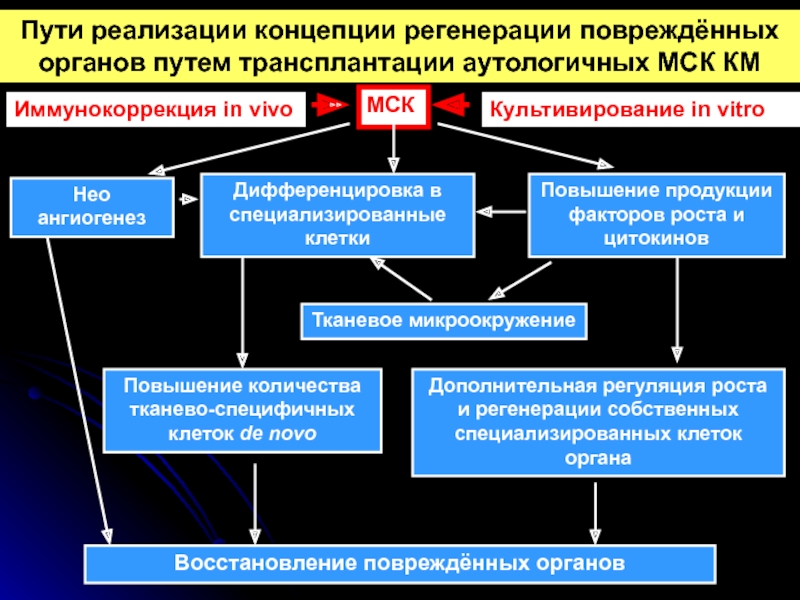
Слайд 28МСК
Нео
ангиогенез
Дифференцировка в специализированные клетки
Тканевое микроокружение
Повышение продукции факторов роста и цитокинов
Повышение количества
Дополнительная регуляция роста и регенерации собственных специализированных клеток органа
Восстановление повреждённых органов
Пути реализации концепции регенерации повреждённых органов путем трансплантации аутологичных МСК КМ
Иммунокоррекция in vivo
Культивирование in vitro