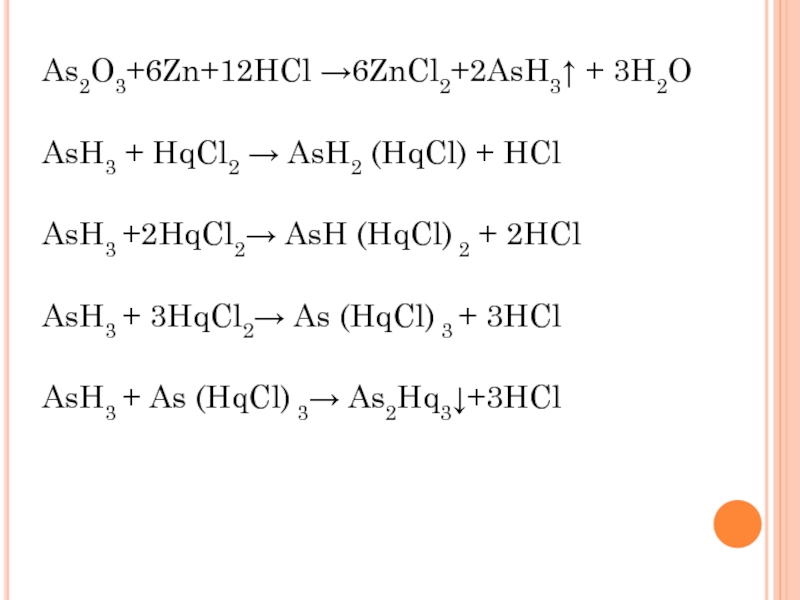- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Источники получения лекарственных средств презентация
Содержание
- 1. Источники получения лекарственных средств
- 2. План: Источники получения лекарственных средств.
- 3. Неорганические лекарственные вещества - получают из природных
- 4. II. Органические лекарственные вещества : 1. а)
- 5. III. Синтетические методы: 1.Полный синтез. Получают
- 6. IV. Биотехнология с использованием генной инженерии
- 7. 1. Замысел создания нового лекарственного вещества. 2.
- 8. Основные источники технологических и специфических
- 9. Примеси допустимые и
- 10. Допустимые примеси - допускаются в
- 11. Берут две одинаковые пробирки. В одну пробирку
- 12. Недопустимые примеси Не допускаются
- 13. В ГФ XI указаны требования и условия
- 14. Метод основан на восстановление мышьяка металлическим цинком
- 15. As2O3+6Zn+12HCl →6ZnCl2+2AsH3↑ + 3H2O AsH3 + HqCl2
- 16. Основан на восстановлении мышьяка в
- 17. 1. Метод высушивания. 2. Метод
- 18. 1. Индикатором. 2. Потенциометрически , pH метром. КИСЛОТНОСТЬ И ЩЕЛОЧНОСТЬ:
- 19. Прозрачность, степень мутности. Определяется
- 20. -Физические определение температуры плавления, затвердевания, плотности, удельный
- 21. Это период, в течения которого
- 22. 1. способ физический - сушка, нанесение защитных
- 23. 1. ГФ 2. ФС 3. ВФС 4.
Слайд 1Лекция №2
"Источники получения
лекарственных средств.
Основные положения и документы,
регламентирующие
фармацевтический
Слайд 2План:
Источники получения лекарственных средств.
Источники и причины недоброкачественности лекарственных веществ.
Сроки годности и
Слайд 3Неорганические лекарственные вещества - получают из природных источников- это минералы, воздух,
Источники получения
лекарственных средств.
Слайд 4II. Органические лекарственные вещества :
1. а) продукты сухой перегонки каменного угля.
в) горючих сланцев.
г) различные фракции нефти.
2. Продукты растительного происхождения.
Применяют около 10000 видов лекарственных растений: листья, цветки, корни, семена, плоды, эфирные и жирные масла, смолы, белки, углеводы.
3. Продукты животного происхождения.
4. Продукты жизнедеятельности микроорганизмов.
5. Продукты морских организмов - гидробионты.
Слайд 5III. Синтетические методы:
1.Полный синтез. Получают более простые алифатические, гетеро-циклические, ароматические соединения,
2. Частичный синтез( полусинтез) – на основе природных веществ. Получают вещества алкалоидов, витаминов, антибиотики.
3. Микробиологический синтез витаминов и коферментов.
Слайд 6IV. Биотехнология с использованием генной инженерии
Это технология получения различных продуктов
Объектами биотехнологии является культивируемые ткани, клетки животных и растений, микроорганизмы, созданные методами генной инженерии.
Слайд 71. Замысел создания нового лекарственного вещества.
2. Синтез предварительно отобранных структур.
3. Отсеивание
4. Клинические проверки.
5. Разработка технологии производства нового лекарственного вещества и наиболее рациональной лекарственной формы.
6. Подготовка НТД , включая контроль качества лекарственного вещества и его лекарственной формы.
7. Внедрение в промышленное производства .
РАЗРАБОТКА ЛЕКАРСТВЕННОГО ВЕЩЕСТВА
ВКЛЮЧАЕТ СЛЕДУЮЩИЕ СТАДИИ.
Слайд 8 Основные источники технологических и специфических примесей (приобретенные):
1. Плохая очистка
2. Примеси материала, из которого приготовлена аппаратура (металл, стекло).
3. Остатки растворителя .
4. Механические загрязнения (вата, фильтровальная бумага)
5. Загрязнения побочными продуктами синтеза.
6. Примеси, возникающие при хранении(влажность, свет, кислород воздуха, температура, качество тары).
ИСТОЧНИКИ И ПРИЧИНЫ
НЕДОБРОКАЧЕСТВЕННОСТИ
ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ.
Слайд 9Примеси допустимые и
Иногда одна и таже примесь допускается в одном препарате и не допускается в другом.
Слайд 10 Допустимые примеси - допускаются в лекарственных веществах в максимально
ЧИСТОТА И ОПРЕДЕЛЕНИЕ ПРИМЕСЕЙ.
Слайд 11Берут две одинаковые пробирки. В одну пробирку наливают 10 мл исследуемого
Методика определения допустимых примесей.
Слайд 12 Недопустимые примеси
Не допускаются в лекарственных веществах, влияют на
Методика определения недопустимых примесей.
Берут две одинаковые пробирки. В одну пробирку наливают 10 мл исследуемого вещества и добавляют сопутствующий реактив. Затем разливают этот раствор на две пробирки поровну , в одну из них добавляют основной реактив. Реактивы в обеих пробирках должны быть одинаковыми.
Слайд 13В ГФ XI указаны требования и условия выполнения испытаний на хлориды,
НАИБОЛЕЕ ЧАСТО ВСТРЕЧАЮЩИЕСЯ ПРИМЕСИ
Слайд 14Метод основан на восстановление мышьяка металлическим цинком до арсина. Затем арсин
ДОПУСТИМАЯ ПРИМЕСЬ МЫШЬЯКА -
МЕТОД ЗАНГЕР – БЛЕККА
(ГУТЦАЙТА).
Слайд 15As2O3+6Zn+12HCl →6ZnCl2+2AsH3↑ + 3H2O
AsH3 + HqCl2 → AsH2 (HqCl) + HCl
AsH3
AsH3 + 3HqCl2→ As (HqCl) 3 + 3HCl
AsH3 + As (HqCl) 3→ As2Hq3↓+3HCl
Слайд 16 Основан на восстановлении мышьяка в свободном виде. В качестве
NaH2PO2 + HCl → NaCl + H3PO2 фосфорноватистая
2H3PO2 →PH3 + H3PO4
As2O3 + PH3→2As↓+ H3PO3 фосфористая
Бурое пятно или осадок.
НЕДОПУСТИМАЯ ПРИМЕСЬ МЫШЬЯКА.
МЕТОД БУГО- ТИЛЕ.
Слайд 17
1. Метод высушивания.
2. Метод дистилляции.
3. Метод акваметрии.
ОПРЕДЕЛЕНИЕ ЛЕТУЧИХ ВЕЩЕСТВ И
Слайд 19 Прозрачность, степень мутности.
Определяется эталонным раствором из белой глины.
Сравнивают с эталонным раствором CoCl2, K2Cr2O7, CuSO4, FeCl3
Примеси органических веществ
С помощью H2SO4 (конц.)- озоление.
Определение золы
Прокаливают в фарфоровом или платиновом тигле.
Слайд 20-Физические определение температуры плавления, затвердевания, плотности, удельный вес, показатель преломления, вращения,
-Физико-химические.
-Химические (качественные реакции на подлинность, примеси, методы количественного анализа).
-Биологические: определение токсичности и стерильности, микробиологические испытания. Стерильность путем посева в пробирках с питательной средой. Отсутствие жизнеспособных микроорганизмов любого вида. Микробиологические испытания в лекарственных формах , которые не стерилизуются в течение производства: таблетки, капсулы, экстракты, спирты, мази. Испытания проводят в аптечных условиях в чашках Петри.
МЕТОДЫ АНАЛИЗА.
Слайд 21 Это период, в течения которого лекарственные средства должны отвечать
СРОКИ ГОДНОСТИ И СТАБИЛИЗАЦИЯ.
Слайд 221. способ физический - сушка, нанесение защитных покрытий, микрокапсулирование.
2. способ химический
МЕТОДЫ СТАБИЛИЗАЦИИ.
Слайд 231. ГФ
2. ФС
3. ВФС
4. Приказы № 214, №305.
Основной документ,
ОСНОВНЫЕ ДОКУМЕНТЫ
ФАРМАЦЕВТИЧЕСКОГО АНАЛИЗА.