- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Антимикробная и антибактериальная терапия. (Лекция 3) презентация
Содержание
- 2. Антиинфекционная химиотерапия Особая разновидность фармакотерапии, поскольку подразумевает использование антиинфекционных химиопрепаратов.
- 3. Антиинфекционные химиопрепараты Лекарственные препараты, основу которых составляют
- 4. Антимикробные препараты ( АМП ) Лекарственные препараты,
- 5. Общее для всех антибактериальных препаратов они влияют
- 6. Общее для всех антибактериальных препаратов Этим объясняется
- 7. Общее для всех антибактериальных препаратов Только длительное
- 8. Практически важный вывод АБП мало полезны при
- 9. Основные принципы рациональной антибиотикотерапии: выделение
- 10. Основные принципы рациональной антибиотикотерапии: своевременное начало
- 11. Основные принципы рациональной антибиотикотерапии: знание характера
- 12. Основные принципы рациональной антибиотикотерапии: комбинирование АБП
- 13. Основная цель антибактериальной терапии элиминация патогенов из организма человека.
- 14. Резистентность микроорганизмов Бактерии достаточно быстро эволюционируют и
- 15. Резистентность микроорганизмов природная приобретенная
- 16. Истинная природная устойчивость Характеризуется отсутствием у м/о
- 17. Истинная природная устойчивость Является постоянным видовым признаком
- 18. Приобретенная устойчивость Свойство отдельных штаммов бактерий сохранять
- 19. Приобретенная резистентность бактерий - первичная -
- 20. Первичная резистентность имеет место до начала
- 21. Вторичная резистентность возникает или возрастает в процессе лечения антибактериальными препаратами
- 22. Приобретенная устойчивость возникает в результате мутации отдельных
- 23. Приобретенная устойчивость Знание варианта формирования приобретенной резистентности
- 24. Приобретенная устойчивость два варианта по скорости
- 25. Бактериальные плазмиды связанные с переносом маркеров лекарственной
- 26. Бактериальные плазмиды В отдельных случаях r-факторы (неконъюгирующие
- 27. Транспозонные элементы это фрагменты ДНК, которые свободно
- 28. Транспозонные элементы Они не подчиняются rec-системам клетки,
- 30. Хромосомный тип передачи резистентности (медленный тип)
- 31. Хромосомный тип передачи резистентности (медленный тип)
- 32. Устойчивость микроорганизмов к АБП в случае как
- 33. Устойчивость микроорганизмов к АБП Инактивация антибиотика
- 34. Инактивация антибиотика наиболее часто встречается на
- 35. Инактивация антибиотика наибольшее значение для клинической практики
- 36. Инактивация антибиотика В таких ситуациях эффективность сохраняют цефалоспорины IV поколения и карбапенемы.
- 37. Нарушение проницаемости внешних структур микробной клетки
- 38. Нарушение проницаемости внешних структур микробной клетки Транспорт
- 39. Активное выведение АМП из микробной клетки
- 40. Модификация чувствительной мишени Структура любого компонента
- 41. Условие рационального выбора АМП предварительная оценка чувствительности
- 42. Основная цель исследований антибиотикорезистентности выявление приобретенной устойчивости
- 43. Проведение исследований по оценке антибиотикорезистентности необходимо для
- 44. Проведение исследований по оценке антибиотикорезистентности необходимо для
- 45. Проведение исследований по оценке антибиотикорезистентности необходимо для
- 46. Показания для проведения исследований антибиотикорезистентности : Если
- 47. Показания для проведения исследований антибиотикорезистентности : Исследованию
- 48. Показания для проведения исследований антибиотикорезистентности : Определение
- 49. Рeкомендации по подбору антибиотиков для включения в
- 50. Рeкомендации по подбору антибиотиков для включения в
- 51. Рeкомендации по подбору антибиотиков для включения в
- 52. Прогнозирование клинической эффективности АБП - на основе
- 53. Перечень АБП, чувствительность к которым рекомендуется определять
- 54. Перечень АБП, чувствительность к которым рекомендуется определять
- 55. Задача врача-бактериолога формирование наборов АБП для определения чувствительности различных видов микроорганизмов в конкретных учреждениях
- 56. Оценка антибиотикорезистентности
- 57. Оценка антибиотикорезистентности
- 58. Оценка антибиотикорезистентности
- 59. Оценка антибиотикорезистентности неферментирующих бактерий Примерный минимальный набор : цефтазидим пиперациллин гентамицин ципрофлоксацин карбенициллин
- 60. Оценка антибиотикорезистентности стафилококков при
- 61. Общая характеристика методов оценки антибиотикочувствительности генотипические
- 62. Общая характеристика методов оценки антибиотикочувствительности
- 63. Фенотипические методы - метод серийных разведений
- 64. Методы серийных разведений позволяют определять основной количественный
- 65. Методы серийных разведений МПК – наименьшая концентрация
- 66. Методы серийных разведений
- 67. Методы серийных разведений В зависимости от объема
- 68. Методы серийных разведений Использование тест-систем на основе
- 69. Методы серийных разведений В классическом
- 70. Методы серийных разведений для практических целей разработаны
- 71. Методы серийных разведений Недостатки метода : -
- 72. Диффузионные методы - диско- диффузионный -
- 73. Диско- диффузионный метод Сандартизованный метод, основан
- 74. Диско- диффузионный метод При проведении
- 75. Диско- диффузионный метод В это же
- 76. Диско- диффузионный метод рост микроорганизма (
- 77. Диско- диффузионный метод позволяет лишь
- 78. Е- тест представляет собой узкую полоску полимера
- 79. Е- тест
- 80. Оценка антибиотикочувствительности предполагает последовательное выполнение нескольких этапов:
- 81. Интерпретация результатов - заключается в прогнозировании
- 82. Интерпретация результатов - в отнесении исследуемого
- 83. Интерпретация результатов Чувствительный –
- 84. Интерпретация результатов Умеренно резистентный- при лечении
- 85. Интерпретация результатов Резистентный микроорганизм – имеет
- 86. Интерпретация результатов Приведенные категории являются клинически ориентированными и не всегда коррелируют с микробиологическими
- 87. Интегральный контроль качества определения лекарственной чувствительности Интегральный
- 88. Интегральный контроль качества определения лекарственной чувствительности Контрольные
- 89. Интегральный контроль качества определения лекарственной чувствительности При
Слайд 1
Лекция
«Принципы
Контроль эффективности антибактериальной терапии»
Слайд 2Антиинфекционная химиотерапия
Особая разновидность фармакотерапии, поскольку подразумевает использование антиинфекционных химиопрепаратов.
Слайд 3Антиинфекционные химиопрепараты
Лекарственные препараты, основу которых составляют химические соединения природного или искусственного
Слайд 4Антимикробные препараты ( АМП )
Лекарственные препараты, основу которых составляют химические соединения
Слайд 5Общее для всех антибактериальных препаратов
они влияют на бактерии в фазе активного
Слайд 6Общее для всех антибактериальных препаратов
Этим объясняется их опережающее воздействие на патогенные
Слайд 7Общее для всех антибактериальных препаратов
Только длительное применение АБП поддерживает их концентрацию
Слайд 8Практически важный вывод
АБП мало полезны при бессимптомном и малосимптомном носительстве болезнетворных
Слайд 9Основные принципы рациональной антибиотикотерапии:
выделение и идентификация возбудителя, изучение его
выбор наиболее активного и наименее токсичного препарата
Слайд 10Основные принципы рациональной антибиотикотерапии:
своевременное начало лечения и проведения курсов антибиотикотерапии
Слайд 11Основные принципы рациональной антибиотикотерапии:
знание характера и частоты побочных явлений при
Слайд 12Основные принципы рациональной антибиотикотерапии:
комбинирование АБП между собой и с другими
Слайд 14Резистентность микроорганизмов
Бактерии достаточно быстро эволюционируют и буквально в течение нескольких лет
Слайд 16Истинная природная устойчивость
Характеризуется отсутствием у м/о мишени действия антибиотика или недоступности
Слайд 17Истинная природная устойчивость
Является постоянным видовым признаком микроорганизмов и легко прогнозируется. При
Слайд 18Приобретенная устойчивость
Свойство отдельных штаммов бактерий сохранять жизнеспособность при тех концентрациях антибиотиков,
Слайд 19Приобретенная резистентность бактерий
- первичная
- вторичная
Оба типа резистентности основаны на
Слайд 20Первичная резистентность
имеет место до начала лечения антибактериальными средствами (например, устойчивость
Слайд 21Вторичная резистентность
возникает или возрастает в процессе лечения антибактериальными препаратами
Слайд 22Приобретенная устойчивость
возникает в результате мутации отдельных штаммов бактерий и селекции устойчивых
Слайд 23Приобретенная устойчивость
Знание варианта формирования приобретенной резистентности является очень важным в прогнозировании
Слайд 24Приобретенная устойчивость
два варианта по скорости формирования :
- хромосомныйй (медленный тип)
- плазмидный или транспозонный (быстрый тип)
Наиболее частой генетической основой резистентности служит наличие в бактериях внехромосомных факторов устойчивости к лекарственным веществам - плазмид и транспозонов
Слайд 25Бактериальные плазмиды
связанные с переносом маркеров лекарственной устойчивости в процессе конъюгации клеток-
— фактор переноса устойчивости RTF, обеспечивающего передачу генетической информации
- r-фактор, отвечающего за резистентность к антибиотикам
Слайд 26Бактериальные плазмиды
В отдельных случаях r-факторы (неконъюгирующие плазмиды) существуют в бактериальных клетках
Слайд 27Транспозонные элементы
это фрагменты ДНК, которые свободно перемещаются от одного репликона к
Слайд 28Транспозонные элементы
Они не подчиняются rec-системам клетки, которые ограничивают передачу хромосомных маркеров
Слайд 30Хромосомный тип передачи резистентности (медленный тип)
Спонтанные мутации происходят с низкой частотой-
Слайд 31Хромосомный тип передачи резистентности (медленный тип)
Для закрепления данной мутации в популяции
Слайд 32Устойчивость микроорганизмов к АБП
в случае как плазмидной, так и хромосомной локализации
Слайд 33Устойчивость микроорганизмов к АБП
Инактивация антибиотика
Модификация мишени действия
Активное выведение антибиотика
Нарушение проницаемости внешних структур микробной клетки
Формирование метаболического "шунта"
Слайд 34Инактивация антибиотика
наиболее часто встречается на
антимикробные препараты группы β-
лактамных АМП, которые
лактамное кольцо антибиотиков. β-
лактамазы, продуцируемые грам+
микробами выделяются из клетки в
межклеточное пространство.
Продуцируемые грам- бактериями не
покидают клетку и циркулируют между
наружной и внутренней мембранами
Слайд 35Инактивация антибиотика
наибольшее значение для клинической практики имеют плазмидные β - лактамазы
Слайд 36Инактивация антибиотика
В таких ситуациях эффективность сохраняют цефалоспорины IV поколения и карбапенемы.
Слайд 37Нарушение проницаемости внешних структур микробной клетки
мишени действия антибиотиков локализованы либо
Слайд 38Нарушение проницаемости внешних структур микробной клетки
Транспорт АМП внутрь микробной клетки осуществляется
Слайд 39 Активное выведение АМП из микробной клетки (эффлюкс)
У микроорганизмов обнаружены
Слайд 40Модификация чувствительной мишени
Структура любого компонента живой клетки подвержена изменчивости в
Слайд 41Условие рационального выбора АМП
предварительная оценка чувствительности патогена для выбора антибиотика и
Слайд 42Основная цель исследований антибиотикорезистентности
выявление приобретенной устойчивости к антибактериальным препаратам у природно-чувствительных
Подтверждение наличия у м/о природной чувствительности или устойчивости к антибиотикам не является целью практических исследований.
Слайд 43Проведение исследований по оценке антибиотикорезистентности необходимо для решения основных задач :
1.Обоснование
Слайд 44Проведение исследований по оценке антибиотикорезистентности необходимо для решения основных задач :
2.
Слайд 45Проведение исследований по оценке антибиотикорезистентности необходимо для решения основных задач :
3.
4. Исследование новых химических соединений на наличие антибактериальной активности
Слайд 46Показания для проведения исследований антибиотикорезистентности :
Если уровень устойчивости микроорганизма к антибактериальным
Слайд 47Показания для проведения исследований антибиотикорезистентности :
Исследованию по оценке антибиотикорезистентности подлежат чистые
Слайд 48Показания для проведения исследований антибиотикорезистентности :
Определение показаний для оценки антибиотикорезистентности микроорганизмов
Обязательному исследованию на антибиотикорезистентность подлежат все микроорганизмы, выделенные из первично стерильных жидкостей, органов и тканей человека.
Слайд 49Рeкомендации по подбору антибиотиков для включения в исследование различных микроорганизмов
Слайд 50Рeкомендации по подбору антибиотиков для включения в исследование различных микроорганизмов.
В исследование
Слайд 51Рeкомендации по подбору антибиотиков для включения в исследование различных микроорганизмов.
Для
Необходимо учитывать фармакокинетические, токсикологические и экономические параметры, а также особенности тактики терапии в конкретном учреждении
Слайд 52Прогнозирование клинической эффективности АБП
- на основе оценки фенотипа ( антибиотикограммы) менее
- прогнозирование на основе выявления генотипа ( набора детерминант резистентности) не всегда осуществимо. В ряде случаев генотипирование может быть заменено оценкой чувствительности к АБП, являющимися маркерами того или иного механизма устойчивости.
Слайд 53Перечень АБП, чувствительность к которым рекомендуется определять
1 группа: подлежащие изучению в
2 группа - дополнительные
Оценка чувствительности к препаратам 1 группы позволяет получить минимально необходимую информацию для обоснования рациональной терапии инфекции. Информативность исследований возрастает по мере увеличения количества включенных в исследование АБП из группы 2.
Слайд 54Перечень АБП, чувствительность к которым рекомендуется определять
Необходимо учитывать закономерности перекрестной резистентности
Слайд 55Задача врача-бактериолога
формирование наборов АБП для определения чувствительности различных видов микроорганизмов в
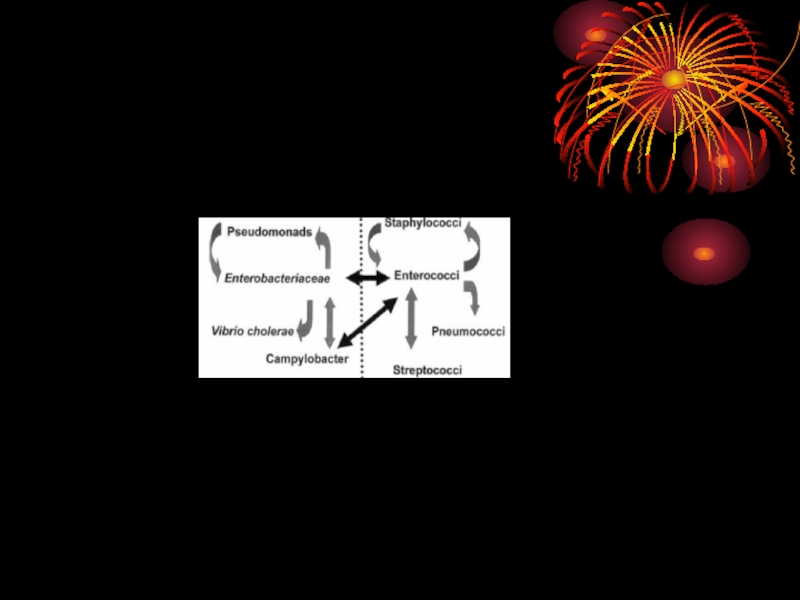
Слайд 56Оценка антибиотикорезистентности
Самостоятельные наборы антибиотиков следует использовать для определения резистограмм:
- микроорганизмов, выделенных при гнойно-воспалительных заболеваниях различной локализации
- возбудителей кишечных инфекций ( Shigella, Salmonella, Escherichia)
- микроорганизмов, выделенных при инфекциях мочевыводящих путей.
Слайд 57Оценка антибиотикорезистентности
Для возбудителей гнойно-септических
ампициллин
защищенный аминопенициллин
цефотаксим или цефтриаксон
цефтазидим
гентамицин
ципрофлоксацин
Слайд 58Оценка антибиотикорезистентности
При кишечных инфекциях :
ампициллин
ко-тримоксазол
фторированные хинолоны
При генерализованных инфекциях целесообразно включать антибиотики и наибольшей клинической эффективностью, а также те, к которым редко встречается приобретенная резистентность: цефалоспорины 3 поколения, хлорамфеникол.
Слайд 59Оценка антибиотикорезистентности неферментирующих бактерий
Примерный минимальный набор :
цефтазидим
пиперациллин
гентамицин
ципрофлоксацин
карбенициллин
Слайд 60Оценка антибиотикорезистентности стафилококков
при прямой детекции продукции бета-лактамазы включает
Пенициллин
оксациллин
эритромицин
клиндамицин
ко- тримоксазол
ванкомин
фузидиевая кислота
Слайд 61Общая характеристика методов оценки антибиотикочувствительности
генотипические
фенотипические
Генотипические методы
Слайд 62Общая характеристика методов оценки антибиотикочувствительности
Фенотипические методы: предполагают оценку влияния
Слайд 63Фенотипические методы
- метод серийных разведений
- диффузионные, основанные на детекции роста исследуемых
Слайд 64Методы серийных разведений
позволяют определять основной количественный показатель, характеризующий антибактериальную активность антибиотика,
Слайд 65Методы серийных разведений
МПК – наименьшая концентрация антибиотика, подавляющая видимый рост исследуемого
Для определения МПК заданные концентрации АБП вносят в питательную среду, которую затем засевают культурой исследуемого микроорганизма, и после инкубации оценивают наличие или отсутствие видимого роста.
Слайд 67Методы серийных разведений
В зависимости от объема используемой жидкой питательной среды выделяют
микроразведений.
Разновидность метода - метод, основанный на использовании только двух концентраций АБП, соответствующих пограничным значениям МПК. Этот принцип используется в автоматизированных системах для определения чувствительности микроорганизмов.
Слайд 68Методы серийных разведений
Использование тест-систем на основе метода микроразведений позволяет:
- избегать трудоемких
обеспечивать получение достоверных количественных результатов по уровню антибиотикорезистентности
Слайд 69Методы серийных разведений
В классическом варианте наличие (появление мутности) или
В коммерческих вариантах метода используют спектрофотометрическое измерение оптической плотности питательной среды
Слайд 70Методы серийных разведений
для практических целей разработаны методы детекции начальных стадий бактериального
Слайд 71Методы серийных разведений
Недостатки метода :
- Наличие субстанций антибиотиков с известным уровнем
- строгое соблюдение режимов хранения
- тщательное выполнение контроля качества питательных сред
- трудоемкость приготовления рабочих растворов антибиотиков
Слайд 72Диффузионные методы
- диско- диффузионный
- эпсилометрический ( Е-тест)
Исторически более старым и наиболее
Слайд 73Диско- диффузионный
метод
Сандартизованный метод, основан ный на формировании вокруг бумажного диска,
Слайд 74Диско- диффузионный
метод
При проведении исследования диск с АБП накладывают на
Слайд 75Диско- диффузионный
метод
В это же время начинается процесс адаптации микроорганизма к
Слайд 76Диско- диффузионный
метод
рост микроорганизма ( образование газона) начнется на тех участках
Слайд 77Диско- диффузионный
метод
позволяет лишь косвенно судить о величине МПК, а
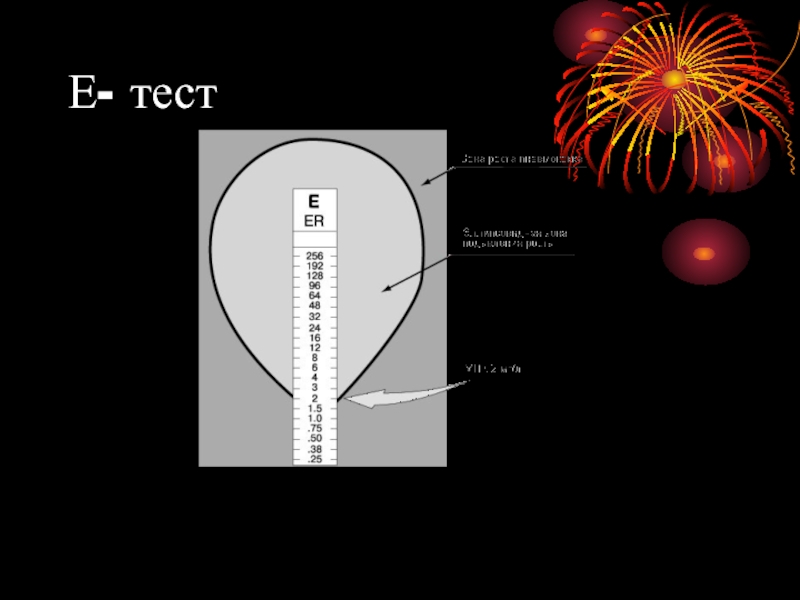
Слайд 78Е- тест
представляет собой узкую полоску полимера ( 0,5-6,0 см ), на
Слайд 80Оценка антибиотикочувствительности
предполагает последовательное выполнение нескольких этапов:
- приготовление питательных сред
- приготовление суспензии
- инокуляция
- инкубация
- учет и интерпретация результатов, формулировка рекомендаций по лечению