- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Моделирование в среде TCAD презентация
Содержание
- 1. Моделирование в среде TCAD
- 2. Моделирование технологических процессов в Sentaurus Process Диффузия. Окисление.
- 3. Моделирование процесса диффузии Диффузия – физический
- 4. Основное уравнение для процесса диффузии (Sentaurus Process)
- 5. Уравнение непрерывности для примеси типа a
- 6. Модели диффузии Модели переноса позволяют рассчитать поток
- 7. Модель диффузии ChargedReact Модель диффузии ChargedReact –
- 8. Реакции в модели диффузии ChargedReact A –
- 9. Дифференциальные уравнения в модели ChargedReact CA –
- 10. Модель ChargedReact : уравнение для заряженных пар
- 11. Поток пар: Потокт дефектов: Скорости для всех комбинаций зарядовых состояний:
- 12. Типы моделей ChargedReact Diffusion Model React Diffusion
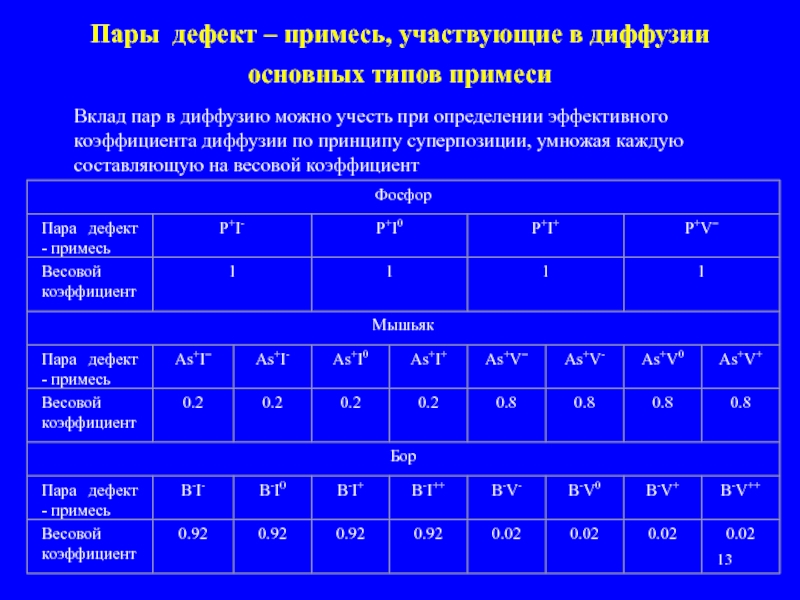
- 13. Пары дефект – примесь, участвующие в диффузии
- 14. Кинетический метод Монте-Карло для расчета процесса диффузии (KMC)
- 15. Кинетический метод Монте-Карло рассчитывает траектории индивидуальных примесей
- 16. Преимущества метода Монте-Карло Уменьшение термического бюджета в
- 17. При обычном подходе к моделированию число решаемых
- 18. Повышение конкурентноспособности метода Монте-Карло С уменьшением размеров
- 19. Основные характеристики KMC Моделируются только дефекты и
- 20. Основные характеристики KMC Входные параметры – энергии
- 21. Основные характеристики KMC КМС (на базе программы
- 22. Атомистический режим Распределения всех величин рассчитываются полностью
- 23. КМС использует ортогональную сетку и разбиение моделируемой области на прямоугольные поддомены.
- 24. Используемые материалы Кремний (монокристаллический) Аморфный кремний Диоксид кремния Поликристаллический кремний Нитрид кремния Газ (внешняя среда)
- 25. Типы частиц
- 26. Точечные дефекты могут взаимодействовать с соседними частицами и перемещаться на расстояние λ в ортогональных направлениях
- 27. Атомы акцепторной или донорной примеси могут диффундировать
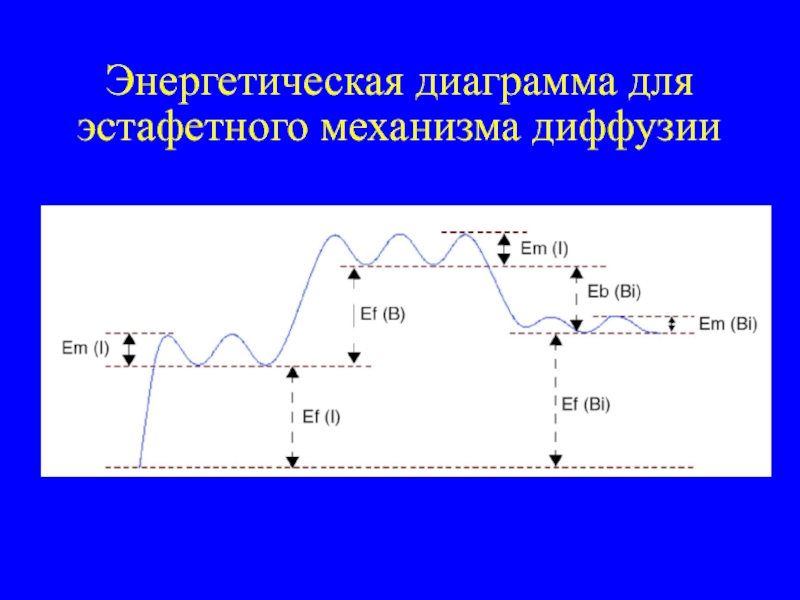
- 28. Энергетическая диаграмма для эстафетного механизма диффузии
- 29. Не все возможные сочетания частиц участвуют в
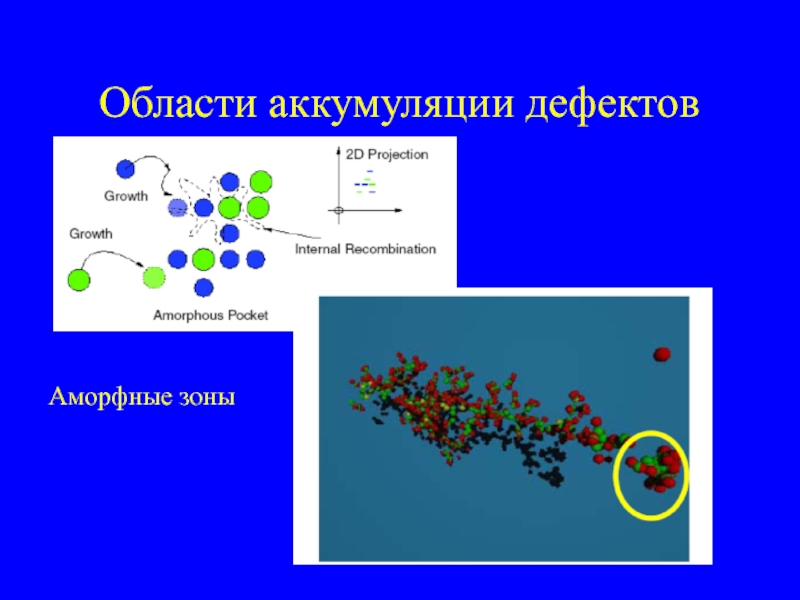
- 30. Области аккумуляции дефектов Аморфные зоны
- 31. Протяженные дефекты {311} дефекты Кольца дислокаций Пустоты (вакансионные кластеры)
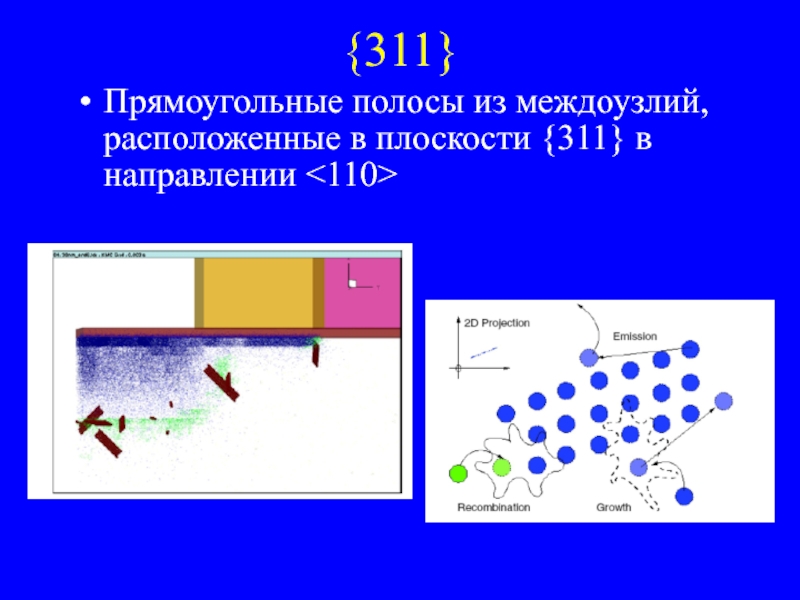
- 32. {311} Прямоугольные полосы из междоузлий, расположенные в плоскости {311} в направлении
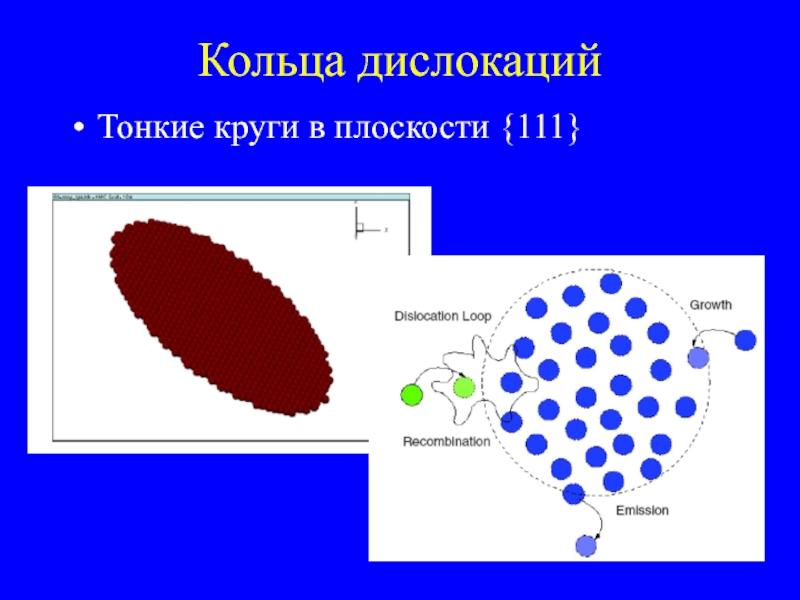
- 33. Кольца дислокаций Тонкие круги в плоскости {111}
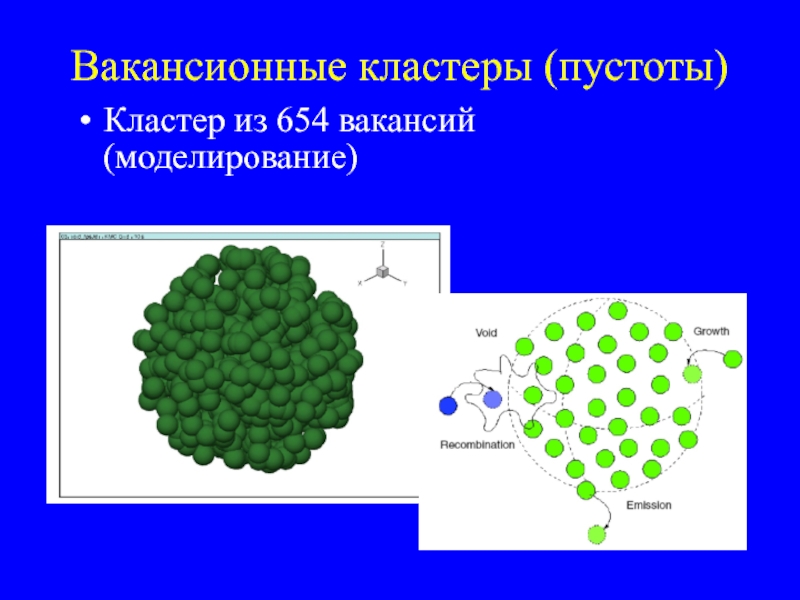
- 34. Вакансионные кластеры (пустоты) Кластер из 654 вакансий (моделирование)
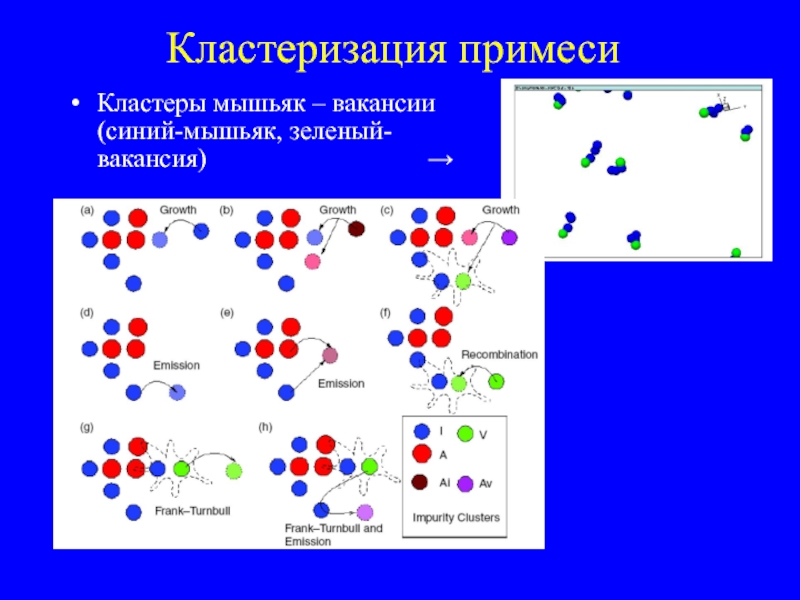
- 35. Кластеризация примеси Кластеры мышьяк – вакансии (синий-мышьяк, зеленый-вакансия) →
- 36. Зарядовые состояния
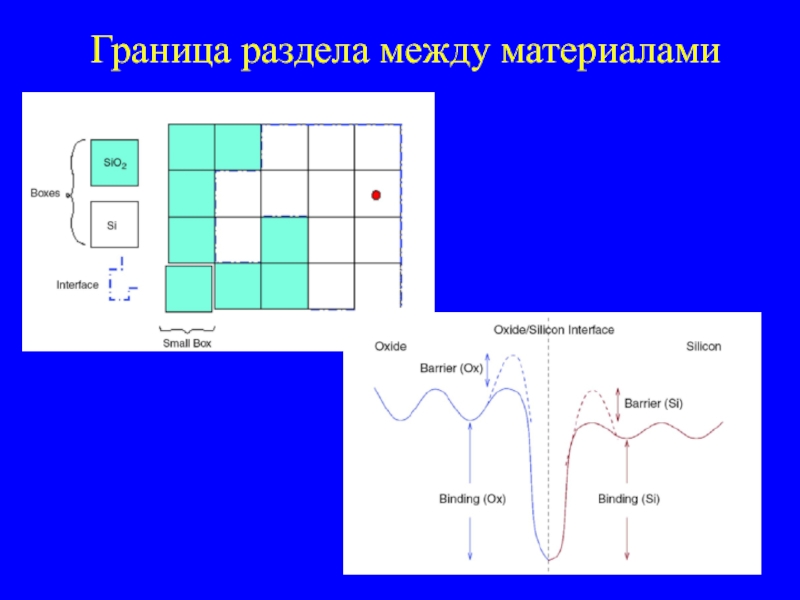
- 37. Граница раздела между материалами
- 38. Моделирование диффузии в процессе окисления На каждом
- 39. Пример: окисление при формировании затвора, КМОП -
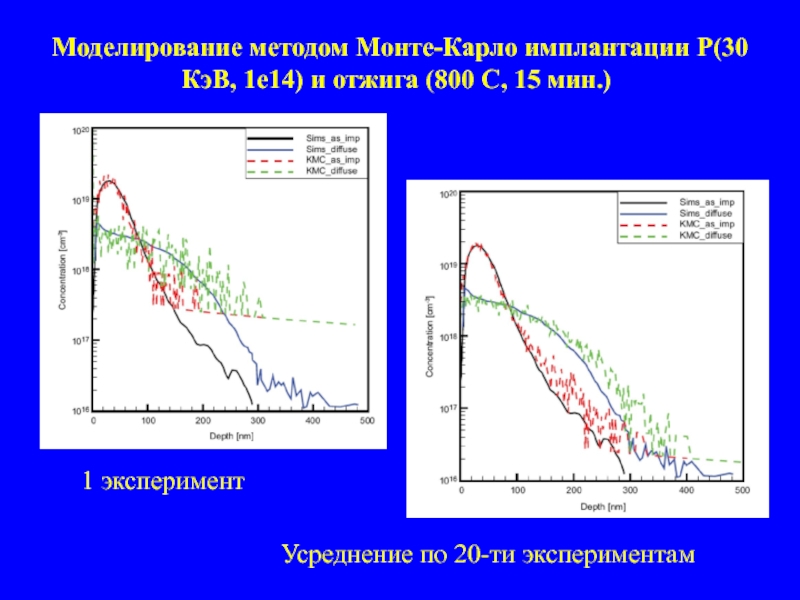
- 40. Моделирование методом Монте-Карло имплантации P(30 КэВ, 1е14)
- 41. Sentaurus Process Kinetic Monte Carlo Неоднородная
- 42. Полное описание см. Sprocess Гл. 5 Atomistic kinetic Monte Carlo diffusion
- 43. Окисление Окислительный процесс включает три этапа: Диффузия
- 44. Уравнения химических реакций: Диффузия
- 45. Модель Дила - Гроува Скорость роста окисла
- 46. Вывод модели Дила - Гроува F1
- 47. F1 = F2
- 48. Модель Массуда эмпирическая модель,
- 49. В = ВО2 +
- 50. 2D и 3D окисление Для точного моделирования
Слайд 3Моделирование процесса диффузии
Диффузия – физический процесс, обуславливающий миграцию атомов легирующих
Диффузия приобретает направленное движение под влиянием либо градиента концентрации, либо градиента температуры
(в микроэлектронном производстве градиенты температуры в подложке – отрицательное явление и не используется на практике)
Слайд 4Основное уравнение для процесса диффузии (Sentaurus Process)
- поток диффундирующих
с – зарядовое состояние,
d – коэффициент диффузии,
A – концентрация примеси типа а,
n – концентрация электронов
Слайд 5
Уравнение непрерывности для примеси типа a в зарядовом состоянии c
- вклад генерации – рекомбинации, связанный с процессом кластеризации
Слайд 6Модели диффузии
Модели переноса позволяют рассчитать поток частиц примеси и являются основой
В дополнение к расчету потоков частиц могут быть учтены возможные реакции взаимодействия частиц в процессе диффузии в зависимости от выбранного типа модели.
Модели переноса обычно используются с одной или несколькими моделями кластеризации или активации. Реакции взаимодействия или модели кластеризации не модифицируют поток частиц, а добавляют в уравнении непрерывности слагаемые к
Слайд 7Модель диффузии ChargedReact
Модель диффузии ChargedReact – наиболее полная модель переноса в
Модель включает неподвижную примесь в замещающем состоянии и до двух подвижных заряженных пар примесь-дефект.
Также в рассмотрение включены подвижные заряженные точечные дефекты.
Слайд 9Дифференциальные уравнения в модели ChargedReact
CA – концентрация замещающих атомов примеси
CI –
CV – концентрация вакансий
CAX- концентрация пар дефект-примесь (I или V)
Слайд 10Модель ChargedReact : уравнение для заряженных пар
Предполагается, что реакция образования пар
где X это I или V, z – заряд примеси A
- Скорость реакции образования пар AX
Слайд 12Типы моделей
ChargedReact Diffusion Model
React Diffusion Model
ChargedPair Diffusion Model
Pair Diffusion Model
ChargedFermi Diffusion
Fermi Diffusion Model
Constant Diffusion Model
NeutralReact Diffusion Model
Слайд 13Пары дефект – примесь, участвующие в диффузии основных типов примеси
Вклад
Слайд 15Кинетический метод Монте-Карло рассчитывает траектории индивидуальных примесей и точечных дефектов и
Метод позволяет изучать процесс диффузии на микроскопическом уровне.
Результаты моделирования с помощью КМС могут быть использованы для калибровки моделей, основанных на решении уравнений диффузии.
Слайд 16Преимущества метода Монте-Карло
Уменьшение термического бюджета в современных технологических маршрутах сокращает продолжительность
Слайд 17При обычном подходе к моделированию число решаемых уравнений быстро возрастает с
С другой стороны, уменьшение размеров приборов приводит к малому количеству атомов примеси, формирующих структуру прибора (десятки или сотни). Приближается предел, когда такие малые дискретизованные распределения уже не могут быть аппроксимированы непрерывными функциями.
Слайд 18Повышение конкурентноспособности метода Монте-Карло
С уменьшением размеров трудоемкость метода Монте-Карло снижается, т.к.
Большое количество различных конфигураций дефект – примесь не усложняет метод, т.к. требует только введения значений вероятностей для дополнительных реакций.
Трудоемкость обычного метода моделирования систем уравнений возрастает из-за неравновесных процессов
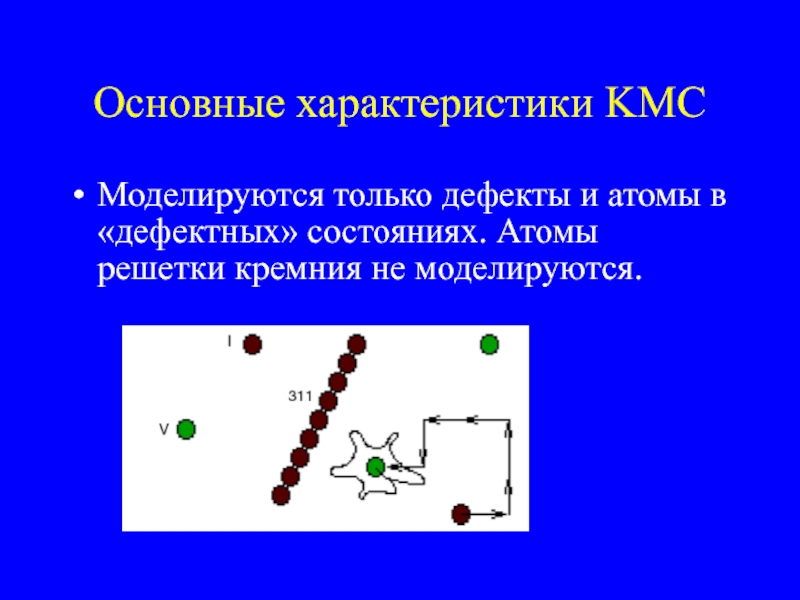
Слайд 19Основные характеристики KMC
Моделируются только дефекты и атомы в «дефектных» состояниях. Атомы
Слайд 20Основные характеристики KMC
Входные параметры – энергии миграции, связи, эмиссии и др.
По
Частицы могут также взаимодействовать с протяженными дефектами или двигаться вдоль них.
Слайд 21Основные характеристики KMC
КМС (на базе программы DADOS) может работать в 2-х
Атомистическом (наиболее точный)
Неатомистическом, с использованием модуля KMC для отдельных операций, прежде всего неравновесных процессов (RTA и др.)
Слайд 22Атомистический режим
Распределения всех величин рассчитываются полностью на основе расчета траекторий отдельных
Основные ограничения данного режима:
Осаждение слоев возможно только без учета примеси;
Имплантация должна моделироваться только с помощью Sentaurus MC
Окисление не моделируется.
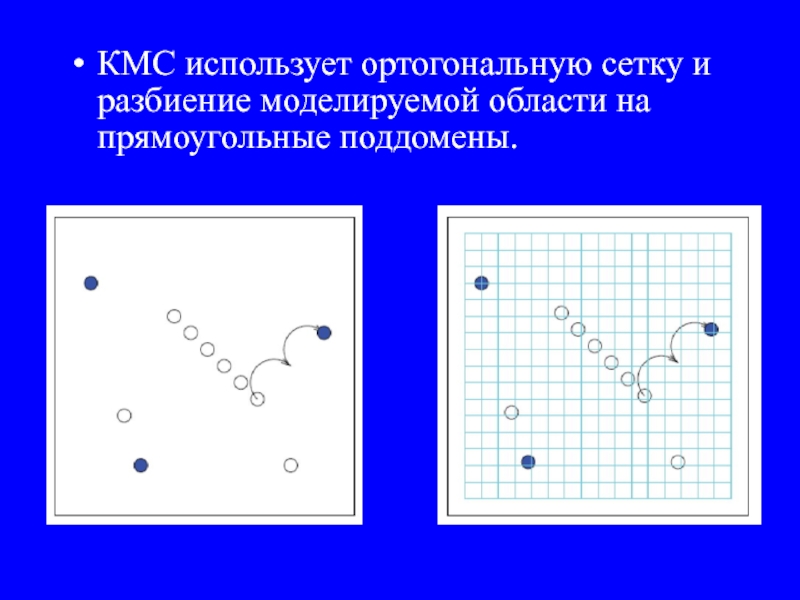
Слайд 23КМС использует ортогональную сетку и разбиение моделируемой области на прямоугольные поддомены.
Слайд 24Используемые материалы
Кремний (монокристаллический)
Аморфный кремний
Диоксид кремния
Поликристаллический кремний
Нитрид кремния
Газ (внешняя среда)
Слайд 26Точечные дефекты могут взаимодействовать с соседними частицами и перемещаться на расстояние
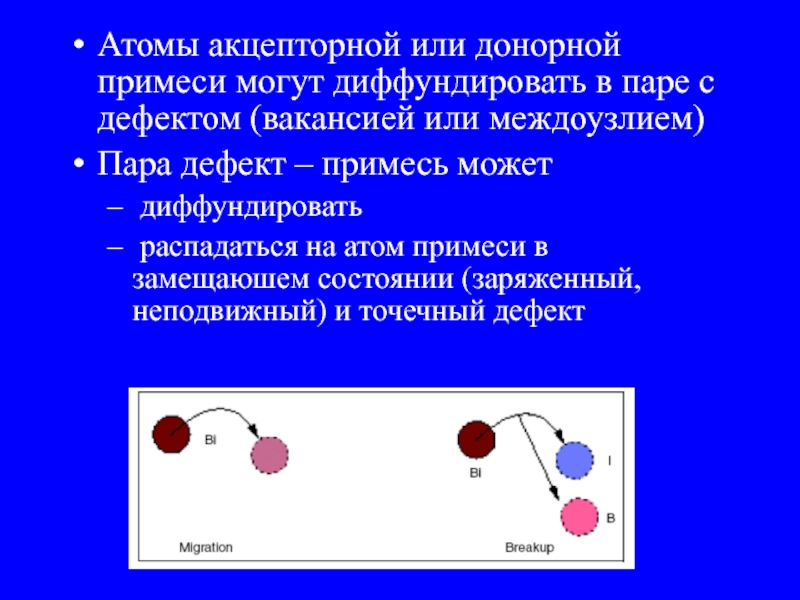
Слайд 27Атомы акцепторной или донорной примеси могут диффундировать в паре с дефектом
Пара дефект – примесь может
диффундировать
распадаться на атом примеси в замещаюшем состоянии (заряженный, неподвижный) и точечный дефект
Слайд 29Не все возможные сочетания частиц участвуют в реакциях.
Возможные реакции включают физически
Рассматриваются только обратимые реакции, реакции со стабильными выходными продуктами.
Например, допустимые реакции для бора:
Слайд 38Моделирование диффузии в процессе окисления
На каждом шаге решается система уравнений для
Перед запуском шага моделирования диффузии методом КМС трансформируется сетка.
Вновь выращенный окисел встраивается в тензорную сетку, используемую в КМС
Материал и свойства частиц изменяются там, где необходимо
Недостаток: несовершенство интерполяции при переходе от непрерывной сетки к тензорной
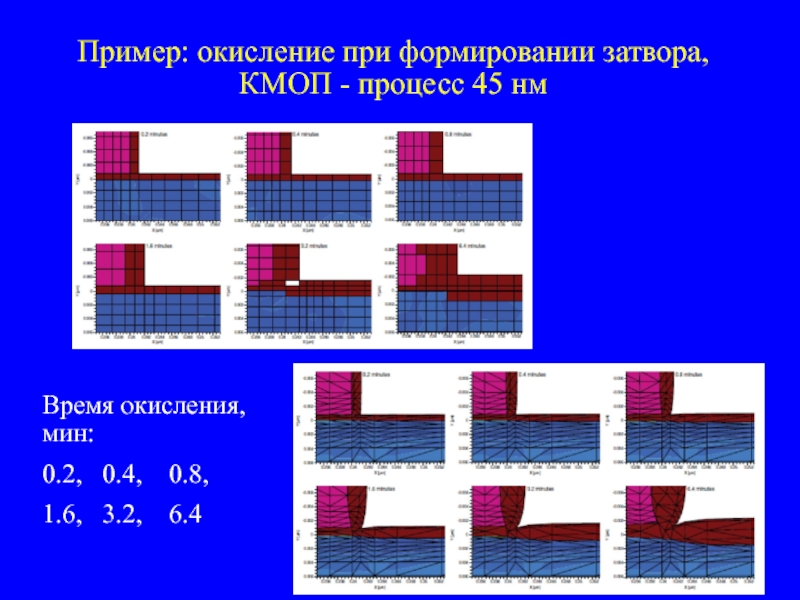
Слайд 39Пример: окисление при формировании затвора, КМОП - процесс 45 нм
Время окисления,
0.2, 0.4, 0.8,
1.6, 3.2, 6.4
Слайд 40Моделирование методом Монте-Карло имплантации P(30 КэВ, 1е14) и отжига (800 С,
1 эксперимент
Усреднение по 20-ти экспериментам
Слайд 41Sentaurus Process
Kinetic Monte Carlo
Неоднородная тензорная сетка
Механические напряжения и SiGe
Дополнительные физические
МОП-транзистор: моделирование с помощью Sentaurus Process KMC.
Слайд 43Окисление
Окислительный процесс включает три этапа:
Диффузия частиц окислителя (H2O, O2) от границы
Химическая реакция между окислителем и кремнием с образованием нового окисла.
Перемещение материалов и границ раздела из-за расширения объема, вызванного образованием оксида.
Слайд 44Уравнения химических реакций:
Диффузия окислителя описывается законом Фика и уравнением непрерывности:
где D
Поток окислителя, поступающий из внешней атмосферы в окисел по нормали к поверхности:
где h – коэффициент массопереноса и c* - концентрация окислителя в атмосфере
Слайд 45Модель Дила - Гроува
Скорость роста окисла в одномерном случае может быть
где xox – толщина слоя окисла.
Уравнение может быть решено аналитически; параметры модели: константа параболического роста B и константа линейного роста B/A.
Более глубокий анализ показывает связь константы параболического роста с коэффициентом диффузии, а константы линейного роста со скоростью химической реакции.
Слайд 46Вывод модели Дила - Гроува
F1 = h(C*-C0) – массоперенос через внешнюю
F2 = D(C0 – Ci)/x – диффузия окислителя через окисел к границе раздела окисел/кремний.
F3 = kCi – химическая реакция на границе раздела окисел/кремний.
В условиях равновесия F1 = F2 = F3
F2 = F3 : Ci = C0 /(1 + kx/D)
F1 = F3 : Ci = C*/(1 + k/h + kx/D)
dx/dt = F3 /N
Слайд 48
Модель Массуда
эмпирическая модель, учитывающая ускоренный рост окисла на начальном этапе
может рассматриваться как расширение модели Дила – Гроува; хорошо согласуется с экспериментом
параметры L и C зависят от кристаллографической ориентации и температуры
Слайд 49
В = ВО2 + ВН2О
ВО2 = FP∙RPO2∙pO2
ВH2О = FP∙RPH2O∙pH2O
Константы параболического и линейного роста зависят от давления и температуры
Слайд 502D и 3D окисление
Для точного моделирования необходимо проводить расчет следующих 2D
Растворение окислительных реагентов на границе газ-окисел ,
Перенос частиц окислителя через существующий окисел,
Химическая реакция на границе окисел-кремний.
Растворение и химическая реакция моделируются как граничные условия;
Для моделирования переноса рассчитывается уравнение диффузии частич в слое окисла