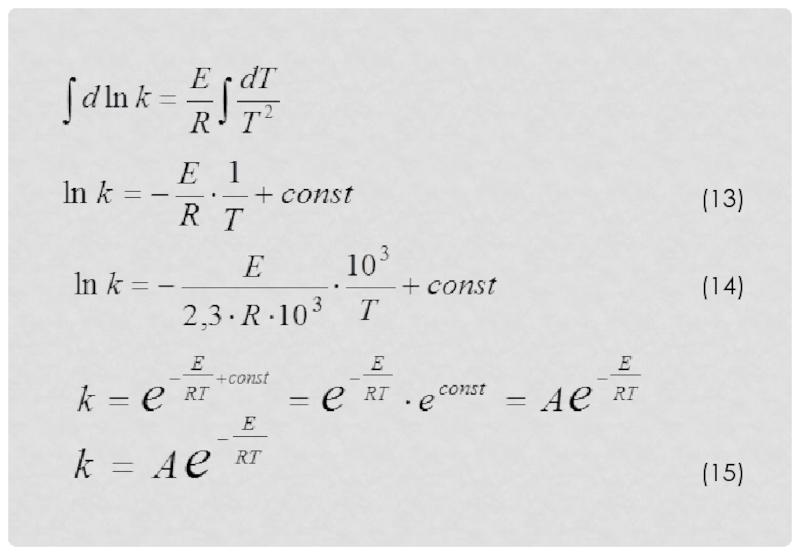- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Зависимость константы скорости химической реакции от температуры презентация
Содержание
- 1. Зависимость константы скорости химической реакции от температуры
- 2. ПРАВИЛО ВАНТ-ГОФФА При увеличении температуры на
- 4. ТЕОРИЯ АРРЕНИУСА. ЭНЕРГИЯ АКТИВАЦИИ РЕАКЦИИ Основные модельные
- 5. Энергию активации (Е) можно трактовать как избыток
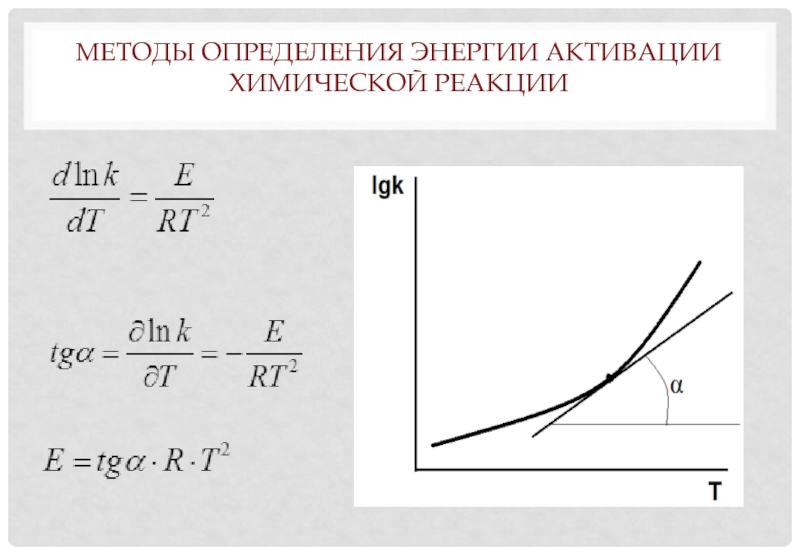
- 8. МЕТОДЫ ОПРЕДЕЛЕНИЯ ЭНЕРГИИ АКТИВАЦИИ ХИМИЧЕСКОЙ РЕАКЦИИ
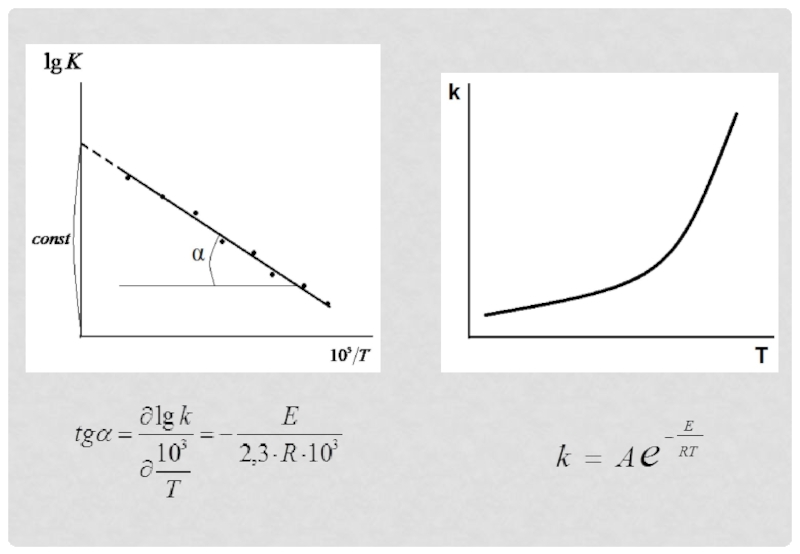
- 12. УРАВНЕНИЕ ВАНТ-ГОФФА - АРРЕНИУСА
Слайд 2 ПРАВИЛО ВАНТ-ГОФФА
При увеличении температуры на 10 градусов скорость реакции возрастает
в 2-4 раза.
Слайд 4ТЕОРИЯ АРРЕНИУСА.
ЭНЕРГИЯ АКТИВАЦИИ РЕАКЦИИ
Основные модельные представления теории:
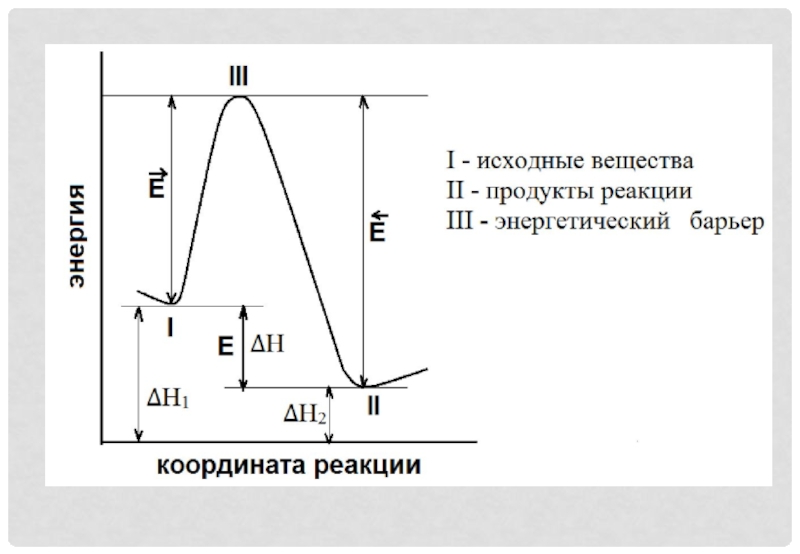
В реакцию способны вступать лишь
те частицы реагентов, которые обладают некоторой избыточной энергией, позволяющей им преодолеть энергетический барьер.
Минимально необходимый запас энергии называют энергией активации.
Минимально необходимый запас энергии называют энергией активации.
Слайд 5Энергию активации (Е) можно трактовать как избыток энергии по сравнению со
средней энергией молекул при данной температуре, которой должны обладать молекулы, чтобы они могли вступить в химическую реакцию.
Источники получения избыточной энергии:
термическая активация;
действие различных излучений (свет, ультразвук, радиация);
действие быстрых частиц (радикалов).
Источники получения избыточной энергии:
термическая активация;
действие различных излучений (свет, ультразвук, радиация);
действие быстрых частиц (радикалов).